Los fármacos utilizados en la diabetes tratan la diabetes mellitus disminuyendo los niveles de glucosa en la sangre . Con excepción de la insulina , la mayoría de los agonistas del receptor GLP-1 ( liraglutida , exenatida y otros) y la pramlintida , todos los medicamentos para la diabetes se administran por vía oral y, por lo tanto, se denominan agentes hipoglucemiantes orales o agentes antihiperglucémicos orales. Existen diferentes clases de fármacos hipoglucemiantes y la selección del agente apropiado depende de la naturaleza de la diabetes, la edad y la situación de la persona, así como de otros factores del paciente.
La diabetes mellitus tipo 1 es una enfermedad causada por la falta de insulina. Por lo tanto, la insulina es el principal agente de tratamiento para el tipo 1 y generalmente se administra mediante inyección subcutánea.
La diabetes mellitus tipo 2 es una enfermedad en la que las células presentan resistencia a la insulina. La diabetes mellitus tipo 2 es el tipo más común de diabetes. Los tratamientos incluyen agentes que (1) aumentan la cantidad de insulina secretada por el páncreas, (2) aumentan la sensibilidad de los órganos diana a la insulina, (3) disminuyen la velocidad a la que se absorbe la glucosa en el tracto gastrointestinal y (4) aumentan la pérdida de glucosa a través de la orina.
Varias clases de fármacos están indicadas para su uso en la diabetes tipo 2 y, a menudo, se utilizan en combinación. Las combinaciones terapéuticas pueden incluir varias isoformas de insulina o distintas clases de agentes antihiperglucémicos orales. En 2020, la FDA aprobó 23 combinaciones únicas de fármacos antihiperglucémicos . [1] La primera combinación triple de antidiabéticos orales se aprobó en 2019, compuesta por metformina , saxagliptina y dapagliflozina . En 2020 se aprobó otra combinación triple de metformina , linagliptina y empagliflozina. [1]
Los medicamentos para la diabetes tienen cuatro mecanismos de acción principales: [ cita requerida ]
La insulina se administra generalmente por vía subcutánea , ya sea mediante inyecciones o mediante una bomba de insulina . En los entornos de cuidados intensivos, la insulina también puede administrarse por vía intravenosa. Las insulinas se caracterizan típicamente por la velocidad a la que son metabolizadas por el cuerpo, lo que produce diferentes tiempos pico y duraciones de acción. [3] Las insulinas de acción más rápida alcanzan su pico rápidamente y luego se metabolizan, mientras que las insulinas de acción más prolongada tienden a tener tiempos pico más prolongados y permanecen activas en el cuerpo durante períodos más significativos. [4]
Ejemplos de insulinas de acción rápida (pico a la hora aproximadamente) son: [ cita requerida ]
Ejemplos de insulinas de acción corta (pico de 2 a 4 horas) son:
Ejemplos de insulinas de acción intermedia (pico a las 4-10 horas) son:
Ejemplos de insulinas de acción prolongada (duración de 24 horas, a menudo sin pico) son:
La insulina degludec a veces se clasifica por separado como una insulina de acción "ultralarga" debido a su duración de acción de aproximadamente 42 horas, en comparación con las 24 horas de la mayoría de las otras preparaciones de insulina de acción prolongada. [4]
Como una revisión sistemática de estudios que comparaban insulina detemir, insulina glargina, insulina degludec e insulina NPH no mostró ningún beneficio claro o efectos adversos graves para ninguna forma particular de insulina para la hipoglucemia nocturna , hipoglucemia grave, hemoglobina glucosilada A1c, infarto de miocardio no fatal / accidente cerebrovascular , calidad de vida relacionada con la salud o mortalidad por todas las causas . [5] La misma revisión no encontró diferencias en los efectos del uso de estos análogos de insulina entre adultos y niños. [5]
La mayoría de los agentes antidiabéticos orales están contraindicados durante el embarazo, en cuyo caso se prefiere la insulina. [6]
La insulina no se administra por otras vías, aunque se ha estudiado este tema. Se autorizó brevemente una forma inhalada, pero luego se retiró. [7]
Los sensibilizadores de insulina abordan el problema central de la diabetes tipo 2: la resistencia a la insulina .
Las biguanidas reducen la producción hepática de glucosa y aumentan la captación de glucosa por la periferia, incluido el músculo esquelético. Aunque debe utilizarse con precaución en pacientes con deterioro de la función hepática o renal , la metformina , una biguanida, se ha convertido en el agente más utilizado para la diabetes tipo 2 en niños y adolescentes. Entre los fármacos diabéticos comunes, la metformina es el único fármaco oral ampliamente utilizado que no provoca aumento de peso. [8]
La reducción típica de los valores de hemoglobina glucosilada (A1C) para la metformina es del 1,5 al 2,0 %.
La metformina es un medicamento de primera línea que se utiliza para el tratamiento de la diabetes tipo 2. Generalmente se prescribe en el momento del diagnóstico inicial junto con ejercicio y pérdida de peso, a diferencia del pasado, cuando se recetaba después de que la dieta y el ejercicio habían fracasado. Existe una formulación de liberación inmediata y otra de liberación prolongada, que normalmente se reserva para pacientes que experimentan efectos secundarios gastrointestinales . También está disponible en combinación con otros medicamentos orales para la diabetes.
Las tiazolidinedionas ( TZD ), también conocidas como "glitazonas", se unen al receptor activado por el proliferador de peroxisomas ( PPARγ ) , un tipo de proteína reguladora nuclear involucrada en la transcripción de genes que regulan el metabolismo de la glucosa y las grasas. Estos PPAR actúan sobre los elementos sensibles al proliferador de peroxisomas (PPRE). [12] Los PPRE influyen en los genes sensibles a la insulina, que mejoran la producción de ARNm de enzimas dependientes de la insulina. El resultado final es un mejor uso de la glucosa por parte de las células. Estos fármacos también mejoran la actividad del PPAR-α y, por lo tanto, conducen a un aumento de HDL y algunos componentes más grandes de LDL. [13]
Las reducciones típicas en los valores de hemoglobina glucosilada (A1C) son del 1,5 al 2,0 %. Algunos ejemplos son:
Múltiples estudios retrospectivos han generado preocupación sobre la seguridad de la rosiglitazona, aunque se ha establecido que el grupo, en su conjunto, tiene efectos beneficiosos sobre la diabetes. La mayor preocupación es un aumento en el número de eventos cardíacos graves en pacientes que lo toman. El estudio ADOPT mostró que la terapia inicial con medicamentos de este tipo puede prevenir la progresión de la enfermedad, [17] al igual que el ensayo DREAM. [18] La Asociación Estadounidense de Endocrinólogos Clínicos (AACE), que proporciona pautas de práctica clínica para el manejo de la diabetes, mantiene las tiazolidinedionas como agentes recomendados de primera, segunda o tercera línea para la diabetes mellitus tipo 2, a partir de su resumen ejecutivo de 2019, sobre las sulfonilureas y los inhibidores de la α-glucosidasa. Sin embargo, son menos preferidos que los agonistas de GLP-1 o los inhibidores de SGLT2, especialmente en pacientes con enfermedad cardiovascular ( para cuyo tratamiento están aprobados por la FDA liraglutida , empagliflozina y canagliflozina ). [19]
Las preocupaciones sobre la seguridad de la rosiglitazona surgieron cuando se publicó un metaanálisis retrospectivo en el New England Journal of Medicine . [20] Desde entonces ha habido una cantidad significativa de publicaciones, y un panel de la Administración de Alimentos y Medicamentos [21] votó, con cierta controversia, 20:3 que los estudios disponibles "respaldaban una señal de daño", pero votó 22:1 para mantener el medicamento en el mercado. El metaanálisis no fue respaldado por un análisis provisional del ensayo diseñado para evaluar el tema, y varios otros informes no han podido concluir la controversia. Esta evidencia débil de efectos adversos ha reducido el uso de rosiglitazona, a pesar de sus efectos importantes y sostenidos en el control glucémico . [22] Los estudios de seguridad continúan.
Por el contrario, al menos un gran estudio prospectivo, PROactive 05, ha demostrado que la pioglitazona puede disminuir la incidencia general de eventos cardíacos en personas con diabetes tipo 2 que ya han tenido un ataque cardíaco. [23]
Se ha informado que el activador de la cinasa LYN , tolimidona, potencia la señalización de la insulina de una manera distinta a la de las glitazonas. [24] El compuesto ha demostrado resultados positivos en un estudio clínico de fase 2a en el que participaron 130 sujetos diabéticos. [25]
Los secretagogos son medicamentos que aumentan la producción de una glándula, en el caso de la insulina del páncreas .
Las sulfonilureas fueron los primeros medicamentos antihiperglucémicos orales ampliamente utilizados. Son secretagogos de insulina , que desencadenan la liberación de insulina al inhibir el canal K ATP de las células beta pancreáticas . Se han comercializado ocho tipos de estas píldoras en América del Norte, pero no todas siguen estando disponibles. Las sulfonilureas de "segunda generación" son las más utilizadas en la actualidad. Son más eficaces que los medicamentos de primera generación y tienen menos efectos secundarios. Todas pueden provocar aumento de peso.
Las guías de práctica clínica actuales de la AACE clasifican las sulfonilureas (así como las glinidas) por debajo de todas las demás clases de fármacos antidiabéticos en términos de uso sugerido como agentes de primera, segunda o tercera línea; esto incluye bromocriptina , el secuestrador de ácidos biliares colesevelam , inhibidores de la α-glucosidasa , tiazolidinedionas (glitazonas) e inhibidores de DPP-4 (gliptinas). [19] Sin embargo, el bajo costo de la mayoría de las sulfonilureas, especialmente cuando se considera su eficacia significativa en la reducción de la glucosa en sangre, tiende a mantenerlas como una opción más factible en muchos pacientes; ni los inhibidores de SGLT2 ni los agonistas de GLP-1, las clases más favorecidas por las pautas de la AACE después de la metformina, están actualmente disponibles como genéricos.
Las sulfonilureas se unen fuertemente a las proteínas plasmáticas . Las sulfonilureas son útiles sólo en la diabetes tipo 2, ya que actúan estimulando la liberación endógena de insulina. Funcionan mejor en pacientes mayores de 40 años que han tenido diabetes mellitus durante menos de diez años. No se pueden utilizar en la diabetes tipo 1 o la diabetes del embarazo. Se pueden utilizar de forma segura con metformina o glitazonas. El principal efecto secundario es la hipoglucemia , que parece ocurrir con más frecuencia con las sulfonilureas que con otros tratamientos. [26]
Una revisión sistemática Cochrane de 2011 mostró que el tratamiento con Sulfonilureas no mejoró el control de los niveles de glucosa más que la insulina a los 3 ni a los 12 meses de tratamiento. [27] Esta misma revisión de hecho encontró evidencia de que el tratamiento con Sulfonilureas podría conducir a una dependencia de insulina más temprana, con un 30% de los casos requiriendo insulina a los 2 años. [27] Cuando los estudios midieron el péptido C en ayunas , ninguna intervención influyó en su concentración, pero la insulina mantuvo la concentración mejor en comparación con la Sulfonilurea. [27] Aún así, es importante destacar que los estudios disponibles para ser incluidos en esta revisión presentaron fallas considerables en calidad y diseño. [27]
Las reducciones típicas en los valores de hemoglobina glucosilada (A1C) para las sulfonilureas de segunda generación son del 1,0 al 2,0 %.
Las meglitinidas ayudan al páncreas a producir insulina y suelen denominarse "secretagogos de acción corta". Actúan sobre los mismos canales de potasio que las sulfonilureas, pero en un sitio de unión diferente. [28] Al cerrar los canales de potasio de las células beta pancreáticas, abren los canales de calcio, mejorando así la secreción de insulina. [29]
Se toman con las comidas o poco antes para aumentar la respuesta de la insulina a cada comida. Si se saltea una comida, también se saltea el medicamento.
Las reducciones típicas en los valores de hemoglobina glucosilada (A1C) son del 0,5 al 1,0 %.
Las reacciones adversas incluyen aumento de peso e hipoglucemia.
Los inhibidores de la alfa-glucosidasa son una clase de medicamentos para la diabetes, sin embargo, técnicamente no son agentes hipoglucemiantes porque no tienen un efecto directo sobre la secreción o sensibilidad a la insulina. Estos agentes retardan la digestión del almidón en el intestino delgado, de modo que la glucosa del almidón ingresa al torrente sanguíneo a un ritmo más lento y puede ser igualada de manera más efectiva por una respuesta o sensibilidad a la insulina alterada. Estos agentes son efectivos por sí solos solo en las primeras etapas de la intolerancia a la glucosa , pero pueden ser útiles en combinación con otros agentes en la diabetes tipo 2 .
Las reducciones típicas en los valores de hemoglobina glucosilada (A1C) son del 0,5 al 1,0 %.
Estos medicamentos rara vez se utilizan en los Estados Unidos debido a la gravedad de sus efectos secundarios (flatulencia e hinchazón). Se recetan con más frecuencia en Europa. Tienen el potencial de provocar pérdida de peso al reducir la cantidad de azúcar metabolizada.
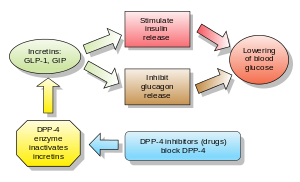
Las incretinas también son secretagogos de insulina . Las dos principales moléculas candidatas que cumplen los criterios para ser una incretina son el péptido similar al glucagón-1 (GLP-1) y el péptido inhibidor gástrico (péptido insulinotrópico dependiente de glucosa, GIP). Tanto el GLP-1 como el GIP son rápidamente inactivados por la enzima dipeptidil peptidasa-4 (DPP-4).
Los agonistas del péptido similar al glucagón (GLP) se unen a un receptor de GLP de membrana. [29] Como consecuencia, aumenta la liberación de insulina de las células beta pancreáticas. El GLP endógeno tiene una vida media de solo unos pocos minutos, por lo que un análogo de GLP no sería práctico. A partir de 2019, la AACE enumera a los agonistas de GLP-1, junto con los inhibidores de SGLT2, como los agentes antidiabéticos más preferidos después de la metformina. La liraglutida en particular puede considerarse de primera línea en pacientes diabéticos con enfermedad cardiovascular, ya que ha recibido la aprobación de la FDA para la reducción del riesgo de eventos cardiovasculares adversos importantes en pacientes con diabetes tipo 2. [19] [30] En una revisión Cochrane de 2011 , los agonistas de GLP-1 mostraron aproximadamente una reducción del 1% en HbA1c en comparación con placebo. [26] Los agonistas de GLP-1 también muestran una mejora de la función de las células beta , pero este efecto no dura después de suspender el tratamiento. [26] Debido a la menor duración de los estudios, esta revisión no permitió evaluar los efectos positivos o negativos a largo plazo. [26]
Estos agentes también pueden causar una disminución de la motilidad gástrica, responsable del efecto secundario común de las náuseas, que tiende a desaparecer con el tiempo. [26]
Los análogos de GLP-1 provocaron pérdida de peso y tuvieron más efectos secundarios gastrointestinales, mientras que en general los inhibidores de la dipeptidil peptidasa-4 (DPP-4) fueron neutros en cuanto al peso y se asociaron con un mayor riesgo de infección y dolor de cabeza. Ambas clases parecen presentar una alternativa a otros fármacos antidiabéticos. Sin embargo, se ha observado aumento de peso y/o hipoglucemia cuando se utilizaron inhibidores de la dipeptidil peptidasa-4 con sulfonilureas; aún se desconocen los efectos sobre la salud a largo plazo y las tasas de morbilidad. [41]
Los inhibidores de DPP-4 aumentan la concentración sanguínea de la incretina GLP-1 al inhibir su degradación por DPP-4.
Algunos ejemplos son:
Los inhibidores de DPP-4 redujeron los valores de hemoglobina A1C en un 0,74%, comparable a otros fármacos antidiabéticos. [42]
Un resultado de un ECA que incluía a 206 pacientes de 65 años o más (HgbA1c basal media de 7,8 %) que recibían 50 o 100 mg/día de sitagliptina demostró reducir la HbA1c en un 0,7 % (resultado combinado de ambas dosis). [43] Un resultado combinado de 5 ECA que incluían a un total de 279 pacientes de 65 años o más (HbA1c basal media de 8 %) que recibían 5 mg/día de saxagliptina demostró reducir la HbA1c en un 0,73 %. [44] Un resultado combinado de 5 ECA que incluían a un total de 238 pacientes de 65 años o más (HbA1c basal media de 8,6 %) que recibían 100 mg/día de vildagliptina demostró reducir la HbA1c en un 1,2 %. [45] Otro conjunto de 6 RCT combinados que incluían alogliptina (aprobados por la FDA en 2013) demostró reducir la HbA1c en un 0,73 % en 455 pacientes de 65 años o más que recibieron 12,5 o 25 mg/día del medicamento. [46]
Los análogos agonistas de amilina retardan el vaciamiento gástrico y suprimen el glucagón . Tienen todas las acciones de las incretinas excepto la estimulación de la secreción de insulina. A partir de 2007 [actualizar], la pramlintida es el único análogo de amilina disponible clínicamente. Al igual que la insulina, se administra por inyección subcutánea . El efecto adverso más frecuente y grave de la pramlintida son las náuseas , que ocurren principalmente al comienzo del tratamiento y se reducen gradualmente. Las reducciones típicas en los valores de A1C son del 0,5 al 1,0%. [47]
Los inhibidores de SGLT2 bloquean las proteínas transportadoras de sodio-glucosa 2 en los túbulos renales de las nefronas en los riñones, la reabsorción de glucosa en los túbulos renales, promoviendo la excreción de glucosa en la orina. Esto causa tanto una pérdida de peso leve como una reducción leve en los niveles de azúcar en sangre con poco riesgo de hipoglucemia. [48] Las preparaciones orales pueden estar disponibles solas o en combinación con otros agentes. [49] Junto con los agonistas de GLP-1, se consideran agentes de segundo o tercer nivel preferidos para diabéticos tipo 2 controlados subóptimamente con metformina sola, según las pautas de práctica clínica más recientes. [19] Debido a que se toman por vía oral, en lugar de inyectarse (como los agonistas de GLP-1), los pacientes que son reacios a las inyecciones pueden preferir estos agentes sobre los primeros. Pueden considerarse de primera línea en pacientes diabéticos con enfermedad cardiovascular, especialmente insuficiencia cardíaca , ya que se ha demostrado que estos medicamentos reducen el riesgo de hospitalización en pacientes con tales comorbilidades. [50] Sin embargo, dado que no están disponibles como medicamentos genéricos, el costo puede limitar su viabilidad para muchos pacientes. Además, hay cada vez más evidencia de que la eficacia y seguridad de esta clase de medicamentos podría depender de la variabilidad genética de los pacientes. [51]
Algunos ejemplos incluyen:
Los efectos secundarios de los inhibidores de SGLT2 se derivan directamente de su mecanismo de acción; estos incluyen un mayor riesgo de: cetoacidosis , infecciones del tracto urinario , vulvovaginitis candidiásica e hipoglucemia . [52]
La siguiente tabla compara algunos agentes antidiabéticos comunes, generalizando las clases, aunque puede haber una variación sustancial en los medicamentos individuales de cada clase. Cuando la tabla hace una comparación como "menor riesgo" o "más conveniente", la comparación se hace con los otros medicamentos de la tabla.
Existen muchos medicamentos antidiabéticos genéricos, entre ellos: [55]
No existen genéricos disponibles para los inhibidores de la dipeptidil peptidasa-4 (Onglyza), las glifozinas, las incretinas y varias combinaciones. La patente de sitagliptina expiró en julio de 2022, lo que llevó al lanzamiento de marcas genéricas de sitagliptina [56] . Esto redujo el costo de la terapia para la diabetes tipo 2 con sitagliptina.
Se ha investigado el efecto de los tratamientos ayurvédicos , sin embargo, debido a fallas metodológicas de estudios e investigaciones relevantes, no ha sido posible sacar conclusiones sobre la eficacia de estos tratamientos y no hay evidencia suficiente para recomendarlos. [57]
{{cite journal}}: CS1 maint: overridden setting (link)