La esclerodermia sistémica, o esclerosis sistémica , es una enfermedad reumática autoinmune caracterizada por la producción y acumulación excesiva de colágeno , llamada fibrosis , en la piel y los órganos internos y por lesiones en las arterias pequeñas . Hay dos subgrupos principales de esclerosis sistémica según el grado de afectación de la piel: limitada y difusa. La forma limitada afecta las áreas debajo, pero no por encima, de los codos y las rodillas con o sin afectación de la cara. La forma difusa también afecta la piel por encima de los codos y las rodillas y también puede extenderse al torso . Los órganos viscerales , incluidos los riñones , el corazón , los pulmones y el tracto gastrointestinal también pueden verse afectados por el proceso fibrótico. El pronóstico está determinado por la forma de la enfermedad y el grado de afectación visceral. Los pacientes con esclerosis sistémica limitada tienen un mejor pronóstico que aquellos con la forma difusa. La muerte es causada con mayor frecuencia por la afectación de los pulmones, el corazón y los riñones. El riesgo de cáncer aumenta ligeramente. [1]
Las tasas de supervivencia han aumentado considerablemente gracias al tratamiento eficaz de la insuficiencia renal . Las terapias incluyen fármacos inmunosupresores y, en algunos casos, glucocorticoides . [2]
La calcinosis , el fenómeno de Raynaud , la disfunción esofágica , la esclerodactilia y la telangiectasia ( síndrome CREST ) se asocian con esclerodermia limitada. Otros síntomas incluyen:

.jpg/440px-Riehl_Zumbusch_Tafel_LXVIII_(1).jpg)
En la piel, la esclerosis sistémica provoca endurecimiento y cicatrización. La piel puede verse tirante, enrojecida o escamosa. Los vasos sanguíneos también pueden ser más visibles. Cuando se ven afectadas áreas extensas, la pérdida de grasa y músculo puede debilitar las extremidades y afectar la apariencia. Los pacientes refieren picazón intensa y recurrente en áreas extensas de la piel. La gravedad de estos síntomas varía mucho entre pacientes: algunos tienen esclerodermia en solo un área limitada de la piel (como los dedos) y poca afectación del tejido subyacente, mientras que otros tienen una afectación progresiva de la piel. [3] Las úlceras digitales (heridas abiertas, especialmente en las puntas de los dedos y, con menos frecuencia, en los nudillos) no son infrecuentes. [4]
La esclerodermia difusa puede causar complicaciones musculoesqueléticas , pulmonares, gastrointestinales, renales y otras. [5] Los pacientes con mayor afectación cutánea tienen más probabilidades de tener afectación de los tejidos y órganos internos. La mayoría de los pacientes (más del 80%) tienen síntomas vasculares y fenómeno de Raynaud, que conduce a ataques de decoloración de las manos y los pies en respuesta al frío. El fenómeno de Raynaud normalmente afecta los dedos de las manos y los pies. La esclerodermia sistémica y el fenómeno de Raynaud pueden causar úlceras dolorosas en los dedos de las manos o los pies, que se conocen como úlceras digitales. La calcinosis (depósito de calcio en bultos debajo de la piel) también es común en la esclerodermia sistémica, y a menudo se observa cerca de los codos, las rodillas u otras articulaciones . [6]
Los primeros síntomas articulares que presentan los pacientes con esclerodermia son típicamente dolores articulares inespecíficos , que pueden derivar en artritis , o causar molestias en tendones o músculos . [5] La movilidad articular, especialmente de las pequeñas articulaciones de la mano, puede verse restringida por calcinosis o engrosamiento de la piel. [7] Los pacientes pueden desarrollar debilidad muscular, o miopatía , ya sea por la enfermedad o por sus tratamientos. [8]
En casi todos los pacientes con esclerodermia difusa, se observa algún deterioro de la función pulmonar en las pruebas de función pulmonar [9] , pero no necesariamente causa síntomas, como dificultad para respirar. Algunos pacientes pueden desarrollar hipertensión pulmonar o elevación de la presión de las arterias pulmonares . Esto puede ser progresivo y puede provocar insuficiencia cardíaca derecha . La manifestación más temprana de esto puede ser una disminución de la capacidad de difusión en las pruebas de función pulmonar. [ cita requerida ] Otras complicaciones pulmonares en la enfermedad más avanzada incluyen neumonía por aspiración , hemorragia pulmonar y neumotórax . [5]

La esclerodermia difusa puede afectar cualquier parte del tracto gastrointestinal. [10] La manifestación más común en el esófago es la esofagitis por reflujo , que puede complicarse con estenosis esofágicas o estrechamiento benigno del esófago. [11] Esto se trata mejor inicialmente con inhibidores de la bomba de protones para la supresión de ácido, [12] pero puede requerir dilatación con bujía en caso de estenosis. [10]
La esclerodermia puede disminuir la motilidad en cualquier parte del tracto gastrointestinal. [10] La fuente más común de disminución de la motilidad es el esófago y el esfínter esofágico inferior, lo que provoca disfagia y dolor en el pecho. A medida que progresa la esclerodermia, la afectación esofágica por anomalías en la disminución de la motilidad puede empeorar debido a la fibrosis progresiva (cicatrización). Si esto no se trata, el ácido del estómago puede retroceder al esófago, causando esofagitis y enfermedad por reflujo gastroesofágico . La formación de cicatrices adicionales por daño ácido en el esófago inferior muchas veces conduce al desarrollo de estrechamiento fibrótico, también conocido como estenosis, que puede tratarse mediante dilatación [ cita requerida ] .
En pacientes con trastornos neuromusculares, en particular esclerosis sistémica progresiva y miopatía visceral, el duodeno se ve frecuentemente afectado. Puede producirse dilatación, que suele ser más pronunciada en la segunda, tercera y cuarta porción. El duodeno dilatado puede tardar en vaciarse y el órgano atónico, muy dilatado, puede producir un efecto de sumidero. [ cita requerida ]
El intestino delgado también puede verse afectado, lo que provoca un sobrecrecimiento bacteriano y una mala absorción de sales biliares , grasas , carbohidratos , proteínas y vitaminas . El colon puede verse afectado y causar pseudoobstrucción o colitis isquémica . [5]
Las complicaciones más raras incluyen neumatosis quística intestinal (bolsas de gas en la pared intestinal), divertículos de boca ancha en el colon y el esófago y fibrosis hepática . Los pacientes con afectación gastrointestinal grave pueden presentar desnutrición profunda . [11]
La esclerodermia también puede estar asociada con ectasia vascular antral gástrica , también conocida como "estómago de sandía". Se trata de una afección en la que proliferan vasos sanguíneos atípicos, generalmente en un patrón radialmente simétrico alrededor del píloro del estómago. Puede ser una causa de hemorragia gastrointestinal superior o anemia por deficiencia de hierro en pacientes con esclerodermia. [11]

La afectación renal en la esclerodermia se considera un factor de mal pronóstico y frecuentemente causa de muerte. [13]
La complicación clínica más importante de la esclerodermia que afecta al riñón es la crisis renal esclerodérmica (CRS), cuyos síntomas son hipertensión maligna (presión arterial alta con evidencia de daño orgánico agudo), hiperreninemia (niveles elevados de renina), azotemia (insuficiencia renal con acumulación de productos de desecho en la sangre) y anemia hemolítica microangiopática (destrucción de glóbulos rojos). [14] Además de la presión arterial alta, la hematuria (sangre en la orina) y la proteinuria (pérdida de proteínas en la orina) pueden ser indicativas de CRS. [15]
En el pasado, la esclerosis múltiple recurrente era casi uniformemente mortal. [16] Aunque los resultados han mejorado significativamente con el uso de inhibidores de la ECA , [17] [18] el pronóstico es a menudo reservado, ya que un número significativo de pacientes son refractarios al tratamiento y desarrollan insuficiencia renal . Alrededor del 7-9% de todos los pacientes con esclerodermia cutánea difusa desarrollan una crisis renal en algún momento del curso de su enfermedad. [19] [20] Los pacientes que tienen una rápida afectación de la piel tienen el mayor riesgo de complicaciones renales. [21] Es más común en la esclerodermia cutánea difusa y a menudo se asocia con anticuerpos contra la ARN polimerasa (en el 59% de los casos). Muchos proceden a diálisis, aunque esta se puede detener en tres años en aproximadamente un tercio de los casos. Una mayor edad y (paradójicamente) una presión arterial más baja en la presentación hacen que sea más probable que se necesite diálisis. [22]
Los tratamientos para la esclerosis múltiple recurrente incluyen inhibidores de la ECA. Actualmente no se recomienda el uso profiláctico de inhibidores de la ECA, ya que datos recientes sugieren un peor pronóstico en pacientes tratados con estos fármacos antes del desarrollo de una crisis renal. [23] [ ¿ Fuente médica poco confiable? ] Se sabe que los riñones trasplantados se ven afectados por la esclerodermia, y se cree que los pacientes con enfermedad renal de inicio temprano (dentro del año del diagnóstico de esclerodermia) tienen el mayor riesgo de recurrencia. [24]
No se ha identificado una causa clara para la esclerodermia y la esclerosis sistémica. La predisposición genética parece ser limitada, ya que la concordancia genética es pequeña; aun así, a menudo se observa una predisposición familiar para la enfermedad autoinmune. Los polimorfismos en COL1A2 y TGF-β1 pueden influir en la gravedad y el desarrollo de la enfermedad. La evidencia que implica al citomegalovirus (CMV) como el epítopo original de la reacción inmunitaria es limitada, al igual que el parvovirus B19. [25] Los disolventes orgánicos y otros agentes químicos se han relacionado con la esclerodermia. [26]
Uno de los mecanismos sospechosos detrás del fenómeno autoinmune es la existencia de microquimerismo , es decir, células fetales que circulan en la sangre materna, desencadenando una reacción inmune a lo que se percibe como material extraño. [26] [27]
En pacientes con insuficiencia renal crónica puede desarrollarse una forma distinta de esclerodermia y esclerosis sistémica . Esta forma, la dermopatía fibrosante nefrogénica o fibrosis sistémica nefrogénica, [28] [29] [30] [31] se ha relacionado con la exposición a medios de contraste radiológico que contienen gadolinio . [32]
La bleomicina [33] (un agente quimioterapéutico) y posiblemente la quimioterapia con taxanos [34] pueden causar esclerodermia, y la exposición ocupacional a solventes se ha vinculado con un mayor riesgo de esclerosis sistémica. [35]
Se cree que la sobreproducción de colágeno es resultado de una disfunción autoinmune, en la que el sistema inmunitario comienza a atacar el cinetocoro de los cromosomas. Esto provocaría un mal funcionamiento genético de los genes cercanos. Las células T se acumulan en la piel; se cree que secretan citocinas y otras proteínas que estimulan la deposición de colágeno. La estimulación de los fibroblastos , en particular, parece ser crucial para el proceso de la enfermedad, y los estudios han convergido en los posibles factores que producen este efecto. [26]
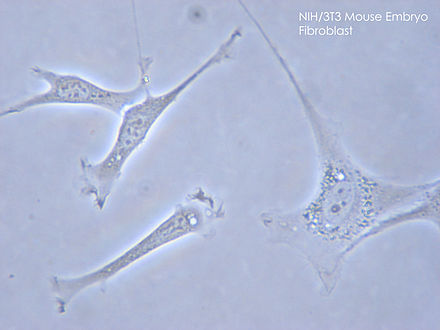
Un factor importante en el proceso es el factor de crecimiento transformante (TGFβ). Esta proteína parece producirse en exceso, y el fibroblasto (posiblemente en respuesta a otros estímulos) también sobreexpresa el receptor para este mediador. Una vía intracelular (que consiste en SMAD2 / SMAD3 , SMAD4 y el inhibidor SMAD7 ) es responsable del sistema de mensajero secundario que induce la transcripción de las proteínas y enzimas responsables de la deposición de colágeno. Sp1 es un factor de transcripción estudiado más de cerca en este contexto. Aparte de TGFβ, el factor de crecimiento del tejido conectivo (CTGF) tiene un posible papel. [26] De hecho, un polimorfismo común del gen CTGF está presente en un nivel aumentado en la esclerosis sistémica. [36]
El daño endotelial es una anomalía temprana en el desarrollo de la esclerodermia y también parece deberse a la acumulación de colágeno por los fibroblastos, aunque también se han implicado alteraciones directas por citocinas, adhesión plaquetaria y una reacción de hipersensibilidad de tipo II. Se ha documentado un aumento de la endotelina y una disminución de la vasodilatación . [26]
Jiménez y Derk [26] describen tres teorías sobre el desarrollo de la esclerodermia:
En 1980, el Colegio Americano de Reumatología acordó los criterios de diagnóstico para la esclerodermia. [37]
El diagnóstico se realiza por sospecha clínica, presencia de autoanticuerpos (específicamente anticentrómero y anti-scl70/antitopoisomerasa) y ocasionalmente por biopsia. De los anticuerpos, el 90% tiene un anticuerpo antinuclear detectable . El anticuerpo anticentrómero es más común en la forma limitada (80-90%) que en la forma difusa (10%), y el anti-scl70 es más común en la forma difusa (30-40%) y en pacientes afroamericanos (que son más susceptibles a la forma sistémica). [26]
Otras enfermedades pueden imitar la esclerosis sistémica al causar endurecimiento de la piel. Los indicios diagnósticos de que otro trastorno es responsable incluyen la ausencia del fenómeno de Raynaud, la falta de anomalías en la piel de las manos, la falta de afectación de órganos internos y un resultado normal en la prueba de anticuerpos antinucleares. [38]
No se conoce ninguna cura para la esclerodermia, aunque existen tratamientos para algunos de los síntomas, incluidos medicamentos que suavizan la piel y reducen la inflamación. Algunos pacientes pueden beneficiarse de la exposición al calor. [39] La atención holística de los pacientes que comprende la educación del paciente adaptada a su nivel educativo es útil en vista de la naturaleza compleja de los síntomas y la evolución de la enfermedad. [40]
El tratamiento tópico para los cambios cutáneos de la esclerodermia no altera el curso de la enfermedad, pero puede mejorar el dolor y la ulceración. Se puede utilizar una variedad de fármacos antiinflamatorios no esteroides , como el naproxeno , para aliviar los síntomas dolorosos. [ cita requerida ] El beneficio de los esteroides como la prednisona es limitado. [ cita requerida ] Los episodios del fenómeno de Raynaud a veces responden a la nifedipina u otros bloqueadores de los canales de calcio; la ulceración digital grave puede responder al análogo de la prostaciclina iloprost , y el antagonista dual del receptor de endotelina bosentán puede ser beneficioso para el fenómeno de Raynaud. [41] La tirantez de la piel se puede tratar sistémicamente con metotrexato y ciclosporina . [41] y el grosor de la piel se puede tratar con penicilamina.
La crisis renal esclerodérmica (CRS) es una complicación potencialmente mortal de la esclerosis sistémica que puede ser la manifestación inicial de la enfermedad. La lesión vascular renal (debida en parte a la deposición de colágeno) conduce a isquemia renal, que da como resultado la activación del sistema renina-angiotensina-aldosterona (SRAA). Esto aumenta la presión arterial y daña aún más la vasculatura renal, lo que causa un círculo vicioso de empeoramiento de la hipertensión y disfunción renal (p. ej., creatinina elevada, edema). La emergencia hipertensiva con disfunción de órganos diana (p. ej., encefalopatía, hemorragia retiniana) es común. Se pueden observar trombocitopenia y anemia hemolítica microangiopática. El análisis de orina suele ser normal, pero puede mostrar proteinuria leve, como en este paciente; los cilindros son inesperados. [ cita requerida ]
El pilar del tratamiento del SRC son los inhibidores de la ECA, que reducen la actividad del SRAA y mejoran la función renal y la presión arterial. Se utilizan inhibidores de la ECA de acción corta (normalmente captopril) porque se pueden aumentar rápidamente las dosis. Un nivel elevado de creatinina sérica no es una contraindicación para los inhibidores de la ECA en esta población, y es habitual que se produzcan elevaciones leves de la creatinina durante el inicio del tratamiento con el fármaco.
La crisis renal esclerodérmica, la aparición de lesión renal aguda y la hipertensión maligna (presión arterial muy alta con evidencia de daño orgánico) en personas con esclerodermia se tratan eficazmente con medicamentos de la clase de los inhibidores de la ECA. El beneficio de los inhibidores de la ECA se extiende incluso a aquellos que tienen que comenzar la diálisis para tratar su enfermedad renal y puede proporcionar un beneficio suficiente para permitir la interrupción de la terapia de reemplazo renal. [41]
La alveolitis activa suele tratarse con pulsos de ciclofosfamida , a menudo junto con una pequeña dosis de esteroides. El beneficio de esta intervención es modesto. [42] [43]
La hipertensión pulmonar se puede tratar con epoprostenol , treprostinil , bosentán y posiblemente iloprost aerolizado. [41] El uso de nintedanib fue aprobado en la Administración de Alimentos y Medicamentos de los Estados Unidos el 6 de septiembre de 2019 para reducir la tasa de disminución de la función pulmonar en pacientes con enfermedad pulmonar intersticial asociada a esclerosis sistémica (ES-EIP). [44] [45]
Algunas evidencias indican que la plasmaféresis (intercambio de plasma terapéutico) puede utilizarse para tratar la forma sistémica de la esclerodermia. En Italia, es una opción de tratamiento aprobada por el gobierno. Esto se hace reemplazando el plasma sanguíneo con un líquido que consiste en albúmina y se cree que mantiene a raya la enfermedad al reducir la circulación de autoanticuerpos de la esclerodermia. [46]
La esclerodermia sistémica es una enfermedad poco frecuente , con una incidencia anual que varía en diferentes poblaciones. Las estimaciones de incidencia (casos nuevos por millón de personas) varían de 3,7 a 43 en el Reino Unido y Europa, 7,2 en Japón, 10,9 en Taiwán, 12,0 a 22,8 en Australia, 13,9 a 21,0 en los Estados Unidos y 21,2 en Buenos Aires. [47] El intervalo de aparición máxima comienza a los 30 años [48] y termina a los 50 años. [48]
A nivel mundial, las estimaciones de prevalencia varían de 31,0 a 658,6 personas afectadas por millón. [47] La esclerosis sistémica tiene una proporción de mujeres:hombres de 3:1 (8:1 en los años fértiles medios y tardíos). La incidencia es el doble entre los afroamericanos. Los nativos americanos choctaw de pura sangre en Oklahoma tienen la prevalencia más alta del mundo (469 por 100.000). [49]
La enfermedad tiene cierta relación hereditaria. También puede ser causada por una reacción inmunitaria a un virus ( mimetismo molecular ) o por toxinas. [2]
La Red de Esclerodermia Juvenil es una organización dedicada a brindar apoyo emocional e información educativa a los padres y sus hijos que viven con esclerodermia juvenil, apoyar la investigación pediátrica para identificar la causa y la cura de la esclerodermia juvenil y mejorar la conciencia pública. [50]
En los EE. UU., la Fundación Esclerodermia se dedica a generar conciencia sobre la enfermedad y ayudar a quienes la padecen. [51]
La Fundación para la Investigación de la Esclerodermia patrocina la investigación sobre esta enfermedad. [52] El comediante y presentador de televisión Bob Saget , miembro de la junta directiva de la SRF, dirigió la película para televisión de ABC de 1996 For Hope , protagonizada por Dana Delany , que retrata a una joven fatalmente afectada por la esclerodermia; la película se basó en las experiencias de la hermana de Saget, Gay. [53]
Scleroderma and Raynaud's UK es una organización benéfica británica formada por la fusión de dos organizaciones más pequeñas en 2016 para brindar apoyo a personas con esclerodermia y financiar investigaciones sobre la enfermedad. [54] [55]
Un estudio de 2018 estimó las tasas de supervivencia a 10 años en un 88 %, sin diferenciación según el subtipo. La esclerosis sistémica difusa, las complicaciones en los órganos internos y la edad avanzada en el momento del diagnóstico se asocian con peores pronósticos. [56]
Dada la dificultad de tratar la esclerodermia, a menudo se intentan tratamientos con una base de evidencia menor para controlar la enfermedad. Entre ellos se encuentran la globulina antitimocítica y el micofenolato de mofetilo ; algunos informes han demostrado mejoras en los síntomas cutáneos, así como un retraso en el progreso de la enfermedad sistémica, pero ninguno de ellos ha sido sometido a ensayos clínicos a gran escala. [41]
El trasplante autólogo de células madre hematopoyéticas (TCMH) se basa en la suposición de que las enfermedades autoinmunes como la esclerosis sistémica se producen cuando los glóbulos blancos del sistema inmunitario atacan al cuerpo. En este tratamiento, se extraen células madre de la sangre del paciente y se almacenan para preservarlas. Los glóbulos blancos del paciente se destruyen con ciclofosfamida y anticuerpos de conejo contra los glóbulos blancos. Luego, la sangre almacenada se devuelve al torrente sanguíneo del paciente para reconstituir una sangre y un sistema inmunitario sanos que no ataquen al cuerpo. Los resultados de un ensayo de fase III, el ensayo Autologous Stem Cell Transplantation International Scleroderma (ASTIS), con 156 pacientes, se publicaron en 2014. El propio TPH tiene una alta mortalidad por tratamiento, por lo que en el primer año, la supervivencia de los pacientes en el grupo de tratamiento fue menor que la del grupo placebo, pero al final de los 10 años, la supervivencia en el grupo de tratamiento fue significativamente mayor. Los autores concluyeron que el TPH podría ser eficaz si se limita a pacientes que estuvieran lo suficientemente sanos como para sobrevivir al propio TPH. Por lo tanto, el TPH debería administrarse en las primeras fases de la progresión de la enfermedad, antes de que produzca daños. Los pacientes con cardiopatías y los fumadores tenían menos probabilidades de sobrevivir. [57] [58] Otro ensayo, el ensayo de trasplante de células madre frente a ciclofosfamida (SCOT), está en curso. [59]
El asengeprast es un fármaco experimental para la esclerodermia sistémica. Es un inhibidor de moléculas pequeñas del receptor acoplado a proteína G GPR68 con actividad antifibrótica.