La epidemiología es el estudio y análisis de la distribución (quién, cuándo y dónde), patrones y determinantes de las condiciones de salud y enfermedad en una población definida .
La epidemiología es una piedra angular de la salud pública y da forma a las decisiones políticas y a la práctica basada en la evidencia al identificar los factores de riesgo de las enfermedades y los objetivos de la atención sanitaria preventiva . Los epidemiólogos ayudan con el diseño de estudios, la recopilación y el análisis estadístico de los datos, modifican la interpretación y la difusión de los resultados (incluida la revisión por pares y la revisión sistemática ocasional ). La epidemiología ha ayudado a desarrollar la metodología utilizada en la investigación clínica , los estudios de salud pública y, en menor medida, la investigación básica en las ciencias biológicas. [1]
Las principales áreas de estudio epidemiológico incluyen la causalidad de las enfermedades, la transmisión , la investigación de brotes , la vigilancia de enfermedades , la epidemiología ambiental , la epidemiología forense , la epidemiología ocupacional , la detección , la biomonitorización y las comparaciones de los efectos del tratamiento, como en los ensayos clínicos . Los epidemiólogos se basan en otras disciplinas científicas como la biología para comprender mejor los procesos de las enfermedades, las estadísticas para hacer un uso eficiente de los datos y extraer conclusiones apropiadas, las ciencias sociales para comprender mejor las causas próximas y distales, y la ingeniería para la evaluación de la exposición .
Epidemiología , que literalmente significa "el estudio de lo que está sobre las personas", se deriva del griego epi "sobre, entre", demos "pueblo, distrito" y logos "estudio, palabra, discurso", lo que sugiere que se aplica solo a las poblaciones humanas. Sin embargo, el término se usa ampliamente en estudios de poblaciones zoológicas (epidemiología veterinaria), aunque el término " epizoología " está disponible, y también se ha aplicado a estudios de poblaciones de plantas ( epidemiología botánica o de enfermedades de las plantas ). [2]
La distinción entre "epidemia" y "endemia" fue establecida por primera vez por Hipócrates , [3] para distinguir entre enfermedades que "se propagan" en una población (epidemia) de aquellas que "residen dentro" de una población (endemia). [4] El término "epidemiología" parece haber sido utilizado por primera vez para describir el estudio de las epidemias en 1802 por el médico español Joaquín de Villalba en Epidemiología Española . [4] Los epidemiólogos también estudian la interacción de las enfermedades en una población, una condición conocida como sindemia .
El término epidemiología se aplica ahora ampliamente para cubrir la descripción y la causalidad no solo de enfermedades infecciosas y epidémicas, sino de enfermedades en general, incluidas las afecciones relacionadas. Algunos ejemplos de temas examinados a través de la epidemiología incluyen la presión arterial alta, las enfermedades mentales y la obesidad . Por lo tanto, esta epidemiología se basa en cómo el patrón de la enfermedad provoca cambios en el funcionamiento de los seres humanos.
El médico griego Hipócrates , enseñado por Demócrito, fue conocido como el padre de la medicina , [5] [6] buscó una lógica para la enfermedad; es la primera persona conocida que examinó las relaciones entre la aparición de enfermedades y las influencias ambientales. [7] Hipócrates creía que la enfermedad del cuerpo humano era causada por un desequilibrio de los cuatro humores (bilis negra, bilis amarilla, sangre y flema). La cura para la enfermedad era eliminar o agregar el humor en cuestión para equilibrar el cuerpo. Esta creencia condujo a la aplicación de sangrías y dietas en medicina. [8] Acuñó los términos endémico (para enfermedades que generalmente se encuentran en algunos lugares pero no en otros) y epidémico (para enfermedades que se ven en algunos momentos pero no en otros). [9]
A mediados del siglo XVI, un médico de Verona llamado Girolamo Fracastoro fue el primero en proponer una teoría según la cual las partículas diminutas e invisibles que causan enfermedades estaban vivas. Se consideraba que podían propagarse por el aire, multiplicarse por sí mismas y ser destruibles por el fuego. De esta manera refutó la teoría de Galeno sobre los miasmas (gases venenosos en personas enfermas). En 1543 escribió un libro De contagione et contagiosis morbis , en el que fue el primero en promover la higiene personal y ambiental para prevenir enfermedades. El desarrollo de un microscopio suficientemente potente por Antonie van Leeuwenhoek en 1675 proporcionó evidencia visual de partículas vivas consistentes con una teoría de los gérmenes de la enfermedad . [ cita requerida ]
Durante la dinastía Ming , Wu Youke (1582-1652) desarrolló la idea de que algunas enfermedades eran causadas por agentes transmisibles, a los que llamó Li Qi (戾气 o factores pestilentes) cuando observó varias epidemias que asolaban su entorno entre 1641 y 1644. [10] Su libro Wen Yi Lun (瘟疫论, Tratado sobre la peste/Tratado de enfermedades epidémicas) puede considerarse como el principal trabajo etiológico que presentó el concepto. [11] Sus conceptos todavía se estaban considerando al analizar el brote de SARS por parte de la OMS en 2004 en el contexto de la medicina tradicional china. [12]
Otro pionero, Thomas Sydenham (1624-1689), fue el primero en distinguir las fiebres de los londinenses a finales del siglo XVII. Sus teorías sobre la cura de las fiebres se encontraron con mucha resistencia por parte de los médicos tradicionales de la época. No pudo encontrar la causa inicial de la fiebre de viruela que investigó y trató. [8]
John Graunt , un mercero y estadístico aficionado, publicó Natural and Political Observations... upon the Bills of Mortality en 1662. En él, analizó los registros de mortalidad en Londres antes de la Gran Peste , presentó una de las primeras tablas de mortalidad e informó sobre las tendencias temporales de muchas enfermedades, nuevas y antiguas. Aportó pruebas estadísticas para muchas teorías sobre las enfermedades y también refutó algunas ideas generalizadas sobre ellas. [ cita requerida ]
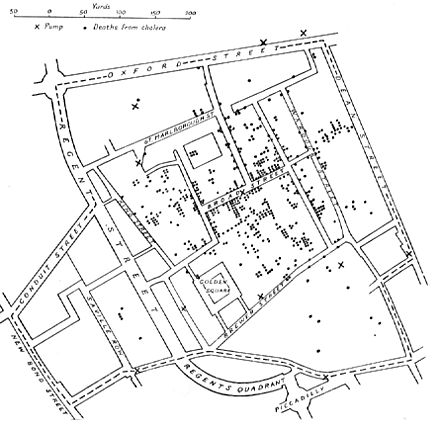
John Snow es famoso por sus investigaciones sobre las causas de las epidemias de cólera del siglo XIX , y también es conocido como el padre de la epidemiología (moderna). [13] [14] Comenzó notando las tasas de mortalidad significativamente más altas en dos áreas abastecidas por Southwark Company. Su identificación de la bomba de Broad Street como la causa de la epidemia de Soho se considera el ejemplo clásico de epidemiología. Snow usó cloro en un intento de limpiar el agua y quitó la manija; esto puso fin al brote. Esto ha sido percibido como un evento importante en la historia de la salud pública y considerado como el evento fundador de la ciencia de la epidemiología, habiendo ayudado a dar forma a las políticas de salud pública en todo el mundo. [15] [16] Sin embargo, la investigación de Snow y las medidas preventivas para evitar más brotes no fueron completamente aceptadas o puestas en práctica hasta después de su muerte debido a la teoría del miasma predominante en la época, un modelo de enfermedad en el que se culpaba a la mala calidad del aire por la enfermedad. Esto se utilizó para racionalizar las altas tasas de infección en áreas empobrecidas en lugar de abordar los problemas subyacentes de mala nutrición y saneamiento, y su trabajo demostró que era falso. [17]
Otros pioneros fueron el médico danés Peter Anton Schleisner, quien en 1849 relató su trabajo sobre la prevención de la epidemia de tétanos neonatal en las islas Vestmanna en Islandia . [18] [19] Otro pionero importante fue el médico húngaro Ignaz Semmelweis , quien en 1847 redujo la mortalidad infantil en un hospital de Viena al instituir un procedimiento de desinfección. Sus hallazgos se publicaron en 1850, pero su trabajo fue mal recibido por sus colegas, quienes interrumpieron el procedimiento. La desinfección no se volvió una práctica generalizada hasta que el cirujano británico Joseph Lister "descubrió" los antisépticos en 1865 a la luz del trabajo de Louis Pasteur . [ cita requerida ]
A principios del siglo XX, Ronald Ross , Janet Lane-Claypon , Anderson Gray McKendrick y otros introdujeron métodos matemáticos en la epidemiología . [20] [21] [22] [23] En un desarrollo paralelo durante la década de 1920, el patólogo germano-suizo Max Askanazy y otros fundaron la Sociedad Internacional de Patología Geográfica para investigar sistemáticamente la patología geográfica del cáncer y otras enfermedades no infecciosas en poblaciones de diferentes regiones. Después de la Segunda Guerra Mundial, Richard Doll y otros no patólogos se unieron al campo y avanzaron métodos para estudiar el cáncer, una enfermedad con patrones y modos de ocurrencia que no podían estudiarse adecuadamente con los métodos desarrollados para epidemias de enfermedades infecciosas. La patología geográfica eventualmente se combinó con la epidemiología de enfermedades infecciosas para formar el campo que es la epidemiología hoy. [24]
Otro gran avance fue la publicación en 1954 de los resultados de un estudio de médicos británicos , dirigido por Richard Doll y Austin Bradford Hill , que brindó un apoyo estadístico muy sólido al vínculo entre el tabaquismo y el cáncer de pulmón . [ cita requerida ]
A finales del siglo XX, con el avance de las ciencias biomédicas, se identificaron varios marcadores moleculares en la sangre, otros bioespecímenes y el medio ambiente como predictores del desarrollo o riesgo de una determinada enfermedad. La investigación epidemiológica para examinar la relación entre estos biomarcadores analizados a nivel molecular y la enfermedad se denominó en términos generales " epidemiología molecular ". En concreto, se ha utilizado la " epidemiología genética " para la epidemiología de la variación genética de la línea germinal y la enfermedad. La variación genética se determina normalmente utilizando ADN de leucocitos de sangre periférica. [ cita requerida ]
Desde la década de 2000, se han realizado comúnmente estudios de asociación del genoma completo (GWAS) para identificar factores de riesgo genéticos para muchas enfermedades y problemas de salud. [25]
Aunque la mayoría de los estudios de epidemiología molecular siguen utilizando sistemas convencionales de diagnóstico y clasificación de enfermedades, cada vez se reconoce más que la progresión de la enfermedad representa procesos inherentemente heterogéneos que difieren de persona a persona. Conceptualmente, cada individuo tiene un proceso de enfermedad único diferente de cualquier otro individuo ("el principio de enfermedad única"), [26] [27] considerando la singularidad del exposoma (una totalidad de exposiciones endógenas y exógenas / ambientales) y su influencia única en el proceso patológico molecular en cada individuo. Los estudios para examinar la relación entre una exposición y la firma patológica molecular de la enfermedad (particularmente el cáncer ) se volvieron cada vez más comunes a lo largo de la década de 2000. Sin embargo, el uso de la patología molecular en epidemiología planteó desafíos únicos, incluida la falta de pautas de investigación y metodologías estadísticas estandarizadas , y la escasez de expertos interdisciplinarios y programas de capacitación. [28] Además, el concepto de heterogeneidad de la enfermedad parece entrar en conflicto con la premisa de larga data en epidemiología de que los individuos con el mismo nombre de enfermedad tienen etiologías y procesos patológicos similares. Para resolver estos problemas y hacer avanzar la ciencia de la salud poblacional en la era de la medicina molecular de precisión , se integraron la "patología molecular" y la "epidemiología" para crear un nuevo campo interdisciplinario de " epidemiología patológica molecular " (MPE), [29] [30] definida como "epidemiología de la patología molecular y heterogeneidad de la enfermedad". En la MPE, los investigadores analizan las relaciones entre (A) factores ambientales, dietéticos, de estilo de vida y genéticos; (B) alteraciones en moléculas celulares o extracelulares; y (C) evolución y progresión de la enfermedad. Una mejor comprensión de la heterogeneidad de la patogénesis de la enfermedad contribuirá aún más a dilucidar las etiologías de la enfermedad. El enfoque de la MPE se puede aplicar no solo a las enfermedades neoplásicas sino también a las enfermedades no neoplásicas. [31] El concepto y paradigma de la MPE se han generalizado en la década de 2010. [32] [33] [34] [35] [36] [37] [38] [ citas excesivas ]
En 2012, se reconoció que la evolución de muchos patógenos es lo suficientemente rápida como para ser muy relevante para la epidemiología y que, por lo tanto, se podría obtener mucho de un enfoque interdisciplinario de las enfermedades infecciosas que integre la epidemiología y la evolución molecular para "informar sobre las estrategias de control o incluso el tratamiento de los pacientes". [39] [40] Los estudios epidemiológicos modernos pueden utilizar estadísticas avanzadas y aprendizaje automático para crear modelos predictivos , así como para definir los efectos del tratamiento. [41] [42] Cada vez se reconoce más que se puede utilizar una amplia gama de fuentes de datos modernas, muchas de las cuales no se originan en la atención médica o la epidemiología, para el estudio epidemiológico. Dicha epidemiología digital puede incluir datos de búsquedas en Internet, registros de teléfonos móviles y ventas minoristas de medicamentos. [ cita requerida ]

Los epidemiólogos emplean una variedad de diseños de estudio, desde el observacional hasta el experimental, y generalmente se clasifican como descriptivos (que implican la evaluación de datos que cubren tiempo, lugar y persona), analíticos (que apuntan a examinar más a fondo las asociaciones conocidas o las relaciones hipotéticas) y experimentales (un término que a menudo se equipara con los ensayos clínicos o comunitarios de tratamientos y otras intervenciones). En los estudios observacionales, se permite que la naturaleza "siga su curso", mientras los epidemiólogos observan desde la barrera. Por el contrario, en los estudios experimentales, el epidemiólogo es quien controla todos los factores que entran en un determinado estudio de caso. [43] Los estudios epidemiológicos tienen como objetivo, cuando sea posible, revelar relaciones imparciales entre exposiciones como el alcohol o el tabaquismo, los agentes biológicos , el estrés o los productos químicos con la mortalidad o la morbilidad . La identificación de relaciones causales entre estas exposiciones y los resultados es un aspecto importante de la epidemiología. Los epidemiólogos modernos utilizan la informática y la infodemiología [44] [45] como herramientas. [ cita requerida ] [46] [47] [48]
Los estudios observacionales tienen dos componentes, descriptivos y analíticos. Las observaciones descriptivas se refieren al "quién, qué, dónde y cuándo se produce un estado de salud". Sin embargo, las observaciones analíticas se ocupan más del "cómo" de un evento relacionado con la salud. [43] La epidemiología experimental contiene tres tipos de casos: ensayos controlados aleatorios (que se utilizan a menudo para un nuevo medicamento o prueba de fármacos), ensayos de campo (realizados en personas con un alto riesgo de contraer una enfermedad) y ensayos comunitarios (investigación sobre enfermedades de origen social). [43]
El término "tríada epidemiológica" se utiliza para describir la intersección del huésped , el agente y el entorno al analizar un brote. [49]
Las series de casos pueden referirse al estudio cualitativo de la experiencia de un solo paciente, o de un pequeño grupo de pacientes con un diagnóstico similar, o a un factor estadístico con el potencial de producir enfermedad con períodos en los que no están expuestos. [50]
El primer tipo de estudio es puramente descriptivo y no se puede utilizar para hacer inferencias sobre la población general de pacientes con esa enfermedad. Este tipo de estudios, en los que un médico astuto identifica una característica inusual de una enfermedad o de la historia de un paciente, puede llevar a la formulación de una nueva hipótesis. Utilizando los datos de la serie, se podrían realizar estudios analíticos para investigar posibles factores causales. Estos pueden incluir estudios de casos y controles o estudios prospectivos. Un estudio de casos y controles implicaría emparejar controles comparables sin la enfermedad con los casos de la serie. Un estudio prospectivo implicaría seguir la serie de casos a lo largo del tiempo para evaluar la historia natural de la enfermedad. [51]
Este último tipo, descrito más formalmente como estudios de series de casos autocontrolados, divide el tiempo de seguimiento de cada paciente en períodos de exposición y no exposición y utiliza procesos de regresión de Poisson de efectos fijos para comparar la tasa de incidencia de un resultado dado entre períodos de exposición y no exposición. Esta técnica se ha utilizado ampliamente en el estudio de reacciones adversas a la vacunación y se ha demostrado que en algunas circunstancias proporciona un poder estadístico comparable al disponible en los estudios de cohorte. [ cita requerida ]
Los estudios de casos y controles seleccionan sujetos en función de su estado de enfermedad. Es un estudio retrospectivo. Se compara un grupo de individuos que son positivos a la enfermedad (el grupo de "casos") con un grupo de individuos negativos a la enfermedad (el grupo de "control"). El grupo de control idealmente debería provenir de la misma población que dio lugar a los casos. El estudio de casos y controles analiza en el tiempo las posibles exposiciones que ambos grupos (casos y controles) pueden haber experimentado. Se construye una tabla de 2x2, que muestra los casos expuestos (A), los controles expuestos (B), los casos no expuestos (C) y los controles no expuestos (D). La estadística generada para medir la asociación es la razón de probabilidades (OR) [52] , que es la razón de las probabilidades de exposición en los casos (A/C) a las probabilidades de exposición en los controles (B/D), es decir, OR = (AD/BC). [ cita requerida ]
Si el OR es significativamente mayor que 1, entonces la conclusión es que "es más probable que quienes padecen la enfermedad hayan estado expuestos", mientras que si es cercano a 1, entonces la exposición y la enfermedad no están probablemente asociadas. Si el OR es mucho menor que uno, esto sugiere que la exposición es un factor protector en la causa de la enfermedad. Los estudios de casos y controles suelen ser más rápidos y más rentables que los estudios de cohorte , pero son sensibles al sesgo (como el sesgo de recuerdo y el sesgo de selección ). El principal desafío es identificar el grupo de control apropiado; la distribución de la exposición entre el grupo de control debe ser representativa de la distribución en la población que dio lugar a los casos. Esto se puede lograr extrayendo una muestra aleatoria de la población original en riesgo. Esto tiene como consecuencia que el grupo de control puede contener personas con la enfermedad en estudio cuando la enfermedad tiene una alta tasa de ataque en una población. [ cita requerida ]
Una desventaja importante de los estudios de casos y controles es que, para que se consideren estadísticamente significativos, el número mínimo de casos requerido en el intervalo de confianza del 95% está relacionado con la razón de probabilidades mediante la ecuación:
donde N es la proporción de casos a controles. A medida que la razón de probabilidades se acerca a 1, el número de casos necesarios para la significación estadística crece hasta el infinito, lo que hace que los estudios de casos y controles sean prácticamente inútiles para razones de probabilidades bajas. Por ejemplo, para una razón de probabilidades de 1,5 y casos = controles, la tabla que se muestra arriba se vería así:
Para una razón de probabilidades de 1,1:
Varios artículos recientes, publicados en revistas científicas revisadas por pares, proporcionan descripciones generales útiles sobre el diseño y la interpretación de los estudios de casos y controles [53] [54] [55] .
Los estudios de cohorte seleccionan sujetos en función de su estado de exposición. Los sujetos del estudio deben estar en riesgo del resultado bajo investigación al comienzo del estudio de cohorte; esto generalmente significa que deben estar libres de enfermedad cuando comienza el estudio de cohorte. La cohorte es seguida a lo largo del tiempo para evaluar su estado de resultado posterior. Un ejemplo de un estudio de cohorte sería la investigación de una cohorte de fumadores y no fumadores a lo largo del tiempo para estimar la incidencia de cáncer de pulmón. Se construye la misma tabla 2×2 que con el estudio de casos y controles. Sin embargo, la estimación puntual generada es el riesgo relativo (RR), que es la probabilidad de enfermedad para una persona en el grupo expuesto, P e = A / ( A + B ) sobre la probabilidad de enfermedad para una persona en el grupo no expuesto, P u = C / ( C + D ), es decir, RR = P e / P u .
Al igual que con el OR, un RR mayor a 1 muestra asociación, donde la conclusión puede leerse "aquellos con exposición tenían más probabilidades de desarrollar la enfermedad".
Los estudios prospectivos tienen muchas ventajas sobre los estudios de casos y controles. El RR es una medida de efecto más potente que el OR, ya que el OR es solo una estimación del RR, ya que la incidencia real no se puede calcular en un estudio de casos y controles en el que los sujetos se seleccionan en función del estado de la enfermedad. La temporalidad se puede establecer en un estudio prospectivo y los factores de confusión se controlan más fácilmente. Sin embargo, son más costosos y existe una mayor probabilidad de perder sujetos durante el seguimiento en función del largo período de tiempo durante el cual se realiza el seguimiento de la cohorte.
Los estudios de cohorte también están limitados por la misma ecuación para el número de casos que los estudios de cohorte, pero, si la tasa de incidencia base en la población del estudio es muy baja, el número de casos requeridos se reduce en 1 ⁄ 2 .
Varios artículos recientes revisados por pares, publicados en revistas científicas, brindan descripciones generales útiles sobre el diseño y la interpretación de estudios de cohorte [56] [57] [58] .
Aunque a veces se considera la epidemiología como un conjunto de herramientas estadísticas utilizadas para dilucidar las asociaciones entre la exposición y los resultados de salud, una comprensión más profunda de esta ciencia es la de descubrir relaciones causales .
" La correlación no implica causalidad " es un tema común en gran parte de la literatura epidemiológica. Para los epidemiólogos, la clave está en el término inferencia . La correlación, o al menos la asociación entre dos variables, es un criterio necesario pero no suficiente para la inferencia de que una variable causa la otra. Los epidemiólogos utilizan datos recopilados y una amplia gama de teorías biomédicas y psicosociales de manera iterativa para generar o expandir la teoría, probar hipótesis y hacer afirmaciones fundamentadas y fundamentadas sobre qué relaciones son causales y exactamente cómo lo son.
Los epidemiólogos enfatizan que la idea de “ una causa – un efecto ” es una creencia errónea simplista. [59] La mayoría de los resultados, ya sea enfermedad o muerte, son causados por una cadena o red que consta de muchas causas componentes. [60] Las causas pueden distinguirse como condiciones necesarias, suficientes o probabilísticas. Si se puede identificar y controlar una condición necesaria (por ejemplo, anticuerpos contra un agente patógeno, energía en una lesión), se puede evitar el resultado dañino (Robertson, 2015). Una herramienta que se utiliza regularmente para conceptualizar la multicausalidad asociada con la enfermedad es el modelo circular causal . [61]
En 1965, Austin Bradford Hill propuso una serie de consideraciones para ayudar a evaluar la evidencia de causalidad, [62] que se han conocido comúnmente como los " criterios de Bradford Hill ". En contraste con las intenciones explícitas de su autor, las consideraciones de Hill se enseñan ahora a veces como una lista de verificación que se debe implementar para evaluar la causalidad. [63] El propio Hill dijo: "Ninguno de mis nueve puntos de vista puede aportar evidencia indiscutible a favor o en contra de la hipótesis de causa y efecto y ninguno puede ser requerido sine qua non ". [62]
Los estudios epidemiológicos sólo pueden servir para demostrar que un agente podría haber causado, pero no que causó, un efecto en un caso particular:
La epidemiología se ocupa de la incidencia de enfermedades en poblaciones y no aborda la cuestión de la causa de la enfermedad de un individuo. Esta cuestión, a veces denominada causalidad específica, está fuera del dominio de la ciencia de la epidemiología. La epidemiología tiene sus límites en el punto en que se hace una inferencia de que la relación entre un agente y una enfermedad es causal (causalidad general) y donde se ha determinado la magnitud del exceso de riesgo atribuido al agente; es decir, la epidemiología aborda si un agente puede causar una enfermedad, no si un agente causó la enfermedad de un demandante específico. [64]
En el derecho de los Estados Unidos, la epidemiología por sí sola no puede demostrar que no existe una asociación causal en general. A la inversa, los tribunales estadounidenses pueden (y lo hacen en algunas circunstancias) utilizarla, en un caso individual, para justificar una inferencia de que sí existe una asociación causal, basándose en un equilibrio de probabilidades .
La subdisciplina de la epidemiología forense está dirigida a la investigación de la causalidad específica de enfermedades o lesiones en individuos o grupos de individuos en casos en los que la causalidad está en disputa o no está clara, para su presentación en entornos legales.
La práctica epidemiológica y los resultados del análisis epidemiológico hacen una contribución significativa a los marcos emergentes de gestión de la salud basados en la población.
La gestión de la salud basada en la población abarca la capacidad de:
La gestión moderna de la salud basada en la población es compleja y requiere un conjunto múltiple de habilidades (médicas, políticas, tecnológicas, matemáticas, etc.) de las cuales la práctica y el análisis epidemiológicos son un componente central, que se unifica con la ciencia de la gestión para proporcionar una atención de salud y una orientación sanitaria eficientes y eficaces a una población. Esta tarea requiere la capacidad de visión de futuro de los enfoques modernos de gestión de riesgos que transforman los factores de riesgo para la salud, la incidencia, la prevalencia y las estadísticas de mortalidad (derivadas del análisis epidemiológico) en parámetros de gestión que no solo orienten la forma en que un sistema de salud responde a los problemas actuales de salud de la población, sino también la forma en que un sistema de salud puede gestionarse para responder mejor a futuros problemas potenciales de salud de la población. [65]
Entre los ejemplos de organizaciones que utilizan la gestión de la salud basada en la población que aprovecha el trabajo y los resultados de la práctica epidemiológica se incluyen la Estrategia Canadiense para el Control del Cáncer, los Programas de Control del Tabaco de Salud Canadá, la Fundación Rick Hansen y la Iniciativa Canadiense de Investigación para el Control del Tabaco. [66] [67] [68]
Cada una de estas organizaciones utiliza un marco de gestión de la salud basado en la población llamado Vida en Riesgo que combina el análisis cuantitativo epidemiológico con la demografía, la investigación operativa de las agencias de salud y la economía para realizar:
La epidemiología aplicada es la práctica de utilizar métodos epidemiológicos para proteger o mejorar la salud de una población. La epidemiología de campo aplicada puede incluir la investigación de brotes de enfermedades transmisibles y no transmisibles, tasas de mortalidad y morbilidad y estado nutricional, entre otros indicadores de salud, con el propósito de comunicar los resultados a quienes pueden implementar políticas o medidas de control de enfermedades adecuadas.
A medida que la vigilancia y la notificación de enfermedades y otros factores de salud se vuelven cada vez más difíciles en situaciones de crisis humanitarias, las metodologías utilizadas para comunicar los datos se ven comprometidas. Un estudio concluyó que menos de la mitad (42,4%) de las encuestas sobre nutrición realizadas en contextos humanitarios calculaban correctamente la prevalencia de la malnutrición y solo un tercio (35,3%) de las encuestas cumplían los criterios de calidad. Entre las encuestas sobre mortalidad, solo el 3,2% cumplía los criterios de calidad. Dado que el estado nutricional y las tasas de mortalidad ayudan a indicar la gravedad de una crisis, el seguimiento y la notificación de estos factores de salud son cruciales.
Los registros vitales suelen ser la forma más eficaz de recopilar datos, pero en contextos humanitarios estos registros pueden ser inexistentes, poco fiables o inaccesibles. Por ello, la mortalidad suele medirse de forma imprecisa mediante la vigilancia demográfica prospectiva o las encuestas de mortalidad retrospectivas. La vigilancia demográfica prospectiva requiere mucha mano de obra y es difícil de implementar en una población dispersa. Las encuestas de mortalidad retrospectivas son propensas a sesgos de selección y notificación. Se están desarrollando otros métodos, pero aún no son una práctica común. [69] [70] [71] [72]
El concepto de olas en las epidemias tiene implicaciones especialmente para las enfermedades transmisibles . Una definición práctica del término "ola epidémica" se basa en dos características clave: 1) comprende períodos de tendencias ascendentes o descendentes, y 2) estos aumentos o disminuciones deben ser sustanciales y sostenidos durante un período de tiempo, para poder distinguirlos de fluctuaciones menores o errores de notificación. [73] El uso de una definición científica consistente tiene como objetivo proporcionar un lenguaje consistente que pueda usarse para comunicar y comprender la progresión de la pandemia de COVID-19, lo que ayudaría a las organizaciones de atención médica y a los responsables de las políticas en la planificación y asignación de recursos.
Los distintos campos de la epidemiología tienen distintos niveles de validez. Una forma de evaluar la validez de los hallazgos es la proporción de falsos positivos (efectos declarados que no son correctos) y falsos negativos (estudios que no respaldan un efecto verdadero). En la epidemiología genética , los estudios de genes candidatos pueden producir más de 100 hallazgos falsos positivos por cada falso negativo. Por el contrario, la asociación a nivel de todo el genoma parece casi lo contrario, con solo un falso positivo por cada 100 o más falsos negativos. [74] Esta proporción ha mejorado con el tiempo en la epidemiología genética, ya que el campo ha adoptado criterios estrictos. Por el contrario, otros campos epidemiológicos no han requerido informes tan rigurosos y, como resultado, son mucho menos confiables. [74]
El error aleatorio es el resultado de fluctuaciones en torno a un valor verdadero debido a la variabilidad del muestreo. El error aleatorio es justamente eso: aleatorio. Puede ocurrir durante la recolección, codificación, transferencia o análisis de datos. Algunos ejemplos de errores aleatorios incluyen preguntas mal redactadas, un malentendido en la interpretación de una respuesta individual de un encuestado en particular o un error tipográfico durante la codificación. El error aleatorio afecta la medición de una manera transitoria e inconsistente y es imposible corregirlo. Existe un error aleatorio en todos los procedimientos de muestreo: el error de muestreo . [ cita requerida ]
La precisión en las variables epidemiológicas es una medida del error aleatorio. La precisión también está inversamente relacionada con el error aleatorio, de modo que reducir el error aleatorio es aumentar la precisión. Los intervalos de confianza se calculan para demostrar la precisión de las estimaciones del riesgo relativo. Cuanto más estrecho sea el intervalo de confianza, más precisa será la estimación del riesgo relativo.
Existen dos formas básicas de reducir el error aleatorio en un estudio epidemiológico . La primera es aumentar el tamaño de la muestra del estudio. En otras palabras, agregar más sujetos al estudio. La segunda es reducir la variabilidad en la medición del estudio. Esto se puede lograr utilizando un dispositivo de medición más preciso o aumentando el número de mediciones.
Cabe señalar que, si se aumenta el tamaño de la muestra o el número de mediciones, o si se adquiere una herramienta de medición más precisa, los costos del estudio suelen aumentar. Suele existir un equilibrio difícil entre la necesidad de precisión adecuada y la cuestión práctica del costo del estudio.
Un error sistemático o sesgo ocurre cuando hay una diferencia entre el valor verdadero (en la población) y el valor observado (en el estudio) por cualquier causa que no sea la variabilidad del muestreo. Un ejemplo de error sistemático es si, sin que usted lo sepa, el oxímetro de pulso que está utilizando está configurado incorrectamente y suma dos puntos al valor verdadero cada vez que se toma una medición. El dispositivo de medición puede ser preciso pero no exacto . Debido a que el error ocurre en todos los casos, es sistemático. Las conclusiones que saque en función de esos datos seguirán siendo incorrectas. Pero el error se puede reproducir en el futuro (por ejemplo, al utilizar el mismo instrumento mal configurado).
Un error en la codificación que afecta a todas las respuestas para esa pregunta en particular es otro ejemplo de error sistemático.
La validez de un estudio depende del grado de error sistemático. La validez suele dividirse en dos componentes:
El sesgo de selección ocurre cuando los sujetos de estudio son seleccionados o pasan a formar parte del estudio como resultado de una tercera variable no medida que está asociada tanto con la exposición como con el resultado de interés. [75] Por ejemplo, se ha observado repetidamente que los fumadores y los no fumadores tienden a diferir en sus tasas de participación en el estudio. (Sackett D cita el ejemplo de Seltzer et al., en el que el 85% de los no fumadores y el 67% de los fumadores devolvieron los cuestionarios enviados por correo.) [76] Tal diferencia en la respuesta no conducirá a un sesgo si no está también asociada con una diferencia sistemática en el resultado entre los dos grupos de respuesta.
El sesgo de información es el que surge de un error sistemático en la evaluación de una variable. [77] Un ejemplo de esto es el sesgo de recuerdo. Un ejemplo típico lo proporciona Sackett en su discusión de un estudio que examina el efecto de exposiciones específicas en la salud fetal: "al interrogar a madres cuyos embarazos recientes habían terminado en muerte o malformación fetal (casos) y a un grupo emparejado de madres cuyos embarazos terminaron normalmente (controles), se encontró que el 28% de las primeras, pero solo el 20% de las segundas, informaron exposición a medicamentos que no se pudo corroborar ni en entrevistas prospectivas anteriores ni en otros registros de salud". [76] En este ejemplo, el sesgo de recuerdo probablemente ocurrió como resultado de que las mujeres que habían tenido abortos espontáneos tenían una tendencia aparente a recordar mejor y, por lo tanto, informar sobre exposiciones anteriores.
Tradicionalmente, la confusión se ha definido como un sesgo que surge de la coocurrencia o mezcla de efectos de factores extraños, denominados factores de confusión, con el efecto o los efectos principales de interés. [77] [78] Una definición más reciente de confusión invoca la noción de efectos contrafácticos . [78] Según este punto de vista, cuando se observa un resultado de interés, digamos Y=1 (en oposición a Y=0), en una población dada A que está totalmente expuesta (es decir, exposición X = 1 para cada unidad de la población), el riesgo de este evento será R A1 . El riesgo contrafáctico o no observado R A0 corresponde al riesgo que se habría observado si estos mismos individuos no hubieran estado expuestos (es decir, X = 0 para cada unidad de la población). Por lo tanto, el verdadero efecto de la exposición es: R A1 − R A0 (si uno está interesado en las diferencias de riesgo) o R A1 / R A0 (si uno está interesado en el riesgo relativo). Dado que el riesgo contrafactual R A0 no es observable, lo aproximamos utilizando una segunda población B y medimos las siguientes relaciones: R A1 − R B0 o R A1 / R B0 . En esta situación, se produce confusión cuando R A0 ≠ R B0 . [78] (NB: El ejemplo supone variables binarias de resultado y exposición).
Algunos epidemiólogos prefieren pensar en la confusión por separado de las categorizaciones comunes de sesgo ya que, a diferencia del sesgo de selección y de información, la confusión surge de efectos causales reales. [75]
Pocas universidades han ofrecido epidemiología como un curso de estudio a nivel de pregrado. [ cita requerida ] Existe un programa de pregrado en la Universidad Johns Hopkins en el que los estudiantes que se especializan en salud pública pueden tomar cursos de nivel de posgrado, incluida epidemiología, durante su último año en la Escuela de Salud Pública Bloomberg . [79] Además de sus títulos de maestría y doctorado en epidemiología, la Escuela de Salud Pública de la Universidad de Michigan ha ofrecido programas de pregrado desde 2017 que incluyen cursos en epidemiología. [80] [81]
Aunque la investigación epidemiológica es realizada por personas de diversas disciplinas, se proporcionan niveles variables de capacitación en métodos epidemiológicos durante los programas de doctorado de farmacia , medicina , veterinaria , trabajo social , podiatría , enfermería , fisioterapia y psicología clínica , además de la capacitación formal que reciben los estudiantes de maestría y doctorado en los campos de la salud pública.
Como profesionales de la salud pública, los epidemiólogos trabajan en varios entornos diferentes. Algunos epidemiólogos trabajan "en el campo" (es decir, en la comunidad; comúnmente [ ¿según quién? ] en un servicio de salud pública), y a menudo están a la vanguardia de la investigación y el combate de brotes de enfermedades. [ cita requerida ] Otros trabajan para organizaciones sin fines de lucro, universidades, hospitales o entidades gubernamentales más grandes (por ejemplo, departamentos de salud estatales y locales en los Estados Unidos), ministerios de salud, Médicos sin Fronteras , los Centros para el Control y la Prevención de Enfermedades (CDC), la Agencia de Protección de la Salud , la Organización Mundial de la Salud (OMS) o la Agencia de Salud Pública de Canadá . Los epidemiólogos también pueden trabajar en organizaciones con fines de lucro (por ejemplo, compañías farmacéuticas y de dispositivos médicos) en grupos como investigación de mercado o desarrollo clínico.
Un artículo de la Universidad del Sur de California de abril de 2020 señaló que “la epidemia de coronavirus … impulsó la epidemiología –el estudio de la incidencia, distribución y control de enfermedades en una población– al frente de las disciplinas científicas en todo el mundo e incluso convirtió en celebridades temporales a algunos de sus practicantes”. [82]
nanlee.net