Un neurotransmisor es una molécula de señalización secretada por una neurona para afectar a otra célula a través de una sinapsis . La célula que recibe la señal, o célula diana, puede ser otra neurona, pero también podría ser una glándula o una célula muscular . [1]
Los neurotransmisores se liberan desde las vesículas sinápticas hacia la hendidura sináptica, donde pueden interactuar con los receptores de neurotransmisores de la célula diana. El efecto del neurotransmisor sobre la célula diana está determinado por el receptor al que se une. Muchos neurotransmisores se sintetizan a partir de precursores simples y abundantes, como los aminoácidos , que están fácilmente disponibles y a menudo requieren una pequeña cantidad de pasos biosintéticos para su conversión.
Los neurotransmisores son esenciales para el funcionamiento de sistemas neuronales complejos. Se desconoce el número exacto de neurotransmisores únicos en los humanos, pero se han identificado más de 100. [2] Los neurotransmisores comunes incluyen glutamato , GABA , acetilcolina , glicina y norepinefrina .
Los neurotransmisores generalmente se sintetizan en las neuronas y están formados o derivados de moléculas precursoras que se encuentran en abundancia en la célula. Las clases de neurotransmisores incluyen aminoácidos , monoaminas y péptidos . Las monoaminas se sintetizan alterando un solo aminoácido. Por ejemplo, el precursor de la serotonina es el aminoácido triptófano. Los transmisores de péptidos, o neuropéptidos, son transmisores de proteínas que a menudo se liberan junto con otros transmisores para tener un efecto modulador. [3] Los neurotransmisores de purina, como el ATP, se derivan de ácidos nucleicos. Otros neurotransmisores se componen de productos metabólicos como el óxido nítrico y el monóxido de carbono . [ cita necesaria ]

Los neurotransmisores generalmente se almacenan en vesículas sinápticas , agrupadas cerca de la membrana celular en la terminal del axón de la neurona presináptica. Sin embargo, algunos neurotransmisores, como los gases metabólicos monóxido de carbono y óxido nítrico, se sintetizan y liberan inmediatamente después de un potencial de acción sin siquiera almacenarse en vesículas. [4]
Generalmente, se libera un neurotransmisor en la terminal presináptica en respuesta a una señal eléctrica llamada potencial de acción en la neurona presináptica. Sin embargo, la liberación "inicial" de bajo nivel también se produce sin estimulación eléctrica. Los neurotransmisores se liberan y difunden a través de la hendidura sináptica , donde se unen a receptores específicos en la membrana de la neurona postsináptica. [5]
Después de ser liberados en la hendidura sináptica, los neurotransmisores se difunden a través de la sinapsis, donde pueden interactuar con los receptores de la célula diana. El efecto del neurotransmisor depende de la identidad de los receptores de la célula diana presentes en la sinapsis. Dependiendo del receptor, la unión de neurotransmisores puede causar excitación , inhibición o modulación de la neurona postsináptica. Vea abajo para más información. [ cita necesaria ]
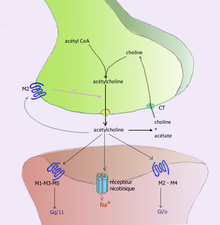
Para evitar la activación continua de receptores en la célula postsináptica o diana, se deben eliminar los neurotransmisores de la hendidura sináptica. [6] Los neurotransmisores se eliminan mediante uno de tres mecanismos:
Por ejemplo, la acetilcolina se elimina al escindir su grupo acetilo mediante la enzima acetilcolinesterasa ; La colina restante luego es absorbida y reciclada por la neurona presináptica para sintetizar más acetilcolina . [9] Otros neurotransmisores pueden difundirse fuera de sus uniones sinápticas objetivo y se eliminan del cuerpo a través de los riñones o se destruyen en el hígado. Cada neurotransmisor tiene vías de degradación muy específicas en puntos reguladores, a los que puede dirigirse el sistema regulador del cuerpo o la medicación. La cocaína bloquea un transportador de dopamina responsable de la recaptación de dopamina. Sin el transportador, la dopamina se difunde mucho más lentamente desde la hendidura sináptica y continúa activando los receptores de dopamina en la célula diana. [10]
Hasta principios del siglo XX, los científicos asumían que la mayor parte de la comunicación sináptica en el cerebro era eléctrica. Sin embargo, mediante exámenes histológicos realizados por Ramón y Cajal , se descubrió una brecha de 20 a 40 nm entre neuronas, conocida hoy como hendidura sináptica . La presencia de tal brecha sugería comunicación a través de mensajeros químicos que atraviesan la hendidura sináptica, y en 1921 el farmacólogo alemán Otto Loewi confirmó que las neuronas pueden comunicarse liberando sustancias químicas. A través de una serie de experimentos con los nervios vagos de las ranas, Loewi pudo reducir manualmente la frecuencia cardíaca de las ranas controlando la cantidad de solución salina presente alrededor del nervio vago. Al finalizar este experimento, Loewi afirmó que la regulación simpática de la función cardíaca puede estar mediada por cambios en las concentraciones químicas. Además, a Otto Loewi se le atribuye el descubrimiento de la acetilcolina (ACh), el primer neurotransmisor conocido. [11]
Para identificar neurotransmisores, normalmente se consideran los siguientes criterios:
Sin embargo, dados los avances en farmacología , genética y neuroanatomía química , el término "neurotransmisor" puede aplicarse a sustancias químicas que:
La localización anatómica de los neurotransmisores generalmente se determina mediante técnicas inmunocitoquímicas , que identifican la ubicación de las propias sustancias transmisoras o de las enzimas que participan en su síntesis. Las técnicas inmunocitoquímicas también han revelado que muchos transmisores, particularmente los neuropéptidos , están co-localizados, es decir, una neurona puede liberar más de un transmisor desde su terminal sináptico . [13] Se pueden utilizar diversas técnicas y experimentos, como la tinción , la estimulación y la recolección, para identificar neurotransmisores en todo el sistema nervioso central . [14]
Las neuronas se comunican entre sí a través de sinapsis , puntos de contacto especializados donde los neurotransmisores transmiten señales. Cuando un potencial de acción llega a la terminal presináptica , el potencial de acción puede desencadenar la liberación de neurotransmisores en la hendidura sináptica. Estos neurotransmisores luego se unen a receptores en la membrana postsináptica, influyendo en la neurona receptora de manera inhibidora o excitadora . Si las influencias excitadoras generales superan las influencias inhibidoras, la neurona receptora puede generar su propio potencial de acción, continuando la transmisión de información a la siguiente neurona de la red. Este proceso permite el flujo de información y la formación de redes neuronales complejas. [15]
Un neurotransmisor puede tener un efecto excitador, inhibidor o modulador sobre la célula diana. El efecto está determinado por los receptores con los que interactúa el neurotransmisor en la membrana postsináptica. El neurotransmisor influye en el flujo de iones transmembrana para aumentar (excitador) o disminuir (inhibidor) la probabilidad de que la célula con la que entra en contacto produzca un potencial de acción. Las sinapsis que contienen receptores con efectos excitadores se denominan sinapsis de tipo I, mientras que las sinapsis de tipo II contienen receptores con efectos inhibidores. [16] Por lo tanto, a pesar de la amplia variedad de sinapsis, todas transmiten mensajes sólo de estos dos tipos. Los dos tipos tienen apariencia diferente y se ubican principalmente en diferentes partes de las neuronas bajo su influencia. [17] Los receptores con efectos moduladores se extienden por todas las membranas sinápticas y la unión de neurotransmisores pone en movimiento cascadas de señalización que ayudan a la célula a regular su función. [18] La unión de neurotransmisores a receptores con efectos moduladores puede tener muchos resultados. Por ejemplo, puede resultar en un aumento o disminución de la sensibilidad a estímulos futuros al reclutar más o menos receptores en la membrana sináptica.
Las sinapsis de tipo I (excitadoras) generalmente se ubican en los ejes o las espinas de las dendritas, mientras que las sinapsis de tipo II (inhibitorias) generalmente se ubican en un cuerpo celular. Además, las sinapsis de tipo I tienen vesículas sinápticas redondas, mientras que las vesículas de las sinapsis de tipo II son aplanadas. El material de las membranas presinápticas y postsinápticas es más denso en una sinapsis de tipo I que en una de tipo II, y la hendidura sináptica de tipo I es más ancha. Finalmente, la zona activa en una sinapsis de tipo I es mayor que la de una sinapsis de tipo II.
Las diferentes ubicaciones de las sinapsis de tipo I y tipo II dividen una neurona en dos zonas: un árbol dendrítico excitador y un cuerpo celular inhibidor. Desde una perspectiva inhibidora, la excitación llega a las dendritas y se extiende al montículo del axón para desencadenar un potencial de acción . Si se va a detener el mensaje, es mejor detenerlo aplicando inhibición en el cuerpo celular, cerca del montículo del axón donde se origina el potencial de acción. Otra forma de conceptualizar la interacción excitadora-inhibitoria es imaginar que la excitación supera la inhibición. Si el cuerpo celular normalmente se encuentra en un estado inhibido, la única forma de generar un potencial de acción en el montículo del axón es reducir la inhibición del cuerpo celular. En esta estrategia de "abrir las puertas", el mensaje excitador es como un caballo de carreras listo para correr por la pista, pero primero se debe eliminar la puerta inhibidora de salida. [19]
Como se explicó anteriormente, la única acción directa de un neurotransmisor es activar un receptor. Por tanto, los efectos de un sistema neurotransmisor dependen de las conexiones de las neuronas que utilizan el transmisor y de las propiedades químicas de los receptores.
Hay muchas formas diferentes de clasificar los neurotransmisores. Dividirlos en aminoácidos , péptidos y monoaminas es suficiente para algunos propósitos de clasificación. [27]
Principales neurotransmisores:
Además, se han encontrado más de 100 péptidos neuroactivos y periódicamente se descubren otros nuevos. [30] [31] Muchos de estos se lanzan conjuntamente junto con un transmisor de molécula pequeña. Sin embargo, en algunos casos, un péptido es el transmisor principal en una sinapsis. La betaendorfina es un ejemplo relativamente conocido de neurotransmisor peptídico porque participa en interacciones altamente específicas con los receptores opioides en el sistema nervioso central .
Algunos también consideran neurotransmisores a los iones individuales (como el zinc liberado sinápticamente), [32] así como a algunas moléculas gaseosas como el óxido nítrico (NO), el monóxido de carbono (CO) y el sulfuro de hidrógeno (H 2 S). [33] Los gases se producen en el citoplasma neural y se difunden inmediatamente a través de la membrana celular hacia el líquido extracelular y hacia las células cercanas para estimular la producción de segundos mensajeros. Los neurotransmisores de gases solubles son difíciles de estudiar, ya que actúan rápidamente y se descomponen inmediatamente, existiendo sólo durante unos segundos.
El transmisor más frecuente es el glutamato , que es excitador en más del 90% de las sinapsis del cerebro humano. [28] El siguiente en frecuencia es el ácido gamma-aminobutírico, o GABA, que es inhibidor en más del 90% de las sinapsis que no utilizan glutamato. Aunque otros transmisores se utilizan en menos sinapsis, pueden ser muy importantes desde el punto de vista funcional: la gran mayoría de las drogas psicoactivas ejercen sus efectos alterando las acciones de algunos sistemas de neurotransmisores, actuando a menudo a través de transmisores distintos del glutamato o el GABA. Las drogas adictivas como la cocaína y las anfetaminas ejercen sus efectos principalmente sobre el sistema de dopamina. Las drogas opiáceas adictivas ejercen sus efectos principalmente como análogos funcionales de los péptidos opioides , que, a su vez, regulan los niveles de dopamina.
Las neuronas que expresan ciertos tipos de neurotransmisores a veces forman sistemas distintos, donde la activación del sistema afecta grandes volúmenes del cerebro, lo que se denomina transmisión de volumen . Los principales sistemas de neurotransmisores incluyen el sistema de noradrenalina (norepinefrina), el sistema de dopamina , el sistema de serotonina y el sistema colinérgico , entre otros. Las trazas de aminas tienen un efecto modulador sobre la neurotransmisión en las vías de las monoaminas (es decir, las vías de la dopamina, la norepinefrina y la serotonina) en todo el cerebro a través de la señalización a través del receptor 1 asociado a las trazas de aminas . [37] [38] A continuación se presenta una breve comparación de estos sistemas:
Comprender los efectos de los fármacos sobre los neurotransmisores comprende una parte importante de las iniciativas de investigación en el campo de la neurociencia . La mayoría de los neurocientíficos involucrados en este campo de investigación creen que tales esfuerzos pueden avanzar aún más en nuestra comprensión de los circuitos responsables de diversas enfermedades y trastornos neurológicos, así como formas de tratar eficazmente y algún día posiblemente prevenir o curar dichas enfermedades. [55] [ cita médica necesaria ]
Las drogas pueden influir en el comportamiento alterando la actividad de los neurotransmisores. Por ejemplo, las drogas pueden disminuir la tasa de síntesis de neurotransmisores al afectar las enzimas sintéticas de ese neurotransmisor. Cuando se bloquea la síntesis de neurotransmisores, la cantidad de neurotransmisores disponibles para liberarse se vuelve sustancialmente menor, lo que resulta en una disminución de la actividad de los neurotransmisores. Algunas drogas bloquean o estimulan la liberación de neurotransmisores específicos. Alternativamente, los fármacos pueden impedir el almacenamiento de neurotransmisores en las vesículas sinápticas al provocar fugas en las membranas de las vesículas sinápticas. Los fármacos que impiden que un neurotransmisor se una a su receptor se denominan antagonistas del receptor . Por ejemplo, los medicamentos utilizados para tratar a pacientes con esquizofrenia, como el haloperidol, la clorpromazina y la clozapina, son antagonistas de los receptores de dopamina en el cerebro. Otras drogas actúan uniéndose a un receptor e imitando al neurotransmisor normal. Estos fármacos se denominan agonistas de los receptores . Un ejemplo de agonista del receptor es la morfina , un opiáceo que imita los efectos del neurotransmisor endógeno β-endorfina para aliviar el dolor. Otras drogas interfieren con la desactivación de un neurotransmisor después de su liberación, prolongando así la acción de un neurotransmisor. Esto se puede lograr bloqueando la recaptación o inhibiendo las enzimas degradativas. Por último, los fármacos también pueden impedir que se produzca un potencial de acción, bloqueando la actividad neuronal en todo el sistema nervioso central y periférico . Los fármacos como la tetrodotoxina , que bloquean la actividad neuronal, suelen ser letales.
Los fármacos que se dirigen al neurotransmisor de los sistemas principales afectan a todo el sistema, lo que puede explicar la complejidad de la acción de algunos fármacos. La cocaína , por ejemplo, bloquea la recaptación de dopamina hacia la neurona presináptica , dejando las moléculas del neurotransmisor en la brecha sináptica durante un período prolongado de tiempo. Dado que la dopamina permanece en la sinapsis por más tiempo, el neurotransmisor continúa uniéndose a los receptores de la neurona postsináptica , provocando una respuesta emocional placentera. La adicción física a la cocaína puede resultar de una exposición prolongada al exceso de dopamina en las sinapsis, lo que conduce a la regulación negativa de algunos receptores postsinápticos. Una vez que los efectos de la droga desaparecen, un individuo puede deprimirse debido a la menor probabilidad de que el neurotransmisor se una a un receptor. La fluoxetina es un inhibidor selectivo de la recaptación de serotonina (ISRS), que bloquea la recaptación de serotonina por parte de las células presinápticas, lo que aumenta la cantidad de serotonina presente en la sinapsis y además le permite permanecer allí por más tiempo, lo que proporciona potencial para el efecto de la recaptación natural. serotonina liberada. [56] AMPT previene la conversión de tirosina en L-DOPA , el precursor de la dopamina; la reserpina previene el almacenamiento de dopamina dentro de las vesículas ; y el deprenilo inhibe la monoaminooxidasa (MAO)-B y, por tanto, aumenta los niveles de dopamina.
Un agonista es una sustancia química capaz de unirse a un receptor, como un receptor de neurotransmisor, e iniciar la misma reacción producida típicamente por la unión de la sustancia endógena. [60] Un agonista de un neurotransmisor iniciará así la misma respuesta del receptor que el transmisor. En las neuronas, un fármaco agonista puede activar los receptores de neurotransmisores directa o indirectamente. Los agonistas de unión directa se pueden caracterizar además como agonistas completos , agonistas parciales y agonistas inversos . [61] [62]
Los agonistas directos actúan de manera similar a un neurotransmisor al unirse directamente a sus sitios receptores asociados, que pueden estar ubicados en la neurona presináptica o postsináptica, o en ambas. [63] Por lo general, los receptores de neurotransmisores se ubican en la neurona postsináptica, mientras que los autorreceptores de neurotransmisores se ubican en la neurona presináptica, como es el caso de los neurotransmisores monoamínicos ; [37] en algunos casos, un neurotransmisor utiliza neurotransmisión retrógrada , un tipo de señalización de retroalimentación en las neuronas donde el neurotransmisor se libera postsinápticamente y se une a receptores objetivo ubicados en la neurona presináptica. [64] [nota 1] La nicotina , un compuesto que se encuentra en el tabaco , es un agonista directo de la mayoría de los receptores nicotínicos de acetilcolina , ubicados principalmente en las neuronas colinérgicas . [59] Los opiáceos , como la morfina , la heroína , la hidrocodona , la oxicodona , la codeína y la metadona , son agonistas de los receptores μ-opioides ; esta acción media en sus propiedades euforiantes y analgésicas . [59]
Los agonistas indirectos aumentan la unión de los neurotransmisores a sus receptores diana estimulando la liberación o impidiendo la recaptación de neurotransmisores. [63] Algunos agonistas indirectos desencadenan la liberación de neurotransmisores y previenen la recaptación de neurotransmisores . La anfetamina , por ejemplo, es un agonista indirecto de los receptores postsinápticos de dopamina, noradrenalina y serotonina en cada una de sus respectivas neuronas; [37] [38] produce la liberación de neurotransmisores en la neurona presináptica y posteriormente en la hendidura sináptica y previene su recaptación desde la hendidura sináptica activando TAAR1 , un receptor presináptico acoplado a proteína G , y uniéndose a un sitio en VMAT2 , un tipo de transportador de monoaminas ubicado en vesículas sinápticas dentro de las neuronas monoaminas . [37] [38]
Un antagonista es una sustancia química que actúa dentro del cuerpo para reducir la actividad fisiológica de otra sustancia química (como un opiáceo); especialmente uno que se opone a la acción sobre el sistema nervioso de una droga o sustancia que se encuentra naturalmente en el cuerpo al combinarse con su receptor nervioso y bloquearlo. [sesenta y cinco]
Hay dos tipos principales de antagonistas: antagonistas de acción directa y antagonistas de acción indirecta:
Un fármaco antagonista es aquel que se une (o se une) a un sitio llamado receptor sin activar ese receptor para producir una respuesta biológica. Por tanto se dice que no tiene actividad intrínseca. Un antagonista también puede denominarse "bloqueador" del receptor porque bloquea el efecto de un agonista en el sitio. Por lo tanto, los efectos farmacológicos de un antagonista tienen como resultado impedir que los agonistas del sitio receptor correspondiente (p. ej., fármacos, hormonas, neurotransmisores) se unan a él y lo activen. Los antagonistas pueden ser "competitivos" o "irreversibles".
Un antagonista competitivo compite con un agonista por unirse al receptor. A medida que aumenta la concentración del antagonista, la unión del agonista se inhibe progresivamente, dando como resultado una disminución de la respuesta fisiológica. Una alta concentración de un antagonista puede inhibir completamente la respuesta. Sin embargo, esta inhibición puede revertirse aumentando la concentración del agonista, ya que el agonista y el antagonista compiten por la unión al receptor. Por lo tanto, los antagonistas competitivos pueden caracterizarse por desplazar la relación dosis-respuesta del agonista hacia la derecha. En presencia de un antagonista competitivo, se necesita una mayor concentración del agonista para producir la misma respuesta observada en ausencia del antagonista.
Un antagonista irreversible se une tan fuertemente al receptor que hace que el receptor no esté disponible para unirse al agonista. Los antagonistas irreversibles pueden incluso formar enlaces químicos covalentes con el receptor. En cualquier caso, si la concentración del antagonista irreversible es suficientemente alta, el número de receptores libres que quedan para la unión del agonista puede ser tan bajo que incluso concentraciones altas del agonista no producen la respuesta biológica máxima. [66]
Si bien la ingesta de precursores de neurotransmisores aumenta la síntesis de neurotransmisores, la evidencia es contradictoria sobre si aumentan la liberación de neurotransmisores y la activación de los receptores postsinápticos. Incluso con una mayor liberación de neurotransmisores, no está claro si esto dará como resultado un aumento a largo plazo en la intensidad de la señal de los neurotransmisores, ya que el sistema nervioso puede adaptarse a cambios como el aumento de la síntesis de neurotransmisores y, por lo tanto, puede mantener una activación constante. [70] [ ¿fuente médica poco confiable? ] Algunos neurotransmisores pueden tener un papel en la depresión y existe cierta evidencia que sugiere que la ingesta de precursores de estos neurotransmisores puede ser útil en el tratamiento de la depresión leve y moderada. [70] [ ¿fuente médica poco confiable? ] [71]
La L -DOPA , un precursor de la dopamina que atraviesa la barrera hematoencefálica , se utiliza en el tratamiento de la enfermedad de Parkinson . Para los pacientes deprimidos en los que está implicada una baja actividad del neurotransmisor norepinefrina , hay poca evidencia del beneficio de la administración de precursores de neurotransmisores. La L-fenilalanina y la L-tirosina son precursoras de la dopamina , la norepinefrina y la epinefrina . Estas conversiones requieren vitamina B6 , vitamina C y S-adenosilmetionina . Algunos estudios sugieren posibles efectos antidepresivos de la L-fenilalanina y la L-tirosina, pero hay mucho espacio para más investigaciones en esta área. [70] [ ¿fuente médica poco confiable? ]
Se ha observado que la administración de L-triptófano , un precursor de la serotonina , duplica la producción de serotonina en el cerebro. Es significativamente más eficaz que un placebo en el tratamiento de la depresión leve y moderada. [70] [ ¿fuente médica poco confiable? ] Esta conversión requiere vitamina C . [25] El 5-hidroxitriptófano (5-HTP), también un precursor de la serotonina , es más eficaz que un placebo. [70] [ ¿fuente médica poco confiable? ]
Las enfermedades y trastornos también pueden afectar sistemas de neurotransmisores específicos. Los siguientes son trastornos implicados en un aumento, disminución o desequilibrio de ciertos neurotransmisores.
Dopamina :
Por ejemplo, los problemas en la producción de dopamina (principalmente en la sustancia negra ) pueden provocar la enfermedad de Parkinson , un trastorno que afecta la capacidad de una persona para moverse como quiera, provocando rigidez, temblores o temblores, y otros síntomas. Algunos estudios sugieren que tener muy poca o demasiada dopamina o problemas para usar la dopamina en las regiones del cerebro que piensan y sienten pueden desempeñar un papel en trastornos como la esquizofrenia o el trastorno por déficit de atención con hiperactividad (TDAH). La dopamina también está implicada en la adicción y el consumo de drogas, ya que la mayoría de las drogas recreativas provocan un influjo de dopamina en el cerebro (especialmente opioides y metanfetaminas ) que produce una sensación placentera, razón por la cual los usuarios anhelan constantemente las drogas.
serotonina :
De manera similar, después de que algunas investigaciones sugirieran que los medicamentos que bloquean el reciclaje o la recaptación de serotonina parecían ayudar a algunas personas diagnosticadas con depresión, se teorizó que las personas con depresión podrían tener niveles de serotonina más bajos de lo normal. Aunque ampliamente popularizada, esta teoría no fue confirmada en investigaciones posteriores. [72] Por lo tanto, los inhibidores selectivos de la recaptación de serotonina (ISRS) se utilizan para aumentar las cantidades de serotonina en las sinapsis.
Glutamato :
Además, los problemas con la producción o el uso de glutamato se han relacionado sugestiva y tentativamente con muchos trastornos mentales, incluidos el autismo , el trastorno obsesivo-compulsivo (TOC), la esquizofrenia y la depresión . [73] Tener demasiado glutamato se ha relacionado con enfermedades neurológicas como la enfermedad de Parkinson , la esclerosis múltiple , la enfermedad de Alzheimer , los accidentes cerebrovasculares y la ELA (esclerosis lateral amiotrófica). [74]

Generalmente, no existen "normas" científicamente establecidas para los niveles o "equilibrios" apropiados de los diferentes neurotransmisores. En la mayoría de los casos, es pragmáticamente imposible siquiera medir los niveles de neurotransmisores en un cerebro o cuerpo en momentos distintos. Los neurotransmisores regulan la liberación de cada uno, y los desequilibrios débiles y consistentes en esta regulación mutua se relacionaron con el temperamento en personas sanas. [75] [76] [77] [78] [79] Fuertes desequilibrios o alteraciones de los sistemas de neurotransmisores se han asociado con muchas enfermedades y trastornos mentales. Estos incluyen el Parkinson, la depresión, el insomnio, el trastorno por déficit de atención e hiperactividad (TDAH), la ansiedad, la pérdida de memoria, los cambios dramáticos de peso y las adicciones. El estrés físico o emocional crónico puede contribuir a los cambios en el sistema de neurotransmisores. La genética también juega un papel en las actividades de los neurotransmisores. Además del uso recreativo, los medicamentos que interactúan directa e indirectamente con uno o más transmisores o sus receptores se recetan comúnmente para problemas psiquiátricos y psicológicos. En particular, los medicamentos que interactúan con la serotonina y la norepinefrina se recetan a pacientes con problemas como depresión y ansiedad, aunque se ha criticado ampliamente la idea de que existe mucha evidencia médica sólida que respalda tales intervenciones. [80] Los estudios han demostrado que el desequilibrio de la dopamina influye en la esclerosis múltiple y otros trastornos neurológicos. [81]
{{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace )consulte las páginas 13 y 14 de la guía
TAAR1 es un receptor de alta afinidad para METH/AMPH y DA
VMAT2 es el transportador vesicular del SNC no solo para las aminas biogénicas DA, NE, EPI, 5-HT y HIS, sino probablemente también para las trazas de aminas TYR, PEA y tironamina (THYR)... [Trazas aminérgicas ] Las neuronas del SNC de los mamíferos serían identificables como neuronas que expresan VMAT2 para su almacenamiento y la enzima biosintética descarboxilasa de aminoácidos aromáticos (AADC).
Diferentes subregiones del VTA reciben aportes glutamatérgicos de la corteza prefrontal, aportes orexinérgicos del hipotálamo lateral, aportes colinérgicos y también glutamatérgicos y GABAérgicos del núcleo tegmental laterodorsal y del núcleo pedunculopontino, aportes noradrenérgicos del locus ceruleus, aportes serotoninérgicos de los núcleos del rafe, y aportes GABAérgicos del núcleo accumbens y pálido ventral.
Las fibras NE descendentes modulan las señales de dolor aferentes. ... El locus ceruleus (LC), que se encuentra en el piso del cuarto ventrículo en el puente rostral, contiene más del 50% de todas las neuronas noradrenérgicas del cerebro; inerva tanto el prosencéfalo (p. ej., proporciona prácticamente todo el NE a la corteza cerebral) como regiones del tronco encefálico y la médula espinal. ... Las otras neuronas noradrenérgicas del cerebro se encuentran en grupos sueltos de células en el tronco del encéfalo, incluidas las regiones tegmentales laterales. Estas neuronas se proyectan en gran medida dentro del tronco del encéfalo y la médula espinal. La NE, junto con la 5HT, la ACh, la histamina y la orexina, es un regulador fundamental del ciclo de sueño-vigilia y de los niveles de excitación. ... La activación de LC también puede aumentar la ansiedad... La estimulación de los receptores β-adrenérgicos en la amígdala da como resultado una memoria mejorada para los estímulos codificados bajo una emoción negativa fuerte... La epinefrina ocurre solo en una pequeña cantidad de neuronas centrales, todas ubicadas en el médula. La epinefrina participa en funciones viscerales, como el control de la respiración.
El sistema de activación reticular ascendente (ARAS) es responsable de un estado de vigilia sostenido. ... La proyección talámica está dominada por neuronas colinérgicas que se originan en el núcleo tegmental pedunculopontino de la protuberancia y el mesencéfalo (PPT) y el núcleo tegmental laterodorsal de la protuberancia y los núcleos del mesencéfalo (LDT) [17, 18]. La proyección hipotalámica involucra neuronas noradrenérgicas del locus coeruleus (LC) y neuronas serotoninérgicas de los núcleos dorsal y mediano del rafe (DR), que pasan a través del hipotálamo lateral y alcanzan los axones del núcleo tuberomamilar histaminérgico (NMT), formando juntas una vía que se extiende hacia el prosencéfalo, la corteza y el hipocampo. La excitación cortical también aprovecha las neuronas dopaminérgicas de la sustancia negra (SN), el área de los tegmentos ventrales (VTA) y el área gris periacueductal (PAG). Menos neuronas colinérgicas de la protuberancia y el mesencéfalo envían proyecciones al prosencéfalo a lo largo de la vía ventral, sin pasar por el tálamo [19, 20].
El ARAS es una estructura compleja que consta de varios circuitos diferentes, incluidas las cuatro vías monoaminérgicas... La vía de la norepinefrina se origina en el locus ceruleus (LC) y los núcleos relacionados del tronco encefálico; las neuronas serotoninérgicas también se originan en los núcleos del rafe dentro del tronco del encéfalo; las neuronas dopaminérgicas se originan en el área tegmental ventral (ATV); y la vía histaminérgica se origina en las neuronas del núcleo tuberomamilar (NTM) del hipotálamo posterior. Como se analizó en el capítulo 6, estas neuronas se proyectan ampliamente por todo el cerebro a partir de conjuntos restringidos de cuerpos celulares. La noradrenalina, la serotonina, la dopamina y la histamina tienen funciones moduladoras complejas y, en general, favorecen la vigilia. El PT en el tronco del encéfalo también es un componente importante del ARAS. La actividad de las neuronas colinérgicas PT (células REM) promueve el sueño REM. Durante la vigilia, las células REM activadas son inhibidas por un subconjunto de neuronas ARAS de norepinefrina y serotonina llamadas células REM desactivadas.
Las neuronas del SNc inervan densamente el cuerpo estriado dorsal, donde desempeñan un papel fundamental en el aprendizaje y la ejecución de programas motores. Las neuronas del VTA inervan el cuerpo estriado ventral (núcleo accumbens), el bulbo olfatorio, la amígdala, el hipocampo, la corteza prefrontal orbital y medial y la corteza cingulada. Las neuronas VTA DA desempeñan un papel fundamental en la motivación, el comportamiento relacionado con la recompensa, la atención y múltiples formas de memoria. ... Así, actuando en diversos campos terminales, la dopamina confiere prominencia motivacional ("querer") a la recompensa misma o a las señales asociadas (región de la capa del núcleo accumbens), actualiza el valor otorgado a diferentes objetivos a la luz de esta nueva experiencia (región prefrontal orbital corteza), ayuda a consolidar múltiples formas de memoria (amígdala e hipocampo), y codifica nuevos programas motores que facilitarán la obtención de esta recompensa en el futuro (región central del núcleo accumbens y estriado dorsal). ... DA tiene múltiples acciones en la corteza prefrontal. Promueve el "control cognitivo" del comportamiento: la selección y seguimiento exitoso del comportamiento para facilitar el logro de las metas elegidas. Los aspectos del control cognitivo en los que la DA desempeña un papel incluyen la memoria de trabajo, la capacidad de mantener información "en línea" para guiar las acciones, la supresión de conductas prepotentes que compiten con las acciones dirigidas a objetivos y el control de la atención y, por tanto, la capacidad de superar las distracciones. ... Las proyecciones noradrenérgicas del LC interactúan con las proyecciones dopaminérgicas del VTA para regular el control cognitivo. ...
Trabajos anteriores han demostrado que la estimulación optogenética de los MSN D1 promueve la recompensa, mientras que la estimulación de los MSN D2 produce aversión.
Estudios recientes sobre la autoadministración intracraneal de neuroquímicos (fármacos) encontraron que las ratas aprenden a autoadministrarse varios fármacos en las estructuras de dopamina mesolímbicas: el área tegmental ventral posterior, el núcleo accumbens de la capa medial y el tubérculo olfatorio medial. ... En la década de 1970 se reconoció que el tubérculo olfatorio contiene un componente estriado, que está lleno de neuronas espinosas medias GABAérgicas que reciben aportes glutamatérgicos de regiones corticales y aportes dopaminérgicos del VTA y se proyectan hacia el pálido ventral al igual que el núcleo accumbens.
Dentro del cerebro, la histamina es sintetizada exclusivamente por neuronas con sus cuerpos celulares en el núcleo tuberomamilar (NMT) que se encuentra dentro del hipotálamo posterior. Hay aproximadamente 64.000 neuronas histaminérgicas por lado en los seres humanos. Estas células se proyectan por todo el cerebro y la médula espinal. Las áreas que reciben proyecciones especialmente densas incluyen la corteza cerebral, el hipocampo, el neostriatum, el núcleo accumbens, la amígdala y el hipotálamo. ... Si bien la función mejor caracterizada del sistema de histamina en el cerebro es la regulación del sueño y la excitación, la histamina también participa en el aprendizaje y la memoria... También parece que la histamina participa en la regulación de la alimentación y el equilibrio energético.
[El] rafe dorsal inerva preferentemente la corteza cerebral, el tálamo, las regiones estriatales (caudado-putamen y núcleo accumbens) y los núcleos dopaminérgicos del mesencéfalo (p. ej., la sustancia negra y el área tegmental ventral), mientras que el rafe mediano inerva el hipocampo. tabique y otras estructuras del prosencéfalo límbico. ... está claro que la 5HT influye en el sueño, la excitación, la atención, el procesamiento de la información sensorial en la corteza cerebral y aspectos importantes de las emociones (probablemente incluyendo la agresión) y la regulación del estado de ánimo. ... Los núcleos rostrales, que incluyen el núcleo lineal, el rafe dorsal, el rafe medial y el rafe pontis, inervan la mayor parte del cerebro, incluido el cerebelo. Los núcleos caudales, que comprenden el rafe mayor, el rafe pálido y el rafe oscuro, tienen proyecciones más limitadas que terminan en el cerebelo, el tronco del encéfalo y la médula espinal.
El rafe dorsal es el sitio principal de las neuronas serotoninérgicas en el cerebro que, al igual que las neuronas noradrenérgicas, modulan de manera generalizada la función cerebral para regular el estado de activación y el estado de ánimo del organismo.
Los núcleos colinérgicos del prosencéfalo basal están compuestos por el núcleo septal medial (Ch1), el núcleo vertical de la banda diagonal (Ch2), la rama horizontal de la banda diagonal (Ch3) y el núcleo basal de Meynert (Ch4). Los núcleos colinérgicos del tronco encefálico incluyen el núcleo pedunculopontino (Ch5), el núcleo tegmental laterodorsal (Ch6), la habénula medial (Ch7) y el núcleo parabigeminal (Ch8).
{{cite book}}: |journal=ignorado ( ayuda ){{cite book}}: |journal=ignorado ( ayuda )