La metionina (símbolo Met o M ) [3] ( / m ɪ ˈ θ aɪ ə n iː n / ) [4] es un aminoácido esencial en los seres humanos.
Como precursor de otros aminoácidos no esenciales como la cisteína y la taurina , compuestos versátiles como el SAM-e y el importante antioxidante glutatión , la metionina desempeña un papel fundamental en el metabolismo y la salud de muchas especies, incluidos los humanos. La metionina también participa en la angiogénesis y en diversos procesos relacionados con la transcripción del ADN, la expresión epigenética y la regulación genética.
La metionina fue aislada por primera vez en 1921 por John Howard Mueller . [5] Está codificado por el codón AUG. Fue nombrado por Satoru Odake en 1925, como una abreviatura de su descripción estructural ácido 2-amino-4-( metiltio ) butanoico . [6]
La metionina (abreviada como Met o M ; codificada por el codón AUG) es un α- aminoácido que se utiliza en la biosíntesis de proteínas . Contiene un grupo carboxilo (que está en la forma desprotonada −COO − en condiciones de pH biológico ), un grupo amino (que está en la forma protonada −NH+
3forma en condiciones biológicas de pH) ubicado en posición α con respecto al grupo carboxilo, y una cadena lateral S -metil tioéter , clasificándolo como un aminoácido alifático no polar .
En los genes nucleares de eucariotas y Archaea , la metionina está codificada por el codón de inicio , lo que significa que indica el inicio de la región codificante y es el primer aminoácido producido en un polipéptido naciente durante la traducción del ARNm . [7]
La cisteína y la metionina son los dos aminoácidos proteinogénicos que contienen azufre . Excluyendo las pocas excepciones en las que la metionina puede actuar como sensor redox (por ejemplo, sulfóxido de metionina [8] ), los residuos de metionina no tienen una función catalítica. [9] Esto contrasta con los residuos de cisteína, donde el grupo tiol tiene un papel catalítico en muchas proteínas. [9] Sin embargo, el tioéter dentro de la metionina tiene un papel estructural menor debido al efecto de estabilidad de las interacciones S/π entre el átomo de azufre de la cadena lateral y los aminoácidos aromáticos en un tercio de todas las estructuras proteicas conocidas. [9] Esta falta de un papel importante se refleja en experimentos en los que se observa poco efecto en proteínas donde la metionina se reemplaza por norleucina , un aminoácido de cadena lateral de hidrocarburo lineal que carece de tioéter. [10] Se ha conjeturado que la norleucina estaba presente en las primeras versiones del código genético, pero la metionina se introdujo en la versión final del código genético debido a que se utiliza en el cofactor S -adenosilmetionina (SAM-e). [11] Esta situación no es única y puede haber ocurrido con la ornitina y la arginina. [12]
La metionina es uno de los dos únicos aminoácidos codificados por un único codón (AUG) en el código genético estándar ( el triptófano , codificado por UGG, es el otro). Como reflejo del origen evolutivo de su codón, los otros codones AUN codifican isoleucina , que también es un aminoácido hidrofóbico. En el genoma mitocondrial de varios organismos, incluidos metazoos y levaduras , el codón AUA también codifica metionina. En el código genético estándar, AUA codifica isoleucina y el ARNt respectivo ( ileX en Escherichia coli ) utiliza la base inusual lisidina (bacterias) o agmatidina (arqueas) para discriminar AUG. [13] [14]
El codón de metionina AUG es también el codón de inicio más común. Un codón de "inicio" es un mensaje para un ribosoma que señala el inicio de la traducción de proteínas a partir de ARNm cuando el codón AUG está en una secuencia de consenso de Kozak . Como consecuencia, la metionina a menudo se incorpora en la posición N -terminal de las proteínas en eucariotas y arqueas durante la traducción, aunque puede eliminarse mediante modificación postraduccional . En las bacterias , el derivado N -formilmetionina se utiliza como aminoácido inicial.
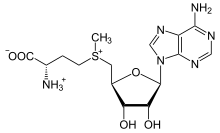
El derivado de metionina S -adenosilmetionina (SAM-e) es un cofactor que sirve principalmente como donante de metilo . SAM-e está compuesto por una molécula de adenosilo (a través del carbono 5') unida al azufre de la metionina, lo que lo convierte en un catión sulfonio (es decir, tres sustituyentes y carga positiva). El azufre actúa como un ácido de Lewis suave (es decir, donante/electrófilo) que permite que el grupo S -metilo se transfiera a un sistema de oxígeno, nitrógeno o aromático, a menudo con la ayuda de otros cofactores como la cobalamina (vitamina B 12 en humanos). Algunas enzimas utilizan SAM-e para iniciar una reacción radical; éstas se denominan enzimas radicales SAM-e . Como resultado de la transferencia del grupo metilo se obtiene S -adenosilhomocisteína. En las bacterias, esto se regenera mediante metilación o se recupera eliminando la adenina y la homocisteína, dejando que el compuesto dihidroxipentandiona se convierta espontáneamente en autoinductor-2 , que se excreta como producto de desecho o señal de quórum.
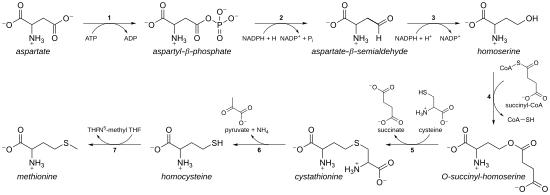
Como aminoácido esencial, la metionina no se sintetiza de novo en humanos y otros animales, que deben ingerir metionina o proteínas que contienen metionina. En plantas y microorganismos, la biosíntesis de metionina pertenece a la familia de los aspartatos , junto con la treonina y la lisina (vía diaminopimelato , pero no vía α-aminoadipato ). La columna vertebral principal se deriva del ácido aspártico , mientras que el azufre puede provenir de cisteína , metanotiol o sulfuro de hidrógeno . [9]
La vía que utiliza cisteína se denomina " vía de transsulfuración ", mientras que la vía que utiliza sulfuro de hidrógeno (o metanotiol) se denomina "vía de sulfurilación directa".
La cisteína se produce de manera similar, es decir, puede prepararse a partir de una serina activada y de homocisteína ("ruta de transsulfurilación inversa") o de sulfuro de hidrógeno ("ruta de sulfurilación directa"); la serina activada es generalmente O -acetilserina (a través de CysK o CysM en E. coli ), pero en Aeropyrum pernix y algunas otras arqueas se utiliza O -fosfoserina. [15] CysK y CysM son homólogos, pero pertenecen al clado tipo III del pliegue PLP.
Enzimas implicadas en la ruta de transsulfurilación de la biosíntesis de metionina de E. coli :

Aunque los mamíferos no pueden sintetizar metionina, aún pueden usarla en una variedad de vías bioquímicas:
La metionina se convierte en S -adenosilmetionina (SAM-e) mediante (1) metionina adenosiltransferasa .
SAM-e sirve como donante de metilo en muchas (2) reacciones de metiltransferasa y se convierte en S -adenosilhomocisteína (SAH).
(3) Cisteína adenosilhomocisteinasa .
La metionina se puede regenerar a partir de homocisteína mediante (4) metionina sintasa en una reacción que requiere vitamina B 12 como cofactor .
La homocisteína también se puede remetilar utilizando glicina betaína ( N , N , N -trimetilglicina, TMG) a metionina a través de la enzima betaína-homocisteína metiltransferasa (EC2.1.1.5, BHMT). La BHMT constituye hasta el 1,5% de toda la proteína soluble del hígado, y la evidencia reciente sugiere que puede tener una mayor influencia en la homeostasis de la metionina y la homocisteína que la metionina sintasa.
La homocisteína se puede convertir en cisteína.
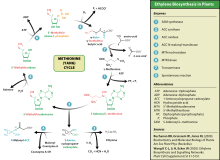
Este aminoácido también es utilizado por las plantas para la síntesis de etileno . El proceso se conoce como ciclo Yang o ciclo de la metionina.
La degradación de la metionina se ve afectada en las siguientes enfermedades metabólicas :
La síntesis industrial combina acroleína , metanotiol y cianuro, lo que produce la hidantoína . [16] La metionina racémica también se puede sintetizar a partir de ftalimidomalonato de dietilo y sodio mediante alquilación con sulfuro de cloroetilmetilo (ClCH 2 CH 2 SCH 3 ) seguida de hidrólisis y descarboxilación. Véase también Metanol. [17]
La suplementación con metionina beneficia a quienes padecen intoxicación por cobre. [18]
El consumo excesivo de metionina, el donante del grupo metilo en la metilación del ADN , está relacionado con el crecimiento del cáncer en varios estudios. [19] [20]
La Junta de Alimentos y Nutrición del Instituto de Medicina de EE. UU. estableció cantidades dietéticas recomendadas (CDR) para los aminoácidos esenciales en 2002. Para metionina combinada con cisteína, para adultos de 19 años o más, 19 mg/kg de peso corporal/día. [21]
Esto se traduce en aproximadamente 1,33 gramos por día para una persona de 70 kilogramos.
Se pueden encontrar niveles elevados de metionina en los huevos, la carne y el pescado; semillas de sésamo, nueces de Brasil y algunas semillas de otras plantas; y granos de cereales . La mayoría de frutas y verduras contienen muy poca. La mayoría de las legumbres , aunque ricas en proteínas, tienen un bajo contenido de metionina. Las proteínas sin metionina adecuada no se consideran proteínas completas . [22] Por esa razón, a veces se agrega metionina racémica como ingrediente a los alimentos para mascotas . [23]
La pérdida de metionina se ha relacionado con el envejecimiento senil del cabello. Su falta provoca una acumulación de peróxido de hidrógeno en los folículos pilosos , una reducción de la eficacia de la tirosinasa y una pérdida gradual del color del cabello. [24] La metionina aumenta la concentración intracelular de glutatión , promoviendo así la defensa celular mediada por antioxidantes y la regulación redox. También protege las células contra la pérdida de células nigrales inducida por la dopamina al unirse a metabolitos oxidativos. [25]
La metionina es un intermediario en la biosíntesis de cisteína , carnitina , taurina , lecitina , fosfatidilcolina y otros fosfolípidos . La conversión inadecuada de metionina puede provocar aterosclerosis [26] debido a la acumulación de homocisteína .
La DL -metionina a veces se administra como suplemento a los perros; Ayuda a reducir las posibilidades de que se formen cálculos renales en los perros. También se sabe que la metionina aumenta la excreción urinaria de quinidina al acidificar la orina. Los antibióticos aminoglucósidos utilizados para tratar las infecciones del tracto urinario funcionan mejor en condiciones alcalinas y la acidificación de la orina por el uso de metionina puede reducir su eficacia. Si un perro sigue una dieta que acidifica la orina, no se debe utilizar metionina. [27]
La metionina está permitida como complemento del alimento orgánico para aves de corral según el programa orgánico certificado de EE. UU. [28]
La metionina se puede utilizar como una opción pesticida no tóxica contra las orugas gigantes de cola de golondrina , que son una plaga grave para los cultivos de naranja. [29]