
La hidrogenación es una reacción química entre el hidrógeno molecular (H2 ) y otro compuesto o elemento, generalmente en presencia de un catalizador como níquel , paladio o platino . El proceso se emplea comúnmente para reducir o saturar compuestos orgánicos . La hidrogenación generalmente constituye la adición de pares de átomos de hidrógeno a una molécula, a menudo un alqueno . Se requieren catalizadores para que la reacción sea utilizable; la hidrogenación no catalítica tiene lugar solo a temperaturas muy altas. La hidrogenación reduce los enlaces dobles y triples en los hidrocarburos . [1]
La hidrogenación tiene tres componentes: el sustrato insaturado , el hidrógeno (o fuente de hidrógeno) y, invariablemente, un catalizador . La reacción de reducción se lleva a cabo a diferentes temperaturas y presiones según el sustrato y la actividad del catalizador.
Los mismos catalizadores y condiciones que se utilizan para las reacciones de hidrogenación también pueden conducir a la isomerización de los alquenos de cis a trans . Este proceso es de gran interés porque la tecnología de hidrogenación genera la mayor parte de las grasas trans en los alimentos. Una reacción en la que se rompen los enlaces mientras se agrega hidrógeno se llama hidrogenólisis , una reacción que puede ocurrir en los enlaces carbono-carbono y carbono-heteroátomo ( oxígeno , nitrógeno o halógeno ). Algunas hidrogenaciones de enlaces polares van acompañadas de hidrogenólisis.
Para la hidrogenación, la fuente obvia de hidrógeno es el propio gas H2 , que normalmente está disponible comercialmente dentro del medio de almacenamiento de un cilindro presurizado. El proceso de hidrogenación a menudo utiliza más de 1 atmósfera de H2 , generalmente transportado desde los cilindros y, a veces, aumentado por "bombas de refuerzo". El hidrógeno gaseoso se produce industrialmente a partir de hidrocarburos mediante el proceso conocido como reformado con vapor . [2] Para muchas aplicaciones, el hidrógeno se transfiere desde moléculas donadoras como el ácido fórmico , el isopropanol y el dihidroantraceno . [3] Estos donantes de hidrógeno experimentan una deshidrogenación a, respectivamente, dióxido de carbono , acetona y antraceno . Estos procesos se denominan hidrogenaciones por transferencia .
Una característica importante de las hidrogenaciones de alquenos y alquinos , tanto las versiones catalizadas de forma homogénea como heterogénea, es que la adición de hidrógeno se produce mediante la " adición syn ", en la que el hidrógeno entra desde el lado menos impedido. [4] Esta reacción se puede realizar en una variedad de grupos funcionales diferentes .
Con raras excepciones, el H 2 no reacciona frente a compuestos orgánicos en ausencia de catalizadores metálicos. El sustrato insaturado se quimisorbe sobre el catalizador, y la mayoría de los sitios quedan cubiertos por el sustrato. En catalizadores heterogéneos, el hidrógeno forma hidruros de superficie (MH) desde los que se pueden transferir hidrógenos al sustrato quimisorbendido. El platino , el paladio , el rodio y el rutenio forman catalizadores muy activos, que funcionan a temperaturas y presiones de H 2 más bajas . También se han desarrollado catalizadores de metales no preciosos, especialmente los basados en níquel (como el níquel Raney y el níquel Urushibara ) como alternativas económicas, pero a menudo son más lentos o requieren temperaturas más altas. La compensación es la actividad (velocidad de reacción) frente al coste del catalizador y el coste del aparato necesario para el uso de altas presiones. Nótese que las hidrogenaciones catalizadas por níquel Raney requieren altas presiones: [8] [9]
Los catalizadores se suelen clasificar en dos grandes clases: homogéneos y heterogéneos . Los catalizadores homogéneos se disuelven en el disolvente que contiene el sustrato insaturado. Los catalizadores heterogéneos son sólidos que se suspenden en el mismo disolvente que el sustrato o se tratan con sustrato gaseoso.
A continuación se indican algunos catalizadores homogéneos conocidos. Se trata de complejos de coordinación que activan tanto el sustrato insaturado como el H 2 . Lo más habitual es que estos complejos contengan metales del grupo del platino, especialmente Rh e Ir.

Los catalizadores homogéneos también se utilizan en la síntesis asimétrica mediante la hidrogenación de sustratos proquirales. Una demostración temprana de este enfoque fue la hidrogenación catalizada por Rh de enamidas como precursores del fármaco L-DOPA . [10] Para lograr la reducción asimétrica, estos catalizadores se vuelven quirales mediante el uso de ligandos de difosfina quirales. [11] La hidrogenación catalizada por rodio también se ha utilizado en la producción del herbicida S-metolaclor, que utiliza un ligando de tipo Josiphos (llamado Xyliphos). [12] En principio, la hidrogenación asimétrica puede ser catalizada por catalizadores heterogéneos quirales, [13] pero este enfoque sigue siendo más una curiosidad que una tecnología útil.
Los catalizadores heterogéneos para la hidrogenación son más comunes industrialmente. En la industria, los catalizadores de hidrogenación de metales preciosos se depositan a partir de una solución como un polvo fino sobre el soporte, que es un material barato, voluminoso, poroso, generalmente granular, como carbón activado , alúmina , carbonato de calcio o sulfato de bario . [14] Por ejemplo, el platino sobre carbón se produce por reducción de ácido cloroplatínico in situ en carbón. Ejemplos de estos catalizadores son rutenio al 5% sobre carbón activado o platino al 1% sobre alúmina. Los catalizadores de metales básicos, como el níquel Raney , suelen ser mucho más baratos y no necesitan un soporte. Además, en el laboratorio, todavía se utilizan catalizadores de metales preciosos sin soporte (masivos) como el negro de platino , a pesar del costo.
Al igual que en los catalizadores homogéneos, la actividad se ajusta a través de cambios en el entorno que rodea al metal, es decir, la esfera de coordinación . Las diferentes caras de un catalizador heterogéneo cristalino muestran actividades distintas, por ejemplo. Esto se puede modificar mezclando metales o utilizando diferentes técnicas de preparación. De manera similar, los catalizadores heterogéneos se ven afectados por sus soportes.
En muchos casos, las modificaciones altamente empíricas implican "venenos" selectivos. Por lo tanto, se puede utilizar un catalizador cuidadosamente elegido para hidrogenar algunos grupos funcionales sin afectar a otros, como la hidrogenación de alquenos sin tocar anillos aromáticos, o la hidrogenación selectiva de alquinos a alquenos utilizando el catalizador de Lindlar . Por ejemplo, cuando el catalizador paladio se coloca sobre sulfato de bario y luego se trata con quinolina , el catalizador resultante reduce los alquinos solo hasta convertirlos en alquenos. El catalizador de Lindlar se ha aplicado a la conversión de fenilacetileno a estireno . [15]
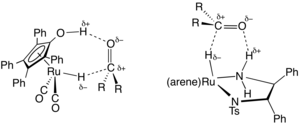
La hidrogenación por transferencia utiliza moléculas donadoras de hidrógeno distintas del H2 molecular . Estos donadores de hidrógeno "sacrificiosos", que también pueden servir como solventes para la reacción, incluyen hidrazina , ácido fórmico y alcoholes como el isopropanol. [18]
En síntesis orgánica , la hidrogenación por transferencia es útil para la hidrogenación asimétrica de sustratos polares insaturados, como cetonas , aldehídos e iminas , mediante el empleo de catalizadores quirales .
Los sustratos polares como los nitrilos se pueden hidrogenar electroquímicamente , utilizando solventes próticos y equivalentes reductores como fuente de hidrógeno. [19]
La adición de hidrógeno a enlaces dobles o triples en hidrocarburos es un tipo de reacción redox que puede ser termodinámicamente favorable. Por ejemplo, la adición de hidrógeno al eteno tiene un cambio de energía libre de Gibbs de -101 kJ·mol −1 , que es altamente exotérmica . [11] En la hidrogenación de aceites vegetales y ácidos grasos, por ejemplo, el calor liberado, alrededor de 25 kcal por mol (105 kJ/mol), es suficiente para elevar la temperatura del aceite en 1,6–1,7 °C por cada caída del índice de yodo .
Sin embargo, la velocidad de reacción de la mayoría de las reacciones de hidrogenación es insignificante en ausencia de catalizadores. El mecanismo de hidrogenación de alquenos y alquinos catalizada por metales se ha estudiado ampliamente. [20] En primer lugar, el marcaje isotópico con deuterio confirma la regioquímica de la adición:
En sólidos, el mecanismo aceptado es el mecanismo de Horiuti- Polanyi : [21] [22]
En el tercer paso, el grupo alquilo puede revertirse a alqueno, que puede desprenderse del catalizador. En consecuencia, el contacto con un catalizador de hidrogenación permite la isomerización cis-trans . El alqueno trans puede reasociarse a la superficie y experimentar hidrogenación. Estos detalles se revelan en parte utilizando D2 ( deuterio), porque los alquenos recuperados a menudo contienen deuterio.
En el caso de los sustratos aromáticos, la primera hidrogenación es la más lenta. El producto de este paso es un ciclohexadieno, que se hidrogena rápidamente y rara vez se detecta. De manera similar, el ciclohexeno se reduce normalmente a ciclohexano.
En muchos procesos de hidrogenación homogénea, [23] el metal se une a ambos componentes para dar un complejo intermedio alqueno-metal(H) 2 . Se supone que la secuencia general de reacciones es la siguiente o una secuencia relacionada de pasos:
La isomerización de alquenos suele acompañar a la hidrogenación. Esta importante reacción secundaria se produce mediante la eliminación del intermediario hidruro de alquilo con beta-hidruro : [24]
A menudo, la olefina liberada es trans.
La hidrogenación de nitrógeno para producir amoníaco se lleva a cabo a gran escala mediante el proceso Haber-Bosch , [25] que consume aproximadamente el 1% del suministro energético mundial .
El oxígeno puede hidrogenarse parcialmente para producir peróxido de hidrógeno , aunque este proceso no se ha comercializado. Una dificultad es evitar que los catalizadores desencadenen la descomposición del peróxido de hidrógeno para formar agua. [26] [27]
La hidrogenación catalítica tiene diversos usos industriales. La hidrogenación industrial más frecuente se basa en catalizadores heterogéneos. [2]
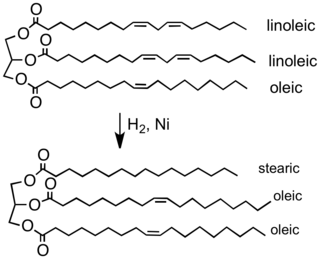
La industria alimentaria hidrogena los aceites vegetales para convertirlos en grasas sólidas o semisólidas que se pueden utilizar en cremas para untar, caramelos, productos horneados y otros productos como la margarina . Los aceites vegetales están hechos de ácidos grasos poliinsaturados (que tienen más de un doble enlace carbono-carbono). La hidrogenación elimina algunos de estos dobles enlaces. [28]
En los procesos petroquímicos, la hidrogenación se utiliza para convertir alquenos y aromáticos en alcanos saturados (parafinas) y cicloalcanos (naftenos), que son menos tóxicos y menos reactivos. En relación con los combustibles líquidos que se almacenan a veces durante largos períodos en el aire, los hidrocarburos saturados exhiben propiedades de almacenamiento superiores. Por otro lado, los alquenos tienden a formar hidroperóxidos , que pueden formar gomas que interfieren con el equipo de manipulación de combustible. Por ejemplo, la trementina mineral suele hidrogenarse. El hidrocraqueo de residuos pesados en diésel es otra aplicación. En los procesos de isomerización y reformado catalítico , se mantiene cierta presión de hidrógeno para hidrogenar el coque formado en el catalizador y evitar su acumulación.
La hidrogenación es un medio útil para convertir compuestos insaturados en derivados saturados. Los sustratos incluyen no solo alquenos y alquinos, sino también aldehídos, iminas y nitrilos, [29] que se convierten en los compuestos saturados correspondientes, es decir, alcoholes y aminas. Por lo tanto, los alquil aldehídos, que se pueden sintetizar con el proceso oxo a partir de monóxido de carbono y un alqueno, se pueden convertir en alcoholes. Por ejemplo, el 1-propanol se produce a partir de propionaldehído, producido a partir de eteno y monóxido de carbono. El xilitol , un poliol , se produce por hidrogenación del azúcar xilosa , un aldehído. Las aminas primarias se pueden sintetizar por hidrogenación de nitrilos , mientras que los nitrilos se sintetizan fácilmente a partir de cianuro y un electrófilo adecuado. Por ejemplo, la diamina de isoforona, un precursor del monómero de poliuretano diisocianato de isoforona , se produce a partir de nitrilo de isoforona mediante una hidrogenación/aminación reductora en tándem de nitrilo con amoníaco, en donde la hidrogenación convierte tanto el nitrilo en una amina como la imina formada a partir del aldehído y el amoníaco en otra amina.
La primera hidrogenación fue la de la adición de hidrógeno al oxígeno catalizada por platino en la lámpara de Döbereiner , un dispositivo comercializado ya en 1823. El químico francés Paul Sabatier es considerado el padre del proceso de hidrogenación. En 1897, basándose en el trabajo anterior de James Boyce , un químico estadounidense que trabajaba en la fabricación de productos de jabón, descubrió que trazas de níquel catalizaban la adición de hidrógeno a moléculas de hidrocarburos gaseosos en lo que ahora se conoce como el proceso Sabatier . Por este trabajo, Sabatier compartió el Premio Nobel de Química de 1912. Wilhelm Normann recibió una patente en Alemania en 1902 y en Gran Bretaña en 1903 por la hidrogenación de aceites líquidos, que fue el comienzo de lo que ahora es una industria mundial. El proceso Haber-Bosch , de importancia comercial , descrito por primera vez en 1905, implica la hidrogenación de nitrógeno. En el proceso Fischer-Tropsch , descrito en 1922, el monóxido de carbono, que se deriva fácilmente del carbón, se hidrogena para obtener combustibles líquidos.
En 1922, Voorhees y Adams describieron un aparato para realizar la hidrogenación a presiones superiores a una atmósfera. [30] El agitador Parr, el primer producto que permitía la hidrogenación utilizando presiones y temperaturas elevadas, se comercializó en 1926 basándose en la investigación de Voorhees y Adams y sigue utilizándose ampliamente. En 1924, Murray Raney desarrolló una forma de níquel en polvo fino, que se utiliza ampliamente para catalizar reacciones de hidrogenación como la conversión de nitrilos en aminas o la producción de margarina.
En la década de 1930, Calvin descubrió que los complejos de cobre (II) oxidaban el H 2 . La década de 1960 fue testigo del desarrollo de catalizadores homogéneos bien definidos utilizando complejos de metales de transición, por ejemplo, el catalizador de Wilkinson (RhCl(PPh 3 ) 3 ). Poco después, se descubrió que el Rh y el Ir catiónicos catalizaban la hidrogenación de alquenos y carbonilos. [31] En la década de 1970, se demostró la hidrogenación asimétrica en la síntesis de L-DOPA , y la década de 1990 vio la invención de la hidrogenación asimétrica de Noyori . [32] El desarrollo de la hidrogenación homogénea estuvo influenciado por el trabajo iniciado en las décadas de 1930 y 1940 en el proceso oxo y la polimerización de Ziegler-Natta .
Para la mayoría de los propósitos prácticos, la hidrogenación requiere un catalizador metálico. Sin embargo, la hidrogenación puede proceder de algunos donantes de hidrógeno sin catalizadores, siendo los donantes de hidrógeno ilustrativos la diimida y el isopropóxido de aluminio , este último ilustrado por la reducción de Meerwein-Ponndorf-Verley . Algunos sistemas catalíticos sin metales se han investigado en la investigación académica. Uno de estos sistemas para la reducción de cetonas consiste en terc -butanol y terc-butóxido de potasio y temperaturas muy altas. [33] La reacción que se muestra a continuación describe la hidrogenación de benzofenona :
Un estudio de cinética química [34] encontró que esta reacción es de primer orden en los tres reactivos, lo que sugiere un estado de transición cíclico de 6 miembros .
Otro sistema de hidrogenación sin metales se basa en el compuesto fosfina - borano 1 , que se ha denominado par de Lewis frustrado . Acepta reversiblemente dihidrógeno a temperaturas relativamente bajas para formar el borato de fosfonio 2, que puede reducir iminas impedidas simples . [35]
Se ha informado que la reducción de nitrobenceno a anilina está catalizada por fulereno , su monoanión, hidrógeno atmosférico y luz ultravioleta. [36]
El químico de laboratorio actual tiene tres opciones principales de equipos de hidrogenación:
La forma original y todavía comúnmente practicada de hidrogenación en laboratorios de enseñanza, este proceso generalmente se efectúa agregando catalizador sólido a un matraz de fondo redondo con reactivo disuelto que ha sido evacuado usando nitrógeno o gas argón y sellando la mezcla con un sello de goma penetrable. Luego se suministra gas hidrógeno desde un globo lleno de H2 . La mezcla trifásica resultante se agita para promover la mezcla. La absorción de hidrógeno se puede monitorear, lo que puede ser útil para monitorear el progreso de una hidrogenación. Esto se logra utilizando un tubo graduado que contiene un líquido coloreado, generalmente sulfato de cobre acuoso o con medidores para cada recipiente de reacción.
Dado que muchas reacciones de hidrogenación, como la hidrogenólisis de grupos protectores y la reducción de sistemas aromáticos , se desarrollan de forma extremadamente lenta a temperatura y presión atmosféricas, los sistemas presurizados son populares. En estos casos, se añade el catalizador a una solución de reactivo bajo una atmósfera inerte en un recipiente a presión . El hidrógeno se añade directamente desde un cilindro o una fuente de hidrógeno incorporada en el laboratorio, y la suspensión presurizada se agita mecánicamente para proporcionar agitación, o se utiliza una cesta giratoria. [37] Los avances recientes en la tecnología de electrólisis han llevado al desarrollo de generadores de hidrógeno de alta presión, que generan hidrógeno hasta 1400 psi (100 bar) a partir del agua. También se puede utilizar calor, ya que la presión compensa la reducción asociada en la solubilidad del gas.
La hidrogenación por flujo se ha convertido en una técnica popular en el laboratorio y, cada vez más, a escala de proceso. Esta técnica implica hacer fluir continuamente una corriente diluida de reactivo disuelto sobre un catalizador de lecho fijo en presencia de hidrógeno. Mediante el uso de tecnología de cromatografía líquida de alto rendimiento establecida , esta técnica permite la aplicación de presiones desde la atmosférica hasta 1450 psi (100 bar). También se pueden utilizar temperaturas elevadas. En el laboratorio, los sistemas utilizan una gama de catalizadores preenvasados que eliminan la necesidad de pesar y filtrar los catalizadores pirofóricos .
La hidrogenación catalítica se realiza en un reactor de flujo de tapón tubular con un catalizador soportado. Las presiones y temperaturas suelen ser altas, aunque esto depende del catalizador. La carga de catalizador suele ser mucho menor que en la hidrogenación por lotes en el laboratorio, y se añaden varios promotores al metal, o se utilizan metales mixtos, para mejorar la actividad, la selectividad y la estabilidad del catalizador. El uso de níquel es común a pesar de su baja actividad, debido a su bajo costo en comparación con los metales preciosos.
Los reactores de inducción de gas-líquido (hidrogenadores) también se utilizan para llevar a cabo la hidrogenación catalítica. [38]
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ); Volúmenes recopilados , vol. 5, pág. 743.