El genoma humano es un conjunto completo de secuencias de ácido nucleico para humanos , codificadas como ADN dentro de los 23 pares de cromosomas en los núcleos celulares y en una pequeña molécula de ADN que se encuentra dentro de las mitocondrias individuales . Generalmente se tratan por separado como genoma nuclear y genoma mitocondrial . [2] Los genomas humanos incluyen tanto secuencias de ADN que codifican proteínas como varios tipos de ADN que no codifican proteínas . Esta última es una categoría diversa que incluye ADN que codifica ARN no traducido, como el ARN ribosómico , ARN de transferencia , ribozimas , ARN nucleares pequeños y varios tipos de ARN reguladores . También incluye promotores y sus elementos reguladores de genes asociados , ADN que desempeña funciones estructurales y replicativas, como regiones de andamiaje , telómeros , centrómeros y orígenes de replicación , además de un gran número de elementos transponibles , ADN viral insertado , pseudogenes no funcionales y genes simples. Secuencias muy repetitivas . Los intrones constituyen un gran porcentaje del ADN no codificante . Parte de este ADN no codificante es ADN basura no funcional , como los pseudogenes, pero no existe un consenso firme sobre la cantidad total de ADN basura.
Los genomas humanos haploides , que están contenidos en las células germinales (las células gametas del óvulo y el espermatozoide creadas en la fase de meiosis de la reproducción sexual antes de la fertilización ) constan de 3.054.815.472 pares de bases de ADN (si se utiliza el cromosoma X), [3] mientras que los genomas diploides femeninos ( que se encuentran en las células somáticas ) tienen el doble de contenido de ADN.
Si bien existen diferencias significativas entre los genomas de los individuos humanos (del orden del 0,1% debido a variantes de un solo nucleótido [4] y del 0,6% cuando se consideran los indeles ), [5] estas son considerablemente menores que las diferencias entre los humanos y sus seres más cercanos. parientes vivos, los bonobos y los chimpancés (~1,1% de variantes fijas de un solo nucleótido [6] y 4% si se incluyen los indeles). [7] El tamaño en los pares de bases también puede variar; la longitud de los telómeros disminuye después de cada ronda de replicación del ADN .
Aunque la secuencia del genoma humano se ha determinado completamente mediante la secuenciación del ADN en 2022 (incluida la metilación ), [3] aún no se comprende completamente. La mayoría de los genes , pero no todos, han sido identificados mediante una combinación de enfoques bioinformáticos y experimentales de alto rendimiento , pero aún queda mucho trabajo por hacer para dilucidar aún más las funciones biológicas de sus productos proteicos y de ARN (en particular, la anotación del código CHM13v2 completo). .0 la secuencia aún está en curso [8] ).
En 2003, los científicos informaron de la secuenciación del 85% de todo el genoma humano, pero en 2020 todavía faltaba al menos el 8%. [ cita necesaria ] En 2021, los científicos informaron haber secuenciado el genoma femenino completo (es decir, sin el cromosoma Y). [9] Esta secuencia identificó 19.969 secuencias codificantes de proteínas , que representan aproximadamente el 1,5% del genoma, y 63.494 genes en total, la mayoría de ellos genes de ARN no codificantes . [3] El genoma consta de secuencias reguladoras de ADN , LINE , SINE , intrones y secuencias para las que aún no se ha determinado ninguna función . El cromosoma Y humano , que consta de 62.460.029 pares de bases de una línea celular diferente y que se encuentra en todos los varones, se secuenció por completo en enero de 2022. [10] [11]
En 2023, se publicó un borrador de referencia del pangenoma humano. [12] Se basa en 47 genomas de personas de variada etnia. [12] Hay planes en marcha para una referencia mejorada que capture aún más biodiversidad a partir de una muestra aún más amplia. [12]
Las primeras secuencias del genoma humano fueron publicadas en forma de borrador casi completo en febrero de 2001 por el Proyecto Genoma Humano [13] y Celera Corporation . [14] La finalización del esfuerzo de secuenciación del Proyecto Genoma Humano se anunció en 2004 con la publicación de un borrador de secuencia del genoma, dejando solo 341 espacios en la secuencia, que representan ADN altamente repetitivo y otro que no se pudo secuenciar con la tecnología disponible en ese momento. . [15] El genoma humano fue el primero de todos los vertebrados en ser secuenciado casi completamente y, a partir de 2018, los genomas diploides de más de un millón de humanos individuales se habían determinado mediante secuenciación de próxima generación . [dieciséis]
Estos datos se utilizan en todo el mundo en ciencias biomédicas , antropología , ciencia forense y otras ramas de la ciencia. Estos estudios genómicos han dado lugar a avances en el diagnóstico y tratamiento de enfermedades y a nuevos conocimientos en muchos campos de la biología, incluida la evolución humana . [ cita necesaria ]
En 2018, el número total de genes se había elevado a al menos 46 831, [17] más otros 2300 genes de microARN . [18] Una encuesta de población de 2018 encontró otros 300 millones de bases del genoma humano que no estaban en la secuencia de referencia. [19] Antes de la adquisición de la secuencia completa del genoma, las estimaciones del número de genes humanos oscilaban entre 50.000 y 140.000 (con vaguedad ocasional sobre si estas estimaciones incluían genes no codificantes de proteínas). [20] A medida que mejoraron la calidad de la secuencia del genoma y los métodos para identificar genes codificadores de proteínas, [15] el recuento de genes codificadores de proteínas reconocidos se redujo a 19.000-20.000. [21]
En junio de 2016, los científicos anunciaron formalmente HGP-Write , un plan para sintetizar el genoma humano. [22] [23]
En 2022, el consorcio Telomere-to-Telomere (T2T) informó la secuencia completa de un genoma femenino humano, [3] llenando todos los vacíos en el cromosoma X (2020) y los 22 autosomas (mayo de 2021). [3] [24] Las partes no secuenciadas previamente contienen genes de respuesta inmune que ayudan a adaptarse y sobrevivir a las infecciones, así como genes que son importantes para predecir la respuesta a los medicamentos . [25] La secuencia completa del genoma humano también proporcionará una mejor comprensión de la formación humana como organismo individual y cómo los humanos varían entre sí y entre otras especies. [25]
Aunque la "finalización" del proyecto del genoma humano se anunció en 2001, [26] seguían existiendo cientos de lagunas, y entre un 5% y un 10% de la secuencia total seguía sin determinarse. La información genética que faltaba se encontraba principalmente en regiones heterocromáticas repetitivas y cerca de los centrómeros y telómeros , pero también en algunas regiones eucromáticas que codifican genes . [27] Quedaban 160 espacios eucromáticos en 2015 cuando se determinaron las secuencias que abarcaban otras 50 regiones anteriormente no secuenciadas. [28] Recién en 2020 se determinó la primera secuencia verdaderamente completa de telómero a telómero de un cromosoma humano, concretamente del cromosoma X. [29] La primera secuencia completa de telómero a telómero de un cromosoma autosómico humano, el cromosoma 8 , se produjo un año después. [30] El genoma humano completo (sin cromosoma Y) se publicó en 2021, mientras que con cromosoma Y en enero de 2022. [3] [9] [31]
En 2023, se publicó un borrador de referencia del pangenoma humano. [12] Se basa en 47 genomas de personas de variada etnia. [12] Hay planes en marcha para una referencia mejorada que capture aún más biodiversidad a partir de una muestra aún más amplia. [12]
La longitud total del genoma humano de referencia no representa la secuencia de ningún individuo específico. El genoma está organizado en 22 cromosomas pares, denominados autosomas , más el par 23 de cromosomas sexuales (XX) en la mujer y (XY) en el hombre. Todos estos cromosomas son grandes moléculas de ADN lineales contenidas dentro del núcleo celular. La versión actual del genoma humano de referencia incluye una copia de cada uno de los autosomas más una copia de los dos cromosomas sexuales (X e Y). La cantidad total de ADN es de 3,1 mil millones de pares de bases (3,1 Mb). [32]
La versión actual del genoma humano de referencia contiene casi 20.000 genes codificadores de proteínas y alrededor de 26.000 genes no codificantes. Es un hecho ampliamente aceptado que existen alrededor de 20.000 genes que codifican proteínas. Los genes no codificantes realizan varias funciones celulares. [33] [34] [35] [36] Hay menos acuerdo sobre el número total de genes no codificantes porque algunos autores creen que muchas de las transcripciones no tienen una función. [37]
El contenido del genoma humano se divide comúnmente en secuencias de ADN codificantes y no codificantes. El ADN codificante se define como aquellas secuencias que pueden transcribirse en ARNm y traducirse en proteínas durante el ciclo de vida humano; estas secuencias ocupan sólo una pequeña fracción del genoma (<2%). El ADN no codificante está formado por todas aquellas secuencias (aproximadamente el 98% del genoma) que no se utilizan para codificar proteínas. [ cita necesaria ]
Parte del ADN no codificante contiene genes para moléculas de ARN con importantes funciones biológicas ( ARN no codificante , por ejemplo, ARN ribosómico y ARN de transferencia ). La exploración de la función y el origen evolutivo del ADN no codificante es un objetivo importante de la investigación genómica contemporánea, incluido el proyecto ENCODE (Encyclopedia of DNA Elements), cuyo objetivo es estudiar todo el genoma humano, utilizando una variedad de herramientas experimentales cuyos resultados son indicativos. de actividad molecular. Sin embargo, se discute si la actividad molecular (transcripción de ADN en ARN) por sí sola implica que el ARN producido tiene una función biológica significativa, ya que los experimentos han demostrado que el ADN aleatorio no funcional también reclutará de manera reproducible factores de transcripción que resultarán en la transcripción en ARN no funcional. [38]
No hay consenso sobre qué constituye un elemento "funcional" en el genoma, ya que los genetistas, los biólogos evolutivos y los biólogos moleculares emplean definiciones y métodos diferentes. [39] [40] Debido a la ambigüedad en la terminología, han surgido diferentes escuelas de pensamiento. [41] En las definiciones evolutivas, el ADN "funcional", ya sea codificante o no codificante, contribuye a la aptitud del organismo y, por lo tanto, se mantiene mediante presión evolutiva negativa, mientras que el ADN "no funcional" no tiene ningún beneficio para el organismo. y por lo tanto está bajo presión selectiva neutral. Este tipo de ADN se ha descrito como ADN basura [42] [43] En las definiciones genéticas, el ADN "funcional" está relacionado con la forma en que los segmentos de ADN se manifiestan por fenotipo y "no funcional" está relacionado con los efectos de pérdida de función en el organismo. [39] En las definiciones bioquímicas, el ADN "funcional" se relaciona con secuencias de ADN que especifican productos moleculares (por ejemplo, ARN no codificantes) y actividades bioquímicas con funciones mecanicistas en la regulación de genes o genoma (es decir, secuencias de ADN que impactan la actividad a nivel celular, como el tipo de célula, la condición y procesos moleculares). [44] [39] No existe consenso en la literatura sobre la cantidad de ADN funcional ya que, dependiendo de cómo se entienda "función", se han estimado rangos de hasta el 90% del genoma humano que probablemente sea ADN no funcional (ADN basura). ) [45] hasta un 80% del genoma probablemente sea funcional. [46] También es posible que el ADN basura adquiera una función en el futuro y, por lo tanto, pueda desempeñar un papel en la evolución, [47] pero es probable que esto ocurra sólo en muy raras ocasiones. [42] Finalmente, el ADN que es perjudicial para el organismo y está bajo presión selectiva negativa se llama ADN basura. [43]
Debido a que el ADN no codificante supera en gran medida al ADN codificante, el concepto de genoma secuenciado se ha convertido en un concepto analítico más centrado que el concepto clásico de gen codificante de ADN. [48] [49]
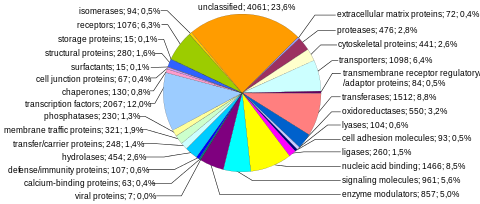
Las secuencias codificantes de proteínas representan el componente más estudiado y mejor comprendido del genoma humano. Estas secuencias conducen en última instancia a la producción de todas las proteínas humanas , aunque varios procesos biológicos (por ejemplo, reordenamientos del ADN y empalmes alternativos de pre-ARNm ) pueden conducir a la producción de muchas más proteínas únicas que la cantidad de genes que codifican proteínas. La capacidad modular completa de codificación de proteínas del genoma está contenida dentro del exoma y consta de secuencias de ADN codificadas por exones que pueden traducirse en proteínas. Debido a su importancia biológica y al hecho de que constituye menos del 2% del genoma, la secuenciación del exoma fue el primer hito importante del Proyecto Genoma Humano. [ cita necesaria ]
Número de genes codificadores de proteínas . Unas 20.000 proteínas humanas han sido anotadas en bases de datos como Uniprot . [51] Históricamente, las estimaciones del número de genes de proteínas han variado ampliamente, alcanzando hasta 2.000.000 a finales de la década de 1960, [52] pero varios investigadores señalaron a principios de la década de 1970 que la carga mutacional estimada de mutaciones nocivas establecía un límite superior de aproximadamente 40.000 para el número total de loci funcionales (esto incluye genes codificantes de proteínas y genes no codificantes funcionales). [53] El número de genes que codifican proteínas humanas no es significativamente mayor que el de muchos organismos menos complejos, como el gusano redondo y la mosca de la fruta . Esta diferencia puede ser el resultado del uso extensivo de empalme de pre-ARNm alternativo en humanos, que proporciona la capacidad de construir una gran cantidad de proteínas modulares mediante la incorporación selectiva de exones.
Capacidad de codificación de proteínas por cromosoma . Los genes que codifican proteínas se distribuyen de manera desigual en los cromosomas, desde unas pocas docenas hasta más de 2000, con una densidad genética especialmente alta dentro de los cromosomas 1, 11 y 19. Cada cromosoma contiene varias regiones ricas y pobres en genes, que puede estar correlacionado con bandas cromosómicas y contenido de GC . [54] La importancia de estos patrones no aleatorios de densidad genética no se comprende bien. [55]
Tamaño de los genes codificadores de proteínas . El tamaño de los genes que codifican proteínas dentro del genoma humano muestra una enorme variabilidad. Por ejemplo, el gen de la histona H1a (HIST1HIA) es relativamente pequeño y simple, carece de intrones y codifica un ARNm de 781 nucleótidos de longitud que produce una proteína de 215 aminoácidos a partir de su marco de lectura abierto de 648 nucleótidos . La distrofina (DMD) fue el gen codificador de proteínas más grande en el genoma humano de referencia de 2001, abarcando un total de 2,2 millones de nucleótidos, [56] mientras que un metanálisis sistemático más reciente de datos actualizados del genoma humano identificó un gen codificador de proteínas aún más grande, RBFOX1 (proteína de unión a ARN, homólogo 1 de fox-1), que abarca un total de 2,47 millones de nucleótidos. [57] La titina (TTN) tiene la secuencia codificante más larga (114.414 nucleótidos), el mayor número de exones (363), [56] y el exón único más largo (17.106 nucleótidos). Según lo estimado en base a un conjunto seleccionado de genes codificadores de proteínas en todo el genoma, el tamaño medio es de 26.288 nucleótidos (media = 66.577), el tamaño medio del exón, 133 nucleótidos (media = 309), el número medio de exones, 8 ( media = 11), y la proteína codificada mediana tiene 425 aminoácidos (media = 553) de longitud. [57]
El ADN no codificante se define como todas las secuencias de ADN dentro de un genoma que no se encuentran dentro de los exones que codifican proteínas y, por lo tanto, nunca están representadas dentro de la secuencia de aminoácidos de las proteínas expresadas. Según esta definición, más del 98% de los genomas humanos están compuestos de ncDNA. [ cita necesaria ]
Se han identificado numerosas clases de ADN no codificante, incluidos genes para ARN no codificante (p. ej., ARNt y ARNr), pseudogenes, intrones, regiones no traducidas de ARNm, secuencias de ADN reguladoras, secuencias de ADN repetitivas y secuencias relacionadas con elementos genéticos móviles. [ cita necesaria ]
Numerosas secuencias que se incluyen dentro de los genes también se definen como ADN no codificante. Estos incluyen genes para ARN no codificante (por ejemplo, ARNt, ARNr) y componentes no traducidos de genes codificadores de proteínas (por ejemplo, intrones y regiones 5' y 3' no traducidas de ARNm).
Las secuencias codificantes de proteínas (específicamente, exones codificantes ) constituyen menos del 1,5% del genoma humano. [26] Además, alrededor del 26% del genoma humano son intrones . [59] Aparte de los genes (exones e intrones) y las secuencias reguladoras conocidas (8-20%), el genoma humano contiene regiones de ADN no codificante. La cantidad exacta de ADN no codificante que desempeña un papel en la fisiología celular ha sido objeto de acalorados debates. Un análisis del proyecto ENCODE indica que el 80% de todo el genoma humano se transcribe, se une a proteínas reguladoras o está asociado con alguna otra actividad bioquímica. [60]
Sin embargo, sigue siendo controvertido si toda esta actividad bioquímica contribuye a la fisiología celular o si una parte sustancial de ella es el resultado del ruido transcripcional y bioquímico, que el organismo debe filtrar activamente. [61] [37] Excluyendo las secuencias codificantes de proteínas, los intrones y las regiones reguladoras, gran parte del ADN no codificante está compuesto por: Muchas secuencias de ADN que no desempeñan un papel en la expresión génica tienen funciones biológicas importantes. Los estudios de genómica comparada indican que alrededor del 5% del genoma contiene secuencias de ADN no codificante que están altamente conservadas , a veces en escalas de tiempo que representan cientos de millones de años, lo que implica que estas regiones no codificantes están bajo una fuerte presión evolutiva y selección purificadora . [62]
Muchas de estas secuencias regulan la estructura de los cromosomas limitando las regiones de formación de heterocromatina y regulando características estructurales de los cromosomas, como los telómeros y centrómeros . Otras regiones no codificantes sirven como orígenes de la replicación del ADN . Finalmente, varias regiones se transcriben en ARN no codificante funcional que regula la expresión de genes codificadores de proteínas (por ejemplo [63] ), la traducción y estabilidad del ARNm (ver miARN ), la estructura de la cromatina (incluidas las modificaciones de histonas , por ejemplo [64] ), el ADN. metilación (por ejemplo [65] ), recombinación de ADN (por ejemplo [66] ) y regulación cruzada de otros ARN no codificantes (por ejemplo [67] ). También es probable que muchas regiones no codificantes transcritas no cumplan ninguna función y que esta transcripción sea producto de la actividad de la ARN polimerasa no específica . [61]
Los pseudogenes son copias inactivas de genes codificadores de proteínas, a menudo generados por duplicación de genes , que han dejado de funcionar debido a la acumulación de mutaciones inactivadoras. El número de pseudogenes en el genoma humano es del orden de 13.000, [68] y en algunos cromosomas es casi el mismo que el número de genes funcionales que codifican proteínas. La duplicación de genes es un mecanismo importante a través del cual se genera nuevo material genético durante la evolución molecular .
Por ejemplo, la familia de genes del receptor olfativo es uno de los ejemplos mejor documentados de pseudogenes en el genoma humano. Más del 60 por ciento de los genes de esta familia son pseudogenes no funcionales en humanos. En comparación, sólo el 20 por ciento de los genes de la familia de genes del receptor olfativo del ratón son pseudogenes. Las investigaciones sugieren que esta es una característica específica de cada especie, ya que los primates más estrechamente relacionados tienen proporcionalmente menos pseudogenes. Este descubrimiento genético ayuda a explicar el sentido del olfato menos agudo en los humanos en comparación con otros mamíferos. [69]
Las moléculas de ARN no codificantes desempeñan muchas funciones esenciales en las células, especialmente en las numerosas reacciones de síntesis de proteínas y procesamiento de ARN . El ARN no codificante incluye ARNt , ARN ribosómico , microARN , ARNsn y otros genes de ARN no codificante, incluidos aproximadamente 60.000 ARN no codificantes de largo (lncRNA). [60] [70] [71] [72] Aunque el número de genes de lncRNA informados continúa aumentando y el número exacto en el genoma humano aún no se ha definido, se argumenta que muchos de ellos no son funcionales. [73]
Muchos ncRNA son elementos críticos en la regulación y expresión de genes. El ARN no codificante también contribuye a la epigenética, la transcripción, el empalme del ARN y la maquinaria de traducción. El papel del ARN en la regulación genética y las enfermedades ofrece un nuevo nivel potencial de complejidad genómica inexplorada. [74]
Además de las moléculas de ARNnc codificadas por genes discretos, las transcripciones iniciales de genes codificantes de proteínas suelen contener secuencias extensas no codificantes, en forma de intrones , regiones 5' no traducidas (5'-UTR) y regiones 3' no traducidas. (3'-UTR). En la mayoría de los genes codificadores de proteínas del genoma humano, la longitud de las secuencias de intrones es de 10 a 100 veces la longitud de las secuencias de exones. [ cita necesaria ]
El genoma humano tiene muchas secuencias reguladoras diferentes que son cruciales para controlar la expresión genética . Las estimaciones conservadoras indican que estas secuencias constituyen el 8% del genoma, [75] sin embargo, las extrapolaciones del proyecto ENCODE dan que el 20 [76] -40% [77] del genoma es una secuencia reguladora de genes. Algunos tipos de ADN no codificante son "interruptores" genéticos que no codifican proteínas, pero sí regulan cuándo y dónde se expresan los genes (llamados potenciadores ). [78]
Las secuencias regulatorias se conocen desde finales de los años 1960. [79] La primera identificación de secuencias reguladoras en el genoma humano se basó en la tecnología del ADN recombinante. [80] Más tarde, con la llegada de la secuenciación genómica, la identificación de estas secuencias podría inferirse mediante conservación evolutiva. La rama evolutiva entre los primates y el ratón , por ejemplo, se produjo hace 70 a 90 millones de años. [81] Por lo tanto, las comparaciones por computadora de secuencias genéticas que identifican secuencias no codificantes conservadas serán una indicación de su importancia en tareas como la regulación genética. [82]
Se han secuenciado otros genomas con la misma intención de ayudar a los métodos guiados por la conservación, por ejemplo el genoma del pez globo . [83] Sin embargo, las secuencias reguladoras desaparecen y vuelven a evolucionar durante la evolución a un ritmo elevado. [84] [85] [86]
A partir de 2012, los esfuerzos se han desplazado hacia la búsqueda de interacciones entre el ADN y las proteínas reguladoras mediante la técnica ChIP-Seq , o espacios donde el ADN no está empaquetado por histonas ( sitios hipersensibles a la ADNasa ), los cuales indican dónde hay secuencias reguladoras activas en el tipo de célula investigada. [75]
Las secuencias repetitivas de ADN comprenden aproximadamente el 50% del genoma humano. [87]
Aproximadamente el 8% del genoma humano consta de conjuntos de ADN en tándem o repeticiones en tándem, secuencias repetidas de baja complejidad que tienen múltiples copias adyacentes (por ejemplo, "CAGCAGCAG..."). [88] Las secuencias en tándem pueden tener longitudes variables, desde dos nucleótidos hasta decenas de nucleótidos. Estas secuencias son muy variables, incluso entre individuos estrechamente relacionados, por lo que se utilizan para pruebas de ADN genealógico y análisis forense de ADN . [89]
Las secuencias repetidas de menos de diez nucleótidos (por ejemplo, la repetición de dinucleótido (AC) n ) se denominan secuencias de microsatélites. Entre las secuencias de microsatélites, las repeticiones de trinucleótidos son de particular importancia, ya que a veces ocurren dentro de las regiones codificantes de genes para proteínas y pueden conducir a trastornos genéticos. Por ejemplo, la enfermedad de Huntington resulta de una expansión de la repetición de trinucleótido (CAG) n dentro del gen de Huntingtina en el cromosoma 4 humano. Los telómeros (los extremos de los cromosomas lineales) terminan con una repetición de hexanucleótido microsatélite de la secuencia (TTAGGG) n . [ cita necesaria ]
Las repeticiones en tándem de secuencias más largas (conjuntos de secuencias repetidas de 10 a 60 nucleótidos de longitud) se denominan minisatélites . [90]
Los elementos genéticos transponibles , secuencias de ADN que pueden replicarse e insertar copias de sí mismas en otras ubicaciones dentro del genoma del huésped, son un componente abundante en el genoma humano. El linaje de transposones más abundante, Alu , tiene alrededor de 50.000 copias activas [91] y puede insertarse en regiones intragénicas e intergénicas. [92] Otro linaje, LINE-1, tiene alrededor de 100 copias activas por genoma (el número varía entre personas). [93] Junto con reliquias no funcionales de transposones antiguos, representan más de la mitad del ADN humano total. [94] A veces llamados "genes saltarines", los transposones han desempeñado un papel importante en la escultura del genoma humano. Algunas de estas secuencias representan retrovirus endógenos , copias de ADN de secuencias virales que se han integrado permanentemente en el genoma y ahora se transmiten a las generaciones siguientes.
Los elementos móviles dentro del genoma humano se pueden clasificar en retrotransposones LTR (8,3% del genoma total), SINE (13,1% del genoma total), incluidos elementos Alu , LINE (20,4% del genoma total), SVA (SINE- VNTR -Alu) y Transposones de ADN de clase II (2,9% del genoma total).
Con la excepción de los gemelos idénticos, todos los humanos muestran una variación significativa en las secuencias de ADN genómico. El genoma humano de referencia (HRG) se utiliza como secuencia de referencia estándar.
Hay varios puntos importantes sobre el genoma humano de referencia:
El Consorcio de Referencia del Genoma es responsable de actualizar el HRG. La versión 38 se publicó en diciembre de 2013. [95]
La mayoría de los estudios sobre la variación genética humana se han centrado en los polimorfismos de un solo nucleótido (SNP), que son sustituciones en bases individuales a lo largo de un cromosoma. La mayoría de los análisis estiman que los SNP se encuentran en 1 de cada 1000 pares de bases, en promedio, en el genoma humano eucromatico , aunque no se presentan con una densidad uniforme. De ahí se sigue la afirmación popular de que "todos somos, independientemente de la raza , genéticamente iguales en un 99,9%", [96] aunque esto sería algo matizado por la mayoría de los genetistas. Por ejemplo, ahora se cree que una fracción mucho mayor del genoma está involucrada en la variación del número de copias . [97] El Proyecto Internacional HapMap está llevando a cabo un esfuerzo de colaboración a gran escala para catalogar las variaciones de SNP en el genoma humano . [ cita necesaria ]
Los loci genómicos y la longitud de ciertos tipos de pequeñas secuencias repetitivas son muy variables de persona a persona, lo cual es la base de las tecnologías de huellas dactilares de ADN y pruebas de paternidad de ADN . También se cree que las porciones heterocromáticas del genoma humano, que suman varios cientos de millones de pares de bases, son bastante variables dentro de la población humana (son tan repetitivas y tan largas que no pueden secuenciarse con precisión con la tecnología actual). Estas regiones contienen pocos genes y no está claro si algún efecto fenotípico significativo resulta de la variación típica en las repeticiones o la heterocromatina.
La mayoría de las mutaciones genómicas importantes en las células germinales de los gametos probablemente den como resultado embriones inviables; sin embargo, varias enfermedades humanas están relacionadas con anomalías genómicas a gran escala. El síndrome de Down , el síndrome de Turner y varias otras enfermedades son el resultado de la falta de disyunción de cromosomas completos. Las células cancerosas frecuentemente tienen aneuploidía de cromosomas y brazos cromosómicos, aunque no se ha establecido una relación de causa y efecto entre aneuploidía y cáncer.
Mientras que una secuencia del genoma enumera el orden de cada base de ADN en un genoma, un mapa del genoma identifica los puntos de referencia. Un mapa del genoma es menos detallado que una secuencia del genoma y ayuda a navegar por el genoma. [98] [99]
Un ejemplo de mapa de variación es el HapMap desarrollado por el Proyecto Internacional HapMap . El HapMap es un mapa de haplotipos del genoma humano, "que describirá los patrones comunes de variación de la secuencia del ADN humano". [100] Cataloga los patrones de variaciones a pequeña escala en el genoma que involucran letras o bases de ADN individuales.
Los investigadores publicaron el primer mapa basado en secuencias de variación estructural a gran escala en todo el genoma humano en la revista Nature en mayo de 2008. [101] [102] Las variaciones estructurales a gran escala son diferencias en el genoma entre personas que van desde unos pocos miles a unos pocos millones de bases de ADN; algunos son ganancias o pérdidas de tramos de secuencia del genoma y otros aparecen como reordenamientos de tramos de secuencia. Estas variaciones incluyen diferencias en el número de copias que tienen los individuos de un gen particular, deleciones, translocaciones e inversiones.
La variación estructural se refiere a variantes genéticas que afectan segmentos más grandes del genoma humano, a diferencia de las mutaciones puntuales . A menudo, las variantes estructurales (SV) se definen como variantes de 50 pares de bases (pb) o más, como deleciones, duplicaciones, inserciones, inversiones y otros reordenamientos. Alrededor del 90% de las variantes estructurales son deleciones no codificantes, pero la mayoría de las personas tienen más de mil de este tipo de deleciones; el tamaño de las eliminaciones varía desde docenas de pares de bases hasta decenas de miles de pb. [103] En promedio, los individuos portan ~3 variantes estructurales raras que alteran las regiones codificantes, por ejemplo, eliminan exones . Alrededor del 2% de las personas portan variantes estructurales ultrararas a escala de megabase, especialmente reordenamientos. Es decir, millones de pares de bases pueden estar invertidos dentro de un cromosoma; Ultrararos significa que sólo se encuentran en individuos o en miembros de sus familias y, por lo tanto, han surgido muy recientemente. [103]
Los polimorfismos de un solo nucleótido (SNP) no ocurren de manera homogénea en todo el genoma humano. De hecho, existe una enorme diversidad en la frecuencia de SNP entre genes, lo que refleja diferentes presiones selectivas sobre cada gen, así como diferentes tasas de mutación y recombinación en todo el genoma. Sin embargo, los estudios sobre SNP están sesgados hacia regiones codificantes; es poco probable que los datos generados a partir de ellos reflejen la distribución general de SNP en todo el genoma. Por lo tanto, el protocolo del Consorcio SNP se diseñó para identificar los SNP sin sesgo hacia las regiones codificantes y los 100.000 SNP del Consorcio generalmente reflejan la diversidad de secuencias en los cromosomas humanos. El Consorcio SNP pretende ampliar el número de SNP identificados en todo el genoma a 300 000 para finales del primer trimestre de 2001. [104]

Los cambios en la secuencia no codificante y los cambios sinónimos en la secuencia codificante son generalmente más comunes que los cambios no sinónimos, lo que refleja una mayor presión selectiva que reduce la diversidad en las posiciones que dictan la identidad de los aminoácidos. Los cambios transicionales son más comunes que las transversiones, y los dinucleótidos CpG muestran la tasa de mutación más alta, presumiblemente debido a la desaminación. [ cita necesaria ]
Una secuencia de genoma personal es una secuencia (casi) completa de los pares de bases químicas que forman el ADN de una sola persona. Debido a que los tratamientos médicos tienen diferentes efectos en diferentes personas debido a variaciones genéticas como los polimorfismos de un solo nucleótido (SNP), el análisis de genomas personales puede conducir a un tratamiento médico personalizado basado en genotipos individuales. [105]
La primera secuencia del genoma personal que se determinó fue la de Craig Venter en 2007. Los genomas personales no habían sido secuenciados en el Proyecto Genoma Humano público para proteger la identidad de los voluntarios que proporcionaron muestras de ADN. Esa secuencia se derivó del ADN de varios voluntarios de una población diversa. [106] Sin embargo, al principio del esfuerzo de secuenciación del genoma de Celera Genomics dirigido por Venter , se tomó la decisión de pasar de la secuenciación de una muestra compuesta al uso de ADN de un solo individuo, que luego se reveló que era el propio Venter. Así, la secuencia del genoma humano de Celera publicada en 2000 era en gran medida la de un hombre. La sustitución posterior de los primeros datos derivados de compuestos y la determinación de la secuencia diploide, que representa ambos conjuntos de cromosomas , en lugar de una secuencia haploide informada originalmente, permitió la liberación del primer genoma personal. [107] En abril de 2008, también se completó el de James Watson . En 2009, Stephen Quake publicó su propia secuencia del genoma derivada de un secuenciador de su propio diseño, el Heliscope. [108] Un equipo de Stanford dirigido por Euan Ashley publicó un marco para la interpretación médica de los genomas humanos implementado en el genoma de Quake y tomó decisiones médicas informadas sobre el genoma completo por primera vez. [109] Ese equipo amplió aún más el enfoque a la familia West, la primera familia secuenciada como parte del programa de secuenciación del genoma personal de Illumina. [110] Desde entonces se han publicado cientos de secuencias de genomas personales, [111] incluidas las de Desmond Tutu , [112] [113] y las de un paleoesquimal . [114] En 2012, se hicieron públicas las secuencias completas del genoma de dos tríos familiares entre 1092 genomas. [4] En noviembre de 2013, una familia española puso a disposición del público cuatro conjuntos de datos de exomas personales (aproximadamente el 1% del genoma) bajo una licencia de dominio público Creative Commons . [115] [116] El Proyecto Genoma Personal (iniciado en 2005) es uno de los pocos que pone a disposición del público tanto las secuencias del genoma como los fenotipos médicos correspondientes. [117] [118]
La secuenciación de genomas individuales reveló aún más niveles de complejidad genética que no se habían apreciado antes. La genómica personal ayudó a revelar el nivel significativo de diversidad en el genoma humano atribuido no sólo a los SNP sino también a las variaciones estructurales. Sin embargo, la aplicación de tales conocimientos al tratamiento de enfermedades y en el campo médico está sólo en sus inicios. [119] La secuenciación del exoma se ha vuelto cada vez más popular como herramienta para ayudar en el diagnóstico de enfermedades genéticas porque el exoma contribuye solo con el 1% de la secuencia genómica pero representa aproximadamente el 85% de las mutaciones que contribuyen significativamente a la enfermedad. [120]
En los seres humanos, los genes knockout se producen naturalmente como knockouts de genes heterocigotos u homocigotos con pérdida de función . Estos knockouts suelen ser difíciles de distinguir, especialmente dentro de entornos genéticos heterogéneos . También son difíciles de encontrar porque se producen en bajas frecuencias.

Las poblaciones con altas tasas de consanguinidad , como los países con altas tasas de matrimonios entre primos hermanos, muestran las frecuencias más altas de genes knockout homocigotos. Estas poblaciones incluyen Pakistán, Islandia y las poblaciones amish. Estas poblaciones con un alto nivel de relación con los padres han sido objeto de investigaciones de eliminación de genes en humanos que han ayudado a determinar la función de genes específicos en humanos. Al distinguir knockouts específicos, los investigadores pueden utilizar análisis fenotípicos de estos individuos para ayudar a caracterizar el gen que ha sido desactivado.

Los knockouts en genes específicos pueden causar enfermedades genéticas, potencialmente tener efectos beneficiosos o incluso no producir ningún efecto fenotípico. Sin embargo, determinar el efecto fenotípico de un knockout en humanos puede resultar un desafío. Los desafíos para caracterizar e interpretar clínicamente los knockouts incluyen la dificultad para identificar variantes de ADN, determinar la interrupción de la función de las proteínas (anotación) y considerar la influencia que tiene el mosaicismo en el fenotipo. [121]
Un estudio importante que investigó los knockouts en humanos es el estudio Pakistán sobre riesgo de infarto de miocardio. Se descubrió que los individuos que poseían un gen heterocigoto de pérdida de función para el gen APOC3 tenían triglicéridos más bajos en la sangre después de consumir una comida rica en grasas en comparación con los individuos sin la mutación. Sin embargo, los individuos que poseen genes homocigotos de pérdida de función knockout del gen APOC3 mostraron el nivel más bajo de triglicéridos en la sangre después de la prueba de carga de grasa, ya que no producen proteína APOC3 funcional. [122]
La mayoría de los aspectos de la biología humana involucran factores tanto genéticos (heredados) como no genéticos (ambientales). Alguna variación heredada influye en aspectos de nuestra biología que no son de naturaleza médica (altura, color de ojos, capacidad para saborear u oler ciertos compuestos, etc.). Además, algunos trastornos genéticos sólo causan enfermedades en combinación con los factores ambientales apropiados (como la dieta). Con estas advertencias, los trastornos genéticos pueden describirse como enfermedades clínicamente definidas causadas por la variación de la secuencia del ADN genómico. En los casos más sencillos, el trastorno puede estar asociado con una variación en un solo gen. Por ejemplo, la fibrosis quística es causada por mutaciones en el gen CFTR y es el trastorno recesivo más común en poblaciones caucásicas con más de 1300 mutaciones diferentes conocidas. [123]
Las mutaciones que causan enfermedades en genes específicos suelen ser graves en términos de función genética y, afortunadamente, son raras, por lo que los trastornos genéticos son igualmente raros individualmente. Sin embargo, dado que hay muchos genes que pueden variar para causar trastornos genéticos, en conjunto constituyen un componente importante de afecciones médicas conocidas, especialmente en medicina pediátrica. Los trastornos genéticos caracterizados molecularmente son aquellos para los cuales se ha identificado el gen causal subyacente. Actualmente hay aproximadamente 2200 trastornos de este tipo anotados en la base de datos OMIM . [123]
Los estudios de trastornos genéticos a menudo se realizan mediante estudios familiares. En algunos casos, se emplean enfoques poblacionales, particularmente en el caso de las llamadas poblaciones fundadoras, como las de Finlandia, el Canadá francés, Utah, Cerdeña, etc. El diagnóstico y el tratamiento de los trastornos genéticos generalmente los realiza un médico genetista . capacitado en genética clínica/médica. Es probable que los resultados del Proyecto Genoma Humano proporcionen una mayor disponibilidad de pruebas genéticas para trastornos relacionados con los genes y, en última instancia, un mejor tratamiento. Se puede examinar a los padres para detectar condiciones hereditarias y asesorarlos sobre las consecuencias, la probabilidad de herencia y cómo evitarla o mejorarla en sus hijos.
Hay muchos tipos diferentes de variación de la secuencia del ADN, que van desde cromosomas extras o faltantes completos hasta cambios de un solo nucleótido. Generalmente se supone que gran parte de la variación genética que ocurre naturalmente en las poblaciones humanas es fenotípicamente neutral, es decir, tiene poco o ningún efecto detectable sobre la fisiología del individuo (aunque puede haber diferencias fraccionarias en la aptitud definida a lo largo de períodos de tiempo evolutivos). Los trastornos genéticos pueden ser causados por cualquiera o todos los tipos conocidos de variación de secuencia. Para caracterizar molecularmente un nuevo trastorno genético, es necesario establecer un vínculo causal entre una variante de secuencia genómica particular y la enfermedad clínica que se está investigando. Estos estudios constituyen el ámbito de la genética molecular humana.
Con la llegada del Genoma Humano y el Proyecto Internacional HapMap , se ha vuelto factible explorar influencias genéticas sutiles en muchas enfermedades comunes como diabetes, asma, migraña, esquizofrenia, etc. Aunque se han establecido algunos vínculos causales entre variantes de secuencia genómica en genes particulares y algunas de estas enfermedades, a menudo con mucha publicidad en los medios generales, generalmente no se consideran trastornos genéticos per se ya que sus causas son complejas e involucran muchos factores genéticos y ambientales diferentes. Por lo tanto, en casos particulares puede haber desacuerdo sobre si una condición médica específica debe denominarse trastorno genético.
Otros trastornos genéticos a mencionar son el síndrome de Kallman y el síndrome de Pfeiffer (gen FGFR1), la distrofia corneal de Fuchs (gen TCF4), la enfermedad de Hirschsprung (genes RET y FECH), el síndrome de Bardet-Biedl 1 (genes CCDC28B y BBS1), el síndrome de Bardet-Biedl 10 (gen BBS10) y distrofia muscular facioescapulohumeral tipo 2 (genes D4Z4 y SMCHD1). [124]
La secuenciación del genoma ahora puede reducir el genoma a ubicaciones específicas para encontrar con mayor precisión mutaciones que resultarán en un trastorno genético. Las variantes del número de copias (CNV) y las variantes de un solo nucleótido (SNV) también se pueden detectar al mismo tiempo que la secuenciación del genoma con procedimientos de secuenciación más nuevos disponibles, llamados secuenciación de próxima generación (NGS). [125] Esto solo analiza una pequeña porción del genoma, alrededor del 1-2%. Los resultados de esta secuenciación se pueden utilizar para el diagnóstico clínico de una afección genética, incluido el síndrome de Usher , enfermedades de la retina, deficiencias auditivas, diabetes, epilepsia, enfermedad de Leigh , cánceres hereditarios, enfermedades neuromusculares, inmunodeficiencias primarias, inmunodeficiencia combinada grave (SCID) y enfermedades de las mitocondrias. [126] La NGS también se puede utilizar para identificar portadores de enfermedades antes de la concepción. Las enfermedades que se pueden detectar en esta secuenciación incluyen la enfermedad de Tay-Sachs , el síndrome de Bloom , la enfermedad de Gaucher , la enfermedad de Canavan , la disautonomía familiar , la fibrosis quística, la atrofia muscular espinal y el síndrome del X frágil . La próxima secuenciación del genoma se puede limitar para buscar específicamente enfermedades más prevalentes en determinadas poblaciones étnicas. [127]
Los estudios genómicos comparativos de genomas de mamíferos sugieren que aproximadamente el 5% del genoma humano se ha conservado mediante la evolución desde la divergencia de los linajes existentes hace aproximadamente 200 millones de años, y contiene la gran mayoría de los genes. [128] [129] El genoma del chimpancé publicado difiere del genoma humano en un 1,23% en comparaciones directas de secuencias. [130] Alrededor del 20% de esta cifra se debe a la variación dentro de cada especie, dejando solo ~1,06% de divergencia de secuencia consistente entre humanos y chimpancés en genes compartidos. [131] Sin embargo, esta diferencia nucleótido por nucleótido se ve eclipsada por la porción de cada genoma que no se comparte, incluido alrededor del 6% de los genes funcionales que son exclusivos de los humanos o los chimpancés. [132]
En otras palabras, las considerables diferencias observables entre humanos y chimpancés pueden deberse tanto o más a la variación a nivel del genoma en el número, función y expresión de los genes que a cambios en la secuencia del ADN en genes compartidos. De hecho, incluso entre los seres humanos, se ha descubierto que existe una cantidad de variación del número de copias (CNV, por sus siglas en inglés) que antes no se había apreciado y que puede representar entre el 5% y el 15% del genoma humano. En otras palabras, entre humanos podría haber +/- 500.000.000 de pares de bases de ADN, siendo algunos genes activos, otros inactivados o activos en diferentes niveles. El significado total de este hallazgo aún está por verse. En promedio, un gen codificador de proteínas humano típico difiere de su ortólogo de chimpancé en sólo dos sustituciones de aminoácidos ; casi un tercio de los genes humanos tienen exactamente la misma traducción de proteínas que sus ortólogos de chimpancé. Una diferencia importante entre los dos genomas es el cromosoma 2 humano , que es equivalente a un producto de fusión de los cromosomas 12 y 13 de chimpancé [133] (posteriormente renombrados como cromosomas 2A y 2B, respectivamente).
Los humanos hemos sufrido una pérdida extraordinaria de genes receptores olfativos durante nuestra evolución reciente, lo que explica nuestro sentido del olfato relativamente tosco en comparación con la mayoría de los demás mamíferos. La evidencia evolutiva sugiere que la aparición de la visión de los colores en los humanos y en varias otras especies de primates ha disminuido la necesidad del sentido del olfato. [134]
En septiembre de 2016, los científicos informaron que, basándose en estudios genéticos del ADN humano, todos los no africanos del mundo actual pueden rastrearse hasta una única población que salió de África hace entre 50.000 y 80.000 años. [135]
El ADN mitocondrial humano es de enorme interés para los genetistas, ya que sin duda desempeña un papel en las enfermedades mitocondriales . También arroja luz sobre la evolución humana; por ejemplo, el análisis de la variación en el genoma mitocondrial humano ha llevado a la postulación de un ancestro común reciente para todos los humanos en la línea de descendencia materna (ver Eva mitocondrial ).
Debido a la falta de un sistema para verificar errores de copia, [136] el ADN mitocondrial (ADNmt) tiene una tasa de variación más rápida que el ADN nuclear. Esta tasa de mutación 20 veces mayor permite que el ADNmt se utilice para un seguimiento más preciso de la ascendencia materna. [ cita necesaria ] Los estudios de ADNmt en poblaciones han permitido rastrear rutas migratorias antiguas, como la migración de nativos americanos de Siberia [137] o polinesios del sudeste asiático . [ cita necesaria ] También se ha utilizado para demostrar que no hay rastro de ADN de neandertal en la mezcla de genes europeos heredada a través del linaje puramente materno. [138] Debido a la forma restrictiva de herencia de todo o nada del ADNmt, este resultado (sin rastro de ADNmt de Neandertal) sería probable a menos que hubiera un gran porcentaje de ascendencia neandertal, o hubiera una fuerte selección positiva para ese ADNmt. Por ejemplo, retrocediendo 5 generaciones, sólo 1 de los 32 ancestros de una persona contribuyó al ADNmt de esa persona, por lo que si uno de estos 32 fuera neandertal puro, se espera que ~3% del ADN autosómico de esa persona sería de origen neandertal, pero tendría una probabilidad de ~97% de no tener rastros de ADNmt de Neandertal. [ cita necesaria ]
La epigenética describe una variedad de características del genoma humano que trascienden su secuencia primaria de ADN, como el empaquetado de cromatina , las modificaciones de histonas y la metilación del ADN , y que son importantes en la regulación de la expresión genética, la replicación del genoma y otros procesos celulares. Los marcadores epigenéticos fortalecen y debilitan la transcripción de ciertos genes, pero no afectan la secuencia real de nucleótidos del ADN. La metilación del ADN es una forma importante de control epigenético sobre la expresión genética y uno de los temas más estudiados en epigenética. Durante el desarrollo, el perfil de metilación del ADN humano experimenta cambios dramáticos. En las células de la línea germinal temprana, el genoma tiene niveles de metilación muy bajos. Estos niveles bajos generalmente describen genes activos. A medida que avanza el desarrollo, las etiquetas de impresión parentales conducen a una mayor actividad de metilación. [139] [140]
Los patrones epigenéticos se pueden identificar entre tejidos dentro de un individuo, así como entre los propios individuos. Los genes idénticos que tienen diferencias sólo en su estado epigenético se denominan epialelos . Los epialelos se pueden clasificar en tres categorías: aquellos directamente determinados por el genotipo de un individuo, aquellos influenciados por el genotipo y aquellos completamente independientes del genotipo. El epigenoma también está influenciado significativamente por factores ambientales. La dieta, las toxinas y las hormonas impactan el estado epigenético. Los estudios sobre manipulación dietética han demostrado que las dietas deficientes en metilo están asociadas con la hipometilación del epigenoma. Dichos estudios establecen que la epigenética es una interfaz importante entre el medio ambiente y el genoma. [141]
{{cite journal}}: Citar diario requiere |journal=( ayuda )Operacionalmente, los elementos funcionales se definen como características de secuencia discretas y ordenadas linealmente que especifican productos moleculares (por ejemplo, genes codificadores de proteínas o ARN no codificantes) o actividades bioquímicas con funciones mecanicistas en la regulación de genes o genoma (por ejemplo, promotores transcripcionales o potenciadores).
Estos datos nos permitieron asignar funciones bioquímicas para el 80% del genoma, en particular fuera de las regiones codificantes de proteínas bien estudiadas..
La proporción de segmentos pequeños (50 a 100 pb) en el genoma de los mamíferos que se encuentran bajo selección (purificadora) se puede estimar en aproximadamente el 5%.
Esta proporción es mucho mayor de lo que puede explicarse únicamente por secuencias codificantes de proteínas, lo que implica que el genoma contiene muchas características adicionales (como regiones no traducidas, elementos reguladores, genes no codificantes de proteínas y elementos estructurales cromosómicos) bajo selección para función biológica. .
Calculamos que la divergencia de nucleótidos de todo el genoma entre humanos y chimpancés es del 1,23%, lo que confirma resultados recientes de estudios más limitados.
Estimamos que el polimorfismo representa entre el 14% y el 22% de la tasa de divergencia observada y, por lo tanto, que la divergencia fija es ~1,06% o menos.
Nuestros resultados implican que los humanos y los chimpancés difieren en al menos un 6% (1.418 de 22.000 genes) en su complemento de genes, lo que contrasta marcadamente con la tan citada diferencia del 1,5% entre secuencias de nucleótidos ortólogas.
El cromosoma 2 humano resultó de una fusión de dos cromosomas ancestrales que permanecieron separados en el linaje de los chimpancés.
La secuenciación a gran escala del genoma del chimpancé es ahora inminente.
Nuestros hallazgos sugieren que el deterioro del repertorio olfativo se produjo concomitantemente con la adquisición de una visión de color tricromática completa en primates.