La espectrometría de masas ( MS ) es una técnica analítica que se utiliza para medir la relación masa-carga de iones . Los resultados se presentan como un espectro de masas , una gráfica de intensidad en función de la relación masa-carga. La espectrometría de masas se utiliza en muchos campos diferentes y se aplica tanto a muestras puras como a mezclas complejas.
Un espectro de masas es un tipo de gráfico de la señal de iones en función de la relación masa-carga. Estos espectros se utilizan para determinar la firma elemental o isotópica de una muestra, las masas de partículas y de moléculas , y para dilucidar la identidad química o estructura de moléculas y otros compuestos químicos .

En un procedimiento típico de MS, se ioniza una muestra, que puede ser sólida, líquida o gaseosa, por ejemplo, bombardeándola con un haz de electrones . Esto puede hacer que algunas de las moléculas de la muestra se rompan en fragmentos cargados positivamente o simplemente se carguen positivamente sin fragmentarse. Luego, estos iones (fragmentos) se separan según su relación masa-carga, por ejemplo acelerándolos y sometiéndolos a un campo eléctrico o magnético: los iones con la misma relación masa-carga sufrirán la misma cantidad de deflexión. . [1] Los iones se detectan mediante un mecanismo capaz de detectar partículas cargadas, como un multiplicador de electrones . Los resultados se muestran como espectros de la intensidad de la señal de los iones detectados en función de la relación masa-carga. Los átomos o moléculas en la muestra se pueden identificar correlacionando masas conocidas (por ejemplo, una molécula completa) con las masas identificadas o mediante un patrón de fragmentación característico.
.jpg/440px-Early_Mass_Spectrometer_(replica).jpg)
En 1886, Eugen Goldstein observó rayos en descargas de gas a baja presión que se alejaban del ánodo y a través de canales en un cátodo perforado , en dirección opuesta a la dirección de los rayos catódicos cargados negativamente (que viajan del cátodo al ánodo). Goldstein llamó a estos rayos anódicos cargados positivamente "Kanalstrahlen"; La traducción estándar de este término al inglés es " rayos de canal ". Wilhelm Wien descubrió que los fuertes campos eléctricos o magnéticos desviaban los rayos del canal y, en 1899, construyó un dispositivo con campos eléctricos y magnéticos perpendiculares que separaba los rayos positivos según su relación carga-masa ( Q/m ). Wien descubrió que la relación carga-masa dependía de la naturaleza del gas en el tubo de descarga. Posteriormente, el científico inglés JJ Thomson mejoró el trabajo de Wien reduciendo la presión para crear el espectrógrafo de masas.

La palabra espectrógrafo se había convertido en parte del vocabulario científico internacional en 1884. [2] [3] Los primeros dispositivos de espectrometría que medían la relación masa-carga de iones se llamaban espectrógrafos de masas y consistían en instrumentos que registraban un espectro de valores de masa en una placa fotográfica . [4] [5] Un espectroscopio de masas es similar a un espectrógrafo de masas excepto que el haz de iones se dirige hacia una pantalla de fósforo . [6] En los primeros instrumentos se utilizaba una configuración de espectroscopio de masas cuando se deseaba que los efectos de los ajustes se observaran rápidamente. Una vez que el instrumento estuvo correctamente ajustado, se insertó y expuso una placa fotográfica. El término espectroscopio de masas siguió utilizándose a pesar de que la iluminación directa de una pantalla de fósforo fue sustituida por mediciones indirectas con un osciloscopio . [7] Actualmente se desaconseja el uso del término espectroscopia de masas debido a la posibilidad de confusión con espectroscopia de luz . [1] [8] La espectrometría de masas a menudo se abrevia como especificación de masas o simplemente como MS . [1]
Las técnicas modernas de espectrometría de masas fueron ideadas por Arthur Jeffrey Dempster y FW Aston en 1918 y 1919 respectivamente.
Los espectrómetros de masas sectoriales conocidos como calutrones fueron desarrollados por Ernest O. Lawrence y utilizados para separar los isótopos de uranio durante el Proyecto Manhattan . [9] Los espectrómetros de masas Calutron se utilizaron para el enriquecimiento de uranio en la planta Y-12 de Oak Ridge, Tennessee, establecida durante la Segunda Guerra Mundial.
En 1989, la mitad del Premio Nobel de Física fue concedida a Hans Dehmelt y Wolfgang Paul por el desarrollo de la técnica de la trampa de iones en los años cincuenta y sesenta.
En 2002, el Premio Nobel de Química fue otorgado a John Bennett Fenn por el desarrollo de la ionización por electropulverización (ESI) y a Koichi Tanaka por el desarrollo de la desorción por láser suave (SLD) y su aplicación a la ionización de macromoléculas biológicas, especialmente proteínas. [10]
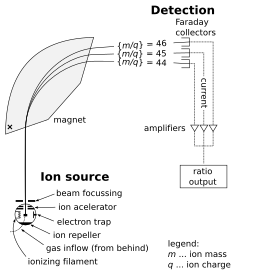
Un espectrómetro de masas consta de tres componentes: una fuente de iones, un analizador de masas y un detector. El ionizador convierte una parte de la muestra en iones. Existe una amplia variedad de técnicas de ionización, dependiendo de la fase (sólida, líquida, gaseosa) de la muestra y de la eficiencia de diversos mecanismos de ionización para las especies desconocidas. Un sistema de extracción elimina los iones de la muestra, que luego pasan por el analizador de masas y llegan al detector . Las diferencias en las masas de los fragmentos permiten que el analizador de masas clasifique los iones según su relación masa-carga. El detector mide el valor de una cantidad indicadora y proporciona así datos para calcular la abundancia de cada ion presente. Algunos detectores también proporcionan información espacial, por ejemplo, una placa multicanal.
A continuación se describe el funcionamiento de un espectrómetro analizador de masas, el cual es del tipo sectorial . (A continuación se tratan otros tipos de analizadores). Considere una muestra de cloruro de sodio (sal de mesa). En la fuente de iones, la muestra se vaporiza (se convierte en gas ) y se ioniza (se transforma en partículas cargadas eléctricamente) en iones de sodio (Na + ) y cloruro (Cl- ) . Los átomos e iones de sodio son monoisotópicos , con una masa de aproximadamente 23 daltons (símbolo: Da o símbolo más antiguo: u). Los átomos e iones de cloruro se presentan en dos isótopos estables con masas de aproximadamente 35 u (con una abundancia natural de aproximadamente el 75 por ciento) y aproximadamente 37 u (con una abundancia natural de aproximadamente el 25 por ciento). La parte analizadora del espectrómetro contiene campos eléctricos y magnéticos que ejercen fuerzas sobre los iones que viajan a través de estos campos. La velocidad de una partícula cargada puede aumentar o disminuir mientras pasa a través del campo eléctrico, y su dirección puede verse alterada por el campo magnético. La magnitud de la desviación de la trayectoria del ion en movimiento depende de su relación masa-carga. Los iones más ligeros son desviados por la fuerza magnética en mayor medida que los iones más pesados (según la segunda ley del movimiento de Newton , F = ma ). Las corrientes de iones clasificados magnéticamente pasan del analizador al detector, que registra la abundancia relativa de cada tipo de ion. Esta información se utiliza para determinar la composición de elementos químicos de la muestra original (es decir, que tanto el sodio como el cloro están presentes en la muestra) y la composición isotópica de sus constituyentes (la proporción de 35 Cl a 37 Cl).

La fuente de iones es la parte del espectrómetro de masas que ioniza el material bajo análisis (el analito). Luego, los iones son transportados mediante campos magnéticos o eléctricos al analizador de masas.
Las técnicas de ionización han sido clave para determinar qué tipos de muestras se pueden analizar mediante espectrometría de masas. La ionización electrónica y la ionización química se utilizan para gases y vapores . En las fuentes de ionización química, el analito se ioniza mediante reacciones químicas ion-molécula durante las colisiones en la fuente. Dos técnicas utilizadas a menudo con muestras biológicas líquidas y sólidas incluyen la ionización por electropulverización (inventada por John Fenn [11] ) y la desorción/ionización por láser asistida por matriz (MALDI, inicialmente desarrollada como una técnica similar "Desorción por láser suave (SLD)" por K. Tanaka [12] por el que recibió el Premio Nobel y como MALDI por M. Karas y F. Hillenkamp [13] ).

En espectrometría de masas, la ionización se refiere a la producción de iones en fase gaseosa adecuados para la resolución en el analizador de masas o filtro de masas. La ionización ocurre en la fuente de iones . Hay varias fuentes de iones disponibles; cada uno tiene ventajas y desventajas para aplicaciones particulares. Por ejemplo, la ionización electrónica (EI) proporciona un alto grado de fragmentación, produciendo espectros de masas muy detallados que, cuando se analizan hábilmente, pueden proporcionar información importante para la elucidación/caracterización estructural y facilitar la identificación de compuestos desconocidos en comparación con bibliotecas de espectros de masas obtenidas en condiciones operativas idénticas. . Sin embargo, la EI no es adecuada para acoplarse a HPLC , es decir, LC-MS , ya que a presión atmosférica, los filamentos utilizados para generar electrones se queman rápidamente. Por lo tanto, EI se acopla predominantemente con GC , es decir, GC-MS , donde todo el sistema está bajo alto vacío.
Las técnicas de ionización dura son procesos que imparten grandes cantidades de energía residual en la molécula en cuestión, provocando grandes grados de fragmentación (es decir, la ruptura sistemática de enlaces actúa para eliminar el exceso de energía, restaurando la estabilidad del ion resultante). Los iones resultantes tienden a tener m/z más bajo que el ion molecular (excepto en el caso de la transferencia de protones y sin incluir los picos de isótopos). El ejemplo más común de ionización dura es la ionización electrónica (EI).
La ionización suave se refiere a los procesos que imparten poca energía residual a la molécula en cuestión y, como tal, dan como resultado poca fragmentación. Los ejemplos incluyen bombardeo atómico rápido (FAB), ionización química (CI), ionización química a presión atmosférica (APCI), fotoionización a presión atmosférica (APPI), ionización por electropulverización (ESI), ionización por electropulverización por desorción (DESI) y láser asistido por matriz. desorción/ionización (MALDI).

Las fuentes de plasma acoplado inductivamente (ICP) se utilizan principalmente para el análisis de cationes de una amplia gama de tipos de muestras. En esta fuente, se utiliza un plasma que es eléctricamente neutro en general, pero al que se le ha ionizado una fracción sustancial de sus átomos por la alta temperatura, para atomizar las moléculas de muestra introducidas y para despojar aún más los electrones externos de esos átomos. El plasma generalmente se genera a partir de gas argón, ya que la primera energía de ionización de los átomos de argón es mayor que la primera de cualquier otro elemento excepto He, F y Ne, pero menor que la segunda energía de ionización de todos los metales excepto los más electropositivos. El calentamiento se logra mediante una corriente de radiofrecuencia que pasa a través de una bobina que rodea el plasma.
La fotoionización se puede utilizar en experimentos que buscan utilizar la espectrometría de masas como medio para resolver mecanismos cinéticos químicos y ramificación de productos isoméricos. [14] En tales casos, se utiliza un fotón de alta energía, ya sea de rayos X o ultravioleta, para disociar moléculas gaseosas estables en un gas portador de He o Ar. En los casos en los que se utiliza una fuente de luz de sincrotrón , se puede utilizar una energía de fotón sintonizable para adquirir una curva de eficiencia de fotoionización que se puede utilizar junto con la relación de carga m/z para identificar especies moleculares e iónicas. Más recientemente, se ha desarrollado la fotoionización a presión atmosférica (APPI) para ionizar moléculas principalmente como efluentes de sistemas LC-MS.
Algunas aplicaciones de la ionización ambiental incluyen aplicaciones ambientales y clínicas. En estas técnicas, los iones se forman en una fuente de iones fuera del espectrómetro de masas. El muestreo se vuelve sencillo ya que las muestras no necesitan separación ni preparación previa. Algunos ejemplos de técnicas de ionización ambiental son el Análisis Directo en Tiempo Real (DART), DESI , SESI , LAESI , la desorción por ionización química a presión atmosférica (DAPCI) y la desorción por fotoionización a presión atmosférica DAPPI , entre otras.
Otros incluyen descarga luminosa , desorción de campo (FD), bombardeo atómico rápido (FAB), termopulverización , desorción/ionización sobre silicio (DIOS), ionización química a presión atmosférica (APCI), espectrometría de masas de iones secundarios (SIMS), ionización por chispa e ionización térmica. (TIMS). [15]
Los analizadores de masas separan los iones según su relación masa-carga . Las dos leyes siguientes gobiernan la dinámica de las partículas cargadas en campos eléctricos y magnéticos en el vacío:
Aquí F es la fuerza aplicada al ion, m es la masa del ion, a es la aceleración, Q es la carga del ion, E es el campo eléctrico y v × B es el producto cruzado vectorial de la velocidad del ion y la campo magnético
Al equiparar las expresiones anteriores para la fuerza aplicada al ion se obtiene:
Esta ecuación diferencial es la clásica ecuación de movimiento de partículas cargadas . Junto con las condiciones iniciales de la partícula, determina completamente el movimiento de la partícula en el espacio y el tiempo en términos de m/Q . Por tanto, los espectrómetros de masas podrían considerarse como "espectrómetros de masa a carga". Al presentar datos, es común utilizar m/z (oficialmente) adimensional , donde z es el número de cargas elementales ( e ) en el ion (z=Q/e). Esta cantidad, aunque informalmente se denomina relación masa-carga, hablando con mayor precisión representa la relación entre el número de masa y el número de carga, z .
Hay muchos tipos de analizadores de masas, que utilizan campos estáticos o dinámicos, y campos magnéticos o eléctricos, pero todos funcionan de acuerdo con la ecuación diferencial anterior. Cada tipo de analizador tiene sus fortalezas y debilidades. Muchos espectrómetros de masas utilizan dos o más analizadores de masas para la espectrometría de masas en tándem (MS/MS) . Además de los analizadores de masas más comunes que se enumeran a continuación, existen otros diseñados para situaciones especiales.
Hay varias características importantes del analizador. El poder de resolución de masa es la medida de la capacidad de distinguir dos picos de m/z ligeramente diferentes . La precisión de la masa es la relación entre el error de medición m/z y el m/z verdadero. La precisión de la masa generalmente se mide en ppm o mili unidades de masa . El rango de masas es el rango de m/z susceptible de análisis mediante un analizador determinado. El rango dinámico lineal es el rango en el que la señal iónica es lineal con la concentración del analito. La velocidad se refiere al período de tiempo del experimento y, en última instancia, se utiliza para determinar la cantidad de espectros por unidad de tiempo que se pueden generar.

Un analizador de masas de campo sectorial utiliza un campo eléctrico y/o magnético estático para afectar la trayectoria y/o la velocidad de las partículas cargadas de alguna manera. Como se muestra arriba, los instrumentos sectoriales doblan las trayectorias de los iones a medida que pasan a través del analizador de masas, de acuerdo con sus relaciones masa-carga, desviando más los iones más cargados, más ligeros y que se mueven más rápido. El analizador se puede utilizar para seleccionar un rango estrecho de m/z o para escanear un rango de m/z para catalogar los iones presentes. [dieciséis]
El analizador de tiempo de vuelo (TOF) utiliza un campo eléctrico para acelerar los iones a través del mismo potencial y luego mide el tiempo que tardan en llegar al detector. Si todas las partículas tienen la misma carga , sus energías cinéticas serán idénticas y sus velocidades dependerán únicamente de sus masas . Los iones con menor masa llegarán primero al detector. [17] Sin embargo, en realidad, incluso partículas con la misma m/z pueden llegar en diferentes momentos al detector, porque tienen diferentes velocidades iniciales. La velocidad inicial a menudo no depende de la masa del ion y se convertirá en una diferencia en la velocidad final. Debido a esto, los iones con la misma relación m/z alcanzarán el detector en una variedad de momentos, lo que amplía los picos mostrados en el gráfico de conteo versus m/z, pero generalmente no cambiará la ubicación central de los picos, ya que la La velocidad inicial de los iones generalmente está centrada en cero. Para solucionar este problema, el enfoque retardado/ extracción retardada se ha combinado con TOF-MS. [18]
Los analizadores de masas cuadrupolos utilizan campos eléctricos oscilantes para estabilizar o desestabilizar selectivamente las trayectorias de los iones que pasan a través de un campo cuadrupolo de radiofrecuencia (RF) creado entre cuatro varillas paralelas. Sólo los iones en un cierto rango de relación masa/carga pasan a través del sistema en cualquier momento, pero los cambios en los potenciales en las barras permiten que un amplio rango de valores m/z sean barridos rápidamente, ya sea de forma continua o en una sucesión de saltos discretos. Un analizador de masas cuadrupolo actúa como un filtro selectivo de masa y está estrechamente relacionado con la trampa de iones cuadrupolo , particularmente la trampa de iones cuadrupolo lineal, excepto que está diseñado para pasar los iones no atrapados en lugar de recolectar los atrapados, y por esa razón se lo conoce como a como un cuadrupolo de transmisión. Un analizador de masas cuadrupolo magnéticamente mejorado incluye la adición de un campo magnético, ya sea aplicado axial o transversalmente. Este novedoso tipo de instrumento conduce a una mejora adicional del rendimiento en términos de resolución y/o sensibilidad dependiendo de la magnitud y orientación del campo magnético aplicado. [19] [20] Una variación común del cuadrupolo de transmisión es el espectrómetro de masas de triple cuadrupolo. El "triple cuadrupolo" tiene tres etapas de cuadrupolo consecutivas, la primera actúa como un filtro de masa para transmitir un ion entrante particular al segundo cuadrupolo, una cámara de colisión, donde ese ion puede romperse en fragmentos. El tercer cuadrupolo también actúa como filtro de masas, para transmitir un fragmento de ion particular al detector. Si se hace que un cuadrupolo realice ciclos rápidos y repetitivos a través de una variedad de configuraciones de filtro de masa, se pueden informar espectros completos. Asimismo, se puede fabricar un triple cuadrilátero para realizar varios tipos de escaneo característicos de la espectrometría de masas en tándem .
La trampa de iones cuadrupolo funciona con los mismos principios físicos que el analizador de masas cuadrupolo, pero los iones quedan atrapados y expulsados secuencialmente. Los iones quedan atrapados en un campo de RF principalmente cuadrupolo, en un espacio definido por un electrodo de anillo (normalmente conectado al potencial de RF principal) entre dos electrodos de extremo (normalmente conectados a potenciales de CC o CA auxiliares). La muestra se ioniza internamente (por ejemplo, con un haz de electrones o láser) o externamente, en cuyo caso los iones a menudo se introducen a través de una abertura en un electrodo terminal.
Existen muchos métodos de separación y aislamiento de masa/carga, pero el más comúnmente utilizado es el modo de inestabilidad de masa en el que el potencial de RF aumenta de modo que la órbita de los iones con una masa a > b sea estable mientras que los iones con masa b se vuelven inestables y expulsado en el eje z sobre un detector. También existen métodos de análisis no destructivos.
Los iones también se pueden expulsar mediante el método de excitación por resonancia, mediante el cual se aplica un voltaje de excitación oscilatorio suplementario a los electrodos de la tapa terminal y se varía la amplitud del voltaje de captura y/o la frecuencia del voltaje de excitación para llevar los iones a una condición de resonancia en orden de su masa/ relación de carga. [21] [22]
El espectrómetro de masas con trampa de iones cilíndrica (CIT) es un derivado de la trampa de iones cuadrupolo donde los electrodos están formados por anillos planos en lugar de electrodos de forma hiperbólica. La arquitectura se presta bien a la miniaturización porque a medida que se reduce el tamaño de una trampa, la forma del campo eléctrico cerca del centro de la trampa, la región donde quedan atrapados los iones, forma una forma similar a la de una trampa hiperbólica.
Una trampa de iones cuadrupolo lineal es similar a una trampa de iones cuadrupolo, pero atrapa iones en un campo cuadrupolo bidimensional, en lugar de un campo cuadrupolo tridimensional como en una trampa de iones cuadrupolo 3D. El LTQ ("cuadrupolo de trampa lineal") de Thermo Fisher es un ejemplo de trampa de iones lineal. [23]
Una trampa de iones toroidal se puede visualizar como un cuadrupolo lineal curvado y conectado en los extremos o como una sección transversal de una trampa de iones 3D girada en el borde para formar la trampa toroidal en forma de rosquilla. La trampa puede almacenar grandes volúmenes de iones distribuyéndolos por toda la estructura de la trampa en forma de anillo. Esta trampa de forma toroidal es una configuración que permite una mayor miniaturización de un analizador de masas de trampa de iones. Además, todos los iones se almacenan en el mismo campo de captura y se expulsan juntos, lo que simplifica la detección que puede complicarse con las configuraciones de la matriz debido a las variaciones en la alineación del detector y el mecanizado de las matrices. [24]
Al igual que con la trampa toroidal, las trampas lineales y las trampas de iones cuadrupolo 3D son los analizadores de masas miniaturizados más comúnmente debido a su alta sensibilidad, tolerancia a la presión mTorr y capacidades para espectrometría de masas en tándem con un solo analizador (por ejemplo, escaneos de iones de producto). [25]

Los instrumentos Orbitrap son similares a los espectrómetros de masas de resonancia ciclotrón de iones de transformada de Fourier (consulte el texto a continuación). Los iones quedan atrapados electrostáticamente en una órbita alrededor de un electrodo central en forma de huso. El electrodo confina los iones de modo que orbitan alrededor del electrodo central y oscilan hacia adelante y hacia atrás a lo largo del eje largo del electrodo central. Esta oscilación genera una corriente de imagen en las placas del detector que es registrada por el instrumento. Las frecuencias de estas corrientes de imagen dependen de las relaciones masa-carga de los iones. Los espectros de masas se obtienen mediante transformación de Fourier de las corrientes de la imagen registrada.
Las Orbitraps tienen una alta precisión de masa, alta sensibilidad y un buen rango dinámico. [26]
_Mass_spectrometer.jpg/440px-IonSpec_FT-ICR_(Fourier_transform_Ion_cyclotron_resonance)_Mass_spectrometer.jpg)
La espectrometría de masas por transformada de Fourier (FTMS), o más precisamente la resonancia de ciclotrón de iones por transformada de Fourier , mide la masa detectando la corriente de imagen producida por el ciclotrón de iones en presencia de un campo magnético. En lugar de medir la desviación de los iones con un detector como un multiplicador de electrones , los iones se inyectan en una trampa de Penning (una trampa de iones eléctrica/magnética estática ) donde efectivamente forman parte de un circuito. Los detectores situados en posiciones fijas en el espacio miden la señal eléctrica de los iones que pasan cerca de ellos a lo largo del tiempo, produciendo una señal periódica. Dado que la frecuencia del ciclo de un ion está determinada por su relación masa-carga, esto se puede desconvolucionar realizando una transformada de Fourier en la señal. FTMS tiene la ventaja de una alta sensibilidad (ya que cada ion se "cuenta" más de una vez) y una resolución y, por tanto, precisión mucho mayores. [27] [28]
La resonancia de ciclotrón de iones (ICR) es una técnica de análisis de masas más antigua similar al FTMS, excepto que los iones se detectan con un detector tradicional. Los iones atrapados en una trampa de Penning son excitados por un campo eléctrico de RF hasta que impactan la pared de la trampa, donde se encuentra el detector. Los iones de diferente masa se resuelven según el tiempo de impacto.

El último elemento del espectrómetro de masas es el detector. El detector registra la carga inducida o la corriente producida cuando un ion pasa o golpea una superficie. En un instrumento de escaneo, la señal producida en el detector durante el transcurso del escaneo versus dónde se encuentra el instrumento en el escaneo (a qué m/Q ) producirá un espectro de masas , un registro de iones en función de m/Q .
Normalmente, se utiliza algún tipo de multiplicador de electrones , aunque también se utilizan otros detectores, incluidas las copas de Faraday y los detectores de iones a fotones . Debido a que el número de iones que salen del analizador de masas en un instante particular suele ser bastante pequeño, a menudo es necesaria una amplificación considerable para obtener una señal. Los detectores de placas de microcanales se utilizan comúnmente en instrumentos comerciales modernos. [29] En FTMS y Orbitraps , el detector consta de un par de superficies metálicas dentro de la región del analizador de masas/trampa de iones cerca de las cuales los iones solo pasan cuando oscilan. No se produce corriente continua, sólo se produce una débil corriente de imagen de CA en un circuito entre los electrodos. También se han utilizado otros detectores inductivos. [30]
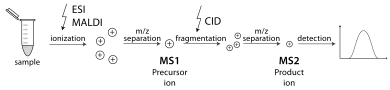
Un espectrómetro de masas en tándem es aquel capaz de realizar múltiples rondas de espectrometría de masas, generalmente separadas por alguna forma de fragmentación de moléculas. Por ejemplo, un analizador de masas puede aislar un péptido de muchos que entran en un espectrómetro de masas. Luego, un segundo analizador de masas estabiliza los iones peptídicos mientras chocan con un gas, lo que hace que se fragmenten mediante disociación inducida por colisión (CID). A continuación, un tercer analizador de masas clasifica los fragmentos producidos a partir de los péptidos. La MS en tándem también se puede realizar en un único analizador de masas a lo largo del tiempo, como en una trampa de iones cuadrupolo . Existen varios métodos para fragmentar moléculas para MS en tándem, incluida la disociación inducida por colisión (CID), la disociación por captura de electrones (ECD), la disociación por transferencia de electrones (ETD), la disociación multifotónica infrarroja (IRMPD), la disociación radiativa infrarroja de cuerpo negro (BIRD), la disociación por radiación infrarroja de cuerpo negro (BIRD) y la disociación inducida por colisión ( CID ). -disociación por desprendimiento (EDD) y disociación inducida por superficie (SID). Una aplicación importante del uso de espectrometría de masas en tándem es la identificación de proteínas. [31]
La espectrometría de masas en tándem permite una variedad de secuencias experimentales. Muchos espectrómetros de masas comerciales están diseñados para acelerar la ejecución de secuencias de rutina como el monitoreo de reacciones seleccionadas (SRM) y el escaneo de iones precursores. En SRM, el primer analizador permite el paso de una sola masa y el segundo analizador monitorea múltiples fragmentos de iones definidos por el usuario. SRM se utiliza con mayor frecuencia con instrumentos de escaneo donde el segundo evento de análisis de masa tiene un ciclo de trabajo limitado. Estos experimentos se utilizan para aumentar la especificidad de la detección de moléculas conocidas, especialmente en estudios farmacocinéticos. El escaneo de iones precursores se refiere al monitoreo de una pérdida específica del ion precursor. El primer y segundo analizadores de masas escanean todo el espectro dividido por un valor m/z definido por el usuario . Este experimento se utiliza para detectar motivos específicos dentro de moléculas desconocidas.
Otro tipo de espectrometría de masas en tándem utilizada para la datación por radiocarbono es la espectrometría de masas con acelerador (AMS), que utiliza voltajes muy altos, generalmente en el rango de megavoltios, para acelerar iones negativos en un tipo de espectrómetro de masas en tándem.
La base de datos de entidades químicas y metabolitos de METLIN [32] [33] [34] es el depósito más grande de datos experimentales de espectrometría de masas en tándem adquiridos a partir de estándares. Los datos de espectrometría de masas en tándem sobre más de 850.000 estándares moleculares (al 24 de agosto de 2020) [32] se proporcionan para facilitar la identificación de entidades químicas a partir de experimentos de espectrometría de masas en tándem. Además de la identificación de moléculas conocidas, también es útil para identificar desconocidas mediante su búsqueda/análisis de similitud. [35] Todos los datos de espectrometría de masas en tándem provienen del análisis experimental de estándares con múltiples energías de colisión y en modos de ionización tanto positiva como negativa. [32]
Cuando una combinación específica de fuente, analizador y detector se vuelve convencional en la práctica, puede surgir un acrónimo compuesto para designarla de manera sucinta. Un ejemplo es MALDI-TOF , que se refiere a una combinación de una fuente de desorción/ionización láser asistida por matriz con un analizador de masas de tiempo de vuelo . Otros ejemplos incluyen espectrometría de masas con plasma acoplado inductivamente (ICP-MS) , espectrometría de masas con acelerador (AMS) , espectrometría de masas con ionización térmica (TIMS) y espectrometría de masas con fuente de chispa (SSMS) .
Ciertas aplicaciones de la espectrometría de masas han desarrollado apodos que, aunque estrictamente hablando parecerían referirse a una aplicación amplia, en la práctica han llegado a connotar un número específico o limitado de configuraciones de instrumentos. Un ejemplo de esto es la espectrometría de masas de relación isotópica (IRMS), que en la práctica se refiere al uso de un número limitado de analizadores de masas sectoriales; este nombre se utiliza para referirse tanto a la aplicación como al instrumento utilizado para la aplicación.
Una mejora importante de las capacidades de resolución y determinación de masas de la espectrometría de masas es su uso junto con técnicas cromatográficas y de separación.

Una combinación común es la cromatografía de gases y la espectrometría de masas (GC/MS o GC-MS). En esta técnica se utiliza un cromatógrafo de gases para separar diferentes compuestos. Esta corriente de compuestos separados se alimenta en línea a la fuente de iones , un filamento metálico al que se aplica voltaje . Este filamento emite electrones que ionizan los compuestos. Luego, los iones pueden fragmentarse aún más, produciendo patrones predecibles. Los iones y fragmentos intactos pasan al analizador del espectrómetro de masas y finalmente se detectan. [36] Sin embargo, las altas temperaturas (300 °C) utilizadas en el puerto de inyección (y el horno) del GC-MS pueden provocar la degradación térmica de las moléculas inyectadas, lo que da lugar a la medición de productos de degradación en lugar de las moléculas reales. de interés. [37]

De manera similar a la cromatografía de gases MS (GC-MS), la cromatografía líquida-espectrometría de masas (LC/MS o LC-MS) separa los compuestos cromatográficamente antes de que se introduzcan en la fuente de iones y el espectrómetro de masas. Se diferencia de la GC-MS en que la fase móvil es líquida, normalmente una mezcla de agua y disolventes orgánicos , en lugar de gas. Lo más habitual es que en LC-MS se utilice una fuente de ionización por electropulverización . Otras fuentes de iones LC-MS populares y disponibles comercialmente son la ionización química a presión atmosférica y la fotoionización a presión atmosférica . También existen algunas técnicas de ionización recientemente desarrolladas, como la pulverización láser .
Electroforesis capilar-espectrometría de masas (CE-MS) es una técnica que combina el proceso de separación de líquidos de la electroforesis capilar con la espectrometría de masas. [38] CE-MS normalmente se combina con ionización por electropulverización. [39]
La espectrometría de movilidad iónica-espectrometría de masas (IMS/MS o IMMS) es una técnica en la que los iones se separan primero mediante un tiempo de deriva a través de un gas neutro bajo un gradiente de potencial eléctrico aplicado antes de introducirlos en un espectrómetro de masas. [40] El tiempo de deriva es una medida del radio relativo a la carga del ion. El ciclo de trabajo del IMS (el tiempo durante el cual se lleva a cabo el experimento) es más largo que el de la mayoría de las técnicas espectrométricas de masas, de modo que el espectrómetro de masas puede tomar muestras a lo largo del curso de la separación del IMS. Esto produce datos sobre la separación IMS y la relación masa-carga de los iones de una manera similar a la LC-MS . [41]
El ciclo de trabajo de IMS es corto en relación con las separaciones de cromatografía líquida o cromatografía de gases y, por lo tanto, puede acoplarse a tales técnicas, produciendo modalidades triples como LC/IMS/MS. [42]

La espectrometría de masas produce varios tipos de datos. La representación de datos más común es el espectro de masas .
Ciertos tipos de datos de espectrometría de masas se representan mejor como un cromatograma de masas . Los tipos de cromatogramas incluyen monitoreo de iones seleccionados (SIM), corriente iónica total (TIC) y monitoreo de reacciones seleccionadas (SRM), entre muchos otros.
Otros tipos de datos de espectrometría de masas están bien representados como un mapa de contorno tridimensional . De esta forma, la masa a carga, m/z está en el eje x , la intensidad en el eje y y un parámetro experimental adicional, como el tiempo, se registra en el eje z .
El análisis de datos de espectrometría de masas es específico del tipo de experimento que produce los datos. Las subdivisiones generales de los datos son fundamentales para comprender cualquier dato.
Muchos espectrómetros de masas funcionan en modo de iones negativos o en modo de iones positivos . Es muy importante saber si los iones observados están cargados negativa o positivamente. Esto suele ser importante para determinar la masa neutra, pero también indica algo sobre la naturaleza de las moléculas.
Los diferentes tipos de fuentes de iones dan como resultado diferentes conjuntos de fragmentos producidos a partir de las moléculas originales. Una fuente de ionización de electrones produce muchos fragmentos y en su mayoría radicales con carga única (1-) (número impar de electrones), mientras que una fuente de electropulverización generalmente produce iones cuasimoleculares no radicales que frecuentemente tienen carga múltiple. La espectrometría de masas en tándem produce intencionalmente iones fragmentados después de la fuente y puede cambiar drásticamente el tipo de datos obtenidos mediante un experimento.
El conocimiento del origen de una muestra puede proporcionar información sobre las moléculas que la componen y sus fragmentaciones. Una muestra de un proceso de síntesis/fabricación probablemente contendrá impurezas químicamente relacionadas con el componente objetivo. Una muestra biológica toscamente preparada probablemente contendrá una cierta cantidad de sal, que puede formar aductos con las moléculas del analito en ciertos análisis.
Los resultados también pueden depender en gran medida de la preparación de la muestra y de cómo se ejecutó/introdujo. Un ejemplo importante es la cuestión de qué matriz se utiliza para la localización MALDI, ya que gran parte de la energía del evento de desorción/ionización está controlada por la matriz en lugar de por la potencia del láser. A veces, las muestras se enriquecen con sodio u otra especie portadora de iones para producir aductos en lugar de una especie protonada.
La espectrometría de masas puede medir la masa molar, la estructura molecular y la pureza de la muestra. Cada una de estas cuestiones requiere un procedimiento experimental diferente; por lo tanto, una definición adecuada del objetivo experimental es un requisito previo para recopilar los datos adecuados e interpretarlos con éxito.
Dado que la estructura precisa o secuencia peptídica de una molécula se descifra a través del conjunto de masas de fragmentos, la interpretación de los espectros de masas requiere el uso combinado de varias técnicas. Por lo general, la primera estrategia para identificar un compuesto desconocido es comparar su espectro de masas experimental con una biblioteca de espectros de masas. Si no se obtienen coincidencias de la búsqueda, se debe realizar la interpretación manual [43] o la interpretación asistida por software de los espectros de masas . La simulación por computadora de los procesos de ionización y fragmentación que ocurren en el espectrómetro de masas es la herramienta principal para asignar estructura o secuencia peptídica a una molécula. Una información estructural a priori se fragmenta in silico y el patrón resultante se compara con el espectro observado. Esta simulación suele estar respaldada por una biblioteca de fragmentación [44] que contiene patrones publicados de reacciones de descomposición conocidas. Se ha desarrollado software que aprovecha esta idea tanto para moléculas pequeñas como para proteínas .
El análisis de espectros de masas también puede ser espectros con masas precisas . Un valor de relación masa-carga ( m/z ) con precisión sólo entera puede representar una inmensa cantidad de estructuras iónicas teóricamente posibles; sin embargo, cifras de masa más precisas reducen significativamente el número de fórmulas moleculares candidatas . Un algoritmo informático llamado generador de fórmulas calcula todas las fórmulas moleculares que teóricamente se ajustan a una masa determinada con una tolerancia específica.
Una técnica reciente para la elucidación de estructuras en espectrometría de masas, llamada huella digital de iones precursores, identifica piezas individuales de información estructural realizando una búsqueda de los espectros en tándem de la molécula bajo investigación en una biblioteca de espectros de iones de producción de iones precursores estructuralmente caracterizados. [45]

La espectrometría de masas tiene usos tanto cualitativos como cuantitativos . Estos incluyen identificar compuestos desconocidos, determinar la composición isotópica de elementos en una molécula y determinar la estructura de un compuesto observando su fragmentación. Otros usos incluyen cuantificar la cantidad de un compuesto en una muestra o estudiar los fundamentos de la química de iones en fase gaseosa (la química de iones y neutros en el vacío). La EM ahora se usa comúnmente en laboratorios analíticos que estudian las propiedades físicas, químicas o biológicas de una gran variedad de compuestos. La cuantificación puede ser relativa (analizada en relación con una muestra de referencia) o absoluta (analizada mediante un método de curva estándar). [46] [47]
Como técnica analítica, posee distintas ventajas como: Mayor sensibilidad sobre la mayoría de las otras técnicas analíticas porque el analizador, como filtro de carga de masa, reduce la interferencia de fondo. Excelente especificidad de los patrones de fragmentación característicos para identificar desconocidos o confirmar la presencia de compuestos sospechosos. Información sobre el peso molecular, Información sobre la abundancia isotópica de elementos, Datos químicos resueltos temporalmente.
Algunas de las desventajas del método es que a menudo no distingue entre isómeros ópticos y geométricos y las posiciones de los sustituyentes en las posiciones o, m y p en un anillo aromático. Además, su alcance es limitado a la hora de identificar hidrocarburos que produzcan iones fragmentados similares.

La espectrometría de masas también se utiliza para determinar la composición isotópica de elementos dentro de una muestra. Las diferencias de masa entre los isótopos de un elemento son muy pequeñas y los isótopos menos abundantes de un elemento suelen ser muy raros, por lo que se requiere un instrumento muy sensible. Estos instrumentos, a veces denominados espectrómetros de masas de relación isotópica (IR-MS), suelen utilizar un solo imán para doblar un haz de partículas ionizadas hacia una serie de copas de Faraday que convierten los impactos de las partículas en corriente eléctrica . Se puede realizar un análisis rápido en línea del contenido de deuterio del agua utilizando espectrometría de masas con luminiscencia residual , FA-MS. Probablemente el espectrómetro de masas más sensible y preciso para este propósito sea el espectrómetro de masas con acelerador (AMS). Esto se debe a que proporciona la máxima sensibilidad, capaz de medir átomos individuales y medir nucleidos con un rango dinámico de ~10 15 en relación con el isótopo estable principal. [48] Las proporciones de isótopos son marcadores importantes de una variedad de procesos. Algunas proporciones de isótopos se utilizan para determinar la edad de los materiales, por ejemplo, en la datación por carbono . El marcaje con isótopos estables también se utiliza para la cuantificación de proteínas. (ver caracterización de proteínas a continuación)
La espectrometría de masas por introducción de membrana combina la relación de isótopos MS con una cámara/celda de reacción separada por una membrana permeable a los gases. Este método permite el estudio de los gases a medida que evolucionan en solución. Este método ha sido ampliamente utilizado para el estudio de la producción de oxígeno por el Fotosistema II . [49]
Varias técnicas utilizan iones creados en una fuente de iones dedicada inyectada en un tubo de flujo o en un tubo de deriva: el tubo de flujo de iones seleccionados (SIFT-MS) y la reacción de transferencia de protones (PTR-MS) son variantes de la ionización química dedicadas al análisis de gases traza. de aire, aliento o espacio de cabeza líquido utilizando un tiempo de reacción bien definido que permite calcular las concentraciones de analitos a partir de la cinética de reacción conocida sin la necesidad de un estándar interno o calibración.
Otra técnica con aplicaciones en el campo del análisis de gases traza es la ionización por electropulverización secundaria (SESI-MS), que es una variante de la ionización por electropulverización . SESI consiste en una columna de electropulverización de disolvente acidificado puro que interactúa con vapores neutros. Las moléculas de vapor se ionizan a presión atmosférica cuando la carga se transfiere de los iones formados en el electrospray a las moléculas. Una ventaja de este enfoque es que es compatible con la mayoría de los sistemas ESI-MS. [50] [51]

Un analizador de gases residuales (RGA) es un espectrómetro de masas pequeño y generalmente resistente , típicamente diseñado para el control de procesos y el monitoreo de la contaminación en sistemas de vacío . Cuando se construye como un analizador de masas cuadrupolo , existen dos implementaciones, que utilizan una fuente de iones abierta (OIS) o una fuente de iones cerrada (CIS). Los RGA se pueden encontrar en aplicaciones de alto vacío, como cámaras de investigación, instalaciones científicas de superficies , aceleradores , microscopios de barrido , etc. Los RGA se utilizan en la mayoría de los casos para monitorear la calidad del vacío y detectar fácilmente rastros diminutos de impurezas en el gas de baja presión. ambiente. Estas impurezas se pueden medir hasta niveles Torr , poseyendo una detectabilidad inferior a ppm en ausencia de interferencias de fondo.
Los RGA también se utilizarían como sensibles detectores de fugas in situ que normalmente utilizan helio , alcohol isopropílico u otras moléculas trazadoras. Con sistemas de vacío bombeados a niveles inferiores a Torr (comprobación de la integridad de los sellos de vacío y la calidad del vacío), se pueden detectar fugas de aire, fugas virtuales y otros contaminantes en niveles bajos antes de que se inicie un proceso.Una sonda atómica es un instrumento que combina espectrometría de masas de tiempo de vuelo y microscopía de evaporación de campo para mapear la ubicación de átomos individuales.
La farmacocinética a menudo se estudia mediante espectrometría de masas debido a la naturaleza compleja de la matriz (a menudo sangre u orina) y la necesidad de una alta sensibilidad para observar dosis bajas y datos puntuales a largo plazo. La instrumentación más común utilizada en esta aplicación es LC-MS con un espectrómetro de masas de triple cuadrupolo . Generalmente se emplea espectrometría de masas en tándem para mayor especificidad. Las curvas estándar y los estándares internos se utilizan para la cuantificación, generalmente, de un único producto farmacéutico en las muestras. Las muestras representan diferentes momentos en los que se administra un producto farmacéutico y luego se metaboliza o elimina del cuerpo. Las muestras en blanco o t=0 tomadas antes de la administración son importantes para determinar los antecedentes y garantizar la integridad de los datos con matrices de muestras tan complejas. Se presta mucha atención a la linealidad de la curva estándar; sin embargo, no es raro utilizar el ajuste de curvas con funciones más complejas, como las cuadráticas, ya que la respuesta de la mayoría de los espectrómetros de masas es menos que lineal en grandes rangos de concentración. [52] [53] [54]
Actualmente existe un interés considerable en el uso de espectrometría de masas de muy alta sensibilidad para estudios de microdosificación , que se consideran una alternativa prometedora a la experimentación con animales .
Estudios recientes muestran que la ionización secundaria por electropulverización (SESI) es una técnica poderosa para monitorear la cinética de fármacos mediante el análisis del aliento. [55] [56] Debido a que la respiración se produce naturalmente, se pueden recopilar fácilmente varios puntos de datos. Esto permite aumentar considerablemente el número de puntos de datos recopilados. [57] En estudios con animales, este enfoque SESI puede reducir el sacrificio de animales. [56] En humanos, el análisis no invasivo del aliento SESI-MS puede ayudar a estudiar la cinética de los fármacos a un nivel personalizado. [55] [58] [59]
La espectrometría de masas es un método importante para la caracterización y secuenciación de proteínas. Los dos métodos principales para la ionización de proteínas completas son la ionización por electropulverización (ESI) y la desorción/ionización por láser asistida por matriz (MALDI). De acuerdo con el rendimiento y el rango de masas de los espectrómetros de masas disponibles, se utilizan dos enfoques para caracterizar proteínas. En el primero, las proteínas intactas se ionizan mediante cualquiera de las dos técnicas descritas anteriormente y luego se introducen en un analizador de masas. Este enfoque se conoce como estrategia " de arriba hacia abajo " de análisis de proteínas. Sin embargo, el enfoque de arriba hacia abajo se limita en gran medida a estudios de proteína única de bajo rendimiento. En el segundo, las proteínas se digieren enzimáticamente en péptidos más pequeños utilizando proteasas como tripsina o pepsina , ya sea en solución o en gel después de la separación electroforética . También se utilizan otros agentes proteolíticos. La colección de productos peptídicos a menudo se separa mediante cromatografía antes de su introducción en el analizador de masas. Cuando se utiliza el patrón característico de los péptidos para la identificación de la proteína, el método se denomina huella peptídica de masa (PMF); si la identificación se realiza utilizando los datos de secuencia determinados en el análisis MS en tándem , se denomina secuenciación de péptidos de novo . Estos procedimientos de análisis de proteínas también se conocen como enfoque " de abajo hacia arriba " y también se han utilizado para analizar la distribución y posición de modificaciones postraduccionales como la fosforilación de proteínas. [60] También se está empezando a utilizar un tercer enfoque: este enfoque intermedio "de abajo hacia abajo" implica analizar péptidos proteolíticos que son más grandes que el péptido tríptico típico. [61]

Como método estándar de análisis, los espectrómetros de masas han llegado a otros planetas y lunas. Dos de ellos fueron llevados a Marte por el programa Viking . A principios de 2005, la misión Cassini-Huygens entregó un instrumento GC-MS especializado a bordo de la sonda Huygens a través de la atmósfera de Titán , la luna más grande del planeta Saturno . Este instrumento analizó muestras atmosféricas a lo largo de su trayectoria de descenso y fue capaz de vaporizar y analizar muestras de la superficie congelada y cubierta de hidrocarburos de Titán una vez que la sonda aterrizó. Estas mediciones comparan la abundancia de isótopos de cada partícula con la abundancia natural de la Tierra. [62] También a bordo de la nave espacial Cassini-Huygens había un espectrómetro de iones y masas neutras que había estado tomando medidas de la composición atmosférica de Titán, así como la composición de las columnas de Encelado . El Mars Phoenix Lander, lanzado en 2007, llevaba un espectrómetro de masas analizador térmico y de gases evolucionados .
Los espectrómetros de masas también se utilizan mucho en misiones espaciales para medir la composición de los plasmas. Por ejemplo, la nave espacial Cassini llevaba el espectrómetro de plasma Cassini (CAPS), [64] que midió la masa de iones en la magnetosfera de Saturno .
Los espectrómetros de masas se utilizaron en hospitales para el análisis de gases respiratorios desde 1975 hasta finales de siglo. Probablemente algunos todavía estén en uso, pero ninguno se está fabricando actualmente. [sesenta y cinco]
Se encuentran principalmente en el quirófano y forman parte de un sistema complejo en el que muestras de gas respirado de pacientes sometidos a anestesia se introducen en el instrumento a través de un mecanismo de válvula diseñado para conectar secuencialmente hasta 32 habitaciones al espectrómetro de masas. Una computadora dirigía todas las operaciones del sistema. Los datos recopilados por el espectrómetro de masas se entregaron a las salas individuales para que los usara el anestesiólogo.
La singularidad de este espectrómetro de masas de sector magnético puede haber sido el hecho de que un plano de detectores, cada uno colocado específicamente para recolectar todas las especies de iones que se espera que estén en las muestras, permitió que el instrumento informara simultáneamente todos los gases respirados por el paciente. . Aunque el rango de masas se limitó a poco más de 120 u , la fragmentación de algunas de las moléculas más pesadas anuló la necesidad de un límite de detección más alto. [66]
La función principal de la espectrometría de masas es ser una herramienta para análisis químicos basados en la detección y cuantificación de iones según su relación masa-carga. Sin embargo, la espectrometría de masas también resulta prometedora para la síntesis de materiales. [48] El aterrizaje suave de iones se caracteriza por la deposición de especies intactas en superficies con bajas energías cinéticas, lo que impide la fragmentación de las especies incidentes. [67] La técnica de aterrizaje suave se informó por primera vez en 1977 para la reacción de iones que contienen azufre de baja energía sobre una superficie de plomo. [68]