
La espectrometría de masas en tándem , también conocida como MS/MS o MS 2 , es una técnica de análisis instrumental en la que se realizan dos o más etapas de análisis utilizando uno o más analizadores de masas con un paso de reacción adicional entre estos análisis para aumentar sus capacidades de análisis. muestras químicas. [1] Un uso común de la EM en tándem es el análisis de biomoléculas , como proteínas y péptidos .
Las moléculas de una muestra determinada se ionizan y el primer espectrómetro (denominado MS1 ) separa estos iones por su relación masa-carga (a menudo dada como m/z o m/Q). Los iones de una relación m/z particular provenientes de MS1 se seleccionan y luego se dividen en fragmentos de iones más pequeños , por ejemplo, mediante disociación inducida por colisión , reacción ion-molécula o fotodisociación . Estos fragmentos luego se introducen en el segundo espectrómetro de masas ( MS2 ), que a su vez separa los fragmentos por su relación m/z y los detecta . El paso de fragmentación permite identificar y separar iones que tienen relaciones m/z muy similares en espectrómetros de masas normales.
Las configuraciones típicas de instrumentación de espectrometría de masas en tándem incluyen espectrómetros de masas de triple cuadrupolo (QqQ), espectrómetro de masas multisectorial , cuadrupolo-tiempo de vuelo (Q-TOF), espectrómetros de masas de resonancia de ciclotrón iónico por transformada de Fourier y espectrómetros de masas híbridos.
Los espectrómetros de masas de triple cuadrupolo utilizan el primer y tercer cuadrupolo como filtros de masa. Cuando los analitos pasan el segundo cuadrupolo, la fragmentación se produce mediante colisión con el gas.
El espectrómetro de masas Q-TOF combina instrumentos TOF y cuadrupolo, lo que genera una alta precisión de masa para los iones del producto, una capacidad de cuantificación precisa y aplicabilidad de experimentos de fragmentación. Este es un método de espectrometría de masas que determina la relación de fragmentación de iones ( m / z ) mediante una medición del tiempo de vuelo.
El espectrómetro de masas híbrido consta de más de dos analizadores de masas.

Se pueden lograr múltiples etapas de separación del análisis de masas con elementos individuales del espectrómetro de masas separados en el espacio o utilizando un solo espectrómetro de masas con los pasos de MS separados en el tiempo. Para la espectrometría de masas en tándem en el espacio, los diferentes elementos a menudo se anotan de forma abreviada, indicando el tipo de selector de masas utilizado.

En la espectrometría de masas en tándem en el espacio , los elementos de separación están físicamente separados y distintos, aunque existe una conexión física entre los elementos para mantener un alto vacío . Estos elementos pueden ser sectores , cuadrupolo de transmisión o tiempo de vuelo. Cuando se utilizan varios cuadrupolos, pueden actuar como analizadores de masas y cámaras de colisión.
La notación común para analizadores de masas es Q – analizador de masas cuadrupolo; q – cuadrupolo de colisión de radiofrecuencia ; TOF – analizador de masas de tiempo de vuelo ; B – sector magnético y E – sector eléctrico. La notación se puede combinar para indicar varios instrumentos híbridos, por ejemplo QqQ' – espectrómetro de masas de triple cuadrupolo ; QTOF : espectrómetro de masas de tiempo de vuelo cuadrupolo (también QqTOF ); y BEBE , espectrómetro de masas de cuatro sectores (geometría inversa).

Al realizar espectrometría de masas en tándem en el tiempo , la separación se logra con iones atrapados en el mismo lugar, con múltiples pasos de separación a lo largo del tiempo. Para dicho análisis se puede utilizar una trampa de iones cuadrupolo o un instrumento de resonancia ciclotrón de iones por transformada de Fourier (FTICR). [2] Los instrumentos de captura pueden realizar múltiples pasos de análisis, lo que a veces se denomina MS n (MS to the n ). [3] A menudo no se indica el número de pasos, n , pero ocasionalmente se especifica el valor; por ejemplo MS 3 indica tres etapas de separación. Los instrumentos de MS en tándem en el tiempo no utilizan los modos que se describen a continuación, pero normalmente recopilan toda la información de un escaneo de iones precursores y un escaneo de iones originales de todo el espectro. Cada configuración instrumental utiliza un modo único de identificación masiva.
Cuando la MS en tándem se realiza con un diseño en el espacio, el instrumento debe funcionar en uno de varios modos. Hay varias configuraciones experimentales de MS/MS en tándem diferentes y cada modo tiene sus propias aplicaciones y proporciona información diferente. La MS en tándem en el espacio utiliza el acoplamiento de dos componentes de instrumentos que miden el mismo rango de espectro de masas pero con un fraccionamiento controlado entre ellos en el espacio, mientras que la MS en tándem en el tiempo implica el uso de una trampa de iones .
Hay cuatro experimentos de escaneo principales posibles usando MS/MS: escaneo de iones precursores, escaneo de iones de producto, escaneo de pérdida neutra y monitoreo de reacciones seleccionadas.
Para una exploración de iones precursores, el ion producto se selecciona en el segundo analizador de masas y las masas precursoras se exploran en el primer analizador de masas. Tenga en cuenta que el ion precursor [4] es sinónimo de ion padre [5] y el ion producto [6] de ion hijo; [7] sin embargo, se desaconseja el uso de estos términos antropomórficos. [8] [9]
En un escaneo de iones de producto, se selecciona un ion precursor en la primera etapa, se le permite fragmentarse y luego todas las masas resultantes se escanean en el segundo analizador de masas y se detectan en el detector que está ubicado después del segundo analizador de masas. Este experimento se realiza comúnmente para identificar las transiciones utilizadas para la cuantificación mediante MS en tándem.
En un escaneo de pérdida neutral, el primer analizador de masas escanea todas las masas. El segundo analizador de masas también escanea, pero con un desplazamiento establecido respecto al primer analizador de masas. [10] Esta compensación corresponde a una pérdida neutra que se observa comúnmente para la clase de compuestos. En una exploración de pérdida de neutral constante, se monitorean todos los precursores que sufren la pérdida de un neutral común específico. Para obtener esta información, ambos analizadores de masas se escanean simultáneamente, pero con una compensación de masa que se correlaciona con la masa del neutro especificado. De manera similar a la exploración de iones precursores, esta técnica también es útil en la identificación selectiva de clases de compuestos estrechamente relacionados en una mezcla.
En la monitorización de reacciones seleccionadas, ambos analizadores de masas se ajustan a una masa seleccionada. Este modo es análogo al monitoreo de iones seleccionados para experimentos de MS. Un modo de análisis selectivo, que puede aumentar la sensibilidad. [11]
La fragmentación de iones en fase gaseosa es esencial para la espectrometría de masas en tándem y ocurre entre diferentes etapas del análisis de masas. Se utilizan muchos métodos para fragmentar los iones y estos pueden dar lugar a diferentes tipos de fragmentación y, por tanto, a información diferente sobre la estructura y composición de la molécula.
A menudo, el proceso de ionización es lo suficientemente violento como para dejar a los iones resultantes con suficiente energía interna para fragmentarse dentro del espectrómetro de masas. Si los iones del producto persisten en su estado de no equilibrio durante un período de tiempo moderado antes de la autodisociación, este proceso se denomina fragmentación metaestable . [12] La fragmentación de la boquilla-desnatadora se refiere a la inducción intencionada de fragmentación en la fuente mediante el aumento del potencial de la boquilla-desnatadora en instrumentos generalmente basados en electropulverización . Aunque la fragmentación en la fuente permite el análisis de fragmentación, técnicamente no es espectrometría de masas en tándem a menos que los iones metaestables se analicen o seleccionen en masa antes de la autodisociación y se realice una segunda etapa de análisis en los fragmentos resultantes. La fragmentación en fuente se puede utilizar en lugar de la espectrometría de masas en tándem mediante la utilización de la tecnología de anotación de fragmentación en fuente mejorada (EISA), que genera una fragmentación que coincide directamente con los datos de espectrometría de masas en tándem. [13] Los fragmentos observados por EISA tienen una intensidad de señal más alta que los fragmentos tradicionales que sufren pérdidas en las celdas de colisión de los espectrómetros de masas en tándem. [14] EISA permite la adquisición de datos de fragmentación en analizadores de masas MS1, como instrumentos de tiempo de vuelo y de cuadrupolo único. La fragmentación en la fuente se utiliza a menudo además de la espectrometría de masas en tándem (con fragmentación posterior a la fuente) para permitir dos pasos de fragmentación en un experimento de tipo pseudo MS 3 . [15]
La fragmentación posterior a la fuente es lo que más se utiliza en un experimento de espectrometría de masas en tándem. También se puede añadir energía a los iones, que normalmente ya están excitados por vibración, mediante colisiones posteriores a la fuente con átomos o moléculas neutros, la absorción de radiación o la transferencia o captura de un electrón por un ion con carga múltiple. La disociación inducida por colisión (CID), también llamada disociación activada por colisión (CAD), implica la colisión de un ion con un átomo o molécula neutro en la fase gaseosa y la posterior disociación del ion. [16] [17] Por ejemplo, considere
donde el ion AB + choca con la especie neutra M y posteriormente se rompe. Los detalles de este proceso se describen en la teoría de colisiones . Debido a la diferente configuración instrumental, son posibles dos tipos principales de CID: (i) tipo haz (en el que los iones precursores se fragmentan en el vuelo) [18] y (ii) tipo trampa de iones (en el que los iones precursores se fragmentan en el vuelo) [18] primero quedan atrapados y luego fragmentados). [19] [20]
Un tercer y más reciente tipo de fragmentación CID es la disociación colisional de mayor energía (HCD). HCD es una técnica de CID específica de los espectrómetros de masas orbittrap en la que la fragmentación tiene lugar fuera de la trampa de iones, [21] [22] ocurre en la celda HCD (en algunos instrumentos se denomina "multipolo de enrutamiento de iones"). [23] HCD es una fragmentación tipo trampa que se ha demostrado que tiene características de tipo haz. [24] [25] Existen bases de datos de espectrometría de masas en tándem de alta resolución y gran escala, disponibles gratuitamente (por ejemplo, METLIN con 850.000 estándares moleculares, cada uno con datos experimentales de CID MS/MS), [26] y normalmente se utilizan para facilitar la identificación de moléculas pequeñas.
La energía liberada cuando un electrón es transferido o capturado por un ion con carga múltiple puede inducir la fragmentación.
Si se añade un electrón a un ion positivo con carga múltiple, se libera energía de Coulomb . Agregar un electrón libre se llama disociación por captura de electrones (ECD) [27] y está representada por
para una molécula M multiprotonada.
La adición de un electrón a través de una reacción ion-ion se llama disociación por transferencia de electrones (ETD). [28] [29] De manera similar a la disociación por captura de electrones, la ETD induce la fragmentación de cationes (por ejemplo, péptidos o proteínas ) transfiriéndoles electrones . Fue inventado por Donald F. Hunt , Joshua Coon , John EP Syka y Jarrod Marto en la Universidad de Virginia . [30]
ETD no utiliza electrones libres, sino aniones radicales (p. ej., antraceno o azobenceno ) para este fin:
donde A es el anión. [31]
ETD se escinde aleatoriamente a lo largo de la cadena principal del péptido (iones cyz), mientras que las cadenas laterales y modificaciones como la fosforilación se dejan intactas. La técnica solo funciona bien para iones con estados de carga más altos (z>2); sin embargo, en relación con la disociación inducida por colisión (CID), la ETD es ventajosa para la fragmentación de péptidos más largos o incluso proteínas enteras. Esto hace que la técnica sea importante para la proteómica de arriba hacia abajo . Al igual que el ECD, el ETD es eficaz para péptidos con modificaciones como la fosforilación. [32]
La transferencia de electrones y la disociación por colisión de mayor energía (EThcD) es una combinación de ETD y HCD en la que el precursor peptídico se somete inicialmente a una reacción ion/ion con aniones fluoranteno en una trampa de iones lineal , que genera iones c y z. [28] [33] En el segundo paso, la fragmentación de todos los iones de HCD se aplica a todos los iones derivados de ETD para generar iones b e y antes del análisis final en el analizador orbitrap. [21] Este método emplea fragmentación dual para generar espectros MS/MS ricos en iones y, por lo tanto, en datos para la secuenciación de péptidos y la localización de PTM . [34]
La fragmentación también puede ocurrir con una especie desprotonada, en la que un electrón se transfiere de la especie a un reactivo catiónico en una disociación por transferencia negativa de electrones (NETD): [35]
Después de este evento de transferencia, el anión deficiente en electrones sufre un reordenamiento interno y se fragmenta . NETD es el análogo ion/ion de la disociación por desprendimiento de electrones (EDD).
NETD es compatible con la fragmentación de péptidos y proteínas a lo largo de la columna vertebral en el enlace C α -C. Los fragmentos resultantes suelen ser iones de producto de tipo • - y x.
La disociación por desprendimiento de electrones (EDD) es un método para fragmentar especies aniónicas en espectrometría de masas. [36] Sirve como un modo contrario negativo a la disociación por captura de electrones. Los iones cargados negativamente se activan mediante irradiación con electrones de energía cinética moderada. El resultado es la expulsión de electrones de la molécula iónica original , lo que provoca la disociación mediante recombinación.
La reacción entre péptidos cargados positivamente y reactivos catiónicos, [37] también conocida como disociación por transferencia de carga (CTD), [38] se ha demostrado recientemente como una vía alternativa de fragmentación de alta energía para péptidos en estado de carga baja (1+ o 2+). . El mecanismo propuesto de CTD utilizando cationes de helio como reactivo es:
Los informes iniciales indican que la CTD provoca la escisión del enlace C α -C de la columna vertebral de los péptidos y proporciona iones de producto de tipo • - y x.
La energía requerida para la disociación se puede agregar mediante absorción de fotones , lo que da como resultado la fotodisociación de iones y se representa por
donde representa el fotón absorbido por el ion. Se pueden utilizar láseres ultravioleta, pero pueden provocar una fragmentación excesiva de las biomoléculas. [39]
Los fotones infrarrojos calentarán los iones y provocarán la disociación si se absorben una cantidad suficiente. Este proceso se llama disociación multifotónica infrarroja (IRMPD) y a menudo se logra con un láser de dióxido de carbono y un espectrómetro de masas que atrapa iones, como un FTMS . [40]
La radiación de cuerpo negro se puede utilizar para la fotodisociación en una técnica conocida como disociación radiativa infrarroja de cuerpo negro (BIRD). [41] En el método BIRD, toda la cámara de vacío del espectrómetro de masas se calienta para crear luz infrarroja . BIRD utiliza esta radiación para excitar vibraciones cada vez más energéticas de los iones, hasta que se rompe un enlace, creando fragmentos. [41] [42] Esto es similar a la disociación multifotónica infrarroja que también utiliza luz infrarroja, pero de una fuente diferente. [17] BIRD se utiliza con mayor frecuencia con espectrometría de masas por resonancia ciclotrón de iones por transformada de Fourier .
Con la disociación inducida por superficie (SID), la fragmentación es el resultado de la colisión de un ion con una superficie en alto vacío. [43] [44] Hoy en día, SID se utiliza para fragmentar una amplia gama de iones. Hace años, solo era común usar SID en especies de menor masa y carga única porque los métodos de ionización y las tecnologías de análisis de masas no estaban lo suficientemente avanzados para formar, transmitir o caracterizar adecuadamente iones de alta m/z. Con el tiempo, las superficies monocapa (SAM) autoensambladas compuestas de CF 3 (CF 2 ) 10 CH 2 CH 2 S sobre oro han sido las superficies de colisión más utilizadas para SID en un espectrómetro en tándem. Los SAM han actuado como los objetivos de colisión más deseables debido a sus características masas efectivas grandes para la colisión de iones entrantes. Además, estas superficies están compuestas de cadenas rígidas de fluorocarbono , que no amortiguan significativamente la energía de los iones del proyectil. Las cadenas de fluorocarbono también son beneficiosas debido a su capacidad para resistir la fácil transferencia de electrones desde la superficie del metal a los iones entrantes. [45] La capacidad de SID para producir subcomplejos que permanecen estables y proporcionan información valiosa sobre la conectividad no tiene comparación con ninguna otra técnica de disociación. Dado que los complejos producidos a partir de SID son estables y retienen la distribución de carga en el fragmento, esto produce un espectro único en el que el complejo se centra alrededor de una distribución m/z más estrecha. Los productos SID y la energía con la que se forman reflejan las fortalezas y la topología del complejo. Los patrones de disociación únicos ayudan a descubrir la estructura cuaternaria del complejo. La distribución de carga simétrica y la dependencia de la disociación son exclusivas de SID y hacen que los espectros producidos se distingan de cualquier otra técnica de disociación. [45]
La técnica SID también es aplicable a la espectrometría de masas de movilidad iónica (IM-MS). Tres métodos diferentes para esta técnica incluyen el análisis de la caracterización de la topología, la conectividad entre subunidades y el grado de despliegue de la estructura de las proteínas. El análisis del desarrollo de la estructura de las proteínas es la aplicación más utilizada de la técnica SID. Para la espectrometría de masas de movilidad iónica (IM-MS), la SID se utiliza para la disociación de los precursores activados en la fuente de tres tipos diferentes de complejos proteicos: proteína C reactiva (CRP), transtiretina (TTR) y concanavalina A (Con A). . Este método se utiliza para observar el grado de desarrollo de cada uno de estos complejos. Para esta observación, SID mostró las estructuras de los iones precursores que existen antes de la colisión con la superficie. IM-MS utiliza el SID como una medida directa de la conformación de la subunidad de cada proteína. [46]
La resonancia ciclotrón de iones por transformada de Fourier (FTICR) puede proporcionar una resolución ultraalta y una alta precisión de masa a los instrumentos que toman medidas de masa. Estas características hacen de los espectrómetros de masas FTICR una herramienta útil para una amplia variedad de aplicaciones, como varios experimentos de disociación [47], como la disociación inducida por colisión (CID, disociación por transferencia de electrones (ETD), [48] y otros. Además, La disociación inducida se ha implementado con este instrumento para el estudio de la fragmentación de péptidos fundamentales. Específicamente, la SID se ha aplicado al estudio de la energía y la cinética de la fragmentación en fase gaseosa dentro de un instrumento ICR. [49] Este enfoque se ha utilizado para comprender la fragmentación en fase gaseosa de péptidos protonados, iones peptídicos de electrones impares, complejos ligando-péptido no covalentes y grupos de metales ligados.
La proteómica cuantitativa se utiliza para determinar la cantidad relativa o absoluta de proteínas en una muestra. [50] [51] [52] Varios métodos de proteómica cuantitativa se basan en la espectrometría de masas en tándem. MS/MS se ha convertido en un procedimiento de referencia para la elucidación estructural de biomoléculas complejas. [53]
Un método comúnmente utilizado para la proteómica cuantitativa es el etiquetado con etiquetas isobáricas. El etiquetado con etiquetas isobáricas permite la identificación y cuantificación simultánea de proteínas de múltiples muestras en un solo análisis. Para cuantificar proteínas, los péptidos se marcan con etiquetas químicas que tienen la misma estructura y masa nominal, pero varían en la distribución de isótopos pesados en su estructura. Estas etiquetas, comúnmente denominadas etiquetas de masa en tándem, están diseñadas para que la etiqueta de masa se escinda en una región enlazadora específica tras una disociación inducida por colisión (HCD) de mayor energía durante la espectrometría de masas en tándem, lo que produce iones indicadores de diferentes masas. La cuantificación de proteínas se logra comparando las intensidades de los iones indicadores en los espectros MS/MS. Dos etiquetas isobáricas disponibles comercialmente son los reactivos iTRAQ y TMT.
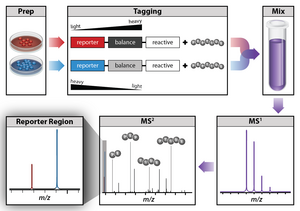
Una etiqueta isobárica para cuantificación relativa y absoluta (iTRAQ) es un reactivo para espectrometría de masas en tándem que se utiliza para determinar la cantidad de proteínas de diferentes fuentes en un solo experimento. [54] [55] [56] Utiliza moléculas marcadas con isótopos estables que pueden formar un enlace covalente con el extremo N y las aminas de cadena lateral de las proteínas. Los reactivos iTRAQ se utilizan para marcar péptidos de diferentes muestras que se combinan y analizan mediante cromatografía líquida y espectrometría de masas en tándem. La fragmentación de la etiqueta adjunta genera un ion indicador de baja masa molecular que puede usarse para cuantificar relativamente los péptidos y las proteínas de las que se originaron.
Una etiqueta de masa en tándem (TMT) es una etiqueta química de etiqueta de masa isobárica que se utiliza para la cuantificación e identificación de proteínas. [57] Las etiquetas contienen cuatro regiones: informador de masas, conector escindible, normalización de masas y grupo reactivo de proteínas. Los reactivos TMT se pueden utilizar para analizar simultáneamente de 2 a 11 muestras de péptidos diferentes preparadas a partir de células, tejidos o fluidos biológicos. Los desarrollos recientes permiten analizar hasta 16 e incluso 18 muestras (16plex o 18plex respectivamente). [58] [59] Hay tres tipos de reactivos TMT disponibles con diferentes reactividades químicas: (1) un grupo funcional éster NHS reactivo para marcar aminas primarias (TMTduplex, TMTsixplex, TMT10plex más TMT11-131C), (2) un reactivo yodoacetilo funcional grupo para marcar sulfhidrilos libres (yodoTMT) y (3) grupo funcional alcoxiamina reactiva para marcar carbonilos (aminoxiTMT).

La espectrometría de masas en tándem se puede utilizar para la secuenciación de proteínas . [60] Cuando las proteínas intactas se introducen en un analizador de masas, esto se llama " proteómica de arriba hacia abajo " y cuando las proteínas se digieren en péptidos más pequeños y posteriormente se introducen en el espectrómetro de masas, esto se llama " proteómica de abajo hacia arriba ". La proteómica de escopeta es una variante de la proteómica de abajo hacia arriba en la que las proteínas de una mezcla se digieren antes de la separación y la espectrometría de masas en tándem.
La espectrometría de masas en tándem puede producir una etiqueta de secuencia peptídica que puede usarse para identificar un péptido en una base de datos de proteínas. [61] [62] [63] Se ha desarrollado una notación para indicar fragmentos de péptidos que surgen de un espectro de masas en tándem. [64] Los iones de fragmentos de péptidos se indican con a, b o c si la carga se retiene en el extremo N y con x, y o z si la carga se mantiene en el extremo C. El subíndice indica el número de residuos de aminoácidos en el fragmento. A veces se utilizan superíndices para indicar pérdidas neutras además de la fragmentación de la columna vertebral, * para pérdida de amoníaco y ° para pérdida de agua. Aunque la escisión del esqueleto peptídico es la más útil para la secuenciación y la identificación de péptidos, se pueden observar otros iones fragmentados en condiciones de disociación de alta energía. Estos incluyen los iones de pérdida de cadena lateral d, v, w e iones de amonio [65] [66] y iones de fragmentos específicos de secuencia adicionales asociados con residuos de aminoácidos particulares. [67]
Los oligosacáridos se pueden secuenciar usando espectrometría de masas en tándem de manera similar a la secuenciación de péptidos. [68] La fragmentación generalmente ocurre en ambos lados del enlace glicosídico (iones b, c, y y z), pero también en condiciones más energéticas a través de la estructura del anillo de azúcar en una escisión de anillos cruzados (iones x). Nuevamente se utilizan subíndices finales para indicar la posición de la escisión a lo largo de la cadena. Para iones de escisión de anillos cruzados, la naturaleza de la escisión de anillos cruzados se indica mediante superíndices anteriores. [69] [70]
La espectrometría de masas en tándem se ha aplicado a la secuenciación de ADN y ARN . [71] [72] Se ha propuesto una notación para la fragmentación en fase gaseosa de iones oligonucleótidos . [73]
El cribado neonatal es el proceso de realizar pruebas a los recién nacidos para detectar enfermedades genéticas , endocrinológicas , metabólicas y hematológicas tratables . [74] [75] El desarrollo de la detección por espectrometría de masas en tándem a principios de la década de 1990 condujo a una gran expansión de enfermedades metabólicas congénitas potencialmente detectables que afectan los niveles sanguíneos de ácidos orgánicos. [76]
Análisis de moléculas pequeñas
Se ha demostrado que los datos de espectrometría de masas en tándem son muy consistentes entre las plataformas de instrumentos y fabricantes, incluida la instrumentación de tiempo de vuelo cuadrupolo (QTOF) y Q Exactive, especialmente a 20 eV. [77]
La espectrometría de masas en tándem no se puede aplicar para análisis de células individuales, ya que es insensible analizar cantidades tan pequeñas de una célula. Estas limitaciones se deben principalmente a una combinación de producción ineficiente de iones y pérdidas de iones dentro de los instrumentos debido a fuentes de ruido químico de los disolventes. [78]
La espectrometría de masas en tándem será una herramienta útil para la caracterización de proteínas, complejos de nucleoproteínas y otras estructuras biológicas. Sin embargo, quedaron algunos retos como analizar cuantitativa y cualitativamente la caracterización del proteoma. [79]
{{cite journal}}: Citar diario requiere |journal=( ayuda )