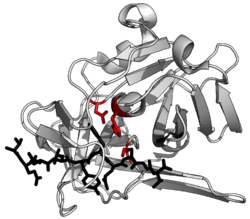
Una proteasa (también llamada peptidasa , proteinasa o enzima proteolítica ) [1] es una enzima que cataliza la proteólisis , descomponiendo las proteínas en polipéptidos más pequeños o aminoácidos individuales y estimulando la formación de nuevos productos proteicos. [2] Lo hacen escindiendo los enlaces peptídicos dentro de las proteínas mediante hidrólisis , una reacción en la que el agua rompe los enlaces . Las proteasas participan en numerosas vías biológicas, incluida la digestión de proteínas ingeridas, el catabolismo de proteínas (descomposición de proteínas viejas), [3] [4] y la señalización celular .
En ausencia de aceleradores funcionales, la proteólisis sería muy lenta y tardaría cientos de años . [5] Las proteasas se pueden encontrar en todas las formas de vida y virus . Han evolucionado independientemente varias veces y diferentes clases de proteasas pueden realizar la misma reacción mediante mecanismos catalíticos completamente diferentes .
Las proteasas se pueden clasificar en siete grandes grupos: [6]
Las proteasas se agruparon por primera vez en 84 familias según su relación evolutiva en 1993, y se clasificaron en cuatro tipos catalíticos: serina , cisteína , aspártico y metaloproteasas . [7] Las proteasas treonina y glutámica no se describieron hasta 1995 y 2004, respectivamente. El mecanismo utilizado para escindir un enlace peptídico implica hacer nucleofílico un residuo de aminoácido que tiene la cisteína y la treonina (proteasas) o una molécula de agua (aspártico, glutámico y metaloproteasas) para que pueda atacar al grupo carbonilo del péptido. Una forma de crear un nucleófilo es mediante una tríada catalítica , donde se utiliza un residuo de histidina para activar la serina , la cisteína o la treonina como nucleófilo. Sin embargo, esta no es una agrupación evolutiva, ya que los tipos de nucleófilos han evolucionado de manera convergente en diferentes superfamilias , y algunas superfamilias muestran una evolución divergente hacia múltiples nucleófilos diferentes. Las metaloproteasas, las proteasas aspárticas y glutámicas utilizan los residuos de su sitio activo para activar una molécula de agua, que luego ataca el enlace escindible. [8]
Un séptimo tipo catalítico de enzimas proteolíticas, la asparagina péptido liasa , se describió en 2011. Su mecanismo proteolítico es inusual ya que, en lugar de hidrólisis , realiza una reacción de eliminación . [9] Durante esta reacción, la asparagina catalítica forma una estructura química cíclica que se escinde en los residuos de asparagina en las proteínas en las condiciones adecuadas. Dado su mecanismo fundamentalmente diferente, su inclusión como peptidasa puede ser discutible. [9]
En la base de datos MEROPS se encuentra una clasificación actualizada de las superfamilias evolutivas de proteasas. [10] En esta base de datos, las proteasas se clasifican en primer lugar por 'clan' ( superfamilia ) según la estructura, el mecanismo y el orden de los residuos catalíticos (por ejemplo, el clan PA , donde P indica una mezcla de familias de nucleófilos). Dentro de cada 'clan', las proteasas se clasifican en familias según la similitud de secuencia (por ejemplo, las familias S1 y C3 dentro del clan PA). Cada familia puede contener cientos de proteasas relacionadas (por ejemplo , tripsina , elastasa , trombina y estreptogrisina dentro de la familia S1).
Actualmente se conocen más de 50 clanes, cada uno de los cuales indica un origen evolutivo independiente de la proteólisis. [10]
Alternativamente, las proteasas pueden clasificarse según el pH óptimo en el que están activas:
Las proteasas participan en la digestión de largas cadenas de proteínas en fragmentos más cortos mediante la división de los enlaces peptídicos que unen los residuos de aminoácidos . Algunas separan los aminoácidos terminales de la cadena proteica ( exopeptidasas , como aminopeptidasas , carboxipeptidasa A ); otros atacan los enlaces peptídicos internos de una proteína ( endopeptidasas , como tripsina , quimotripsina , pepsina , papaína , elastasa ).
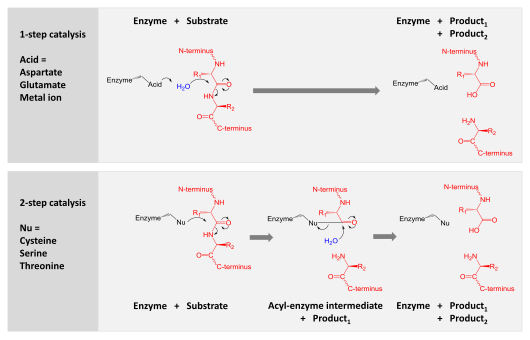
La catálisis se logra mediante uno de dos mecanismos:
La proteólisis puede ser muy promiscua, de modo que se hidroliza una amplia gama de sustratos proteicos. Este es el caso de las enzimas digestivas como la tripsina , que deben poder escindir el conjunto de proteínas ingeridas en fragmentos peptídicos más pequeños. Las proteasas promiscuas normalmente se unen a un solo aminoácido del sustrato y, por lo tanto, solo tienen especificidad por ese residuo. Por ejemplo, la tripsina es específica para las secuencias ...K\... o ...R\... ('\'=sitio de escisión). [12]
Por el contrario, algunas proteasas son muy específicas y sólo escinden sustratos con una secuencia determinada. La coagulación sanguínea (como la trombina ) y el procesamiento de poliproteínas virales (como la proteasa TEV ) requieren este nivel de especificidad para lograr eventos de escisión precisos. Esto se logra mediante proteasas que tienen una hendidura o túnel de unión larga con varias bolsas que se unen a residuos específicos. Por ejemplo, la proteasa TEV es específica para la secuencia ...ENLYFQ\S... ('\'=sitio de escisión). [13]
Las proteasas, al ser proteínas, son escindidas por otras moléculas de proteasa, a veces de la misma variedad. Esto actúa como un método de regulación de la actividad de las proteasas. Algunas proteasas son menos activas después de la autólisis (por ejemplo, proteasa TEV ), mientras que otras son más activas (por ejemplo, tripsinógeno ).
Las proteasas se encuentran en todos los organismos, desde procariotas hasta eucariotas y virus . Estas enzimas participan en una multitud de reacciones fisiológicas, desde la simple digestión de proteínas alimentarias hasta cascadas altamente reguladas (p. ej., la cascada de coagulación sanguínea , el sistema del complemento , las vías de apoptosis y la cascada activadora de la profenoloxidasa de invertebrados). Las proteasas pueden romper enlaces peptídicos específicos ( proteólisis limitada ), dependiendo de la secuencia de aminoácidos de una proteína, o descomponer completamente un péptido en aminoácidos ( proteólisis ilimitada ). La actividad puede ser un cambio destructivo (abolir la función de una proteína o digerirla en sus componentes principales), puede ser una activación de una función o puede ser una señal en una vía de señalización.
Los genomas de las plantas codifican cientos de proteasas, en gran parte de función desconocida. Aquellos con función conocida participan en gran medida en la regulación del desarrollo . [14] Las proteasas vegetales también desempeñan un papel en la regulación de la fotosíntesis . [15]
Las proteasas se utilizan en todo el organismo para diversos procesos metabólicos. Las proteasas ácidas secretadas en el estómago (como la pepsina ) y las serina proteasas presentes en el duodeno ( tripsina y quimotripsina ) nos permiten digerir las proteínas de los alimentos. Las proteasas presentes en el suero sanguíneo ( trombina , plasmina , factor de Hageman , etc.) juegan un papel importante en la coagulación de la sangre, así como en la lisis de los coágulos y en la correcta acción del sistema inmunológico. Otras proteasas están presentes en los leucocitos ( elastasa , catepsina G ) y desempeñan varias funciones diferentes en el control metabólico. Algunos venenos de serpiente también son proteasas, como la hemotoxina de la víbora , e interfieren en la cascada de coagulación sanguínea de la víctima. Las proteasas determinan la vida útil de otras proteínas que desempeñan funciones fisiológicas importantes, como hormonas, anticuerpos u otras enzimas. Éste es uno de los mecanismos reguladores de "encendido" y "apagado" más rápidos en la fisiología de un organismo.
Mediante una acción cooperativa compleja, las proteasas pueden catalizar reacciones en cascada , que dan como resultado una amplificación rápida y eficiente de la respuesta de un organismo a una señal fisiológica.
Las bacterias secretan proteasas para hidrolizar los enlaces peptídicos de las proteínas y, por lo tanto, descomponerlas en sus aminoácidos constituyentes . Las proteasas bacterianas y fúngicas son particularmente importantes para los ciclos globales del carbono y el nitrógeno en el reciclaje de proteínas, y dicha actividad tiende a estar regulada por señales nutricionales en estos organismos. [16] El impacto neto de la regulación nutricional de la actividad de las proteasas entre las miles de especies presentes en el suelo se puede observar a nivel general de la comunidad microbiana a medida que las proteínas se descomponen en respuesta a la limitación de carbono, nitrógeno o azufre. [17]
Las bacterias contienen proteasas responsables del control general de la calidad de las proteínas (por ejemplo, el proteasoma AAA+ ) al degradar las proteínas desplegadas o mal plegadas .
Una proteasa bacteriana secretada también puede actuar como exotoxina y ser un ejemplo de factor de virulencia en la patogénesis bacteriana (por ejemplo, toxina exfoliativa ). Las proteasas exotóxicas bacterianas destruyen las estructuras extracelulares.
Los genomas de algunos virus codifican una poliproteína masiva , que necesita una proteasa para dividirla en unidades funcionales (por ejemplo, el virus de la hepatitis C y los picornavirus ). [18] Estas proteasas (por ejemplo, proteasa TEV ) tienen una alta especificidad y solo escinden un conjunto muy restringido de secuencias de sustrato. Por tanto, son un objetivo común para los inhibidores de proteasa . [19] [20]
Archaea utiliza proteasas para regular diversos procesos celulares, desde la señalización celular , el metabolismo , la secreción y el control de la calidad de las proteínas. [21] [22] Sólo dos proteasas dependientes de ATP se encuentran en las arqueas: la proteasa LonB asociada a la membrana y un complejo de proteosoma soluble 20S . [21]
El campo de la investigación de las proteasas es enorme. Desde 2004, cada año se publicaron aproximadamente 8.000 artículos relacionados con este campo. [23] Las proteasas se utilizan en la industria, la medicina y como herramienta de investigación biológica básica. [24] [25]
Las proteasas digestivas forman parte de muchos detergentes para ropa y también se utilizan ampliamente en la industria del pan como mejorantes del pan . En medicina se utilizan diversas proteasas tanto para su función nativa (p. ej., control de la coagulación sanguínea) como para funciones completamente artificiales ( p. ej., para la degradación selectiva de proteínas patógenas). Proteasas altamente específicas como la proteasa TEV y la trombina se usan comúnmente para escindir proteínas de fusión y etiquetas de afinidad de forma controlada. Las soluciones vegetales que contienen proteasa llamadas cuajo vegetariano se han utilizado durante cientos de años en Europa y Medio Oriente para elaborar quesos kosher y halal . El cuajo vegetariano de Withania coagulans se utiliza desde hace miles de años como remedio ayurvédico para la digestión y la diabetes en el subcontinente indio. También se utiliza para hacer Paneer .
La actividad de las proteasas es inhibida por los inhibidores de proteasas . [26] Un ejemplo de inhibidores de proteasa es la superfamilia de serpinas . Incluye alfa 1-antitripsina (que protege al cuerpo de los efectos excesivos de sus propias proteasas inflamatorias ), alfa 1-antiquimotripsina (que hace lo mismo), inhibidor de C1 (que protege al cuerpo de la activación excesiva de su propio sistema del complemento desencadenada por proteasas). ), antitrombina (que protege al cuerpo de una coagulación excesiva ), inhibidor-1 del activador del plasminógeno (que protege al cuerpo de una coagulación inadecuada al bloquear la fibrinólisis desencadenada por proteasas ) y neuroserpina . [27]
Los inhibidores de proteasas naturales incluyen la familia de proteínas lipocalinas , que desempeñan un papel en la regulación y diferenciación celular. Se ha descubierto que los ligandos lipofílicos , unidos a proteínas lipocalinas, poseen propiedades inhibidoras de proteasas tumorales. Los inhibidores de proteasa naturales no deben confundirse con los inhibidores de proteasa utilizados en la terapia antirretroviral. Algunos virus , entre ellos el VIH/SIDA , dependen de proteasas en su ciclo reproductivo. Por tanto, los inhibidores de proteasa se desarrollan como agentes terapéuticos antivirales .
Otros inhibidores de proteasas naturales se utilizan como mecanismos de defensa. Ejemplos comunes son los inhibidores de tripsina que se encuentran en las semillas de algunas plantas, siendo los más notables para los humanos la soja, un cultivo alimentario importante, donde actúan para disuadir a los depredadores. La soja cruda es tóxica para muchos animales, incluidos los humanos, hasta que los inhibidores de proteasa que contienen se desnaturalizan.
Evaluar las competencias relativas de las enzimas que catalizan la hidrólisis de los enlaces peptídicos internos y C-terminales [...]