El embarazo ectópico es una complicación del embarazo en la que el embrión se adhiere fuera del útero . [5] Los signos y síntomas incluyen clásicamente dolor abdominal y sangrado vaginal , pero menos del 50 por ciento de las mujeres afectadas tienen ambos síntomas. [1] El dolor puede describirse como agudo, sordo o tipo calambres. [1] El dolor también puede extenderse al hombro si se ha producido sangrado en el abdomen. [1] El sangrado grave puede provocar una frecuencia cardíaca rápida , desmayos o shock . [5] [1] Con muy raras excepciones, el feto no puede sobrevivir. [6]
En general, los embarazos ectópicos afectan anualmente a menos del 2% de los embarazos en todo el mundo. [5] Los factores de riesgo para el embarazo ectópico incluyen enfermedad inflamatoria pélvica , a menudo debido a infección por clamidia ; tabaquismo ; endometriosis ; cirugía tubárica previa; antecedentes de infertilidad ; y el uso de tecnología de reproducción asistida . [2] Aquellos que previamente han tenido un embarazo ectópico tienen un riesgo mucho mayor de tener otro. [2] La mayoría de los embarazos ectópicos (90%) ocurren en las trompas de Falopio , que se conocen como embarazos tubáricos, [2] pero la implantación también puede ocurrir en el cuello uterino , los ovarios , la cicatriz de la cesárea o dentro del abdomen . [1] La detección del embarazo ectópico generalmente se realiza mediante análisis de sangre para gonadotropina coriónica humana (hCG) y ecografía . [1] Esto puede requerir pruebas en más de una ocasión. [1] Otras causas de síntomas similares incluyen: aborto espontáneo , torsión ovárica y apendicitis aguda . [1]
La prevención consiste en disminuir los factores de riesgo, como las infecciones por clamidia, mediante la detección y el tratamiento. [7] Si bien algunos embarazos ectópicos se abortan sin tratamiento, [2] el tratamiento estándar para el embarazo ectópico es un procedimiento para extraer el embrión de la trompa de Falopio o para extirpar la trompa de Falopio por completo. El uso del medicamento metotrexato funciona tan bien como la cirugía en algunos casos. [2] Específicamente, funciona bien cuando el beta-HCG es bajo y el tamaño del ectópico es pequeño. [2] La cirugía, como la salpingectomía , todavía se recomienda típicamente si la trompa se ha roto, hay un latido cardíaco fetal o los signos vitales de la mujer son inestables. [2] La cirugía puede ser laparoscópica o mediante una incisión más grande, conocida como laparotomía . [5] La morbilidad y la mortalidad maternas se reducen con el tratamiento. [2]
La tasa de embarazo ectópico es de aproximadamente 11 a 20 por cada 1.000 nacidos vivos en los países desarrollados, aunque puede ser tan alta como el 4% entre quienes utilizan tecnología de reproducción asistida . [5] Es la causa más común de muerte entre las mujeres durante el primer trimestre con aproximadamente el 6-13% del total. [2] En el mundo desarrollado los resultados han mejorado mientras que en el mundo en desarrollo a menudo siguen siendo malos. [7] El riesgo de muerte entre las personas en el mundo desarrollado es de entre el 0,1 y el 0,3 por ciento, mientras que en el mundo en desarrollo es de entre el uno y el tres por ciento. [4] La primera descripción conocida de un embarazo ectópico es de Al-Zahrawi en el siglo XI. [7] La palabra "ectópico" significa "fuera de lugar". [8]
Hasta un 10% de las mujeres con embarazo ectópico no presentan síntomas y un tercio no presenta signos médicos . [5] En muchos casos, los síntomas tienen una especificidad baja y pueden ser similares a los de otros trastornos genitourinarios y gastrointestinales , como apendicitis , salpingitis , ruptura de un quiste del cuerpo lúteo , aborto espontáneo, torsión ovárica o infección del tracto urinario . [5] La presentación clínica del embarazo ectópico ocurre una media de 7,2 semanas después del último período menstrual normal, con un rango de cuatro a ocho semanas. Las presentaciones más tardías son más comunes en comunidades privadas de la capacidad de diagnóstico moderna. [ cita requerida ]
Los signos y síntomas de un embarazo ectópico incluyen aumento de hCG, sangrado vaginal (en cantidades variables), dolor abdominal inferior repentino, [5] dolor pélvico, cuello uterino sensible, una masa anexial o sensibilidad anexial. [1] En ausencia de ecografía o evaluación de hCG , un sangrado vaginal abundante puede llevar a un diagnóstico erróneo de aborto espontáneo. [5] Las náuseas , los vómitos y la diarrea son síntomas más raros de un embarazo ectópico. [5]
La ruptura de un embarazo ectópico puede provocar síntomas como distensión abdominal , dolor a la palpación , peritonismo y shock hipovolémico . [5] Una persona con un embarazo ectópico roto puede sentir dolor al acostarse y puede preferir mantener una postura erguida, ya que el flujo sanguíneo intrapélvico puede provocar hinchazón de la cavidad abdominal y causar dolor adicional. [9]
La complicación más frecuente es la rotura con hemorragia interna que puede derivar en un shock hipovolémico. El daño a las trompas de Falopio puede dificultar el embarazo en el futuro. La otra trompa de Falopio de la mujer puede funcionar lo suficiente para el embarazo. Después de la extirpación de una trompa de Falopio dañada, el embarazo sigue siendo posible en el futuro. Si se extirpan ambas, la fertilización in vitro sigue siendo una opción para las mujeres que esperan quedarse embarazadas. [10] [11] [12]
Existen varios factores de riesgo para los embarazos ectópicos. Sin embargo, en hasta un tercio [13] a la mitad [14] no se pueden identificar factores de riesgo. Los factores de riesgo incluyen: enfermedad inflamatoria pélvica , infertilidad, uso de un dispositivo intrauterino (DIU), exposición previa al dietilestilbestrol (DES), cirugía de trompas, cirugía intrauterina (p. ej ., D&C ), tabaquismo , embarazo ectópico previo, endometriosis y ligadura de trompas . [15] [16] Un aborto inducido previo no parece aumentar el riesgo. [17] El DIU no aumenta el riesgo de embarazo ectópico, pero con un DIU si se produce el embarazo es más probable que sea ectópico que intrauterino. [18] El riesgo de embarazo ectópico después de una infección por clamidia es bajo. [19] El mecanismo exacto a través del cual la clamidia aumenta el riesgo de embarazo ectópico es incierto, aunque algunas investigaciones sugieren que la infección puede afectar la estructura de las trompas de Falopio. [20]

El embarazo tubárico es cuando el óvulo se implanta en las trompas de Falopio. Los cilios similares a pelos ubicados en la superficie interna de las trompas de Falopio llevan el óvulo fertilizado al útero. Los cilios de Falopio a veces se ven en cantidades reducidas después de un embarazo ectópico, lo que lleva a la hipótesis de que el daño de los cilios en las trompas de Falopio probablemente conduzca a un embarazo ectópico. [23] Las mujeres que fuman tienen una mayor probabilidad de un embarazo ectópico en las trompas de Falopio. Fumar conduce a factores de riesgo de daño y destrucción de los cilios. [23] A medida que los cilios se degeneran, aumenta la cantidad de tiempo que tarda el óvulo fertilizado en llegar al útero. El óvulo fertilizado, si no llega al útero a tiempo, eclosionará de la zona pelúcida no adhesiva y se implantará dentro de la trompa de Falopio, causando así el embarazo ectópico. [ cita requerida ]
Las mujeres con enfermedad inflamatoria pélvica (EIP) tienen una alta incidencia de embarazo ectópico. [24] Esto resulta de la acumulación de tejido cicatricial en las trompas de Falopio, causando daño a los cilios. [25] Sin embargo, si ambas trompas estuvieran completamente bloqueadas, de modo que el espermatozoide y el óvulo fueran físicamente incapaces de encontrarse, entonces la fertilización del óvulo sería naturalmente imposible, y no podría ocurrir ni un embarazo normal ni un embarazo ectópico. Las adherencias intrauterinas (IUA) presentes en el síndrome de Asherman pueden causar un embarazo cervical ectópico o, si las adherencias bloquean parcialmente el acceso a las trompas a través de los ostia , un embarazo tubárico ectópico. [26] [27] [28] El síndrome de Asherman generalmente ocurre por cirugía intrauterina, más comúnmente después de D&C . [26] La tuberculosis endometrial/pélvica/genital , otra causa del síndrome de Asherman, también puede provocar un embarazo ectópico ya que la infección puede provocar adherencias tubáricas además de adherencias intrauterinas. [29]
La ligadura de trompas puede predisponer a un embarazo ectópico. La reversión de la esterilización tubárica ( reversión tubárica ) conlleva un riesgo de embarazo ectópico. Este riesgo es mayor si se han utilizado métodos más destructivos de ligadura de trompas (cauterio tubárico, extirpación parcial de las trompas) que si se han utilizado métodos menos destructivos (clipaje tubárico). Los antecedentes de embarazo tubárico aumentan el riesgo de que se produzcan en el futuro hasta aproximadamente el 10 %. [25] Este riesgo no se reduce con la extirpación de la trompa afectada, incluso si la otra trompa parece normal. El mejor método para diagnosticar esto es realizar una ecografía temprana. [ cita requerida ]
La endometriosis es una enfermedad en la que células similares a las del endometrio , el tejido que recubre el interior del útero, crecen fuera del útero. Un embrión que se adhiere a dichas lesiones da lugar a un embarazo ectópico. Los resultados de un estudio de 30 años sobre los resultados reproductivos y del embarazo, en el que participaron más de 14.000 mujeres en edad fértil, se presentaron en el congreso anual de 2015 de la Sociedad Europea de Reproducción Humana y Embriología (ESHRE). [22] El 39% del grupo de estudio tenía endometriosis confirmada quirúrgicamente. En comparación con sus pares, el subgrupo de endometriosis tenía un riesgo 76% mayor de aborto espontáneo y un riesgo 270% mayor de embarazo ectópico. Los mayores riesgos de endometriosis se atribuyeron a una mayor inflamación pélvica y a cambios estructurales y funcionales en el revestimiento del útero. [ cita requerida ]
Aunque algunas investigaciones han demostrado que las pacientes pueden tener un mayor riesgo de embarazo ectópico con el avance de la edad, se cree que la edad es una variable que podría actuar como un sustituto de otros factores de riesgo. Algunos piensan que las duchas vaginales aumentan los embarazos ectópicos. [25] Las mujeres expuestas al DES en el útero (también conocidas como "hijas del DES") también tienen un riesgo elevado de embarazo ectópico. [30] Sin embargo, el DES no se ha utilizado desde 1971 en los Estados Unidos. [30] También se ha sugerido que la generación patológica de óxido nítrico a través del aumento de la producción de iNOS puede disminuir los latidos ciliares tubáricos y las contracciones del músculo liso y, por lo tanto, afectar el transporte del embrión, lo que en consecuencia puede dar lugar a un embarazo ectópico. [31] El bajo nivel socioeconómico también puede ser un factor de riesgo de embarazo ectópico. [32]
Un embarazo ectópico debe considerarse como la causa de dolor abdominal o sangrado vaginal en todas las personas que tienen una prueba de embarazo positiva . [1] El objetivo principal de los procedimientos de diagnóstico en un posible embarazo ectópico es clasificar según el riesgo en lugar de establecer la ubicación del embarazo. [5]
Una ecografía que muestra un saco gestacional con corazón fetal en la trompa de Falopio tiene una especificidad muy alta de embarazo ectópico. Implica un transductor largo y delgado, cubierto con el gel conductor y una funda de plástico/látex e insertado en la vagina. [33] La ecografía transvaginal tiene una sensibilidad de al menos el 90% para el embarazo ectópico. [5] El hallazgo ecográfico diagnóstico en el embarazo ectópico es una masa anexial que se mueve separada del ovario. En alrededor del 60% de los casos, es una masa anexial no homogénea o no quística a veces conocida como el "signo de la mancha". Generalmente es esférica, pero puede verse una apariencia más tubular en caso de hematosálpinx . Se ha estimado que este signo tiene una sensibilidad del 84% y una especificidad del 99% en el diagnóstico de embarazo ectópico. [5] En el estudio que estimó estos valores, el signo de la mancha tuvo un valor predictivo positivo del 96% y un valor predictivo negativo del 95%. [5] La visualización de un saco gestacional extrauterino vacío se conoce a veces como el "signo del bagel" y está presente en alrededor del 20% de los casos. [5] En otro 20% de los casos, se visualiza un saco gestacional que contiene un saco vitelino o un embrión. [5] Los embarazos ectópicos en los que se visualiza la actividad cardíaca a veces se denominan "ectópicos viables". [5]

La combinación de una prueba de embarazo positiva y la presencia de lo que parece ser un embarazo intrauterino normal no excluye un embarazo ectópico, ya que puede haber un embarazo heterotópico o un "pseudosaco ", que es una acumulación de dentro de la cavidad endometrial que puede observarse en hasta el 20% de las mujeres. [5]
Una pequeña cantidad de líquido libre anecógénico en la bolsa rectouterina se encuentra comúnmente tanto en embarazos intrauterinos como ectópicos. [5] La presencia de líquido ecogénico se estima entre el 28 y el 56% de las mujeres con un embarazo ectópico, e indica fuertemente la presencia de hemoperitoneo . [5] Sin embargo, no necesariamente resulta de una ruptura tubárica, sino que comúnmente es el resultado de una fuga de la abertura tubárica distal . [5] Como regla general, el hallazgo de líquido libre es significativo si alcanza el fondo o está presente en la bolsa vesicouterina . [5] Otro marcador de sangrado intraabdominal grave es la presencia de líquido en el receso hepatorrenal del espacio subhepático . [5]
Actualmente, no se considera que la ecografía Doppler contribuya significativamente al diagnóstico del embarazo ectópico. [5]
Un diagnóstico erróneo común de un embarazo intrauterino normal es cuando el embarazo se implanta lateralmente en un útero arqueado , pudiendo diagnosticarse erróneamente como un embarazo intersticial . [5]

Cuando no se observa un embarazo intrauterino (IUP) en la ecografía, la medición de los niveles de β-gonadotropina coriónica humana (β-hCG) puede ayudar en el diagnóstico. La razón es que un nivel bajo de β-hCG puede indicar que el embarazo es intrauterino pero demasiado pequeño para ser visible en la ecografía. Si bien algunos médicos consideran que el umbral en el que un embarazo intrauterino debería ser visible en la ecografía transvaginal es alrededor de 1500 mUI/ml de β-hCG, una revisión en la serie de exámenes clínicos racionales de JAMA mostró que no existe un umbral único para la β-gonadotropina coriónica humana que confirme un embarazo ectópico. En cambio, la mejor prueba en una mujer embarazada es una ecografía transvaginal de alta resolución. [1] La presencia de una masa anexial en ausencia de un embarazo intrauterino en la ecografía transvaginal aumenta la probabilidad de un embarazo ectópico 100 veces (LR+ 111). Cuando no hay anomalías anexiales en la ecografía transvaginal, la probabilidad de un embarazo ectópico disminuye (LR- 0,12). Un útero vacío con niveles superiores a 1500 mIU/mL puede ser evidencia de un embarazo ectópico, pero también puede ser consistente con un embarazo intrauterino que es simplemente demasiado pequeño para ser visto en la ecografía. Si el diagnóstico es incierto, puede ser necesario esperar unos días y repetir el análisis de sangre. Esto se puede hacer midiendo el nivel de β-hCG aproximadamente 48 horas después y repitiendo la ecografía. Los índices de hCG sérica y los modelos de regresión logística parecen ser mejores que el nivel absoluto de hCG sérica única. [35] Si el nivel de β-hCG cae en el examen repetido, esto sugiere fuertemente un aborto espontáneo o una ruptura. La caída en la hCG sérica durante 48 horas se puede medir como el índice de hCG, que se calcula como: [5]
Una proporción de hCG de 0,87, es decir, una disminución de hCG del 13% en 48 horas, tiene una sensibilidad del 93% y una especificidad del 97% para predecir un embarazo fallido de localización desconocida (PUL). [5] La mayoría de los casos de embarazo ectópico tendrán niveles séricos seriados de hCG que aumentan más lentamente de lo que se esperaría con un IUP (es decir, un aumento subóptimo ), o disminuyen más lentamente de lo que se esperaría con un PUL fallido. Sin embargo, hasta el 20% de los casos de embarazo ectópico tienen tiempos de duplicación de hCG sérica similares a los de un IUP, y alrededor del 10% de los casos de EP tienen patrones de hCG similares a un PUL fallido. [5]
También se puede realizar una laparoscopia o laparotomía para confirmar visualmente un embarazo ectópico. Esto generalmente se reserva para mujeres que presentan signos de abdomen agudo y shock hipovolémico . [5] A menudo, si se ha producido un aborto tubárico o una rotura tubárica, es difícil encontrar el tejido del embarazo. Una laparoscopia en un embarazo ectópico muy temprano rara vez muestra una trompa de Falopio de aspecto normal. [ cita requerida ]
La culdocentesis , en la que se extrae líquido del espacio que separa la vagina y el recto, es una prueba que se realiza con menos frecuencia y que puede utilizarse para detectar hemorragias internas. En esta prueba, se inserta una aguja en el espacio que se encuentra en la parte superior de la vagina, detrás del útero y delante del recto. La sangre o el líquido que se encuentren pueden proceder de un embarazo ectópico roto. [ cita requerida ]
Los niveles de progesterona inferiores a 20 nmol/L tienen un alto valor predictivo de embarazos fallidos, mientras que los niveles superiores a 25 nmol/L probablemente predicen embarazos viables, y los niveles superiores a 60 nmol/L tienen un fuerte valor predictivo. Esto puede ayudar a identificar los PUL fallidos que tienen un riesgo bajo y, por lo tanto, necesitan menos seguimiento. [5] La inhibina A también puede ser útil para predecir la resolución espontánea del PUL, pero no es tan buena como la progesterona para este propósito. [5]
Existen varios modelos matemáticos, como los modelos de regresión logística y las redes bayesianas, para la predicción del resultado de PUL en función de múltiples parámetros. [5] Los modelos matemáticos también tienen como objetivo identificar PUL que son de bajo riesgo , es decir, PUL fallidos y PIU fallidos. [5]
La dilatación y el legrado (D&C) se utilizan a veces para diagnosticar la ubicación del embarazo con el objetivo de diferenciar entre un embarazo no deseado y un embarazo intrauterino no viable en situaciones en las que se puede descartar un embarazo intrauterino viable. Las indicaciones específicas para este procedimiento incluyen cualquiera de las siguientes: [5]
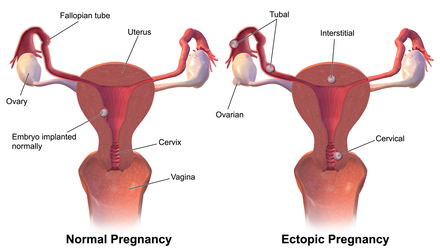
La gran mayoría de los embarazos ectópicos se implantan en la trompa de Falopio. Los embarazos pueden desarrollarse en el extremo fimbrial (5% de todos los embarazos ectópicos), la sección ampular (80%), el istmo (12%) y la parte cornual e intersticial de la trompa (2%). [25] La mortalidad de un embarazo tubárico en el istmo o dentro del útero (embarazo intersticial) es mayor debido a que existe una mayor vascularidad que puede resultar más probable en un sangrado interno repentino importante. Una revisión publicada en 2010 apoya la hipótesis de que el embarazo ectópico tubárico es causado por una combinación de retención del embrión dentro de la trompa de Falopio debido a un transporte embrión-tubárico deficiente y alteraciones en el entorno tubárico que permiten que se produzca una implantación temprana. [36]
El dos por ciento de los embarazos ectópicos se producen en el ovario, el cuello uterino o son intraabdominales. La ecografía transvaginal suele ser capaz de detectar un embarazo cervical . Un embarazo ovárico se diferencia de un embarazo tubárico según los criterios de Spiegelberg . [37]
Aunque el feto de un embarazo ectópico no suele ser viable, muy raramente se ha producido un parto de un feto vivo a partir de un embarazo abdominal . En tal situación, la placenta se asienta sobre los órganos intraabdominales o el peritoneo y ha encontrado suficiente suministro de sangre. Generalmente se trata del intestino o el mesenterio, pero se han descrito otros sitios, como la arteria renal (riñón), el hígado o la arteria hepática (hígado) o incluso la aorta. En ocasiones se ha descrito el apoyo a la viabilidad cercana, pero incluso en los países del Tercer Mundo , el diagnóstico se realiza con mayor frecuencia entre las 16 y 20 semanas de gestación. Un feto de este tipo tendría que nacer por laparotomía. La morbilidad y la mortalidad maternas por embarazo extrauterino son altas, ya que los intentos de extraer la placenta de los órganos a los que está adherida suelen provocar un sangrado incontrolable en el sitio de unión. Si el órgano al que está adherida la placenta es extraíble, como una sección del intestino, entonces la placenta debe extraerse junto con ese órgano. Este es un fenómeno tan poco frecuente que no se dispone de datos reales y se debe confiar en informes anecdóticos. [38] [39] [40] Sin embargo, la gran mayoría de los embarazos abdominales requieren intervención mucho antes de la viabilidad fetal debido al riesgo de sangrado.
Con el aumento de las cesáreas realizadas en todo el mundo, [41] [42] los embarazos ectópicos por cesárea (CSP) son raros, pero se están volviendo más comunes. La incidencia de CSP no se conoce bien, sin embargo, ha habido estimaciones basadas en diferentes poblaciones de 1:1800–1:2216. [43] [44] Los CSP se caracterizan por la implantación anormal en la cicatriz de una cesárea anterior, [45] y si se permite que continúen pueden causar complicaciones graves como ruptura uterina y hemorragia. [44] Las pacientes con CSP generalmente no presentan síntomas, sin embargo, los síntomas pueden incluir sangrado vaginal que puede o no estar asociado con dolor. [46] [47] El diagnóstico de CSP se realiza mediante ecografía y se observan cuatro características: (1) Cavidad uterina vacía con franja endometrial hiperecogénica brillante (2) Canal cervical vacío (3) Masa intrauterina en la parte anterior del istmo uterino, y (4) Ausencia de la capa muscular uterina anterior, y/o ausencia o adelgazamiento entre la vejiga y el saco gestacional, que mide menos de 5 mm. [45] [48] [49] Dada la rareza del diagnóstico, las opciones de tratamiento tienden a describirse en informes de casos y series, que van desde médicas con metotrexato o KCl [50] hasta quirúrgicas con dilatación y legrado, [51] resección uterina en cuña, [ cita requerida ] o histerectomía. [47] También se ha descrito una técnica de catéter de doble balón, [52] que permite la preservación uterina. El riesgo de recurrencia de CSP es desconocido, y se recomienda una ecografía temprana en el siguiente embarazo. [45]
En casos poco frecuentes de embarazo ectópico, puede haber dos óvulos fertilizados, uno fuera del útero y el otro dentro. Esto se llama embarazo heterotópico . [1] A menudo, el embarazo intrauterino se descubre más tarde que el ectópico, principalmente debido a la naturaleza dolorosa de emergencia de los embarazos ectópicos. Dado que los embarazos ectópicos normalmente se descubren y se eliminan muy temprano en el embarazo, es posible que una ecografía no encuentre el embarazo adicional dentro del útero. Cuando los niveles de hCG continúan aumentando después de la eliminación del embarazo ectópico, existe la posibilidad de que un embarazo dentro del útero aún sea viable. Esto normalmente se descubre a través de una ecografía. [ cita requerida ]
Aunque son poco frecuentes, los embarazos heterotópicos son cada vez más frecuentes, probablemente debido al aumento del uso de la FIV. La tasa de supervivencia del feto uterino de un embarazo heterotópico es de alrededor del 70 %. [53]
Un embarazo en un cuerno rudimentario se refiere a una condición rara y potencialmente mortal que ocurre cuando un óvulo fertilizado se implanta dentro del pequeño cuerno rudimentario de un útero unicorne , que es un tipo de anomalía uterina congénita causada por el desarrollo incompleto de uno de los conductos de Müller . Este tipo de embarazo ectópico a menudo resulta en la ruptura del cuerno rudimentario entre las 10 y 15 semanas de gestación, lo que conlleva un alto riesgo de morbilidad y mortalidad. [54]
Un embarazo ectópico persistente se refiere a la continuación del crecimiento trofoblástico después de una intervención quirúrgica para extirpar un embarazo ectópico. Después de un procedimiento conservador que intenta preservar la trompa de Falopio afectada, como una salpingotomía , en aproximadamente el 15-20% se puede haber extirpado la mayor parte del crecimiento ectópico, pero algo de tejido trofoblástico, tal vez profundamente incrustado, ha escapado a la extracción y continúa creciendo, generando un nuevo aumento en los niveles de hCG. [55] Después de semanas, esto puede provocar nuevos síntomas clínicos, incluido el sangrado. Por esta razón, es posible que se deban controlar los niveles de hCG después de la extirpación de un embarazo ectópico para asegurar su disminución; también se puede administrar metotrexato en el momento de la cirugía de manera profiláctica. [ cita requerida ]
El término embarazo de localización desconocida (PUL, por sus siglas en inglés) se utiliza para referirse a un embarazo en el que el resultado de la prueba de embarazo es positivo, pero no se ha visualizado ningún embarazo mediante una ecografía transvaginal. [5] Los departamentos especializados en embarazos tempranos han estimado que entre el 8 % y el 10 % de las mujeres que se presentan para una evaluación ecográfica en las primeras etapas del embarazo serán clasificadas como que tienen un PUL. [5] La verdadera naturaleza del embarazo puede ser un embarazo intrauterino viable en curso, un embarazo fallido, un embarazo ectópico o, en raras ocasiones, un PUL persistente. [5]
Debido a la frecuente ambigüedad en los exámenes ultrasonográficos, se propone la siguiente clasificación: [5]
En mujeres con un embarazo de localización desconocida, entre el 6% y el 20% tienen un embarazo ectópico. [5] En los casos de embarazo de localización desconocida y antecedentes de sangrado abundante, se ha estimado que aproximadamente el 6% tiene un embarazo ectópico subyacente. [5] Entre el 30% y el 47% de las mujeres con un embarazo de localización desconocida son finalmente diagnosticadas con un embarazo intrauterino en curso, de las cuales la mayoría (50-70%) tendrán embarazos fallidos en los que nunca se confirma la localización. [5]

La PUL persistente es aquella en la que el nivel de hCG no disminuye espontáneamente y no se identifica un embarazo intrauterino o ectópico en la ecografía transvaginal de seguimiento. [5] Es probable que una PUL persistente sea un embarazo ectópico pequeño que no se ha visualizado o un trofoblasto retenido en la cavidad endometrial. [5] El tratamiento solo debe considerarse cuando se haya excluido definitivamente un embarazo intrauterino potencialmente viable. [5] Una PUL persistente tratada se define como una manejada médicamente (generalmente con metotrexato) sin confirmación de la ubicación del embarazo, como por ecografía, laparoscopia o evacuación uterina. [5] Una PUL persistente resuelta se define como una hCG sérica que alcanza un valor no gestacional (generalmente menor a 5 UI/L) después del manejo expectante o después de la evacuación uterina sin evidencia de vellosidades coriónicas en el examen histopatológico . [5] Por el contrario, un nivel relativamente bajo y no resuelto de hCG sérica indica la posibilidad de un tumor secretor de hCG. [5]
Otras afecciones que causan síntomas similares incluyen: aborto espontáneo, torsión ovárica, apendicitis aguda, quiste ovárico roto, cálculos renales y enfermedad inflamatoria pélvica, entre otras. [1]
La mayoría de las mujeres con un PUL son seguidas con mediciones de hCG sérica y exámenes repetidos de TVS hasta que se confirma un diagnóstico final. [5] Los casos de PUL de bajo riesgo que parecen ser embarazos fallidos pueden ser seguidos con una prueba de embarazo en orina después de dos semanas y obtener asesoramiento telefónico posterior. [5] Los casos de PUL de bajo riesgo que probablemente sean embarazos intrauterinos pueden tener otro TVS en dos semanas para evaluar la viabilidad. [5] Los casos de PUL de alto riesgo requieren una evaluación adicional, ya sea con un TVS dentro de las 48 h o una medición adicional de hCG. [5]
El tratamiento temprano de un embarazo ectópico con metotrexato es una alternativa viable al tratamiento quirúrgico [56] que se desarrolló en la década de 1980. [57] Si se administra al principio del embarazo, el metotrexato detiene el crecimiento del embrión en desarrollo; el embrión en desarrollo puede ser reabsorbido por el cuerpo de la mujer o expulsarse con un período menstrual . Las contraindicaciones incluyen enfermedades hepáticas, renales o sanguíneas, así como una masa embrionaria ectópica > 3,5 cm. [ cita requerida ]
Además, puede conducir a la terminación inadvertida de un embarazo intrauterino no detectado o a una anomalía grave en cualquier embarazo superviviente. [5] Por lo tanto, se recomienda que el metotrexato solo se administre cuando se haya controlado en serie la hCG con un aumento inferior al 35 % durante 48 horas, lo que prácticamente excluye un embarazo intrauterino viable. [5]
En el caso del embarazo ectópico no tubárico, la evidencia de ensayos clínicos aleatorizados en mujeres con CSP es incierta en cuanto al éxito del tratamiento, las complicaciones y los efectos secundarios del metotrexato en comparación con la cirugía ( embolización arterial uterina o quimioembolización arterial uterina). [58]
En Estados Unidos se utiliza un protocolo de dosis múltiples de metotrexato (MTX), que implica cuatro dosis intramusculares junto con una inyección intramuscular de ácido folínico para proteger las células de los efectos de los fármacos y reducir los efectos secundarios. En Francia se sigue el protocolo de dosis única, pero una dosis única tiene mayores probabilidades de fallar. [59]


Si ya se ha producido un sangrado, puede ser necesaria una intervención quirúrgica. Sin embargo, decidir si se debe recurrir a una intervención quirúrgica suele ser una decisión difícil en un paciente estable con evidencia mínima de coágulo sanguíneo en la ecografía. [ cita requerida ]
Los cirujanos utilizan la laparoscopia o laparotomía para acceder a la pelvis y pueden incidir en la trompa de Falopio afectada y extirpar solo el embarazo ( salpingostomía ) o extirpar la trompa afectada con el embarazo ( salpingectomía ). La primera cirugía exitosa para un embarazo ectópico fue realizada por Robert Lawson Tait en 1883. [60] Se estima que una tasa aceptable de PUL que finalmente se someten a cirugía es entre 0,5 y 11%. [5] Las personas que se someten a salpingectomía y salpingostomía tienen una tasa similar de embarazo ectópico recurrente de 5% y 8% respectivamente. Además, sus tasas de embarazo intrauterino también son similares, 56% y 61%. [61]
La autotransfusión de la propia sangre de la mujer drenada durante una cirugía puede ser útil en aquellas que tienen mucho sangrado en el abdomen. [62]
Los informes publicados de que un embrión reimplantado sobrevivió hasta el nacimiento fueron desacreditados como falsos. [63]
En los países occidentales, cuando se tratan los embarazos ectópicos, el pronóstico para la madre es muy bueno; la muerte materna es poco frecuente, pero todos los bebés mueren o son abortados. Por ejemplo, en el Reino Unido, entre 2003 y 2005 hubo 32.100 embarazos ectópicos que dieron lugar a 10 muertes maternas (lo que significa que murió 1 de cada 3.210 mujeres con un embarazo ectópico). [64] En 2006-2008, la Investigación confidencial del Reino Unido sobre muertes maternas determinó que el embarazo ectópico es la causa de 6 muertes maternas (0,26/100.000 embarazos). [18]
Sin embargo, en el mundo en desarrollo, especialmente en África, la tasa de mortalidad es muy alta y los embarazos ectópicos son una de las principales causas de muerte entre las mujeres en edad fértil. [ cita requerida ]
En las mujeres que han tenido un embarazo ectópico, el riesgo de sufrir otro en el siguiente embarazo es de alrededor del 10%. [65]
La fertilidad después de un embarazo ectópico depende de varios factores, el más importante de los cuales es una historia previa de infertilidad. [66] La elección del tratamiento no juega un papel importante; un estudio aleatorizado en 2013 concluyó que las tasas de embarazo intrauterino dos años después del tratamiento del embarazo ectópico son aproximadamente del 64% con cirugía radical, 67% con medicación y 70% con cirugía conservadora. [67] En comparación, la tasa de embarazo acumulada de mujeres menores de 40 años en la población general durante dos años es superior al 90%. [68]
El metotrexato no afecta a los tratamientos de fertilidad futuros. El número de ovocitos que se recuperaron antes y después del tratamiento con metotrexato no cambia. [69]
En caso de embarazo ectópico ovárico, el riesgo de un embarazo ectópico posterior o de infertilidad es bajo. [70]
No hay evidencia de que el masaje mejore la fertilidad después de un embarazo ectópico. [71]

La tasa de embarazo ectópico es de alrededor del 1% y el 2% de la de los nacidos vivos en los países desarrollados, aunque es tan alta como el 4% en los embarazos que involucran tecnología de reproducción asistida. [5] Entre el 93% y el 97% de los embarazos ectópicos se localizan en una trompa de Falopio. [1] De estos, a su vez, el 13% se localizan en el istmo , el 75% se localizan en la ampolla y el 12% en las fimbrias . [5] El embarazo ectópico es responsable del 6% de las muertes maternas durante el primer trimestre del embarazo, lo que lo convierte en la principal causa de muerte materna durante esta etapa del embarazo. [1]
Entre el 5% y el 42% de las mujeres que se someten a una ecografía y dan positivo en la prueba de embarazo tienen un embarazo de localización desconocida, es decir, una prueba de embarazo positiva pero no se visualiza ningún embarazo en la ecografía transvaginal. [5] Entre el 6% y el 20% de los embarazos de localización desconocida son posteriormente diagnosticados como un embarazo ectópico real. [5]
La salpingectomía como tratamiento del embarazo ectópico es uno de los casos más comunes en los que el principio del doble efecto puede utilizarse para justificar la aceleración de la muerte del embrión por parte de médicos y pacientes que se oponen al aborto directo. [73]
En la Iglesia Católica existen debates morales sobre ciertos tratamientos. Un número significativo de moralistas católicos considera que el uso del metotrexato y la intervención de la salpingostomía no son "moralmente permisibles" porque destruyen el embrión; sin embargo, se consideran de manera diferente las situaciones en las que se pone en peligro la salud de la madre y se extirpa toda la trompa de Falopio con el embrión en desarrollo en su interior. [74] [75]
Existen organizaciones que brindan información y apoyo para ayudar a quienes experimentan un embarazo ectópico. Los estudios muestran que las personas pueden experimentar estrés postraumático, depresión y ansiedad para lo cual necesitarían terapias especializadas. [76] Las parejas también pueden experimentar estrés postraumático. [77]
Ha habido casos en los que el embarazo ectópico duró muchos meses y terminó en un bebé vivo nacido por laparotomía.
En julio de 1999, Lori Dalton dio a luz por cesárea en Ogden, Utah , Estados Unidos, a una niña sana, Saige, que se había desarrollado fuera del útero. Las ecografías anteriores no habían descubierto el problema. "El parto de [Dalton] se programó como una cesárea de rutina en el Centro Médico Regional de Ogden en Utah. Cuando el Dr. Naisbitt realizó la cesárea de Lori, se sorprendió al encontrar a Saige dentro de la membrana amniótica fuera del útero..." [78] "Pero lo que hace que este caso sea tan raro es que no solo sobrevivieron la madre y el bebé, sino que ambos están en perfecto estado de salud. El padre, John Dalton, grabó en video el interior de la sala de partos. Saige salió extremadamente bien porque, aunque había sido implantada fuera del útero, un rico suministro de sangre de un fibroma uterino a lo largo de la pared externa del útero la había nutrido con una rica fuente de sangre". [79]
En septiembre de 1999, una mujer inglesa, Jane Ingram (de 32 años) dio a luz a trillizos: Olivia, Mary y Ronan, con un feto extrauterino (Ronan) debajo del útero y gemelos en el útero. Los tres sobrevivieron. Los gemelos que estaban en el útero fueron extraídos primero. [80]
El 29 de mayo de 2008, una mujer australiana, Meera Thangarajah (34 años), que había tenido un embarazo ectópico en el ovario , dio a luz a una niña sana de 2,8 kg, Durga, mediante cesárea. No tuvo problemas ni complicaciones durante las 38 semanas de embarazo. [81] [82]
La gestación ectópica existe en otros mamíferos además del ser humano. En las ovejas , puede llegar a término, con preparación mamaria para el parto y esfuerzos de expulsión . El feto puede ser extraído mediante cesárea. Imágenes de cesárea de una oveja sacrificada , cinco días después del parto.
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )