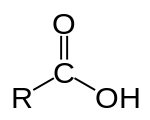


En química orgánica , un ácido carboxílico es un ácido orgánico que contiene un grupo carboxilo ( −C(=O)−OH ) [1] unido a un grupo R. La fórmula general de un ácido carboxílico se escribe a menudo como R−COOH o R−CO 2 H , a veces como R−C(O)OH con R haciendo referencia a un grupo organilo (por ejemplo, alquilo , alquenilo , arilo ), o hidrógeno , u otros grupos. Los ácidos carboxílicos se producen ampliamente. Ejemplos importantes incluyen los aminoácidos y los ácidos grasos . La desprotonación de un ácido carboxílico da un anión carboxilato .
Los ácidos carboxílicos se identifican comúnmente por sus nombres comunes . A menudo tienen el sufijo -ácido ico .También existen nombres recomendados por la IUPAC ; en este sistema, los ácidos carboxílicos tienen un sufijo de ácido -oico . [2] Por ejemplo, el ácido butírico ( CH 3 CH 2 CH 2 CO 2 H ) es ácido butanoico según las pautas de la IUPAC. Para la nomenclatura de moléculas complejas que contienen un ácido carboxílico, el carboxilo puede considerarse la posición uno de la cadena principal incluso si hay otros sustituyentes , como el ácido 3-cloropropanoico . Alternativamente, puede nombrarse como un sustituyente "carboxi" o "ácido carboxílico" en otra estructura principal, como 2-carboxifurano .
El anión carboxilato ( R−COO − o R−CO−2) de un ácido carboxílico se nombra generalmente con el sufijo -ato , de acuerdo con el patrón general de -ico y -ato para un ácido conjugado y su base conjugada, respectivamente. Por ejemplo, la base conjugada del ácido acético es acetato .
El ácido carbónico , que se encuentra en sistemas tampón de bicarbonato en la naturaleza, generalmente no se clasifica como uno de los ácidos carboxílicos, a pesar de que tiene una fracción que parece un grupo COOH.
Los ácidos carboxílicos son polares . Debido a que son aceptores de enlaces de hidrógeno (el carbonilo −C(=O)− ) y donantes de enlaces de hidrógeno (el hidroxilo −OH ), también participan en la formación de enlaces de hidrógeno . Juntos, el grupo hidroxilo y el carbonilo forman el grupo funcional carboxilo. Los ácidos carboxílicos suelen existir como dímeros en medios no polares debido a su tendencia a "autoasociarse". Los ácidos carboxílicos más pequeños (de 1 a 5 carbonos) son solubles en agua, mientras que los ácidos carboxílicos más grandes tienen una solubilidad limitada debido a la naturaleza cada vez más hidrófoba de la cadena alquílica. Estos ácidos de cadena más larga tienden a ser solubles en disolventes menos polares, como éteres y alcoholes. [3] El hidróxido de sodio acuoso y los ácidos carboxílicos, incluso los hidrófobos, reaccionan para producir sales de sodio solubles en agua. Por ejemplo, el ácido enántico tiene una baja solubilidad en agua (0,2 g/L), pero su sal de sodio es muy soluble en agua.
Los ácidos carboxílicos tienden a tener puntos de ebullición más altos que el agua, debido a sus mayores áreas superficiales y su tendencia a formar dímeros estabilizados a través de enlaces de hidrógeno . Para que se produzca la ebullición, se deben romper los enlaces de los dímeros o se debe vaporizar toda la disposición de los dímeros, lo que aumenta significativamente los requisitos de entalpía de vaporización .

Los ácidos carboxílicos son ácidos de Brønsted-Lowry porque son donantes de protones (H + ). Son el tipo más común de ácido orgánico .
Los ácidos carboxílicos son típicamente ácidos débiles , lo que significa que solo se disocian parcialmente en cationes [H 3 O] + y R−CO −2 aniones en solución acuosa neutra . Por ejemplo, a temperatura ambiente, en una solución 1 molar de ácido acético , solo se disocia el 0,001% del ácido (es decir, 10 −5 moles de 1 mol). Los sustituyentes que atraen electrones, como el grupo -CF 3 , dan lugar a ácidos más fuertes (el p K a del ácido acético es 4,76 mientras que el ácido trifluoroacético, con un sustituyente trifluorometilo , tiene un p K a de 0,23). Los sustituyentes que donan electrones dan lugar a ácidos más débiles (el p K a del ácido fórmico es 3,75 mientras que el ácido acético, con un sustituyente metilo , tiene un p K a de 4,76).
La desprotonación de los ácidos carboxílicos produce aniones carboxilato; estos se estabilizan por resonancia , porque la carga negativa se deslocaliza sobre los dos átomos de oxígeno, lo que aumenta la estabilidad del anión. Cada uno de los enlaces carbono-oxígeno en el anión carboxilato tiene un carácter de doble enlace parcial. La carga positiva parcial del carbono carbonílico también se debilita por las cargas negativas - 1 / 2 en los dos átomos de oxígeno.
Los ácidos carboxílicos suelen tener olores ácidos fuertes. Los ésteres de ácidos carboxílicos tienden a tener olores frutales y agradables, y muchos se utilizan en perfumes .
Los ácidos carboxílicos se identifican fácilmente como tales mediante espectroscopia infrarroja . Presentan una banda nítida asociada con la vibración del enlace carbonílico C=O ( ν C=O ) entre 1680 y 1725 cm −1 . Una banda ν O–H característica aparece como un pico ancho en la región de 2500 a 3000 cm −1 . [3] [6] Mediante espectrometría de RMN de 1 H , el hidrógeno hidroxílico aparece en la región de 10–13 ppm, aunque a menudo se ensancha o no se observa debido al intercambio con trazas de agua.
Muchos ácidos carboxílicos se producen industrialmente a gran escala y también se encuentran con frecuencia en la naturaleza. Los ésteres de ácidos grasos son los principales componentes de los lípidos y las poliamidas de ácidos aminocarboxílicos son los principales componentes de las proteínas .
Los ácidos carboxílicos se utilizan en la producción de polímeros, productos farmacéuticos, disolventes y aditivos alimentarios. Los ácidos carboxílicos de importancia industrial incluyen el ácido acético (componente del vinagre, precursor de disolventes y recubrimientos), los ácidos acrílico y metacrílico (precursores de polímeros, adhesivos), el ácido adípico (polímeros), el ácido cítrico (un saborizante y conservante en alimentos y bebidas), el ácido etilendiaminotetraacético (agente quelante), los ácidos grasos (recubrimientos), el ácido maleico (polímeros), el ácido propiónico (conservante de alimentos) y el ácido tereftálico (polímeros). Las sales de carboxilato importantes son los jabones.
En general, las rutas industriales para obtener ácidos carboxílicos difieren de las utilizadas a menor escala porque requieren equipos especializados.
Los métodos preparativos para reacciones a pequeña escala para investigación o para la producción de productos químicos finos a menudo emplean reactivos consumibles costosos.
Muchas reacciones producen ácidos carboxílicos pero se utilizan sólo en casos específicos o son principalmente de interés académico.

Los ácidos carboxílicos reaccionan con bases para formar sales de carboxilato, en las que el hidrógeno del grupo hidroxilo (–OH) se reemplaza por un catión metálico . Por ejemplo, el ácido acético presente en el vinagre reacciona con el bicarbonato de sodio (bicarbonato de sodio) para formar acetato de sodio , dióxido de carbono y agua:
Las reacciones ampliamente practicadas convierten los ácidos carboxílicos en ésteres , amidas , sales de carboxilato , cloruros de ácido y alcoholes . Su conversión a ésteres se usa ampliamente, por ejemplo, en la producción de poliésteres . Del mismo modo, los ácidos carboxílicos se convierten en amidas , pero esta conversión típicamente no ocurre por reacción directa del ácido carboxílico y la amina. En cambio, los ésteres son precursores típicos de las amidas. La conversión de aminoácidos en péptidos es un proceso bioquímico significativo que requiere ATP .
La conversión de un ácido carboxílico en una amida es posible, pero no es sencilla. En lugar de actuar como nucleófilo, una amina reaccionará como base en presencia de un ácido carboxílico para dar la sal de carboxilato de amonio . Calentar la sal a más de 100 °C eliminará el agua y conducirá a la formación de la amida. Este método de síntesis de amidas es importante a nivel industrial y también tiene aplicaciones de laboratorio. [9] En presencia de un catalizador ácido fuerte, los ácidos carboxílicos pueden condensarse para formar anhídridos de ácido. Sin embargo, la condensación produce agua, que puede hidrolizar el anhídrido de nuevo a los ácidos carboxílicos iniciales. Por lo tanto, la formación del anhídrido a través de la condensación es un proceso de equilibrio.
En condiciones catalizadas por ácidos, los ácidos carboxílicos reaccionan con alcoholes para formar ésteres mediante la reacción de esterificación de Fischer , que también es un proceso de equilibrio. Alternativamente, se puede utilizar diazometano para convertir un ácido en un éster. Si bien las reacciones de esterificación con diazometano suelen dar rendimientos cuantitativos, el diazometano solo es útil para formar ésteres metílicos. [9]
Al igual que los ésteres , la mayoría de los ácidos carboxílicos se pueden reducir a alcoholes mediante hidrogenación o utilizando agentes de transferencia de hidruro, como el hidruro de litio y aluminio . Los agentes de transferencia de alquilo fuertes, como los compuestos de organolitio , pero no los reactivos de Grignard , reducirán los ácidos carboxílicos a cetonas junto con la transferencia del grupo alquilo.
El reactivo de Vilsmaier ( cloruro de N , N -dimetil(clorometilen)amonio; [ClHC=N + (CH3 ) 2 ] Cl− ) es un agente altamente quimioselectivo para la reducción de ácido carboxílico. Activa selectivamente el ácido carboxílico para dar la sal de carboximetilenamonio, que puede reducirse con un reductor suave como el hidruro de litio tris( t -butoxi)aluminio para producir un aldehído en un procedimiento de un solo paso. Se sabe que este procedimiento tolera funcionalidades carbonílicas reactivas como cetona, así como fracciones de éster, olefina, nitrilo y haluro moderadamente reactivas. [10]
El grupo hidroxilo de los ácidos carboxílicos se puede reemplazar con un átomo de cloro usando cloruro de tionilo para dar cloruros de acilo . En la naturaleza, los ácidos carboxílicos se convierten en tioésteres . El cloruro de tionilo se puede usar para convertir los ácidos carboxílicos en sus cloruros de acilo correspondientes. Primero, el ácido carboxílico 1 ataca al cloruro de tionilo y el ion cloruro sale. El ion oxonio resultante 2 se activa hacia el ataque nucleofílico y tiene un buen grupo saliente, lo que lo distingue de un ácido carboxílico normal. En el siguiente paso, 2 es atacado por el ion cloruro para dar el intermedio tetraédrico 3 , un clorosulfito. El intermedio tetraédrico colapsa con la pérdida de dióxido de azufre y el ion cloruro, dando cloruro de acilo protonado 4. El ion cloruro puede eliminar el protón en el grupo carbonilo, dando el cloruro de acilo 5 con una pérdida de HCl .
El cloruro de fósforo (III) (PCl 3 ) y el cloruro de fósforo (V) (PCl 5 ) también convierten los ácidos carboxílicos en cloruros de ácido, mediante un mecanismo similar. Un equivalente de PCl 3 puede reaccionar con tres equivalentes de ácido, produciendo un equivalente de H 3 PO 3 , o ácido fosforoso , además del cloruro de ácido deseado. El PCl 5 reacciona con los ácidos carboxílicos en una proporción de 1:1 y produce oxicloruro de fósforo (V) (POCl 3 ) y cloruro de hidrógeno (HCl) como subproductos.
Los ácidos carboxílicos reaccionan con reactivos de Grignard y organolitios para formar cetonas. El primer equivalente de nucleófilo actúa como base y desprotona el ácido. Un segundo equivalente atacará al grupo carbonilo para crear un dianión alcóxido geminal , que se protona durante el procesamiento para dar el hidrato de una cetona. Debido a que la mayoría de los hidratos de cetonas son inestables en relación con sus cetonas correspondientes, el equilibrio entre los dos se desplaza considerablemente a favor de la cetona. Por ejemplo, la constante de equilibrio para la formación de hidrato de acetona a partir de acetona es solo 0,002. El grupo carboxílico es el más ácido en los compuestos orgánicos. [11]
El radical carboxilo , •COOH, solo existe brevemente. [12] La constante de disociación ácida de •COOH se ha medido utilizando espectroscopia de resonancia paramagnética electrónica . [13] El grupo carboxilo tiende a dimerizarse para formar ácido oxálico .