El dextrometorfano ( DXM ), que se comercializa bajo el nombre Robitussin, entre otros, es un supresor de la tos que se utiliza en muchos medicamentos para la tos y el resfriado . [6] En 2022, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó la combinación de dextrometorfano/bupropión para que sirva como antidepresivo de acción rápida en pacientes con trastorno depresivo mayor . [7]
Pertenece a la clase de medicamentos morfinanos con propiedades sedantes , disociativas y estimulantes (en dosis más bajas). El dextrometorfano no tiene una afinidad significativa por la actividad del receptor opioide mu típica de los compuestos morfinanos y ejerce sus efectos terapéuticos a través de varios otros receptores. [8] En su forma pura, el dextrometorfano se presenta como un polvo blanco. [9]
Cuando se exceden las dosis aprobadas, el dextrometorfano actúa como un alucinógeno disociativo . Tiene múltiples mecanismos de acción , incluyendo acciones como inhibidor no selectivo de la recaptación de serotonina [10] y un agonista del receptor sigma-1 . [11] [12] El dextrometorfano y su principal metabolito , el dextrorfano , también bloquean el receptor NMDA en dosis altas, lo que produce efectos similares a otros anestésicos disociativos como la ketamina , el óxido nitroso y la fenciclidina .
Fue patentado en 1949 y aprobado para uso médico en 1953. [13]

El uso principal del dextrometorfano es como supresor de la tos , para el alivio temporal de la tos causada por una irritación menor de la garganta y los bronquios (como la que comúnmente acompaña a la gripe y el resfriado común ), o por irritantes de partículas inhaladas, así como la tos crónica en dosis más altas. [14] [15] El dextrometorfano está disponible solo en forma de jarabe para la tos y pastillas , así como en combinación con otros agentes.
En 2010, la FDA aprobó el fármaco combinado dextrometorfano/quinidina bajo la marca Nuedexta [16] para el tratamiento del afecto pseudobulbar (risa/llanto incontrolable). El dextrometorfano es el agente terapéutico activo en la combinación; la quinidina simplemente sirve para inhibir la degradación enzimática del dextrometorfano y, por lo tanto, aumentar sus concentraciones circulantes a través de la inhibición de CYP2D6 . [17]
El medicamento combinado dextrometorfano/bupropión está aprobado para el trastorno depresivo mayor bajo la marca Auvelity. [18] [19]
Los efectos secundarios del dextrometorfano en dosis terapéuticas normales pueden incluir: [5] [15] [20]
Un efecto secundario poco común es la depresión respiratoria . [15]
En un principio se pensó que el dextrometorfano causaba lesiones de Olney cuando se administraba por vía intravenosa ; sin embargo, más tarde se demostró que esto no era concluyente, debido a la falta de investigación en humanos. Se realizaron pruebas en ratas, administrándoles 50 mg o más todos los días durante un mes. Se observaron cambios neurotóxicos, incluida la vacuolización, en las cortezas cingulada posterior y retroesplenial de ratas a las que se les administraron otros antagonistas del receptor NMDA , como PCP, pero no con dextrometorfano. [21] [22]
En muchos casos documentados [ cita requerida ] , el dextrometorfano ha producido dependencia psicológica en personas que lo usaron recreativamente. Se considera menos adictivo que otros supresores de la tos comunes, como el opiáceo codeína . [5] Dado que el dextrometorfano también actúa como un inhibidor de la recaptación de serotonina, los usuarios informan que el uso recreativo regular durante un largo período de tiempo puede causar síntomas de abstinencia similares a los del síndrome de interrupción del tratamiento con antidepresivos . Además, se han informado alteraciones en el sueño, los sentidos, el movimiento, el estado de ánimo y el pensamiento.
Efectos adversos del dextrometorfano en sobredosis en dosis de 3 a 10 veces la dosis terapéutica recomendada: [23] [ verificación fallida ]
En dosis de 11 a 75 veces la dosis terapéutica recomendada: [23] [ verificación fallida ] [24]
La psicosis aguda episódica puede ocurrir cuando se toman dosis altas de dextrometorfano para uso recreativo, y puede resultar en una abundancia de síntomas psiquiátricos, incluyendo disociación y otros síntomas similares a los del PCP. [24]
El síndrome serotoninérgico puede ser consecuencia del uso combinado de dextrometorfano y antidepresivos serotoninérgicos como los inhibidores selectivos de la recaptación de serotonina (ISRS) o los inhibidores de la monoaminooxidasa (IMAO). [25] Se necesitan más investigaciones para determinar si se necesitan dosis de dextrometorfano más allá de las que se usan normalmente con fines terapéuticos para producir este efecto. [10] En cualquier caso, no se debe tomar dextrometorfano con IMAO debido a la posibilidad de esta complicación. [20] El síndrome serotoninérgico es una afección potencialmente mortal que puede ocurrir rápidamente, debido a una acumulación excesiva de serotonina en el cuerpo.
La combinación de alcohol con dextrometorfano aumenta significativamente el riesgo de sobredosis y otras complicaciones de salud graves, según el NIAAA . [26]
Los compuestos del pomelo afectan a varios fármacos , incluido el dextrometorfano, a través de la inhibición del sistema del citocromo P450 en el hígado, y pueden provocar una acumulación excesiva del fármaco, lo que aumenta y prolonga los efectos. En general, se recomienda evitar el pomelo y los jugos de pomelo (especialmente el jugo de pomelo blanco, pero también otros cítricos como la bergamota y la lima , así como varias frutas no cítricas [27] ) mientras se usa dextrometorfano y muchos otros medicamentos.
Se ha descubierto que el dextrometorfano posee las siguientes acciones (<1 μM) utilizando tejidos de rata: [17] [34]
El dextrometorfano es un profármaco del dextrorfano , que es el mediador real de la mayoría de sus efectos disociativos al actuar como un antagonista del receptor NMDA más potente que el propio dextrometorfano. [35] No está del todo claro qué papel, si es que tiene alguno, desempeña el (+)- 3-metoximorfinano , el otro metabolito principal del dextrometorfano, en sus efectos. [36]
Tras la administración oral, el dextrometorfano se absorbe rápidamente en el tracto gastrointestinal , donde ingresa al torrente sanguíneo y cruza la barrera hematoencefálica . [ cita requerida ]
En dosis terapéuticas, el dextrometorfano actúa de forma central (es decir, actúa sobre el cerebro ) en lugar de hacerlo de forma local (sobre el tracto respiratorio ). Eleva el umbral de la tos, sin inhibir la actividad ciliar . El dextrometorfano se absorbe rápidamente en el tracto gastrointestinal y se convierte en el metabolito activo dextrorfano en el hígado por acción de la enzima CYP2D6 del citocromo P450 . La dosis media necesaria para una terapia antitusiva eficaz es de entre 10 y 45 mg, dependiendo del individuo. La Sociedad Internacional para el Estudio de la Tos recomienda que "una primera dosis adecuada del medicamento es de 60 mg en el adulto y que la repetición de la dosis sea poco frecuente en lugar de una vez al día, como se recomienda". [37]
El dextrometorfano tiene una vida media de eliminación de aproximadamente 4 horas en individuos con un fenotipo metabolizador extenso; esto aumenta a aproximadamente 13 horas cuando se administra dextrometorfano en combinación con quinidina . [30] La duración de la acción después de la administración oral es de aproximadamente tres a ocho horas para el bromhidrato de dextrometorfano y de 10 a 12 horas para el dextrometorfano polistirex. [ cita requerida ] Alrededor de uno de cada 10 de la población caucásica tiene poca o ninguna actividad de la enzima CYP2D6, lo que lleva a altos niveles de fármaco de larga duración. [37]

El primer paso a través de la vena porta hepática da lugar a que una parte del fármaco se metabolice por O-desmetilación en un metabolito activo del dextrometorfano llamado dextrorfano, el derivado 3-hidroxi del dextrometorfano. Se cree que la actividad terapéutica del dextrometorfano es causada tanto por el fármaco como por este metabolito. El dextrometorfano también sufre N-desmetilación (a 3-metoximorfinano o MEM), [39] y conjugación parcial con ácido glucurónico e iones sulfato. Horas después de la terapia con dextrometorfano, (en humanos) los metabolitos (+)-3-hidroxi-N-metilmorfinano, (+)-3-morfinano y trazas del fármaco inalterado son detectables en la orina. [20]
Un importante catalizador metabólico involucrado es la enzima citocromo P450 conocida como 2D6 o CYP2D6. Una parte significativa de la población tiene una deficiencia funcional de esta enzima y se les conoce como metabolizadores deficientes de CYP2D6. La O-desmetilación del dextrometorfano a dextrorfano contribuye a al menos el 80% del dextrorfano formado durante el metabolismo de este último. [39] Como CYP2D6 es una vía metabólica importante en la inactivación del dextrometorfano, la duración de la acción y los efectos del dextrometorfano pueden aumentar hasta tres veces en estos metabolizadores deficientes. [40] En un estudio sobre 252 estadounidenses, se encontró que el 84,3% eran metabolizadores "rápidos" (extensos), el 6,8% eran metabolizadores "intermedios" y el 8,8% eran metabolizadores "lentos" del dextrometorfano. [41] Se conocen varios alelos para CYP2D6, incluidas varias variantes completamente inactivas. La distribución de alelos es desigual entre los grupos étnicos .
Una gran cantidad de medicamentos son potentes inhibidores de CYP2D6 . Algunos tipos de medicamentos que se sabe que inhiben CYP2D6 incluyen ciertos ISRS y antidepresivos tricíclicos , algunos antipsicóticos y el antihistamínico comúnmente disponible difenhidramina . Por lo tanto, existe la posibilidad de interacciones entre el dextrometorfano y los medicamentos que inhiben esta enzima, particularmente en metabolizadores lentos.
El dextrometorfano también es metabolizado por el CYP3A4 . La N-desmetilación se lleva a cabo principalmente por el CYP3A4, contribuyendo a al menos el 90% del MEM formado como metabolito primario del dextrometorfano. [39]
Varias otras enzimas CYP están implicadas como vías menores del metabolismo del dextrometorfano. CYP2D6 es más eficaz que CYP3A4 en la N-desmetilación del dextrometorfano, pero dado que el individuo promedio tiene un contenido de CYP2D6 mucho menor en el hígado en comparación con CYP3A4, la mayor parte de la N-desmetilación del dextrometorfano es catalizada por CYP3A4. [39]
El dextrometorfano es el enantiómero dextrógiro del levometorfano , que es el metiléter del levorfanol , ambos analgésicos opioides . Se denomina de acuerdo con las reglas de la IUPAC como (+)-3-metoxi-17-metil-9α,13α,14α- morfinano . En su forma pura, el dextrometorfano se presenta como un polvo blanco opalescente inodoro. Es libremente soluble en cloroformo e insoluble en agua ; la sal de bromhidrato es soluble en agua hasta 1,5 g/100 ml a 25 °C. [42] El dextrometorfano está comúnmente disponible como la sal de bromhidrato monohidratada, y también está disponible en formulaciones de liberación prolongada (vendidas como dextrometorfano polistirex) que contienen dextrometorfano unido a una resina de intercambio iónico a base de ácido poliestireno sulfónico . La rotación específica del dextrometorfano en agua es de +27,6° (20 °C, línea D de sodio) . [ cita requerida ]
Existen varias vías para la síntesis del dextrometorfano. Aunque muchas de las síntesis se conocen desde mediados del siglo XX, los investigadores siguen trabajando hoy en día para seguir desarrollando la síntesis del dextrometorfano y, por ejemplo, para que sea más respetuosa con el medio ambiente .
Esto incluye la síntesis mediante líquidos iónicos. [ cita requerida ]
Puesto que sólo uno de los estereoisómeros tiene el efecto deseado, la separación de una mezcla racémica de hidroxi N-metil morfinano mediante ácido tartárico y la posterior metilación del grupo hidroxilo es un método adecuado. Al utilizar (D)-tartrato, el isómero (+) permanece como producto.
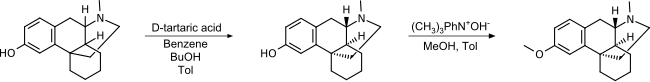
Esta vía sintética fue patentada por Roche en 1950.
La ruta sintética tradicional utiliza níquel Raney y se ha mejorado aún más con el tiempo, por ejemplo, mediante el uso de ibuprofeno y AlCl 3 .

En general, es un método rentable con condiciones de reacción moderadas, fácil de manejar y adecuado para la producción industrial. [ cita requerida ]

La ciclización de Grewe es más fácil de manejar en términos de los productos químicos utilizados, produce mayores rendimientos y una mayor pureza del producto. [43]
La formilación de la octabase antes de la ciclización evita la escisión del éter como reacción secundaria y produce mayores rendimientos que sin la N-sustitución o la N-metilación. En este ejemplo, la purificación se realizó mediante la formación de una sal de brucina. [ cita requerida ]

Este proceso también ha sido patentado por Roche.
El compuesto racémico parental racemorfano fue descrito por primera vez en una solicitud de patente suiza y estadounidense de Hoffmann-La Roche en 1946 y 1947, respectivamente; se concedió una patente en 1950. Una resolución de los dos isómeros del racemorfano con ácido tartárico se publicó en 1952, [44] y el dextrometorfano se probó con éxito en 1954 como parte de una investigación financiada por la Marina de los EE. UU. y la CIA sobre sustitutos no adictivos para la codeína . [45] [ fuente no primaria necesaria ] El dextrometorfano fue aprobado por la FDA en 1958 como un antitusivo de venta libre . [44] Como se había esperado inicialmente, el dextrometorfano fue una solución para algunos de los problemas asociados con el uso de fosfato de codeína como supresor de la tos, como la sedación y la dependencia de opiáceos , pero al igual que los anestésicos disociativos fenciclidina y ketamina , el dextrometorfano más tarde se asoció con el uso no médico. [44] [46]
Durante los años 1960 y 1970, el dextrometorfano se comercializó en forma de comprimidos sin receta bajo la marca Romilar. En 1973, Romilar se retiró de los estantes después de un aumento repentino de las ventas debido al mal uso frecuente. Unos años más tarde, se introdujeron productos con un sabor desagradable (como Robitussin, Vicks-44 y Dextrotussion), pero más tarde los mismos fabricantes comenzaron a producir productos con un mejor sabor. [46] La llegada del acceso generalizado a Internet en la década de 1990 permitió a los usuarios difundir rápidamente información sobre el dextrometorfano, y se formaron grupos de discusión en línea en torno al uso y la adquisición del fármaco. Ya en 1996, el polvo de bromhidrato de dextrometorfano se podía comprar a granel a los minoristas en línea, lo que permitía a los usuarios evitar el consumo de dextrometorfano en preparaciones de jarabe. [44]
Los paneles de la FDA consideraron mover el dextrometorfano al estado de prescripción debido a su potencial de abuso, pero votaron en contra de la recomendación en septiembre de 2010, citando la falta de evidencia de que hacer que solo se venda con receta frenaría el abuso. [47] Algunos estados han restringido la venta de dextrometorfano a adultos o han puesto otras restricciones en su compra, similares a las de la pseudoefedrina . A partir del 1 de enero de 2012, se prohíbe la venta de dextrometorfano a menores en el estado de California y en el estado de Oregón a partir del 1 de enero de 2018, excepto con receta médica. [48] Varios otros estados también han comenzado a regular las ventas de dextrometorfano a menores.
En Indonesia , la Agencia Nacional de Control de Alimentos y Medicamentos (BPOM-RI) prohibió la venta de dextrometorfano, un medicamento monocomponente, con o sin receta médica. Indonesia es el único país que prohíbe la venta sin receta y con receta médica del dextrometorfano monocomponente [49] y los infractores pueden ser procesados por ley. La Agencia Nacional Antinarcóticos (BNN RI) ha amenazado con revocar las licencias de farmacias y droguerías si aún tienen dextrometorfano en existencias, y notificará a la policía para su procesamiento penal. [50] Como resultado de esta regulación, 130 medicamentos han sido retirados del mercado, pero aquellos que contienen dextrometorfano multicomponente todavía pueden venderse sin receta médica. [51] [52]
Puede utilizarse en etiquetas genéricas y marcas de tiendas , Benylin DM, Mucinex DM, tabletas Camydex-20, Robitussin, Komix DT, NyQuil , Dimetapp , Vicks , Coricidin , Delsym, TheraFlu , Charcoal D, Cinfatós y otros. Se ha utilizado en medicamentos falsificados. [ cita requerida ]

Las preparaciones de venta libre que contienen dextrometorfano se han utilizado de maneras que no coinciden con las que se indican en las etiquetas, a menudo como una droga recreativa. [46] En dosis mucho más altas que las recomendadas médicamente, el dextrometorfano y su principal metabolito, el dextrorfano , actúa como un antagonista del receptor NMDA , que produce estados alucinógenos disociativos algo similares a la ketamina y la fenciclidina . [53]
Puede producir distorsiones del campo visual (sensaciones de disociación , percepción corporal distorsionada, excitación y pérdida del sentido del tiempo). Algunos usuarios informan de una euforia similar a la de los estimulantes , en particular en respuesta a la música. El dextrometorfano suele proporcionar sus efectos recreativos de forma no lineal, de modo que se experimentan en etapas significativamente variadas. Estas etapas se denominan comúnmente "mesetas". Estas mesetas se numeran del uno al cuatro, siendo la primera la que tiene los efectos más leves y la cuarta la más intensa. Se dice que cada meseta viene con diferentes efectos y experiencias relacionadas. [54]
Se dice que la primera meseta induce euforia musical y estimulación leve, similar a la del MDMA . La segunda meseta se asemeja a un estado de consumo de cantidades moderadas de alcohol y cannabis al mismo tiempo, con euforia, sedación y alucinaciones menores. La tercera meseta induce un estado disociativo significativo que a menudo puede causar ansiedad en los usuarios. Se dice que alcanzar la cuarta meseta causa sedación extrema y un estado alucinatorio significativo, así como una disociación completa de la realidad. Los adolescentes tienden a tener una mayor probabilidad de consumir drogas relacionadas con el dextrometorfano, ya que son más fáciles de acceder; los jóvenes y adultos jóvenes con trastornos psiquiátricos corren el riesgo de abusar de la droga. [55]
El fármaco combinado dextrometorfano/quinidina (AVP-923), [56] [57] utilizado tradicionalmente para tratar el afecto pseudobulbar , está bajo investigación para el tratamiento de una variedad de otras afecciones neurológicas y neuropsiquiátricas, incluida la agitación asociada con la enfermedad de Alzheimer , entre otras. [17] [58] En 2013, un ensayo clínico aleatorizado encontró que el dextrometorfano puede reducir el malestar general y la duración de los síntomas de abstinencia asociados con el trastorno por consumo de opioides . Cuando se combina con clonidina , el dextrometorfano reduce el tiempo general necesario para que los síntomas de abstinencia alcancen su punto máximo en 24 horas, al tiempo que reduce la gravedad de los síntomas en comparación con la clonidina sola. [59]
Por ventas, el dextrometorfano es el fármaco antitusivo de venta libre más utilizado en los Estados Unidos, y aproximadamente entre el 85% y el 90% de los medicamentos de venta libre para la tos contienen dextrometorfano.
![]() Medios relacionados con Dextrometorfano en Wikimedia Commons
Medios relacionados con Dextrometorfano en Wikimedia Commons