El óxido nitroso (óxido de dinitrógeno o monóxido de dinitrógeno), comúnmente conocido como gas de la risa , nitroso , nitro o nos , [4] es un compuesto químico , un óxido de nitrógeno con la fórmula N
2O. A temperatura ambiente, es un gas incoloro , no inflamable , y tiene un olor y sabor ligeramente dulce. [5] A temperaturas elevadas, el óxido nitroso es un potente oxidante similar al oxígeno molecular.
El óxido nitroso tiene importantes usos médicos , especialmente en cirugía y odontología , por sus efectos anestésicos y analgésicos . [6] Su nombre coloquial, "gas de la risa", acuñado por Humphry Davy , se debe a los efectos eufóricos al inhalarlo, propiedad que ha propiciado su uso recreativo como anestésico disociativo . [6] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [7] También se utiliza como oxidante en propulsores de cohetes y en carreras de motor para aumentar la potencia de los motores .
La concentración atmosférica de óxido nitroso alcanzó las 333 partes por mil millones (ppb) en 2020, aumentando a un ritmo de aproximadamente 1 ppb anualmente. [8] [9] Es un importante eliminador del ozono estratosférico , con un impacto comparable al de los CFC . [10] Alrededor del 40% de las emisiones causadas por el hombre provienen de la agricultura . [11] [12] El nitrógeno se añade al suelo a través de la orina y el estiércol de los animales y de los fertilizantes sintéticos: los microorganismos lo liberan luego en forma de óxido nitroso. [13] Al ser el tercer gas de efecto invernadero más importante , el óxido nitroso contribuye sustancialmente al calentamiento global . [14] [15] La reducción de emisiones es un tema popular en la política del cambio climático . [dieciséis]
El óxido nitroso se utiliza como propulsor y tiene una variedad de aplicaciones, desde cohetes hasta la elaboración de crema batida. Se utiliza como droga recreativa por su potencial para inducir un breve "subidón". Cuando se usa de forma crónica, el óxido nitroso tiene el potencial de causar daño neurológico mediante la inactivación de la vitamina B 12 .
El óxido nitroso se puede utilizar como oxidante en un motor de cohete . Tiene ventajas sobre otros oxidantes porque es mucho menos tóxico y, debido a su estabilidad a temperatura ambiente, también es más fácil de almacenar y relativamente seguro de transportar en un vuelo. Como beneficio secundario, puede descomponerse fácilmente para formar aire respirable. Su alta densidad y baja presión de almacenamiento (cuando se mantiene a bajas temperaturas) le permiten ser altamente competitivo con los sistemas de gas almacenado a alta presión. [17]
En una patente de 1914, el pionero estadounidense de los cohetes, Robert Goddard, sugirió óxido nitroso y gasolina como posibles propulsores para un cohete de combustible líquido. [18] El óxido nitroso ha sido el oxidante elegido en varios diseños de cohetes híbridos (que utilizan combustible sólido con un oxidante líquido o gaseoso). SpaceShipOne y otros han utilizado la combinación de óxido nitroso con combustible de polibutadieno terminado en hidroxilo . También se utiliza especialmente en cohetes de aficionados y de alta potencia con diversos plásticos como combustible.
El óxido nitroso también puede usarse en un cohete monopropulsor . En presencia de un catalizador calentado , N
2El O se descompondrá exotérmicamente en nitrógeno y oxígeno, a una temperatura de aproximadamente 1070 °F (577 °C). [19] Debido a la gran liberación de calor, la acción catalítica rápidamente se vuelve secundaria, a medida que la autodescomposición térmica se vuelve dominante. En un propulsor de vacío, esto puede proporcionar un impulso específico monopropulsor ( I sp ) de hasta 180 s. Si bien es notablemente menor que el I sp disponible en los propulsores de hidracina (monopropulsor o bipropulsor con tetróxido de dinitrógeno ), la menor toxicidad hace que el óxido nitroso sea una opción que vale la pena investigar.
Se dice que el óxido nitroso deflagra a aproximadamente 600 °C (1112 °F) a una presión de 309 psi (21 atmósferas). [20] A 600 psi , por ejemplo, la energía de ignición requerida es sólo 6 julios, mientras que N
2O a 130 psi, una entrada de energía de ignición de 2500 julios es insuficiente. [21] [22]
En las carreras de vehículos , el óxido nitroso (a menudo llamado " nitroso ") permite que el motor queme más combustible al proporcionar más oxígeno durante la combustión. El aumento de oxígeno permite un aumento en la inyección de combustible, permitiendo que el motor produzca más potencia . El gas no es inflamable a baja presión/temperatura, pero libera más oxígeno que el aire atmosférico al descomponerse a temperaturas elevadas, alrededor de 570 grados F (~300 C). Por lo tanto, muchas veces se mezcla con otro combustible que es más fácil de deflagrar. El óxido nitroso es un agente oxidante fuerte, aproximadamente equivalente al peróxido de hidrógeno y mucho más fuerte que el oxígeno gaseoso.
El óxido nitroso se almacena como un líquido comprimido; La evaporación y expansión del óxido nitroso líquido en el colector de admisión provoca una gran caída en la temperatura de la carga de admisión, lo que resulta en una carga más densa, lo que permite además que ingrese más mezcla de aire y combustible al cilindro. A veces, el óxido nitroso se inyecta en (o antes) el colector de admisión, mientras que otros sistemas lo inyectan directamente, justo antes del cilindro (inyección directa en el puerto) para aumentar la potencia.
La técnica fue utilizada durante la Segunda Guerra Mundial por aviones de la Luftwaffe con el sistema GM-1 para aumentar la potencia de los motores de los aviones . Originalmente destinado a proporcionar al avión estándar de la Luftwaffe un rendimiento superior a gran altitud, las consideraciones tecnológicas limitaron su uso a altitudes extremadamente altas. En consecuencia, solo fue utilizado por aviones especializados como aviones de reconocimiento de gran altitud , bombarderos de alta velocidad y aviones interceptores de gran altitud . A veces se podía encontrar en aviones de la Luftwaffe que también estaban equipados con otro sistema de propulsión de motor, el MW 50 , una forma de inyección de agua para motores de aviación que utilizaba metanol para su capacidad de propulsión.
Uno de los principales problemas del uso de óxido nitroso en un motor alternativo es que puede producir suficiente energía para dañar o destruir el motor. Son posibles aumentos de potencia muy grandes y, si la estructura mecánica del motor no se refuerza adecuadamente, el motor puede sufrir graves daños o destruirse durante este tipo de operación. Es importante con el aumento de óxido nitroso de los motores de gasolina mantener temperaturas de funcionamiento y niveles de combustible adecuados para evitar la " preignición ", [23] o la "detonación" (a veces denominada "detonación"). La mayoría de los problemas asociados con el óxido nitroso no provienen de fallas mecánicas debido al aumento de potencia. Dado que el óxido nitroso permite una carga mucho más densa en el cilindro, aumenta drásticamente la presión del cilindro. El aumento de presión y temperatura puede causar problemas como derretir los pistones o las válvulas. También puede agrietar o deformar el pistón o la culata del cilindro y provocar un preencendido debido a un calentamiento desigual.
El óxido nitroso líquido de grado automotriz difiere ligeramente del óxido nitroso de grado médico. Una pequeña cantidad de dióxido de azufre ( SO
2) se agrega para prevenir el abuso de sustancias. [24]

El gas está aprobado para su uso como aditivo alimentario ( número E : E942), específicamente como propulsor de aerosol . Sus usos más comunes en este contexto son los botes de crema batida en aerosol y los aerosoles para cocinar .
El gas es extremadamente soluble en compuestos grasos. En la nata montada en aerosol, se disuelve en la nata grasa hasta que sale del bote, cuando se vuelve gaseosa y crea espuma. Utilizado de esta manera, produce crema batida que tiene un volumen cuatro veces mayor que el líquido, mientras que batir aire en la crema sólo produce el doble de volumen. Si se utilizara aire como propulsor, el oxígeno aceleraría la rancidificación de la grasa láctea, pero el óxido nitroso inhibe dicha degradación. El dióxido de carbono no se puede utilizar para la crema batida porque es ácido en el agua, lo que cuajaría la crema y le daría una sensación "espumosa" similar a la del agua mineral.
La nata montada producida con óxido nitroso es inestable y volverá a un estado más líquido entre media hora y una hora. [25] Por lo tanto, el método no es adecuado para decorar alimentos que no se servirán inmediatamente.
En diciembre de 2016, algunos fabricantes informaron de una escasez de cremas batidas en aerosol en Estados Unidos debido a una explosión en la instalación de óxido nitroso de Air Liquide en Florida a finales de agosto. Con una importante instalación fuera de servicio, la interrupción provocó una escasez que obligó a la empresa a desviar el suministro de óxido nitroso a clientes médicos en lugar de a la fabricación de alimentos. La escasez se produjo durante la temporada navideña y festiva, cuando el uso de crema batida enlatada normalmente es mayor. [26]
De manera similar, el aerosol para cocinar, que se elabora a partir de varios tipos de aceites combinados con lecitina (un emulsionante ), puede usar óxido nitroso como propulsor . Otros propulsores utilizados en el aerosol para cocinar incluyen alcohol y propano de calidad alimentaria .

El óxido nitroso se ha utilizado en odontología y cirugía, como anestésico y analgésico, desde 1844. [27] En los primeros días, el gas se administraba a través de inhaladores simples que consistían en una bolsa respiratoria hecha de tela de goma. [28] Hoy en día, el gas se administra en los hospitales mediante una máquina automatizada de analgesia relativa , con un vaporizador de anestésico y un ventilador médico , que suministra un flujo de óxido nitroso mezclado con oxígeno, dosificado con precisión y accionado por la respiración, en una relación 2:1. relación.
El óxido nitroso es un anestésico general débil , por lo que generalmente no se usa solo en anestesia general, sino como gas portador (mezclado con oxígeno) para fármacos anestésicos generales más potentes como el sevoflurano o el desflurano . Tiene una concentración alveolar mínima del 105% y un coeficiente de partición sangre/gas de 0,46. El uso de óxido nitroso en anestesia puede aumentar el riesgo de náuseas y vómitos posoperatorios. [29] [30] [31]
Los dentistas utilizan una máquina más sencilla que sólo suministra una N
2O / O
2mezcla para que el paciente la inhale mientras está consciente, pero aún así debe ser un medidor de flujo analgésico relativo dedicado diseñado específicamente para tal fin con un mínimo de 30 % de oxígeno en todo momento y un límite superior máximo de 70 % de óxido nitroso. El paciente se mantiene consciente durante todo el procedimiento y conserva las facultades mentales adecuadas para responder a las preguntas e instrucciones del dentista. [32]
La inhalación de óxido nitroso se utiliza frecuentemente para aliviar el dolor asociado con el parto , traumatismos , cirugía bucal y síndrome coronario agudo (incluidos ataques cardíacos). Se ha demostrado que su uso durante el parto es una ayuda segura y eficaz para las mujeres que dan a luz. [33] Se desconoce el beneficio de su uso para el síndrome coronario agudo. [34]
En Canadá y el Reino Unido, el personal de ambulancias (incluidos los médicos no registrados) utilizan comúnmente Entonox y Nitronox como gases analgésicos rápidos y muy eficaces.
Se puede considerar el uso de óxido nitroso al 50% por parte de socorristas no profesionales capacitados en entornos prehospitalarios, dada la relativa facilidad y seguridad de administrar óxido nitroso al 50% como analgésico. La rápida reversibilidad de su efecto también evitaría que impida el diagnóstico. [35]



La inhalación recreativa de óxido nitroso , con el propósito de provocar euforia y/o alucinaciones leves , comenzó como un fenómeno para la clase alta británica en 1799, conocido como "fiestas del gas de la risa". [36]
A partir del siglo XIX, la amplia disponibilidad del gas para fines médicos y culinarios permitió que su uso recreativo se expandiera enormemente a nivel mundial. En el Reino Unido, en 2014, se estimaba que casi medio millón de jóvenes utilizaban óxido nitroso en locales nocturnos, festivales y fiestas. [37]
El uso recreativo generalizado de la droga en todo el Reino Unido apareció en el documental de Vice de 2017 Inside The Laughing Gas Black Market , en el que el periodista Matt Shea se reunió con traficantes de la droga que la robaban de los hospitales. [38]
Un tema importante citado en la prensa de Londres es el efecto de la basura de los botes de óxido nitroso, que es muy visible y provoca importantes quejas de las comunidades. [39]
Antes del 8 de noviembre de 2023, el óxido nitroso estaba sujeto a la Ley de Sustancias Psicoactivas de 2016 en el Reino Unido. Ya era ilegal producir, suministrar, importar o exportar óxido nitroso para uso recreativo. Sin embargo, el gobierno del Reino Unido actualizó la ley el 8 de noviembre de 2023 para incluir la posesión de óxido nitroso clasificándolo como droga de Clase C según la Ley de Uso Indebido de Drogas de 1971. [40]
Si bien la mayoría de los usuarios recreativos entienden que el uso ocasional de óxido nitroso es una ruta hacia una "euforia segura", muchos desconocen que el consumo excesivo tiene el potencial de causar daño neurológico que, si no se trata, puede resultar en daño neurológico permanente. [41] En Australia, el uso recreativo se convirtió en un problema de salud pública luego de un aumento en los casos reportados de neurotoxicidad y un aumento en las admisiones a las salas de emergencia , y en (el estado de) Australia del Sur se aprobó una legislación en 2020 para restringir las ventas de botes. [42]
El óxido nitroso es un riesgo laboral importante para cirujanos, dentistas y enfermeras. Debido a que el óxido nitroso se metaboliza mínimamente en humanos (con una tasa de 0,004%), conserva su potencia cuando el paciente lo exhala en la habitación y puede representar un riesgo de exposición prolongada y de intoxicación para el personal de la clínica si la habitación está mal ventilada. Cuando se administra óxido nitroso, un sistema de ventilación de aire fresco de flujo continuo o N
2 El sistema de eliminación de O se utiliza para evitar la acumulación de gases residuales. [ cita necesaria ]
El Instituto Nacional de Seguridad y Salud Ocupacional recomienda que se controle la exposición de los trabajadores al óxido nitroso durante la administración de gas anestésico en operadores médicos, odontológicos y veterinarios. [43] Estableció un límite de exposición recomendado (REL) de 25 ppm (46 mg/m 3 ) al anestésico que se escapaba. [44]
La exposición al óxido nitroso provoca disminuciones a corto plazo en el rendimiento mental, la capacidad audiovisual y la destreza manual. [45] Estos efectos, junto con la desorientación espacial y temporal inducida, podrían provocar daños físicos al usuario debido a peligros ambientales. [46]
El óxido nitroso es neurotóxico y existe evidencia de que el consumo habitual a mediano o largo plazo de cantidades significativas puede causar daño neurológico con potencial de daño permanente si no se trata. [42] [41]
Al igual que otros antagonistas del receptor NMDA , se ha sugerido que N
2O produce neurotoxicidad en forma de lesiones de Olney en roedores tras una exposición prolongada (varias horas). [47] [48] [49] [50]
Se ha argumentado que, debido a que N
2El O se expulsa rápidamente del cuerpo en circunstancias normales y es menos probable que sea neurotóxico que otros antagonistas de NMDAR. [51] De hecho, en los roedores, la exposición a corto plazo produce solo lesiones leves que son rápidamente reversibles, y la muerte neuronal ocurre solo después de una exposición constante y sostenida. [47] El óxido nitroso también puede causar neurotoxicidad después de una exposición prolongada debido a la hipoxia . Esto es especialmente cierto en el caso de formulaciones no médicas como los cargadores de crema batida (también conocidos como "whippets" o "nangs"), [52] que nunca contienen oxígeno, ya que el oxígeno vuelve rancia la crema. [53]
En consumidores intensos (≥400 g o ≥200 L de gas N 2 O en una sesión) o frecuentes (regulares, es decir, diarios o semanales) informados a los centros de control de intoxicaciones, se han observado signos de neuropatía periférica : la presencia de ataxia ( anomalías de la marcha) o parestesia (percepción de sensaciones anormales, por ejemplo, hormigueo, entumecimiento, hormigueo, principalmente en las extremidades). Estos se consideran un signo temprano de daño neurológico e indican toxicidad crónica . [54]
El óxido nitroso al 75% en volumen reduce la muerte neuronal inducida por isquemia inducida por la oclusión de la arteria cerebral media en roedores y disminuye la entrada de Ca 2+ inducida por NMDA en cultivos de células neuronales, un evento crítico involucrado en la excitotoxicidad . [51]
La exposición ocupacional al óxido nitroso ambiental se ha asociado con daños en el ADN, debido a interrupciones en la síntesis del ADN. [55] Esta correlación depende de la dosis [56] [57] y no parece extenderse al uso recreativo ocasional; sin embargo, se necesitan más investigaciones para confirmar la duración y la cantidad de exposición necesarias para causar daños.
Si se inhala óxido nitroso puro sin oxígeno, puede producirse falta de oxígeno, lo que provoca presión arterial baja, desmayos e incluso ataques cardíacos. Esto puede ocurrir si el usuario inhala grandes cantidades continuamente, como ocurre con una máscara con correa conectada a un bote de gas. También puede ocurrir si el usuario contiene excesivamente la respiración o utiliza cualquier otro sistema de inhalación que corte el suministro de aire fresco. [ cita necesaria ]
La exposición prolongada al óxido nitroso puede causar deficiencia de vitamina B 12 . Esto puede causar neurotoxicidad grave si el usuario tiene una deficiencia preexistente de vitamina B 12 . [58] Inactiva la forma cobalamina de la vitamina B 12 por oxidación. Los síntomas de la deficiencia de vitamina B 12 , incluyendo neuropatía sensorial , mielopatía y encefalopatía , pueden ocurrir a los pocos días o semanas de exposición a la anestesia con óxido nitroso en personas con deficiencia subclínica de vitamina B 12 .
Los síntomas se tratan con altas dosis de vitamina B 12 , pero la recuperación puede ser lenta e incompleta. [59]
Las personas con niveles normales de vitamina B 12 tienen reservas que hacen que los efectos del óxido nitroso sean insignificantes, a menos que la exposición sea repetida y prolongada (abuso de óxido nitroso). Se deben controlar los niveles de vitamina B 12 en personas con factores de riesgo de deficiencia de vitamina B 12 antes de usar anestesia con óxido nitroso. [60]
Varios estudios experimentales en ratas indican que la exposición crónica de hembras preñadas al óxido nitroso puede tener efectos adversos en el feto en desarrollo. [61] [62] [63]
A temperatura ambiente (20 °C [68 °F]), la presión de vapor saturado es de 50,525 bar, aumentando hasta 72,45 bar a 36,4 °C (97,5 °F), la temperatura crítica . Por tanto, la curva de presión es inusualmente sensible a la temperatura. [64]
Como ocurre con muchos oxidantes fuertes, la contaminación de piezas con combustibles ha estado implicada en accidentes de cohetes, donde pequeñas cantidades de mezclas de nitroso y combustible explotan debido a efectos similares al " golpe de ariete " (a veces llamado "dieseling", calentamiento debido a la compresión adiabática de gases) . puede alcanzar temperaturas de descomposición). [65] Algunos materiales de construcción comunes, como el acero inoxidable y el aluminio, pueden actuar como combustibles con oxidantes fuertes como el óxido nitroso, al igual que los contaminantes que pueden encenderse debido a la compresión adiabática. [66]
También ha habido incidentes en los que la descomposición del óxido nitroso en las tuberías ha provocado la explosión de grandes tanques. [20]
El mecanismo de acción farmacológico de N.
2O en medicina no se conoce completamente. Sin embargo, se ha demostrado que modula directamente una amplia gama de canales iónicos activados por ligandos , y esto probablemente desempeña un papel importante en muchos de sus efectos. Bloquea moderadamente los canales NMDAR y nACh que contienen la subunidad β 2 , inhibe débilmente los receptores AMPA , kainato , GABA C y 5-HT 3 y potencia ligeramente los receptores GABA A y glicina . [67] [68] También se ha demostrado que activa el K de dominio de dos poros.+
canales . [69] Mientras que N
2El O afecta a bastantes canales iónicos, sus efectos anestésicos, alucinógenos y eufóricos probablemente se deben predominante o totalmente a través de la inhibición de las corrientes mediadas por el receptor NMDA. [67] [70] Además de sus efectos sobre los canales iónicos, N
2El O puede actuar imitando el óxido nítrico (NO) en el sistema nervioso central, y esto puede estar relacionado con sus propiedades analgésicas y ansiolíticas . [70] El óxido nitroso es de 30 a 40 veces más soluble que el nitrógeno.
Se sabe que los efectos de la inhalación de dosis subanestésicas de óxido nitroso varían según varios factores, incluidos los entornos y las diferencias individuales; [71] [72] sin embargo, a partir de su discusión, Jay (2008) [46] sugiere que se sabe de manera confiable que induce los siguientes estados y sensaciones:
Una minoría de usuarios también presentará vocalizaciones incontroladas y espasmos musculares. Estos efectos generalmente desaparecen minutos después de eliminar la fuente de óxido nitroso. [46]
En pruebas conductuales de ansiedad , una dosis baja de N
2El O es un ansiolítico eficaz y este efecto ansiolítico se asocia con una mayor actividad de los receptores GABA A , ya que los antagonistas de los receptores de benzodiazepinas lo revierten parcialmente . Reflejando esto, los animales que han desarrollado tolerancia a los efectos ansiolíticos de las benzodiazepinas son parcialmente tolerantes al N
2O. [73] De hecho, en humanos que reciben 30% N
2O , los antagonistas de los receptores de benzodiazepinas redujeron los informes subjetivos de sentirse "drogado", pero no alteraron el rendimiento psicomotor , en estudios clínicos en humanos. [74] [75]
Los efectos analgésicos del N.
2O están vinculados a la interacción entre el sistema opioide endógeno y el sistema noradrenérgico descendente . Cuando los animales reciben morfina de forma crónica, desarrollan tolerancia a sus efectos analgésicos, y esto también los vuelve tolerantes a los efectos analgésicos del N.
2O. [76] La administración de anticuerpos que se unen y bloquean la actividad de algunos opioides endógenos (no la β-endorfina ) también bloquea los efectos antinociceptivos del N
2O. [77] Los fármacos que inhiben la descomposición de los opioides endógenos también potencian los efectos antinociceptivos del N
2O. [77] Varios experimentos han demostrado que los antagonistas de los receptores opioides aplicados directamente al cerebro bloquean los efectos antinociceptivos del N.
2O , pero estos medicamentos no tienen ningún efecto cuando se inyectan en la médula espinal .
Aparte de una acción indirecta, el óxido nitroso, como la morfina [78], también interactúa directamente con el sistema opioide endógeno uniéndose a los sitios de unión de los receptores opioides. [79] [80]
Por el contrario, los antagonistas de los receptores adrenérgicos α 2 bloquean los efectos analgésicos del N
2O cuando se administra directamente a la médula espinal, pero no cuando se aplica directamente al cerebro. [81] De hecho, los ratones knockout para receptores adrenérgicos α 2B o los animales con niveles reducidos de norepinefrina son casi completamente resistentes a los efectos antinociceptivos del N
2O. [82] Al parecer N
2La liberación de opioides endógenos inducida por O provoca la desinhibición de las neuronas noradrenérgicas del tronco encefálico , que liberan noradrenalina en la médula espinal e inhiben la señalización del dolor. [83] Exactamente cómo N
2O causa la liberación de péptidos opioides endógenos sigue siendo incierta.
El óxido nitroso es un gas incoloro con un olor suave y dulce.
El óxido nitroso favorece la combustión liberando el radical de oxígeno unido dipolarmente y, por tanto, puede volver a encender una férula incandescente .
norte
2El O es inerte a temperatura ambiente y tiene pocas reacciones. A temperaturas elevadas, su reactividad aumenta. Por ejemplo, el óxido nitroso reacciona con NaNH
2a 187 °C (369 °F) para dar NaN3:
La reacción anterior es la ruta adoptada por la industria química comercial para producir sales de azida , que se utilizan como detonantes. [84]
El gas fue sintetizado por primera vez en 1772 por el filósofo natural y químico inglés Joseph Priestley, quien lo llamó aire nitroso desflogistizado (ver teoría del flogisto ) [85] o aire nitroso inflamable . [86] Priestley publicó su descubrimiento en el libro Experiments and Observations on Different Kinds of Air (1775) , donde describió cómo producir la preparación de "aire nitroso disminuido", calentando limaduras de hierro humedecidas con ácido nítrico . [87]

El primer uso importante del óxido nitroso fue posible gracias a Thomas Beddoes y James Watt , quienes trabajaron juntos para publicar el libro Consideraciones sobre el uso médico y la producción de aires facticios (1794) . Este libro fue importante por dos razones. En primer lugar, James Watt había inventado una nueva máquina para producir " aires ficticios " (incluido el óxido nitroso) y un novedoso "aparato respiratorio" para inhalar el gas. En segundo lugar, el libro también presenta las nuevas teorías médicas de Thomas Beddoes, según las cuales la tuberculosis y otras enfermedades pulmonares podrían tratarse mediante la inhalación de "aires facticios". [27]

La máquina para producir "Aire Facticio" constaba de tres partes: un horno para quemar el material necesario, un recipiente con agua por donde pasaba el gas producido a través de un tubo en espiral (para "lavar" las impurezas) y finalmente el cilindro de gas. con un gasómetro donde el gas producido, "aire", podía introducirse en bolsas de aire portátiles (hechas de seda aceitosa hermética). El aparato respiratorio consistía en una de las bolsas de aire portátiles conectadas por un tubo a una boquilla. Con la ingeniería y producción de este nuevo equipo en 1794, se allanó el camino para los ensayos clínicos , [ se necesita aclaración ] que comenzaron en 1798 cuando Thomas Beddoes estableció la " Institución neumática para aliviar enfermedades mediante aires médicos" en Hotwells ( Bristol ). En el sótano del edificio, una máquina a gran escala producía gases bajo la supervisión de un joven Humphry Davy, a quien se animó a experimentar con nuevos gases para que los pacientes los inhalaran. [27] El primer trabajo importante de Davy fue el examen del óxido nitroso y la publicación de sus resultados en el libro: Investigaciones químicas y filosóficas (1800) . En esa publicación, Davy señala el efecto analgésico del óxido nitroso en la página 465 y su potencial para ser utilizado en operaciones quirúrgicas en la página 556. [88] Davy acuñó el nombre "gas de la risa" para el óxido nitroso. [89]
A pesar del descubrimiento de Davy de que la inhalación de óxido nitroso podía aliviar el dolor de una persona consciente, transcurrieron otros 44 años antes de que los médicos intentaran utilizarlo como anestesia . El uso de óxido nitroso como droga recreativa en las "fiestas del gas de la risa", organizadas principalmente para la clase alta británica , se convirtió en un éxito inmediato a partir de 1799. Si bien los efectos del gas generalmente hacen que el usuario parezca estuporoso, soñador y sedado, algunos la gente también "se ríe" en un estado de euforia y con frecuencia estalla en carcajadas. [90]
Uno de los primeros productores comerciales en Estados Unidos fue George Poe , primo del poeta Edgar Allan Poe , quien también fue el primero en licuar el gas. [91]
La primera vez que se utilizó óxido nitroso como fármaco anestésico en el tratamiento de un paciente fue cuando el dentista Horace Wells , con la ayuda de Gardner Quincy Colton y John Mankey Riggs , demostró insensibilidad al dolor de una extracción dental el 11 de diciembre de 1844. [92] En las semanas siguientes, Wells trató a los primeros 12 a 15 pacientes con óxido nitroso en Hartford, Connecticut , y, según su propio registro, sólo fracasó en dos casos. [93] A pesar de que Wells informó estos resultados convincentes a la sociedad médica de Boston en diciembre de 1844, otros dentistas no adoptaron inmediatamente este nuevo método. La razón de esto probablemente fue que Wells, en enero de 1845, en su primera demostración pública ante la facultad de medicina de Boston, no había tenido éxito en parte, dejando a sus colegas con dudas sobre su eficacia y seguridad. [94] El método no se generalizó hasta 1863, cuando Gardner Quincy Colton comenzó a utilizarlo con éxito en todas sus clínicas de la "Asociación Dental Colton", que acababa de establecer en New Haven y la ciudad de Nueva York . [27] Durante los tres años siguientes, Colton y sus asociados administraron con éxito óxido nitroso a más de 25.000 pacientes. [28] Hoy en día, el óxido nitroso se utiliza en odontología como ansiolítico, como complemento del anestésico local .
Sin embargo, no se encontró que el óxido nitroso fuera un anestésico lo suficientemente fuerte para su uso en cirugía mayor en entornos hospitalarios. En cambio, el éter dietílico , que es un anestésico más fuerte y potente, fue demostrado y aceptado para su uso en octubre de 1846, junto con el cloroformo en 1847. [27] Sin embargo, cuando Joseph Thomas Clover inventó el "inhalador de éter gaseoso" en 1876, Se convirtió en una práctica común en los hospitales iniciar todos los tratamientos anestésicos con un flujo suave de óxido nitroso y luego aumentar gradualmente la anestesia con éter más fuerte o cloroformo. El inhalador de éter de gas de Clover fue diseñado para suministrar al paciente óxido nitroso y éter al mismo tiempo, siendo la mezcla exacta controlada por el operador del dispositivo. Siguió utilizándose en muchos hospitales hasta la década de 1930. [28] Aunque los hospitales hoy en día utilizan una máquina de anestesia más avanzada , estas máquinas todavía utilizan el mismo principio iniciado con el inhalador de gas-éter de Clover, para iniciar la anestesia con óxido nitroso, antes de la administración de un anestésico más potente.
La popularización del óxido nitroso por parte de Colton llevó a su adopción por varios charlatanes de poca reputación , que lo promocionaban como una cura para la tisis , la escrófula , el catarro y otras enfermedades de la sangre, la garganta y los pulmones. El tratamiento con óxido nitroso fue administrado y autorizado como medicamento patentado por empresas como CL Blood y Jerome Harris en Boston y Charles E. Barney de Chicago. [95] [96]
Se publica una revisión de varios métodos para producir óxido nitroso. [97]
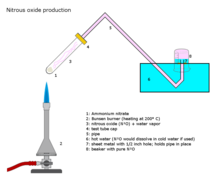
El óxido nitroso se prepara a escala industrial calentando cuidadosamente nitrato de amonio [97] a unos 250 °C, que se descompone en óxido nitroso y vapor de agua. [98]
La adición de diversas sales de fosfato favorece la formación de un gas más puro a temperaturas ligeramente más bajas. Esta reacción puede ser difícil de controlar y provocar una detonación . [99]
La descomposición del nitrato de amonio también es un método común de laboratorio para preparar el gas. De manera equivalente, se puede obtener calentando una mezcla de nitrato de sodio y sulfato de amonio : [100]
Otro método implica la reacción de urea, ácido nítrico y ácido sulfúrico: [101]
Se ha informado de la oxidación directa de amoníaco con un catalizador de dióxido de manganeso y óxido de bismuto : [102] cf. Proceso de Ostwald .
El cloruro de hidroxilamonio reacciona con el nitrito de sodio para dar óxido nitroso. Si se añade nitrito a la solución de hidroxilamina, el único subproducto que queda es agua salada. Sin embargo, si se añade la solución de hidroxilamina a la solución de nitrito (el nitrito está en exceso), se forman también óxidos de nitrógeno superiores, tóxicos:
Tratamiento del HNO
3con SnCl
2y HCl también se ha demostrado:
El ácido hiponitro se descompone en N 2 O y agua con una vida media de 16 días a 25 °C con un pH de 1 a 3. [103]
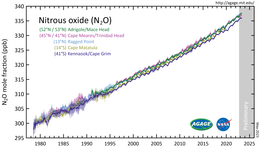



El óxido nitroso es un componente menor de la atmósfera terrestre y es una parte activa del ciclo planetario del nitrógeno . Según el análisis de muestras de aire recopiladas en sitios de todo el mundo, su concentración superó las 330 ppb en 2017. [8] La tasa de crecimiento de aproximadamente 1 ppb por año también se ha acelerado durante las últimas décadas. [9] La abundancia atmosférica del óxido nitroso ha aumentado más del 20% desde un nivel base de aproximadamente 270 ppb en el año 1750. [105]
Propiedades atmosféricas importantes del N
2O se resumen en la siguiente tabla:
En 2022, el IPCC informó que: "La perturbación humana del ciclo natural del nitrógeno mediante el uso de fertilizantes y estiércol sintéticos, así como la deposición de nitrógeno resultante de la agricultura terrestre y la quema de combustibles fósiles, ha sido el mayor impulsor del aumento de la contaminación atmosférica. N2O de 31,0 ± 0,5 ppb (10%) entre 1980 y 2019." [108]
17,0 (12,2 a 23,5) millones de toneladas de nitrógeno promedio anual total en N
2O se emitió en 2007-2016. [108] Alrededor del 40% del N
2Las emisiones de O provienen de los humanos y el resto es parte del ciclo natural del nitrógeno . [109] El norte
2El O emitido cada año por los humanos tiene un efecto invernadero equivalente a alrededor de 3 mil millones de toneladas de dióxido de carbono: en comparación, los humanos emitieron 37 mil millones de toneladas de dióxido de carbono real en 2019, y metano equivalente a 9 mil millones de toneladas de dióxido de carbono. [110]
La mayor parte del N.
2El O emitido a la atmósfera, de fuentes naturales y antropogénicas, es producido por microorganismos como bacterias desnitrificantes y hongos en suelos y océanos. [111] Los suelos bajo vegetación natural son una fuente importante de óxido nitroso y representan el 60% de todas las emisiones producidas naturalmente. Otras fuentes naturales incluyen los océanos (35%) y las reacciones químicas atmosféricas (5%). [112] Los humedales también pueden ser emisores de óxido nitroso . [113] [114] Las emisiones derivadas del deshielo del permafrost pueden ser significativas, pero a partir de 2022 esto no es seguro. [108]
Los principales componentes de las emisiones antropogénicas son los suelos agrícolas fertilizados y el estiércol de ganado (42%), la escorrentía y lixiviación de fertilizantes (25%), la quema de biomasa (10%), la quema de combustibles fósiles y procesos industriales (10%), la degradación biológica de otros emisiones atmosféricas que contienen nitrógeno (9%) y aguas residuales humanas (5%). [115] [116] [117] [118] [119] La agricultura mejora la producción de óxido nitroso mediante el cultivo del suelo, el uso de fertilizantes nitrogenados y el manejo de desechos animales. [120] Estas actividades estimulan a las bacterias naturales a producir más óxido nitroso. Las emisiones de óxido nitroso del suelo pueden ser difíciles de medir ya que varían notablemente en el tiempo y el espacio, [121] y la mayoría de las emisiones de un año pueden ocurrir cuando las condiciones son favorables durante los "momentos calurosos" [122] [123] y/o en ubicaciones favorables conocidas como "hotspots". [124]
Entre las emisiones industriales, la producción de ácido nítrico y ácido adípico son las mayores fuentes de emisiones de óxido nitroso. Las emisiones de ácido adípico surgen específicamente de la degradación del intermedio de ácido nitrólico derivado de la nitración de ciclohexanona. [115] [125] [126]
Los procesos naturales que generan óxido nitroso pueden clasificarse en nitrificación y desnitrificación . En concreto, incluyen:
Estos procesos se ven afectados por las propiedades físicas y químicas del suelo, como la disponibilidad de nitrógeno mineral y materia orgánica , la acidez y el tipo de suelo, así como por factores relacionados con el clima, como la temperatura del suelo y el contenido de agua.
La emisión del gas a la atmósfera está muy limitada por su consumo en el interior de las células, mediante un proceso catalizado por la enzima óxido nitroso reductasa . [127]
Contabilidad global de N
2Las fuentes y sumideros de O durante la década que terminó en 2016 indica que alrededor del 40% del promedio de 17 TgN/año ( teragramos , o millones de toneladas métricas, de nitrógeno por año) de emisiones se originaron en la actividad humana, y muestra que el crecimiento de las emisiones se debió principalmente a la expansión. agricultura . [11] [12]

El óxido nitroso tiene un importante potencial de calentamiento global como gas de efecto invernadero . Por molécula, considerada durante un período de 100 años, el óxido nitroso tiene 265 veces la capacidad de atrapar calor atmosférico que el dióxido de carbono ( CO
2). [107] Sin embargo, debido a su baja concentración (menos de 1/1.000 de la del CO
2), su contribución al efecto invernadero es inferior a un tercio de la del dióxido de carbono, y también inferior a la del metano . [128] Por otro lado, dado que alrededor del 40% del N
2El O que ingresa a la atmósfera es el resultado de la actividad humana, [115] el control del óxido nitroso es parte de los esfuerzos para frenar las emisiones de gases de efecto invernadero. [129]
La mayor parte del óxido nitroso liberado a la atmósfera causado por el hombre es una emisión de gases de efecto invernadero procedente de la agricultura , cuando los agricultores añaden fertilizantes a base de nitrógeno a los campos y mediante la descomposición del estiércol animal. La reducción de emisiones puede ser un tema candente en la política del cambio climático . [130]
El óxido nitroso también se libera como subproducto de la quema de combustibles fósiles, aunque la cantidad liberada depende del combustible que se utilizó. También se emite mediante la fabricación de ácido nítrico , que se utiliza en la síntesis de fertilizantes nitrogenados. La producción de ácido adípico, un precursor del nailon y otras fibras sintéticas para prendas de vestir, también libera óxido nitroso. [131]
Se ha implicado un aumento en las concentraciones atmosféricas de óxido nitroso como un posible contribuyente al calentamiento global extremadamente intenso durante el evento límite Cenomaniano-Turoniano . [132]
El óxido nitroso también ha sido implicado en el adelgazamiento de la capa de ozono . Un estudio de 2009 sugirió que N
2Las emisiones de O2 eran las emisiones que agotan la capa de ozono más importantes y se esperaba que siguieran siendo las más importantes durante todo el siglo XXI. [10] [133]
La transferencia de óxido nitroso de cilindros a granel a tanques de tipo E, más pequeños y transportables, con capacidad de 1.590 litros [134] es legal cuando el uso previsto del gas es para anestesia médica.
El Ministerio de Salud ha advertido que el óxido nitroso es un medicamento recetado y su venta o posesión sin receta constituye un delito según la Ley de Medicamentos. [135] Esta declaración aparentemente prohibiría todos los usos no medicinales del óxido nitroso, aunque se da a entender que sólo el uso recreativo será objetivo legal.
En agosto de 2015, el Consejo del distrito londinense de Lambeth ( Reino Unido ) prohibió el uso de la droga con fines recreativos, exponiendo a los infractores a una multa inmediata de hasta 1.000 libras esterlinas. [136]
En septiembre de 2023, el Gobierno anunció que el óxido nitroso sería ilegal antes de fin de año, y que su posesión podría conllevar hasta dos años de prisión o una multa ilimitada. [137]
La posesión de óxido nitroso es legal según la ley federal y no está sujeta al ámbito de la DEA . [138] Sin embargo, está regulado por la Administración de Alimentos y Medicamentos en virtud de la Ley de Alimentos, Medicamentos y Cosméticos; El procesamiento es posible en virtud de sus cláusulas de "mala rotulación", que prohíben la venta o distribución de óxido nitroso para el consumo humano . Muchos estados tienen leyes que regulan la posesión, venta y distribución de óxido nitroso. Estas leyes suelen prohibir la distribución a menores o limitar la cantidad de óxido nitroso que puede venderse sin una licencia especial. [ cita necesaria ] Por ejemplo, en el estado de California, la posesión para uso recreativo está prohibida y califica como un delito menor. [139]
{{cite journal}}: Mantenimiento CS1: bot: estado de la URL original desconocido ( enlace )... Autopresurizante (la presión de vapor a 20 ° C es ~ 50,1 bar... No tóxico, baja reactividad -> manipulación relativamente segura (seguridad general ???). .Energía adicional por descomposición (como monopropulsor: ISP de 170 s)...El impulso específico no cambia mucho con O/F...[página 2] N
2
O es un monopropulsor (como H
2
O
2
o hidrazina ...)
Por ejemplo, el N2O que fluye a 130 psi en una tubería compuesta de epoxi no reaccionaría incluso con una entrada de energía de ignición de 2500 J. Sin embargo, a 600 psi, la energía de ignición requerida era sólo de 6 J.