
Las bacterias Gram-negativas son bacterias que no retienen la tinción violeta cristal utilizada en el método de diferenciación bacteriana de tinción de Gram . [1] Su característica definitoria es su envoltura celular , que consiste en una delgada pared celular de peptidoglicano intercalada entre una membrana interna ( citoplasmática ) y una membrana externa . [ cita necesaria ] Estas bacterias se encuentran en todos los entornos que sustentan la vida en la Tierra .
Dentro de esta categoría, las especies notables incluyen el organismo modelo Escherichia coli , junto con diversas bacterias patógenas , como Pseudomonas aeruginosa , Chlamydia trachomatis y Yersinia pestis . Plantean desafíos importantes en el campo médico debido a su membrana externa, que actúa como una barrera protectora contra numerosos antibióticos (incluida la penicilina ), detergentes que normalmente dañarían la membrana celular interna y la enzima antimicrobiana lisozima producida por los animales como parte de su Sistema inmune innato . Además, la valva exterior de esta membrana contiene un lipopolisacárido complejo (LPS), cuyo componente lípido A puede desencadenar una reacción tóxica cuando las bacterias son lisadas por las células inmunitarias. Esta reacción puede provocar un shock séptico , lo que resulta en presión arterial baja , insuficiencia respiratoria , reducción del suministro de oxígeno y acidosis láctica . [2]
Se han desarrollado varias clases de antibióticos para atacar las bacterias gramnegativas, incluidas aminopenicilinas , ureidopenicilinas , cefalosporinas , combinaciones de betalactámicos e inhibidores de betalactamasas (como piperacilina-tazobactam ), antagonistas de folato , quinolonas y carbapenémicos . Muchos de estos antibióticos también cubren las bacterias grampositivas . Los antibióticos que se dirigen específicamente a los organismos gramnegativos incluyen aminoglucósidos , monobactamas (como aztreonam ) y ciprofloxacina .


Las bacterias gramnegativas convencionales (LPS-diderm) muestran estas características : [ cita necesaria ]
Junto con la forma de las células, la tinción de Gram es una herramienta de diagnóstico rápido y alguna vez se usó para agrupar especies en la subdivisión de bacterias.Históricamente , el reino Monera se dividió en cuatro divisiones según la tinción de Gram: Firmacutes (+), Gracillicutes (-), Mollicutes (0) y Mendocutes (var.). [3] Desde 1987, la monofilia de las bacterias gramnegativas ha sido refutada mediante estudios moleculares . [4] Sin embargo, algunos autores, como Cavalier-Smith, todavía los tratan como un taxón monofilético (aunque no como un clado ; su definición de monofilia requiere un único ancestro común pero no requiere holofilia , la propiedad de que todos los descendientes estén abarcados por el taxón) . ) y referirse al grupo como un subreino "Negibacteria". [5]
Las bacterias se clasifican tradicionalmente según su respuesta a la tinción de Gram en bacterias grampositivas y gramnegativas. Al tener una sola membrana, las bacterias grampositivas también se conocen como bacterias monodermas , mientras que las bacterias gramnegativas, al tener dos membranas, también se conocen como bacterias didermas . Tradicionalmente se pensaba que los grupos representan linajes, es decir, que la membrana adicional sólo evolucionó una vez, de modo que las bacterias gramnegativas están más estrechamente relacionadas entre sí que con cualquier bacteria grampositiva. Si bien esto suele ser cierto, el sistema de clasificación falla en algunos casos y las agrupaciones de linajes no coinciden con el resultado de la tinción. [6] [7] [8] [9] Por lo tanto, la tinción de Gram no se puede utilizar de manera confiable para evaluar las relaciones familiares de las bacterias. Sin embargo, la tinción suele dar información fiable sobre la composición de la membrana celular, distinguiendo entre la presencia o ausencia de una membrana lipídica externa . [6] [10]
De estos dos grupos estructuralmente distintos de organismos procarióticos , se cree que los procariotas monodermos son ancestrales. Basándose en una serie de observaciones diferentes, entre ellas que las bacterias grampositivas son las más sensibles a los antibióticos y que las bacterias gramnegativas son, en general, resistentes a los antibióticos, se ha propuesto que la membrana celular externa de las bacterias gramnegativas Las bacterias (diderms) evolucionaron como un mecanismo protector contra la presión de selección de antibióticos . [6] [7] [10] [11] Algunas bacterias como Deinococcus , que se tiñen como grampositivas debido a la presencia de una capa gruesa de peptidoglicano , pero que también poseen una membrana celular externa, se sugieren como intermediarias en la transición entre monodermo ( bacterias grampositivas) y diderm (gramnegativas). [6] [11] Las bacterias diderm también se pueden diferenciar aún más entre diderms simples que carecen de lipopolisacárido (LPS); las bacterias arquetípicas diderm, en las que la membrana celular externa contiene lipopolisacárido; y las bacterias diderm, en las que la membrana celular externa está formada por ácido micólico (p. ej. Mycobacterium ). [8] [9] [11] [12]
El grupo convencional de bacterias gramnegativas LPS- didermo (p. ej., Pseudomonadota , Aquificota , Chlamydiota , Bacteroidota , Chlorobiota , " Cianobacteria ", Fibrobacterota , Verrucomicrobiota , Planctomycetota , Spirochaetota , Acidobacteriota ; " Hidrobacteria ") se identifican de forma única mediante unas pocas firmas conservadas. indel (CSI) en la proteína HSP60 ( GroEL ). Además, varios taxones bacterianos (incluidos Negativicutes , Fusobacteriota , Synergistota y Elusimicrobiota ) que forman parte del filo Bacillota (un grupo monodermo) o ramas en sus proximidades también poseen una estructura celular diderma. [9] [11] [12] Carecen de la firma GroEL . [11] La presencia de este CSI en todas las especies secuenciadas de filos de bacterias gramnegativas que contienen lipopolisacáridos convencionales proporciona evidencia de que estos filos de bacterias forman un clado monofilético y que no se ha producido pérdida de la membrana externa de ninguna especie de este grupo. [11]
Las proteobacterias son un superfilo importante de bacterias gramnegativas, incluidas E. coli , Salmonella , Shigella y otras enterobacterias , Pseudomonas , Moraxella , Helicobacter , Stenotrophomonas , Bdellovibrio , bacterias del ácido acético , Legionella , etc. Otros grupos notables de bacterias gramnegativas incluyen las cianobacterias , las espiroquetas , las bacterias verdes del azufre y las bacterias verdes sin azufre . [ cita necesaria ]
Los cocos gramnegativos de relevancia médica incluyen los cuatro tipos que causan una enfermedad de transmisión sexual ( Neisseria gonorrhoeae [13] ), una meningitis ( Neisseria meningitidis [14] ) y síntomas respiratorios ( Moraxella catarrhalis , [15] Haemophilus influenzae ). [dieciséis]
Los bacilos gramnegativos de importancia médica incluyen una multitud de especies. Algunos de ellos causan principalmente problemas respiratorios ( Klebsiella pneumoniae , Legionella pneumophila , Pseudomonas aeruginosa ), principalmente problemas urinarios ( Escherichia coli , Proteus mirabilis , Enterobacter cloacae , Serratia marcescens ) y principalmente problemas gastrointestinales ( Helicobacter pylori , Salmonella enteritidis , Salmonella typhi ). [ cita necesaria ]
Las bacterias gramnegativas asociadas con infecciones adquiridas en hospitales incluyen Acinetobacter baumannii , que causa bacteriemia , meningitis secundaria y neumonía asociada a ventiladores en las unidades de cuidados intensivos de los hospitales .
La transformación es uno de los tres procesos de transferencia horizontal de genes , en los que el material genético exógeno pasa de una bacteria a otra, siendo los otros dos la conjugación (transferencia de material genético entre dos células bacterianas en contacto directo) y la transducción (inyección de ADN extraño por una virus bacteriófago en la bacteria huésped). [17] [18] En la transformación, el material genético pasa a través del medio intermedio y la absorción depende completamente de la bacteria receptora. [17]
En 2014, se sabía que alrededor de 80 especies de bacterias eran capaces de transformación, divididas aproximadamente en partes iguales entre bacterias grampositivas y gramnegativas; la cifra podría ser una sobreestimación, ya que varios de los informes están respaldados por artículos únicos. [17] La transformación se ha estudiado en especies de bacterias gramnegativas de importancia médica, como Helicobacter pylori , Legionella pneumophila , Neisseria meningitidis , Neisseria gonorrhoeae , Haemophilus influenzae y Vibrio cholerae . [19] También se ha estudiado en especies gramnegativas que se encuentran en el suelo como Pseudomonas stutzeri , Acinetobacter baylyi y patógenos vegetales gramnegativos como Ralstonia solanacearum y Xylella fastidiosa . [19]
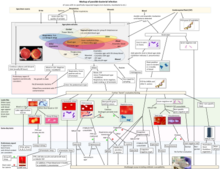
Una de las varias características únicas de las bacterias gramnegativas es la estructura de la membrana externa bacteriana . La valva exterior de esta membrana contiene lipopolisacárido (LPS), cuya porción de lípido A actúa como una endotoxina . [1] Si las bacterias gramnegativas ingresan al sistema circulatorio , el LPS puede desencadenar una respuesta inmune innata , activando el sistema inmunológico y produciendo citocinas (reguladores hormonales). Esto provoca inflamación y puede provocar una reacción tóxica que provoca fiebre, aumento de la frecuencia respiratoria y presión arterial baja . Es por eso que algunas infecciones por bacterias gramnegativas pueden provocar un shock séptico potencialmente mortal . [2]
La membrana externa protege a las bacterias de varios antibióticos , colorantes y detergentes que normalmente dañarían la membrana interna o la pared celular (hecha de peptidoglicano ). La membrana externa proporciona a estas bacterias resistencia a la lisozima y la penicilina . El espacio periplásmico (espacio entre las dos membranas celulares) también contiene enzimas que descomponen o modifican los antibióticos. Los medicamentos comúnmente utilizados para tratar infecciones por gramnegativos incluyen amino, carboxi y ureidopenicilinas ( ampicilina , amoxicilina , pipercilina , ticarcilina ). Estos medicamentos se pueden combinar con inhibidores de betalactamasas para combatir la presencia de enzimas que pueden digerir estos medicamentos (conocidas como beta-lactamasas) . lactamasas ) en el espacio periplásmico. Otras clases de fármacos que tienen espectro gramnegativo incluyen cefalosporinas , monobactamas ( aztreonam ), aminoglucósidos, quinolonas , macrólidos , cloranfenicol , antagonistas del folato y carbapenémicos . [20]
Los adjetivos grampositivos y gramnegativos derivan del apellido de Hans Christian Gram , bacteriólogo danés; como adjetivos epónimos , su letra inicial puede ser G mayúscula o g minúscula , dependiendo de qué guía de estilo (por ejemplo, la del CDC ), si la hay, rige el documento que se está escribiendo. [21] Esto se explica con más detalle en Tinción de Gram § Nota ortográfica .