
Un polímero es una sustancia compuesta de macromoléculas. [2] Una macromolécula es una molécula de masa molecular relativa elevada, cuya estructura comprende esencialmente la repetición múltiple de unidades derivadas, real o conceptualmente, de moléculas de masa molecular relativa baja. [3]
Un polímero ( / ˈ p ɒ l ɪ m ər / [4] [5] ) es una sustancia o material que consiste en moléculas muy grandes, o macromoléculas , que están constituidas por muchas subunidades repetidas derivadas de una o más especies de monómeros . [6] Debido a su amplio espectro de propiedades, [7] tanto los polímeros sintéticos como los naturales juegan papeles esenciales y omnipresentes en la vida cotidiana. [8] Los polímeros van desde los plásticos sintéticos familiares como el poliestireno hasta los biopolímeros naturales como el ADN y las proteínas que son fundamentales para la estructura y función biológicas. Los polímeros, tanto naturales como sintéticos, se crean mediante la polimerización de muchas moléculas pequeñas, conocidas como monómeros . Su masa molecular consecuentemente grande , en relación con los compuestos de moléculas pequeñas , produce propiedades físicas únicas que incluyen tenacidad , alta elasticidad , viscoelasticidad y una tendencia a formar estructuras amorfas y semicristalinas en lugar de cristales .
Los polímeros se estudian en los campos de la ciencia de polímeros (que incluye la química de polímeros y la física de polímeros ), la biofísica y la ciencia e ingeniería de materiales . Históricamente, los productos que surgen de la unión de unidades repetidas por enlaces químicos covalentes han sido el foco principal de la ciencia de polímeros. Un área importante emergente ahora se centra en los polímeros supramoleculares formados por enlaces no covalentes. El poliisopreno de caucho de látex es un ejemplo de polímero natural, y el poliestireno de poliestireno es un ejemplo de polímero sintético. En contextos biológicos, esencialmente todas las macromoléculas biológicas —es decir, proteínas (poliamidas), ácidos nucleicos (polinucleótidos) y polisacáridos— son puramente poliméricas o están compuestas en gran parte de componentes poliméricos.

El término "polímero" deriva del griego πολύς (polus) 'mucho, mucho' y μέρος (meros) 'parte'. El término fue acuñado en 1833 por Jöns Jacob Berzelius , aunque con una definición distinta de la definición moderna de la IUPAC . [9] [10] El concepto moderno de polímeros como estructuras macromoleculares unidas covalentemente fue propuesto en 1920 por Hermann Staudinger , [11] quien pasó la siguiente década encontrando evidencia experimental para esta hipótesis. [12]

Los polímeros son de dos tipos: naturales y sintéticos o creados por el hombre .
Los materiales poliméricos naturales como el cáñamo , la goma laca , el ámbar , la lana , la seda y el caucho natural se han utilizado durante siglos. Existe una variedad de otros polímeros naturales, como la celulosa , que es el componente principal de la madera y el papel.
La hemoglicina (anteriormente denominada hemolitina ) es un polímero espacial que es el primer polímero de aminoácidos encontrado en los meteoritos . [13] [14] [15]
La lista de polímeros sintéticos , aproximadamente en orden de demanda mundial, incluye polietileno , polipropileno , poliestireno , cloruro de polivinilo , caucho sintético , resina de fenol formaldehído (o baquelita ), neopreno , nailon , poliacrilonitrilo , PVB , silicona y muchos más. Cada año se fabrican más de 330 millones de toneladas de estos polímeros (2015). [16]
Por lo general, la cadena principal de enlaces continuos de un polímero utilizado para la preparación de plásticos consta principalmente de átomos de carbono . Un ejemplo sencillo es el polietileno ('polythene' en inglés británico), cuya unidad repetitiva o monómero es el etileno . Existen muchas otras estructuras; por ejemplo, elementos como el silicio forman materiales familiares como las siliconas, como por ejemplo la masilla Silly Putty y el sellador de tuberías a prueba de agua. El oxígeno también suele estar presente en las cadenas principales de polímeros, como las del polietilenglicol , los polisacáridos (en enlaces glucosídicos ) y el ADN (en enlaces fosfodiéster ).

La polimerización es el proceso de combinar muchas moléculas pequeñas conocidas como monómeros en una cadena o red unida covalentemente. Durante el proceso de polimerización, algunos grupos químicos pueden perderse de cada monómero. Esto sucede en la polimerización del poliéster PET . Los monómeros son ácido tereftálico (HOOC—C 6 H 4 —COOH) y etilenglicol (HO—CH 2 —CH 2 —OH) pero la unidad repetitiva es —OC—C 6 H 4 —COO—CH 2 —CH 2 —O—, que corresponde a la combinación de los dos monómeros con la pérdida de dos moléculas de agua. La pieza distintiva de cada monómero que se incorpora al polímero se conoce como unidad repetitiva o residuo monomérico.
Los métodos sintéticos se dividen generalmente en dos categorías, polimerización por crecimiento en etapas y polimerización en cadena . [17] La diferencia esencial entre las dos es que en la polimerización en cadena, los monómeros se agregan a la cadena uno a la vez solamente, [18] como en el poliestireno , mientras que en la polimerización por crecimiento en etapas las cadenas de monómeros pueden combinarse entre sí directamente, [19] como en el poliéster . La polimerización por crecimiento en etapas se puede dividir en policondensación , en la que se forma un subproducto de baja masa molar en cada paso de reacción, y poliadición .
Los métodos más nuevos, como la polimerización por plasma , no encajan perfectamente en ninguna de las dos categorías. Las reacciones de polimerización sintética pueden llevarse a cabo con o sin catalizador . La síntesis de biopolímeros en el laboratorio, especialmente de proteínas , es un área de intensa investigación.
Existen tres clases principales de biopolímeros: polisacáridos , polipéptidos y polinucleótidos . En las células vivas, pueden sintetizarse mediante procesos mediados por enzimas, como la formación de ADN catalizada por la ADN polimerasa . La síntesis de proteínas implica múltiples procesos mediados por enzimas para transcribir la información genética del ADN al ARN y, posteriormente, traducir esa información para sintetizar la proteína específica a partir de aminoácidos . La proteína puede modificarse aún más después de la traducción para proporcionar la estructura y el funcionamiento adecuados. Existen otros biopolímeros como el caucho , la suberina , la melanina y la lignina .
Los polímeros naturales como el algodón , el almidón y el caucho eran materiales conocidos durante años antes de que aparecieran en el mercado polímeros sintéticos como el polietileno y el perspex . Muchos polímeros de importancia comercial se sintetizan mediante la modificación química de polímeros naturales. Algunos ejemplos destacados incluyen la reacción del ácido nítrico y la celulosa para formar nitrocelulosa y la formación de caucho vulcanizado mediante el calentamiento del caucho natural en presencia de azufre . Las formas en que se pueden modificar los polímeros incluyen la oxidación , la reticulación y el recubrimiento de los extremos .
La estructura de un material polimérico se puede describir en diferentes escalas de longitud, desde la escala de longitud sub-nm hasta la macroscópica. De hecho, existe una jerarquía de estructuras, en la que cada etapa proporciona las bases para la siguiente. [20] El punto de partida para la descripción de la estructura de un polímero es la identidad de sus monómeros constituyentes. A continuación, la microestructura describe esencialmente la disposición de estos monómeros dentro del polímero a escala de una sola cadena. La microestructura determina la posibilidad de que el polímero forme fases con diferentes disposiciones, por ejemplo a través de la cristalización , la transición vítrea o la separación de microfases . [21] Estas características juegan un papel importante en la determinación de las propiedades físicas y químicas de un polímero.
La identidad de las unidades repetidas (residuos monoméricos, también conocidos como "meros") que componen un polímero es su primer y más importante atributo. La nomenclatura de los polímeros se basa generalmente en el tipo de residuos monoméricos que componen el polímero. Un polímero que contiene solo un tipo de unidad repetida se conoce como homopolímero , mientras que un polímero que contiene dos o más tipos de unidades repetidas se conoce como copolímero . [22] Un terpolímero es un copolímero que contiene tres tipos de unidades repetidas. [23]
El poliestireno está compuesto únicamente de unidades repetidas basadas en estireno y se clasifica como un homopolímero. El tereftalato de polietileno , aunque se produce a partir de dos monómeros diferentes ( etilenglicol y ácido tereftálico ), generalmente se considera un homopolímero porque solo se forma un tipo de unidad repetida. El etileno-acetato de vinilo contiene más de una variedad de unidad repetida y es un copolímero. Algunos polímeros biológicos están compuestos de una variedad de residuos monoméricos diferentes pero estructuralmente relacionados; por ejemplo, los polinucleótidos como el ADN están compuestos de cuatro tipos de subunidades de nucleótidos .
Un polímero que contiene subunidades ionizables (por ejemplo, grupos carboxílicos colgantes ) se conoce como polielectrolito o ionómero , cuando la fracción de unidades ionizables es grande o pequeña respectivamente.
La microestructura de un polímero (a veces llamada configuración) se relaciona con la disposición física de los residuos monoméricos a lo largo de la cadena principal. [24] Estos son los elementos de la estructura del polímero que requieren la ruptura de un enlace covalente para cambiar. Se pueden producir varias estructuras de polímeros dependiendo de los monómeros y las condiciones de reacción: Un polímero puede consistir en macromoléculas lineales que contienen cada una solo una cadena no ramificada. En el caso del polietileno no ramificado, esta cadena es un n- alcano de cadena larga. También hay macromoléculas ramificadas con una cadena principal y cadenas laterales, en el caso del polietileno las cadenas laterales serían grupos alquilo . En particular, las macromoléculas no ramificadas pueden estar en estado sólido semicristalinas, secciones de cadena cristalinas resaltadas en rojo en la figura siguiente.
Mientras que los polímeros ramificados y no ramificados suelen ser termoplásticos, muchos elastómeros tienen una reticulación de malla ancha entre las "cadenas principales". La reticulación de malla cerrada, por otro lado, da lugar a termoendurecibles . Las reticulaciones y las ramificaciones se muestran como puntos rojos en las figuras. Los polímeros muy ramificados son amorfos y las moléculas del sólido interactúan aleatoriamente.

Una característica microestructural importante de un polímero es su arquitectura y forma, que se relaciona con la forma en que los puntos de ramificación conducen a una desviación de una cadena lineal simple. [25] Una molécula de polímero ramificada se compone de una cadena principal con una o más cadenas laterales o ramificaciones sustituyentes. Los tipos de polímeros ramificados incluyen polímeros en estrella , polímeros en peine , polímeros en cepillo , polímeros dendronizados , polímeros en escalera y dendrímeros . [25] También existen polímeros bidimensionales (2DP) que se componen de unidades repetidas topológicamente planas. La arquitectura de un polímero afecta muchas de sus propiedades físicas, incluida la viscosidad de la solución, la viscosidad de la masa fundida, la solubilidad en varios solventes, la temperatura de transición vítrea y el tamaño de las bobinas de polímero individuales en solución. Se puede emplear una variedad de técnicas para la síntesis de un material polimérico con una gama de arquitecturas, por ejemplo, la polimerización viva .
Un medio común para expresar la longitud de una cadena es el grado de polimerización , que cuantifica el número de monómeros incorporados a la cadena. [26] [27] Al igual que con otras moléculas, el tamaño de un polímero también puede expresarse en términos de peso molecular . Dado que las técnicas de polimerización sintética suelen producir una distribución estadística de longitudes de cadena, el peso molecular se expresa en términos de promedios ponderados. El peso molecular promedio en número ( M n ) y el peso molecular promedio en peso ( M w ) son los que se informan con mayor frecuencia. [28] [29] La relación de estos dos valores ( M w / M n ) es la dispersidad ( Đ ), que se utiliza comúnmente para expresar el ancho de la distribución del peso molecular. [30]
Las propiedades físicas [31] del polímero dependen fuertemente de la longitud (o equivalentemente, el peso molecular) de la cadena del polímero. [32] Un ejemplo importante de las consecuencias físicas del peso molecular es la escala de la viscosidad (resistencia al flujo) en la masa fundida. [33] La influencia del peso molecular promedio en peso ( ) en la viscosidad de la masa fundida ( ) depende de si el polímero está por encima o por debajo del inicio de los enredos . Por debajo del peso molecular de enredo [ aclaración necesaria ] , , mientras que por encima del peso molecular de enredo, . En el último caso, aumentar la longitud de la cadena del polímero 10 veces aumentaría la viscosidad más de 1000 veces. [34] [ página necesaria ] Además, aumentar la longitud de la cadena tiende a disminuir la movilidad de la cadena, aumentar la resistencia y la tenacidad y aumentar la temperatura de transición vítrea (T g ). [35] Esto es el resultado del aumento de las interacciones de la cadena, como las atracciones de van der Waals y los enredos que vienen con el aumento de la longitud de la cadena. [36] [37] Estas interacciones tienden a fijar las cadenas individuales más fuertemente en su posición y a resistir deformaciones y rupturas de la matriz, tanto a tensiones más altas como a temperaturas más elevadas.
Los copolímeros se clasifican como copolímeros estadísticos, copolímeros alternados, copolímeros en bloque, copolímeros de injerto o copolímeros de gradiente. En la figura esquemática que aparece a continuación, Ⓐ y Ⓑ simbolizan las dos unidades repetidas .
Los monómeros dentro de un copolímero pueden organizarse a lo largo de la cadena principal de diversas maneras. Un copolímero que contiene una disposición controlada de monómeros se denomina polímero controlado por secuencia . [44] Los copolímeros alternados, periódicos y en bloque son ejemplos simples de polímeros controlados por secuencia .
La tacticidad describe la estereoquímica relativa de los centros quirales en unidades estructurales vecinas dentro de una macromolécula. Existen tres tipos de tacticidad: isotáctica (todos los sustituyentes en el mismo lado), atáctica (ubicación aleatoria de los sustituyentes) y sindiotáctica (ubicación alternada de los sustituyentes).
La morfología de los polímeros describe en general la disposición y el ordenamiento a microescala de las cadenas de polímeros en el espacio. Las propiedades físicas macroscópicas de un polímero están relacionadas con las interacciones entre las cadenas de polímeros.
Cuando se aplica a polímeros, el término cristalino tiene un uso algo ambiguo. En algunos casos, el término cristalino encuentra un uso idéntico al utilizado en la cristalografía convencional . Por ejemplo, la estructura de una proteína o polinucleótido cristalino, como una muestra preparada para cristalografía de rayos X , puede definirse en términos de una celda unitaria convencional compuesta de una o más moléculas de polímero con dimensiones de celda de cientos de angstroms o más. Un polímero sintético puede describirse libremente como cristalino si contiene regiones de ordenamiento tridimensional en escalas de longitud atómica (en lugar de macromolecular), que generalmente surgen del plegamiento o apilamiento intramolecular de cadenas adyacentes. Los polímeros sintéticos pueden constar de regiones tanto cristalinas como amorfas; el grado de cristalinidad puede expresarse en términos de una fracción de peso o fracción de volumen de material cristalino. Pocos polímeros sintéticos son completamente cristalinos. [47] La cristalinidad de los polímeros se caracteriza por su grado de cristalinidad, que varía desde cero para un polímero completamente no cristalino hasta uno para un polímero teórico completamente cristalino. Los polímeros con regiones microcristalinas son generalmente más duros (se pueden doblar más sin romperse) y más resistentes al impacto que los polímeros totalmente amorfos. [48] Los polímeros con un grado de cristalinidad cercano a cero o uno tenderán a ser transparentes, mientras que los polímeros con grados intermedios de cristalinidad tenderán a ser opacos debido a la dispersión de la luz por las regiones cristalinas o vítreas. Para muchos polímeros, la cristalinidad también puede estar asociada con una menor transparencia.
El espacio ocupado por una molécula de polímero se expresa generalmente en términos de radio de giro , que es una distancia promedio desde el centro de masa de la cadena hasta la cadena misma. Alternativamente, se puede expresar en términos de volumen permeado , que es el volumen abarcado por la cadena de polímero y escala con el cubo del radio de giro. [49] Los modelos teóricos más simples para polímeros en estado fundido y amorfo son las cadenas ideales .
Las propiedades de los polímeros dependen de su estructura y se dividen en clases según sus bases físicas. Muchas propiedades físicas y químicas describen cómo se comporta un polímero como un material macroscópico continuo. Se clasifican como propiedades en masa o propiedades intensivas según la termodinámica .

Las propiedades generales de un polímero son las que más suelen interesar en el uso final. Son las propiedades que determinan cómo se comporta realmente el polímero a escala macroscópica.
La resistencia a la tracción de un material cuantifica la cantidad de tensión de elongación que soportará el material antes de fallar. [50] [51] Esto es muy importante en aplicaciones que dependen de la resistencia física o durabilidad de un polímero. Por ejemplo, una banda de goma con una mayor resistencia a la tracción soportará un mayor peso antes de romperse. En general, la resistencia a la tracción aumenta con la longitud de la cadena de polímero y la reticulación de las cadenas de polímero.
El módulo de Young cuantifica la elasticidad del polímero. Se define, para pequeñas deformaciones , como la relación entre la tasa de cambio de la tensión y la deformación. Al igual que la resistencia a la tracción, es muy relevante en aplicaciones de polímeros que involucran las propiedades físicas de los polímeros, como las bandas de goma. El módulo depende en gran medida de la temperatura. La viscoelasticidad describe una respuesta elástica compleja dependiente del tiempo, que exhibirá histéresis en la curva de tensión-deformación cuando se retira la carga. El análisis mecánico dinámico o DMA mide este módulo complejo oscilando la carga y midiendo la deformación resultante en función del tiempo.
Las propiedades de transporte, como la difusividad, describen la rapidez con la que las moléculas se desplazan a través de la matriz polimérica. Estas propiedades son muy importantes en muchas aplicaciones de polímeros para películas y membranas.
El movimiento de macromoléculas individuales se produce mediante un proceso llamado reptación , en el que cada molécula de la cadena se ve limitada por enredos con las cadenas vecinas para moverse dentro de un tubo virtual. La teoría de la reptación puede explicar la dinámica de las moléculas de polímeros y la viscoelasticidad . [52]
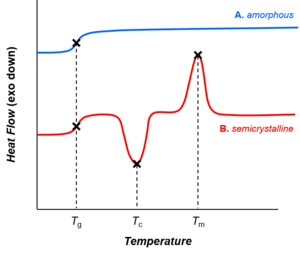
Dependiendo de sus estructuras químicas, los polímeros pueden ser semicristalinos o amorfos. Los polímeros semicristalinos pueden experimentar transiciones de cristalización y fusión , mientras que los polímeros amorfos no. En los polímeros, la cristalización y la fusión no sugieren transiciones de fase sólido-líquido, como en el caso del agua u otros fluidos moleculares. En cambio, la cristalización y la fusión se refieren a las transiciones de fase entre dos estados sólidos ( es decir , semicristalino y amorfo). La cristalización ocurre por encima de la temperatura de transición vítrea ( T g ) y por debajo de la temperatura de fusión ( T m ).
Todos los polímeros (amorfos o semicristalinos) pasan por transiciones vítreas . La temperatura de transición vítrea ( T g ) es un parámetro físico crucial para la fabricación, el procesamiento y el uso de polímeros. Por debajo de T g , los movimientos moleculares se congelan y los polímeros son frágiles y vítreos. Por encima de T g , los movimientos moleculares se activan y los polímeros son gomosos y viscosos. La temperatura de transición vítrea se puede diseñar alterando el grado de ramificación o reticulación en el polímero o mediante la adición de plastificantes . [53]
Mientras que la cristalización y la fusión son transiciones de fase de primer orden , la transición vítrea no lo es. [54] La transición vítrea comparte características de las transiciones de fase de segundo orden (como la discontinuidad en la capacidad térmica, como se muestra en la figura), pero generalmente no se considera una transición termodinámica entre estados de equilibrio.

En general, las mezclas poliméricas son mucho menos miscibles que las mezclas de materiales de moléculas pequeñas . Este efecto resulta del hecho de que la fuerza impulsora para la mezcla es generalmente la entropía , no la energía de interacción. En otras palabras, los materiales miscibles generalmente forman una solución no porque su interacción entre sí sea más favorable que su autointeracción, sino debido a un aumento en la entropía y, por lo tanto, la energía libre asociada con el aumento de la cantidad de volumen disponible para cada componente. Este aumento en la entropía se escala con el número de partículas (o moles) que se mezclan. Dado que las moléculas poliméricas son mucho más grandes y, por lo tanto, generalmente tienen volúmenes específicos mucho más altos que las moléculas pequeñas, el número de moléculas involucradas en una mezcla polimérica es mucho menor que el número en una mezcla de moléculas pequeñas de igual volumen. La energía de la mezcla, por otro lado, es comparable en una base por volumen para mezclas poliméricas y de moléculas pequeñas. Esto tiende a aumentar la energía libre de la mezcla para soluciones de polímeros y, por lo tanto, hace que la solvatación sea menos favorable y, por lo tanto, hace que la disponibilidad de soluciones concentradas de polímeros sea mucho más rara que las de moléculas pequeñas.
Además, el comportamiento de las fases de las soluciones y mezclas de polímeros es más complejo que el de las mezclas de moléculas pequeñas. Mientras que la mayoría de las soluciones de moléculas pequeñas presentan solo una transición de fase de temperatura crítica de solución superior (UCST), en la que la separación de fases ocurre con el enfriamiento, las mezclas de polímeros suelen presentar una transición de fase de temperatura crítica de solución inferior (LCST), en la que la separación de fases ocurre con el calentamiento.
En soluciones diluidas, las propiedades del polímero se caracterizan por la interacción entre el solvente y el polímero. En un buen solvente, el polímero aparece hinchado y ocupa un gran volumen. En este escenario, las fuerzas intermoleculares entre las subunidades de solvente y monómero dominan sobre las interacciones intramoleculares. En un mal solvente o solvente deficiente, las fuerzas intramoleculares dominan y la cadena se contrae. En el solvente theta , o el estado de la solución de polímero donde el valor del segundo coeficiente virial se convierte en 0, la repulsión intermolecular polímero-solvente equilibra exactamente la atracción intramolecular monómero-monómero. Bajo la condición theta (también llamada condición de Flory ), el polímero se comporta como una bobina aleatoria ideal . La transición entre los estados se conoce como transición bobina-glóbulo .
La inclusión de plastificantes tiende a reducir la T g y aumentar la flexibilidad del polímero. La adición del plastificante también modificará la dependencia de la temperatura de transición vítrea T g de la velocidad de enfriamiento. [55] La movilidad de la cadena puede cambiar aún más si las moléculas de plastificante dan lugar a la formación de enlaces de hidrógeno. Los plastificantes son generalmente moléculas pequeñas que son químicamente similares al polímero y crean espacios entre las cadenas de polímero para una mayor movilidad y menos interacciones entre cadenas. Un buen ejemplo de la acción de los plastificantes está relacionado con los cloruros de polivinilo o PVC. Un uPVC, o cloruro de polivinilo no plastificado, se utiliza para cosas como tuberías. Una tubería no tiene plastificantes en ella, porque necesita permanecer fuerte y resistente al calor. El PVC plastificado se utiliza en la ropa para una calidad flexible. Los plastificantes también se ponen en algunos tipos de película adhesiva para hacer que el polímero sea más flexible.
Las fuerzas de atracción entre las cadenas de polímeros desempeñan un papel importante en la determinación de las propiedades del polímero. Debido a que las cadenas de polímeros son tan largas, tienen muchas interacciones entre cadenas por molécula, lo que amplifica el efecto de estas interacciones en las propiedades del polímero en comparación con las atracciones entre moléculas convencionales. Diferentes grupos laterales en el polímero pueden hacer que el polímero forme enlaces iónicos o enlaces de hidrógeno entre sus propias cadenas. Estas fuerzas más fuertes generalmente dan como resultado una mayor resistencia a la tracción y puntos de fusión cristalinos más altos.
Las fuerzas intermoleculares en los polímeros pueden verse afectadas por dipolos en las unidades monoméricas. Los polímeros que contienen grupos amida o carbonilo pueden formar enlaces de hidrógeno entre cadenas adyacentes; los átomos de hidrógeno parcialmente cargados positivamente en los grupos NH de una cadena son fuertemente atraídos por los átomos de oxígeno parcialmente cargados negativamente en los grupos C=O de otra. Estos fuertes enlaces de hidrógeno, por ejemplo, dan como resultado la alta resistencia a la tracción y el punto de fusión de los polímeros que contienen enlaces de uretano o urea . Los poliésteres tienen enlaces dipolo-dipolo entre los átomos de oxígeno en los grupos C=O y los átomos de hidrógeno en los grupos HC. El enlace dipolar no es tan fuerte como el enlace de hidrógeno, por lo que el punto de fusión y la resistencia de un poliéster son más bajos que los del Kevlar ( Twaron ), pero los poliésteres tienen mayor flexibilidad. Los polímeros con unidades no polares como el polietileno interactúan solo a través de fuerzas de Van der Waals débiles . Como resultado, normalmente tienen temperaturas de fusión más bajas que otros polímeros.
Cuando un polímero se dispersa o se disuelve en un líquido, como en productos comerciales como pinturas y pegamentos, las propiedades químicas y las interacciones moleculares influyen en la forma en que fluye la solución e incluso pueden provocar el autoensamblaje del polímero en estructuras complejas. Cuando un polímero se aplica como revestimiento, las propiedades químicas influirán en la adhesión del revestimiento y en cómo interactúa con materiales externos, como los revestimientos de polímeros superhidrofóbicos que dan lugar a la resistencia al agua. En general, las propiedades químicas de un polímero son elementos importantes para el diseño de nuevos productos de materiales poliméricos.
Los polímeros como PMMA y HEMA:MMA se utilizan como matrices en el medio de ganancia de los láseres de colorante de estado sólido , también conocidos como láseres de polímero dopado con colorante de estado sólido. Estos polímeros tienen una alta calidad de superficie y también son altamente transparentes, de modo que las propiedades del láser están dominadas por el colorante láser utilizado para dopar la matriz de polímero. Se sabe que este tipo de láseres, que también pertenecen a la clase de láseres orgánicos , producen anchos de línea muy estrechos que son útiles para aplicaciones espectroscópicas y analíticas. [56] Un parámetro óptico importante en el polímero utilizado en aplicaciones láser es el cambio en el índice de refracción con la temperatura, también conocido como dn/dT. Para los polímeros mencionados aquí, (dn/dT) ~ −1,4 × 10 −4 en unidades de K −1 en el rango de 297 ≤ T ≤ 337 K. [57]
La mayoría de los polímeros convencionales, como el polietileno, son aislantes eléctricos , pero el desarrollo de polímeros que contienen enlaces π-conjugados ha dado lugar a una gran cantidad de semiconductores basados en polímeros , como los politiofenos , lo que ha dado lugar a muchas aplicaciones en el campo de la electrónica orgánica .
En la actualidad, los polímeros sintéticos se utilizan en casi todos los ámbitos de la vida. La sociedad moderna sería muy distinta sin ellos. La expansión del uso de polímeros está relacionada con sus propiedades únicas: baja densidad, bajo coste, buenas propiedades de aislamiento térmico y eléctrico, alta resistencia a la corrosión, fabricación de polímeros con bajo consumo energético y fácil procesamiento para obtener productos finales. Para una aplicación determinada, las propiedades de un polímero se pueden ajustar o mejorar mediante la combinación con otros materiales, como en el caso de los compuestos . Su aplicación permite ahorrar energía (automóviles y aviones más ligeros, edificios con aislamiento térmico), proteger los alimentos y el agua potable (envases), ahorrar tierra y reducir el uso de fertilizantes (fibras sintéticas), conservar otros materiales (recubrimientos), proteger y salvar vidas (higiene, aplicaciones médicas). A continuación se ofrece una lista representativa, no exhaustiva, de aplicaciones.
Existen múltiples convenciones para nombrar sustancias poliméricas. Muchos polímeros de uso común, como los que se encuentran en productos de consumo, se conocen con un nombre común o trivial. El nombre trivial se asigna en función de precedentes históricos o usos populares en lugar de una convención de nomenclatura estandarizada. Tanto la American Chemical Society (ACS) [58] como la IUPAC [59] han propuesto convenciones de nomenclatura estandarizadas; las convenciones de la ACS y la IUPAC son similares pero no idénticas. [60] En la siguiente tabla se ofrecen ejemplos de las diferencias entre las diversas convenciones de nomenclatura:
En ambas convenciones estandarizadas, los nombres de los polímeros tienen como objetivo reflejar el monómero o los monómeros a partir de los cuales se sintetizan (nomenclatura basada en la fuente) en lugar de la naturaleza precisa de la subunidad repetitiva. Por ejemplo, el polímero sintetizado a partir del alqueno simple eteno se llama polietileno y conserva el sufijo -eno , aunque el doble enlace se elimina durante el proceso de polimerización:
Sin embargo, la nomenclatura basada en la estructura de la IUPAC se basa en la denominación de la unidad repetitiva constitucional preferida . [61]
La IUPAC también ha publicado directrices para abreviar los nombres de nuevos polímeros. [62] 138 abreviaturas de polímeros comunes también están estandarizadas en la norma ISO 1043-1. [63]
La caracterización de polímeros abarca muchas técnicas para determinar la composición química, la distribución del peso molecular y las propiedades físicas. Algunas técnicas comunes incluyen las siguientes:

La degradación de un polímero es un cambio en las propiedades (resistencia a la tracción, color , forma o peso molecular) de un polímero o un producto a base de polímero bajo la influencia de uno o más factores ambientales, como el calor , la luz y la presencia de ciertas sustancias químicas , oxígeno y enzimas . Este cambio en las propiedades suele ser el resultado de la ruptura de enlaces en la cadena principal del polímero ( escisión de la cadena ), que puede ocurrir en los extremos de la cadena o en posiciones aleatorias en la cadena.
Aunque estos cambios son frecuentemente indeseables, en algunos casos, como la biodegradación y el reciclado , pueden tener como objetivo prevenir la contaminación ambiental . La degradación también puede ser útil en entornos biomédicos. Por ejemplo, se emplea un copolímero de ácido poliláctico y ácido poliglicólico en suturas hidrolizables que se degradan lentamente después de ser aplicadas a una herida.
La susceptibilidad de un polímero a la degradación depende de su estructura. Los epóxidos y las cadenas que contienen funcionalidades aromáticas son especialmente susceptibles a la degradación por rayos UV , mientras que los poliésteres son susceptibles a la degradación por hidrólisis . Los polímeros que contienen una cadena principal insaturada se degradan mediante craqueo por ozono . Los polímeros a base de carbono son más susceptibles a la degradación térmica que los polímeros inorgánicos como el polidimetilsiloxano y, por lo tanto, no son ideales para la mayoría de las aplicaciones de alta temperatura. [ cita requerida ]
La degradación del polietileno se produce por escisión aleatoria, es decir, una ruptura aleatoria de los enlaces que mantienen unidos los átomos del polímero. Cuando se calienta por encima de los 450 °C, el polietileno se degrada para formar una mezcla de hidrocarburos. En el caso de la escisión del extremo de la cadena, se liberan monómeros y este proceso se conoce como descompresión o despolimerización . El mecanismo que predomine dependerá del tipo de polímero y de la temperatura; en general, los polímeros sin sustituyentes o con un solo sustituyente pequeño en la unidad repetida se descompondrán mediante escisión aleatoria de la cadena.
La clasificación de residuos de polímeros con fines de reciclaje puede facilitarse mediante el uso de los códigos de identificación de resina desarrollados por la Sociedad de la Industria del Plástico para identificar el tipo de plástico.

El fallo de componentes de polímero críticos para la seguridad puede provocar accidentes graves, como incendios en el caso de tuberías de combustible de polímero agrietadas y degradadas . El agrietamiento inducido por cloro de las juntas de tuberías de resina de acetal y las tuberías de polibutileno ha causado muchas inundaciones graves en propiedades domésticas, especialmente en los EE. UU. en la década de 1990. Los rastros de cloro en el suministro de agua atacaron los polímeros presentes en las tuberías, un problema que ocurre más rápido si alguna de las piezas ha sido mal extruida o moldeada por inyección . El ataque de la junta de acetal se produjo debido a un moldeo defectuoso, lo que provocó el agrietamiento a lo largo de las roscas del accesorio donde hay concentración de tensión .

La oxidación de polímeros ha causado accidentes relacionados con dispositivos médicos . Uno de los modos de falla más antiguos conocidos es el agrietamiento por ozono causado por la escisión de la cadena cuando el gas ozono ataca a elastómeros susceptibles , como el caucho natural y el caucho de nitrilo . Poseen enlaces dobles en sus unidades repetidas que se escinden durante la ozonólisis . Las grietas en las líneas de combustible pueden penetrar el orificio del tubo y causar fugas de combustible. Si el agrietamiento ocurre en el compartimiento del motor, las chispas eléctricas pueden encender la gasolina y causar un incendio grave. En el uso médico, la degradación de polímeros puede provocar cambios en las características físicas y químicas de los dispositivos implantables. [64]
El nailon 66 es susceptible a la hidrólisis ácida y, en un accidente, una tubería de combustible fracturada provocó un derrame de diésel en la carretera. Si el combustible diésel se derrama en la carretera, los vehículos que lo siguen pueden sufrir accidentes debido a la naturaleza resbaladiza del depósito, que es como el hielo negro . Además, la superficie de la carretera de hormigón asfáltico sufrirá daños como resultado de que el combustible diésel disuelva los asfaltenos del material compuesto, lo que provoca la degradación de la superficie del asfalto y la integridad estructural de la carretera.
Los polímeros han sido componentes esenciales de los productos básicos desde los primeros tiempos de la humanidad. El uso de lana ( queratina ), fibras de algodón y lino ( celulosa ) para prendas de vestir, y de juncos de papel ( celulosa ) para papel son sólo algunos ejemplos de cómo las sociedades antiguas explotaban las materias primas que contenían polímeros para obtener artefactos. La savia de látex de los árboles de "caucho" ( goma natural ) llegó a Europa en el siglo XVI desde América del Sur mucho después de que los olmecas , los mayas y los aztecas hubieran comenzado a utilizarla como material para hacer pelotas, textiles impermeables y recipientes. [65]
La manipulación química de los polímeros se remonta al siglo XIX, aunque en aquella época no se conocía la naturaleza de estas especies. El comportamiento de los polímeros se racionalizó inicialmente según la teoría propuesta por Thomas Graham , que los consideraba como agregados coloidales de pequeñas moléculas unidas por fuerzas desconocidas.
A pesar de la falta de conocimiento teórico, el potencial de los polímeros para proporcionar materiales innovadores, accesibles y baratos se comprendió inmediatamente. El trabajo realizado por Braconnot , Parkes , Ludersdorf, Hayward y muchos otros sobre la modificación de polímeros naturales determinó muchos avances significativos en el campo. [66] Sus contribuciones llevaron al descubrimiento de materiales como el celuloide , la galalita , la parkesina , el rayón , el caucho vulcanizado y, más tarde, la baquelita : todos materiales que entraron rápidamente en los procesos de fabricación industrial y llegaron a los hogares como componentes de prendas de vestir ( p. ej ., telas, botones), vajillas y artículos decorativos.
En 1920, Hermann Staudinger publicó su obra fundamental "Über Polymerisation", [67] en la que propuso que los polímeros eran en realidad largas cadenas de átomos unidos por enlaces covalentes. Su trabajo fue debatido extensamente, pero finalmente fue aceptado por la comunidad científica. Debido a este trabajo, Staudinger recibió el Premio Nobel en 1953. [68]
Después de la década de 1930, los polímeros entraron en una época dorada durante la cual se descubrieron nuevos tipos y rápidamente se les dieron aplicaciones comerciales, reemplazando a los materiales de origen natural. Este desarrollo fue impulsado por un sector industrial con un fuerte impulso económico y fue apoyado por una amplia comunidad académica que contribuyó con síntesis innovadoras de monómeros a partir de materias primas más baratas, procesos de polimerización más eficientes, técnicas mejoradas para la caracterización de polímeros y un conocimiento teórico avanzado de los polímeros. [66]

Desde 1953, se han concedido seis premios Nobel en el área de la ciencia de los polímeros, excluyendo los de investigación sobre macromoléculas biológicas . Esto es un testimonio más de su impacto en la ciencia y la tecnología modernas. Como resumió Lord Todd en 1980: "Me inclino a pensar que el desarrollo de la polimerización es quizás lo más importante que ha hecho la química, lo que ha tenido el mayor efecto en la vida cotidiana". [70]