El colesterol es el esterol principal de todos los animales superiores , distribuido en los tejidos corporales, especialmente en el cerebro y la médula espinal , y en las grasas y aceites animales . [3] [4]
El colesterol es biosintetizado por todas las células animales y es un componente estructural esencial de las membranas de las células animales . En los vertebrados , las células hepáticas suelen producir las mayores cantidades. En el cerebro los astrocitos producen colesterol y lo transportan a las neuronas. [5] Está ausente entre los procariotas ( bacterias y arqueas ), aunque hay algunas excepciones, como Mycoplasma , que requieren colesterol para crecer. [6] El colesterol también sirve como precursor para la biosíntesis de hormonas esteroides , ácidos biliares [7] y vitamina D.
Los niveles elevados de colesterol en la sangre, especialmente cuando está unido a lipoproteínas de baja densidad (LDL, a menudo denominadas "colesterol malo"), pueden aumentar el riesgo de enfermedad cardiovascular . [8]
François Poulletier de la Salle identificó por primera vez el colesterol en forma sólida en los cálculos biliares en 1769. En 1815, el químico Michel Eugène Chevreul denominó al compuesto "colesterina". [9] [10]
La palabra colesterol proviene del griego antiguo chole- 'bilis ' y stereos 'sólido', seguido del sufijo químico -ol para alcohol .
El colesterol es esencial para toda la vida animal. Si bien la mayoría de las células son capaces de sintetizarlo, la mayor parte del colesterol es ingerida o sintetizada por los hepatocitos y transportada en la sangre a las células periféricas. Los niveles de colesterol en los tejidos periféricos están dictados por un equilibrio entre la absorción y la exportación. [11] En condiciones normales, el colesterol cerebral está separado del colesterol periférico, es decir, el colesterol dietético y el hepático no cruzan la barrera hematoencefálica. Más bien, los astrocitos producen y distribuyen colesterol en el cerebro. [12]
La síntesis de novo, tanto en astrocitos como en hepatocitos, se produce mediante un proceso complejo de 37 pasos. Esto comienza con la vía del mevalonato o HMG-CoA reductasa , el objetivo de las estatinas , que engloba los primeros 18 pasos. A esto le siguen 19 pasos adicionales para convertir el lanosterol resultante en colesterol. [13] Un hombre humano que pesa 68 kg (150 lb) normalmente sintetiza alrededor de 1 gramo (1000 mg) de colesterol por día, y su cuerpo contiene alrededor de 35 g, la mayor parte dentro de las membranas celulares.
La ingesta diaria típica de colesterol para un hombre en los Estados Unidos es de 307 mg. [14] La mayor parte del colesterol ingerido está esterificado , lo que hace que el intestino lo absorba mal. El cuerpo también compensa la absorción del colesterol ingerido reduciendo su propia síntesis de colesterol. [15] Por estas razones, el colesterol en los alimentos, de siete a diez horas después de la ingestión, tiene poco o ningún efecto sobre las concentraciones de colesterol en la sangre. Sorprendentemente, en ratas, el colesterol en sangre está inversamente correlacionado con el consumo de colesterol. Cuanto más colesterol come una rata, más bajo es el colesterol en sangre. [16] Durante las primeras siete horas después de la ingestión de colesterol, a medida que las diversas lipoproteínas (que transportan todas las grasas en el agua fuera de las células) distribuyen las grasas absorbidas por el cuerpo dentro del agua extracelular, las concentraciones aumentan. [17]
Las plantas producen colesterol en cantidades muy pequeñas. [18] En mayores cantidades producen fitoesteroles , sustancias químicamente similares que pueden competir con el colesterol por la reabsorción en el tracto intestinal, reduciendo así potencialmente la reabsorción de colesterol. [19] Cuando las células del revestimiento intestinal absorben fitoesteroles, en lugar de colesterol, generalmente excretan las moléculas de fitoesteroles de regreso al tracto gastrointestinal , un importante mecanismo de protección. La ingesta de fitoesteroles naturales, que incluyen esteroles y estanoles vegetales , oscila entre ≈200 y 300 mg/día, dependiendo de los hábitos alimentarios. [20] Se han producido dietas experimentales vegetarianas especialmente diseñadas que producen más de 700 mg/día. [21]
El colesterol está presente en diversos grados en todas las membranas celulares animales , pero está ausente en los procariotas. [22] Es necesario para construir y mantener membranas y modular la fluidez de las membranas en el rango de temperaturas fisiológicas. El grupo hidroxilo de cada molécula de colesterol interactúa con las moléculas de agua que rodean la membrana, al igual que las cabezas polares de los fosfolípidos y esfingolípidos de la membrana , mientras que el esteroide voluminoso y la cadena de hidrocarburos están incrustados en la membrana, junto con la cadena de ácidos grasos no polares de la membrana. otros lípidos. A través de la interacción con las cadenas de fosfolípidos y ácidos grasos, el colesterol aumenta el empaquetamiento de la membrana, lo que altera la fluidez de la membrana [23] y mantiene la integridad de la membrana, de modo que las células animales no necesitan construir paredes celulares (como las plantas y la mayoría de las bacterias). La membrana permanece estable y duradera sin ser rígida, lo que permite que las células animales cambien de forma y que los animales se muevan.
La estructura del anillo tetracíclico del colesterol contribuye a la fluidez de la membrana celular, ya que la molécula está en una conformación trans , lo que hace que todas las cadenas del colesterol, excepto la lateral, sean rígidas y planas. [24] En esta función estructural, el colesterol también reduce la permeabilidad de la membrana plasmática a solutos neutros, [25] iones de hidrógeno e iones de sodio . [26]
El colesterol regula el proceso biológico de presentación de sustratos y las enzimas que utilizan la presentación de sustratos como mecanismo de su activación. La fosfolipasa D2 ( PLD2 ) es un ejemplo bien definido de una enzima activada por la presentación de sustrato. [27] La enzima está palmitoilada , lo que hace que la enzima se dirija a dominios lipídicos dependientes del colesterol, a veces llamados " balsas lipídicas ". El sustrato de la fosfolipasa D es la fosfatidilcolina (PC), que es insaturada y poco abundante en las balsas lipídicas. La PC se localiza en la región desordenada de la célula junto con el lípido poliinsaturado fosfatidilinositol 4,5-bisfosfato (PIP2). PLD2 tiene un dominio de unión PIP2 . Cuando aumenta la concentración de PIP2 en la membrana, PLD2 abandona los dominios dependientes del colesterol y se une a PIP2, donde luego obtiene acceso a su sustrato PC y comienza la catálisis basada en la presentación del sustrato.
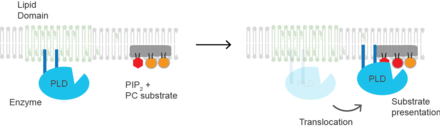
El colesterol también está implicado en los procesos de señalización celular, ayudando en la formación de balsas de lípidos en la membrana plasmática , lo que acerca las proteínas receptoras a altas concentraciones de moléculas de segundo mensajero. [28] En múltiples capas, el colesterol y los fosfolípidos, ambos aislantes eléctricos, pueden facilitar la velocidad de transmisión de los impulsos eléctricos a lo largo del tejido nervioso. Para muchas fibras neuronales, una vaina de mielina , rica en colesterol ya que se deriva de capas compactadas de células de Schwann o de membranas de oligodendrocitos, proporciona aislamiento para una conducción más eficiente de los impulsos. [29] Se cree que la desmielinización (pérdida de mielina) es parte de la base de la esclerosis múltiple .
El colesterol se une y afecta la activación de varios canales iónicos , como el receptor nicotínico de acetilcolina , el receptor GABA A y el canal rectificador interno de potasio . [30] El colesterol también activa el receptor alfa relacionado con el estrógeno (ERRα) y puede ser el ligando endógeno del receptor . [31] [32] La naturaleza constitutivamente activa del receptor puede explicarse por el hecho de que el colesterol está omnipresente en el cuerpo. [32] La inhibición de la señalización de ERRα mediante la reducción de la producción de colesterol se ha identificado como un mediador clave de los efectos de las estatinas y los bifosfonatos en los huesos , los músculos y los macrófagos . [31] [32] Sobre la base de estos hallazgos, se ha sugerido que el ERRα debería dejar de huérfano y clasificarse como un receptor del colesterol. [31] [32]
Dentro de las células, el colesterol también es una molécula precursora de varias vías bioquímicas . Por ejemplo, es la molécula precursora de la síntesis de vitamina D en el metabolismo del calcio y de todas las hormonas esteroides , incluidas las hormonas de la glándula suprarrenal cortisol y aldosterona , así como las hormonas sexuales progesterona , estrógenos y testosterona , y sus derivados. [7] [33]
El estrato córneo es la capa más externa de la epidermis. [34] [35] Está compuesto por corneocitos enucleados y diferenciados terminalmente que residen dentro de una matriz lipídica, como "ladrillos y mortero". [34] [35] Junto con las ceramidas y los ácidos grasos libres, el colesterol forma el mortero lipídico, una barrera impermeable al agua que previene la pérdida de agua por evaporación. Como regla general, la matriz lipídica epidérmica está compuesta por una mezcla equimolar de ceramidas (≈50% en peso), colesterol (≈25% en peso) y ácidos grasos libres (≈15% en peso), con cantidades más pequeñas. de que también estén presentes otros lípidos. [34] [35] El sulfato de colesterol alcanza su concentración más alta en la capa granular de la epidermis. La sulfatosulfatasa esteroide luego disminuye su concentración en el estrato córneo, la capa más externa de la epidermis. [36] La abundancia relativa de sulfato de colesterol en la epidermis varía según las diferentes partes del cuerpo y el talón del pie tiene la concentración más baja. [35]
El colesterol se recicla en el cuerpo. El hígado excreta colesterol en los líquidos biliares , que luego se almacenan en la vesícula biliar , que luego los excreta en forma no esterificada (a través de la bilis) hacia el tracto digestivo. Normalmente, alrededor del 50% del colesterol excretado se reabsorbe en el intestino delgado y regresa al torrente sanguíneo.
Casi todos los tejidos animales sintetizan colesterol a partir de acetil-CoA . Todas las células animales (existen excepciones dentro de los invertebrados) fabrican colesterol, tanto para la estructura de la membrana como para otros usos, con tasas de producción relativas que varían según el tipo de célula y la función del órgano. Alrededor del 80% de la producción diaria total de colesterol se produce en el hígado y los intestinos ; [37] Otros sitios de tasas de síntesis más altas incluyen el cerebro , las glándulas suprarrenales y los órganos reproductivos .
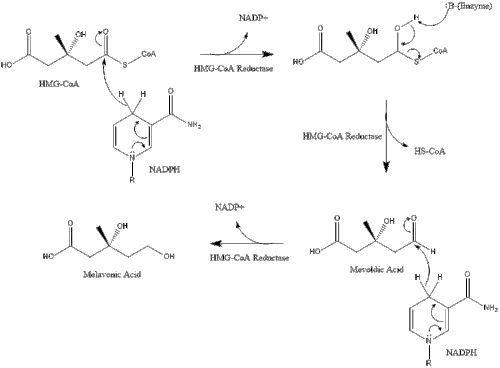
La síntesis dentro del cuerpo comienza con la vía del mevalonato , donde dos moléculas de acetil CoA se condensan para formar acetoacetil-CoA . A esto le sigue una segunda condensación entre acetil CoA y acetoacetil-CoA para formar 3-hidroxi-3-metilglutaril CoA ( HMG-CoA ). [38]

Luego, esta molécula se reduce a mevalonato mediante la enzima HMG-CoA reductasa . La producción de mevalonato es el paso irreversible y limitante de la velocidad de la síntesis de colesterol y es el lugar de acción de las estatinas (una clase de fármacos para reducir el colesterol).
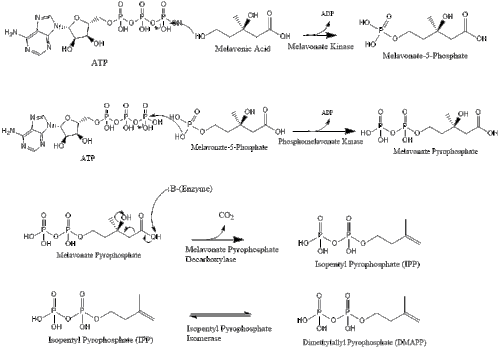
El mevalonato finalmente se convierte en pirofosfato de isopentenilo (IPP) mediante dos pasos de fosforilación y un paso de descarboxilación que requiere ATP .
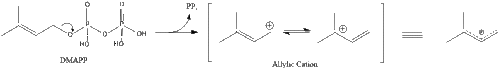
Tres moléculas de pirofosfato de isopentenilo se condensan para formar pirofosfato de farnesilo mediante la acción de la geranil transferasa.

Luego, dos moléculas de pirofosfato de farnesilo se condensan para formar escualeno por la acción de la escualeno sintasa en el retículo endoplásmico . [38]
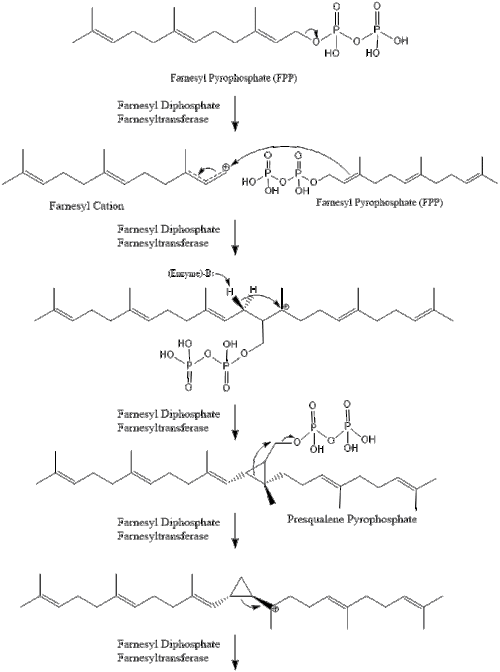
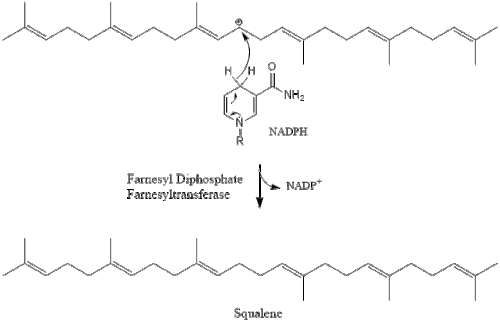
La oxidascualeno ciclasa luego cicla el escualeno para formar lanosterol .
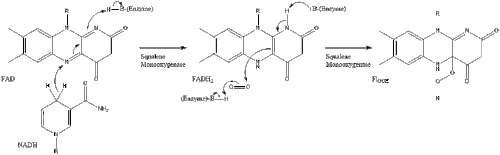
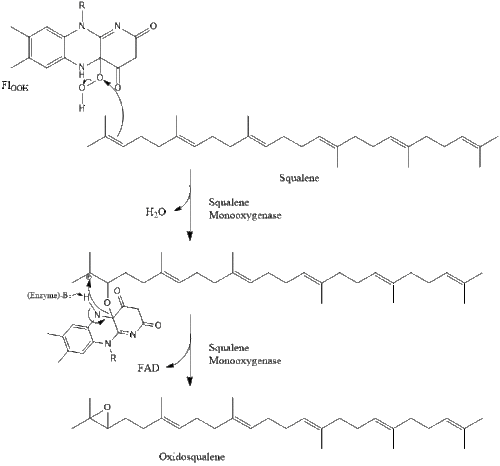
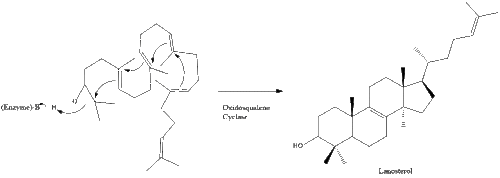
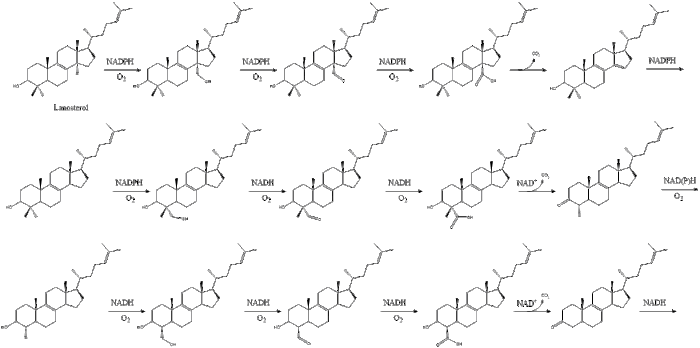
Finalmente, el lanosterol se convierte en colesterol mediante cualquiera de dos vías: la vía de Bloch o la vía de Kandutsch-Russell. [39] [40] [41] [42] [43] Los 19 pasos finales para el colesterol contienen NADPH y oxígeno para ayudar a oxidar los grupos metilo para la eliminación de carbonos, mutasas para mover los grupos alquenos y NADH para ayudar a reducir las cetonas .

Konrad Bloch y Feodor Lynen compartieron el Premio Nobel de Fisiología o Medicina en 1964 por sus descubrimientos sobre algunos de los mecanismos y métodos de regulación del colesterol y del metabolismo de los ácidos grasos . [44]
La biosíntesis del colesterol está regulada directamente por los niveles de colesterol presentes, aunque los mecanismos homeostáticos implicados sólo se conocen parcialmente. Una mayor ingesta de alimentos conduce a una disminución neta de la producción endógena, mientras que una menor ingesta de alimentos tiene el efecto contrario. El principal mecanismo regulador es la detección del colesterol intracelular en el retículo endoplasmático por la proteína SREBP (proteína 1 y 2 de unión a elementos reguladores de esteroles). [45] En presencia de colesterol, SREBP está unida a otras dos proteínas: SCAP (proteína activadora de escisión de SREBP) e INSIG-1 . Cuando los niveles de colesterol caen, INSIG-1 se disocia del complejo SREBP-SCAP, lo que permite que el complejo migre al aparato de Golgi . Aquí, SREBP es escindida por S1P y S2P (proteasa del sitio 1 y proteasa del sitio 2), dos enzimas que se activan mediante SCAP cuando los niveles de colesterol son bajos.
La SREBP escindida luego migra al núcleo y actúa como factor de transcripción para unirse al elemento regulador de esteroles (SRE), que estimula la transcripción de muchos genes. Entre ellos se encuentran el receptor de lipoproteínas de baja densidad ( LDL ) y la HMG-CoA reductasa . El receptor de LDL elimina la LDL circulante del torrente sanguíneo, mientras que la HMG-CoA reductasa conduce a un aumento en la producción endógena de colesterol. [46] Una gran parte de esta vía de señalización fue aclarada por el Dr. Michael S. Brown y el Dr. Joseph L. Goldstein en la década de 1970. En 1985 recibieron el Premio Nobel de Fisiología o Medicina por su trabajo. Su trabajo posterior muestra cómo la vía SREBP regula la expresión de muchos genes que controlan la formación y el metabolismo de lípidos y la asignación de combustible corporal.
La síntesis de colesterol también puede interrumpirse cuando los niveles de colesterol son altos. La HMG-CoA reductasa contiene un dominio citosólico (responsable de su función catalítica) y un dominio de membrana. El dominio de membrana detecta señales de su degradación. Las concentraciones crecientes de colesterol (y otros esteroles) provocan un cambio en el estado de oligomerización de este dominio, lo que lo hace más susceptible a la destrucción por parte del proteosoma . La actividad de esta enzima también puede reducirse mediante la fosforilación mediante una proteína quinasa activada por AMP . Debido a que esta quinasa es activada por el AMP, que se produce cuando se hidroliza el ATP, se deduce que la síntesis de colesterol se detiene cuando los niveles de ATP son bajos. [47]

Como molécula aislada, el colesterol es mínimamente soluble en agua o hidrófilo . Debido a esto, se disuelve en la sangre en concentraciones extremadamente pequeñas. Para ser transportado eficazmente, el colesterol se empaqueta dentro de lipoproteínas , partículas discoidales complejas con proteínas y lípidos anfifílicos exteriores , cuyas superficies exteriores son solubles en agua y las superficies interiores son lípidos solubles. Esto le permite viajar a través de la sangre mediante emulsificación . El colesterol libre, al ser anfipático, se transporta en la superficie monocapa de la partícula lipoproteica junto con los fosfolípidos y las proteínas. Los ésteres de colesterol unidos a ácidos grasos, por otro lado, se transportan dentro del núcleo graso hidrofóbico de la lipoproteína, junto con los triglicéridos. [48]
Hay varios tipos de lipoproteínas en la sangre. En orden creciente de densidad, son quilomicrones , lipoproteínas de muy baja densidad (VLDL), lipoproteínas de densidad intermedia (IDL), lipoproteínas de baja densidad (LDL) y lipoproteínas de alta densidad (HDL). Las proporciones más bajas de proteínas/lípidos producen lipoproteínas menos densas. El colesterol dentro de diferentes lipoproteínas es idéntico, aunque algunos se transportan como su forma nativa de alcohol "libre" (el grupo colesterol-OH frente al agua que rodea las partículas), mientras que otros como ésteres de acilo graso, conocidos también como ésteres de colesterol, dentro de las partículas. [48]
Las partículas de lipoproteínas están organizadas por apolipoproteínas complejas , típicamente de 80 a 100 proteínas diferentes por partícula, que pueden ser reconocidas y unidas por receptores específicos en las membranas celulares, dirigiendo su carga lipídica a células y tejidos específicos que actualmente ingieren estas partículas de transporte de grasa. Estos receptores de superficie sirven como firmas moleculares únicas, que luego ayudan a determinar la distribución de la grasa en todo el cuerpo. [48]
Los quilomicrones, las partículas transportadoras de colesterol menos densas, contienen apolipoproteína B-48 , apolipoproteína C y apolipoproteína E (el principal transportador de colesterol en el cerebro [49] ) en sus cáscaras. Los quilomicrones transportan grasas desde el intestino hasta los músculos y otros tejidos que necesitan ácidos grasos para obtener energía o producir grasa. El colesterol no utilizado permanece en restos de quilomicrones más ricos en colesterol y desde allí es transportado al torrente sanguíneo por el hígado. [48]
Las partículas de VLDL son producidas por el hígado a partir de triacilglicerol y colesterol que no se utilizan en la síntesis de ácidos biliares. Estas partículas contienen apolipoproteína B100 y apolipoproteína E en sus cubiertas y pueden ser degradadas por la lipoproteína lipasa en la pared arterial a IDL. Esta escisión de la pared arterial permite la absorción de triacilglicerol y aumenta la concentración de colesterol circulante. Luego, las partículas de IDL se consumen en dos procesos: la mitad es metabolizada por HTGL y absorbida por el receptor de LDL en las superficies de las células del hígado, mientras que la otra mitad continúa perdiendo triacilgliceroles en el torrente sanguíneo hasta que se convierten en partículas de LDL cargadas de colesterol. [48]
Las partículas de LDL son los principales portadores de colesterol en sangre. Cada uno contiene aproximadamente 1.500 moléculas de éster de colesterol. Las capas de partículas de LDL contienen solo una molécula de apolipoproteína B100 , reconocida por los receptores de LDL en los tejidos periféricos. Tras la unión de la apolipoproteína B100 , muchos receptores de LDL se concentran en fosas recubiertas de clatrina . Tanto el LDL como su receptor forman vesículas dentro de una célula mediante endocitosis . Estas vesículas luego se fusionan con un lisosoma , donde la enzima lipasa ácida lisosomal hidroliza los ésteres de colesterol. Luego, el colesterol puede usarse para la biosíntesis de la membrana o esterificarse y almacenarse dentro de la célula, para no interferir con las membranas celulares. [48]
Los receptores de LDL se agotan durante la absorción del colesterol, y su síntesis está regulada por la SREBP , la misma proteína que controla la síntesis de colesterol de novo , según su presencia en el interior de la célula. Una célula con abundante colesterol verá bloqueada la síntesis del receptor de LDL, para evitar que se absorba nuevo colesterol en las partículas de LDL. Por el contrario, la síntesis del receptor de LDL se produce cuando una célula tiene deficiencia de colesterol. [48]
Cuando este proceso se desregula, comienzan a aparecer partículas de LDL sin receptores en la sangre. Estas partículas de LDL son oxidadas y absorbidas por los macrófagos , que se hinchan y forman células espumosas. Estas células espumosas a menudo quedan atrapadas en las paredes de los vasos sanguíneos y contribuyen a la formación de placa aterosclerótica . Las diferencias en la homeostasis del colesterol afectan el desarrollo de la aterosclerosis temprana (grosor de la íntima-media carotídea). [50] Estas placas son las principales causas de ataques cardíacos, accidentes cerebrovasculares y otros problemas médicos graves, lo que lleva a la asociación del llamado colesterol LDL (en realidad una lipoproteína ) con el colesterol "malo". [47]
Se cree que las partículas HDL transportan el colesterol de regreso al hígado, ya sea para su excreción o para otros tejidos que sintetizan hormonas, en un proceso conocido como transporte inverso de colesterol (RCT). [51] Un gran número de partículas de HDL se correlaciona con mejores resultados de salud, [52] mientras que un número bajo de partículas de HDL se asocia con la progresión de la enfermedad ateromatosa en las arterias. [53]
El colesterol es susceptible a la oxidación y forma fácilmente derivados oxigenados llamados oxiesteroles . Tres mecanismos diferentes pueden formar estos: autooxidación, oxidación secundaria a peroxidación lipídica y oxidación de enzimas que metabolizan el colesterol. Surgió un gran interés en los oxiesteroles cuando se demostró que ejercían acciones inhibidoras sobre la biosíntesis del colesterol. [54] Este hallazgo se conoció como la "hipótesis del oxisterol". Las funciones adicionales de los oxiesteroles en la fisiología humana incluyen su participación en la biosíntesis de ácidos biliares, su función como formas de transporte de colesterol y la regulación de la transcripción genética. [55]
En experimentos bioquímicos se utilizan formas de colesterol radiomarcadas, como el colesterol tritiado. Estos derivados se degradan durante el almacenamiento y es esencial purificar el colesterol antes de su uso. El colesterol se puede purificar utilizando pequeñas columnas Sephadex LH-20. [56]
El hígado oxida el colesterol en una variedad de ácidos biliares . [57] Estos, a su vez, están conjugados con glicina , taurina , ácido glucurónico o sulfato . Una mezcla de ácidos biliares conjugados y no conjugados, junto con el propio colesterol, se excreta del hígado a la bilis . Aproximadamente el 95% de los ácidos biliares se reabsorben en los intestinos y el resto se pierde en las heces. [58] La excreción y reabsorción de ácidos biliares forma la base de la circulación enterohepática , que es esencial para la digestión y absorción de las grasas dietéticas. En determinadas circunstancias, cuando está más concentrado, como en la vesícula biliar , el colesterol cristaliza y es el componente principal de la mayoría de los cálculos biliares ( también se producen cálculos de lecitina y bilirrubina , pero con menos frecuencia). [59] Cada día, hasta 1 g de colesterol ingresa al colon. Este colesterol se origina en la dieta, la bilis y las células intestinales descamadas y puede ser metabolizado por las bacterias del colon. El colesterol se convierte principalmente en coprostanol , un esterol no absorbible que se excreta en las heces. [ cita necesaria ]
Aunque el colesterol es un esteroide generalmente asociado a los mamíferos, el patógeno humano Mycobacterium tuberculosis es capaz de degradar completamente esta molécula y contiene una gran cantidad de genes que están regulados por su presencia. [60] Muchos de estos genes regulados por el colesterol son homólogos de genes de β-oxidación de ácidos grasos , pero han evolucionado de tal manera que se unen a grandes sustratos esteroides como el colesterol. [61] [62]
Las grasas animales son mezclas complejas de triglicéridos , con cantidades menores de fosfolípidos y moléculas de colesterol a partir de las cuales se construyen todas las membranas celulares animales (y humanas). Dado que todas las células animales fabrican colesterol, todos los alimentos de origen animal contienen colesterol en cantidades variables. [63] Las principales fuentes dietéticas de colesterol incluyen carnes rojas , yemas de huevo y huevos enteros , hígado , riñones , menudencias , aceite de pescado y mantequilla . [64] La leche materna humana también contiene cantidades significativas de colesterol. [sesenta y cinco]
Las células vegetales sintetizan colesterol como precursor de otros compuestos, como los fitoesteroles y los glicoalcaloides esteroides , y el colesterol permanece en los alimentos vegetales sólo en cantidades menores o ausente. [64] [66] Algunos alimentos vegetales, como el aguacate , las semillas de lino y el maní , contienen fitoesteroles, que compiten con el colesterol por la absorción en los intestinos y reducen la absorción del colesterol dietético y biliar. [67] Una dieta típica aporta del orden de 0,2 gramos de fitoesteroles, lo que no es suficiente para tener un impacto significativo en el bloqueo de la absorción de colesterol. La ingesta de fitoesteroles se puede complementar mediante el uso de alimentos funcionales que contengan fitosterol o suplementos dietéticos que se reconozca que tienen potencial para reducir los niveles de colesterol LDL . [68]
En 2015, el panel científico asesor del Departamento de Salud y Servicios Humanos de EE. UU . y del Departamento de Agricultura de EE. UU. para la versión de 2015 de las Guías Alimentarias para los Estadounidenses redujo el límite de consumo de colesterol dietético previamente recomendado a 300 mg por día con una nueva recomendación de "comer la menor cantidad posible de colesterol en la dieta" y reconocer una asociación entre una dieta baja en colesterol y un riesgo reducido de enfermedad cardiovascular. [69]
Un informe de 2013 de la Asociación Estadounidense del Corazón y el Colegio Estadounidense de Cardiología recomendó centrarse en patrones dietéticos saludables en lugar de límites específicos de colesterol, ya que son difíciles de implementar para los médicos y consumidores. Recomiendan la dieta DASH y la mediterránea , que son bajas en colesterol. [70] Una revisión de 2017 realizada por la Asociación Estadounidense del Corazón recomienda cambiar las grasas saturadas por grasas poliinsaturadas para reducir el riesgo de enfermedad cardiovascular . [71]
Algunas pautas complementarias han recomendado dosis de fitoesteroles en el rango de 1,6 a 3,0 gramos por día (Health Canada, EFSA, ATP III, FDA). Un metanálisis demostró una reducción del 12% en el colesterol LDL con una dosis media de 2,1 gramos por día. [72] También se han cuestionado los beneficios de una dieta suplementada con fitoesteroles. [73]

Según la hipótesis de los lípidos , los niveles elevados de colesterol en la sangre provocan aterosclerosis , lo que puede aumentar el riesgo de ataque cardíaco , accidente cerebrovascular y enfermedad arterial periférica . Dado que las concentraciones más altas de LDL en sangre (especialmente las concentraciones más altas de LDL y el tamaño más pequeño de las partículas de LDL) contribuyen a este proceso más que el contenido de colesterol de las partículas de HDL, [8] las partículas de LDL a menudo se denominan "colesterol malo". Las altas concentraciones de HDL funcional, que pueden eliminar el colesterol de las células y los ateromas, ofrecen protección y comúnmente se denominan "colesterol bueno". Estos equilibrios están determinados principalmente genéticamente, pero pueden modificarse mediante la composición corporal, los medicamentos , la dieta [74] y otros factores. [75] Un estudio de 2007 demostró que los niveles de colesterol total en sangre tienen un efecto exponencial sobre la mortalidad cardiovascular y total, siendo la asociación más pronunciada en sujetos más jóvenes. Debido a que las enfermedades cardiovasculares son relativamente raras en la población más joven, el impacto del colesterol alto en la salud es mayor en las personas mayores. [76]
Los niveles elevados de las fracciones de lipoproteínas LDL, IDL y VLDL, más que el nivel de colesterol total, se correlacionan con la extensión y el progreso de la aterosclerosis. [77] Por el contrario, el colesterol total puede estar dentro de los límites normales, pero estar formado principalmente por pequeñas partículas de LDL y HDL, en cuyas condiciones las tasas de crecimiento del ateroma son altas. Un análisis post hoc de los estudios prospectivos IDEAL y EPIC encontró una asociación entre niveles elevados de colesterol HDL (ajustado por apolipoproteína AI y apolipoproteína B) y un mayor riesgo de enfermedad cardiovascular, lo que pone en duda el papel cardioprotector del "colesterol bueno". [78] [79]
Aproximadamente una de cada 250 personas puede tener una mutación genética en el receptor de colesterol LDL que les provoca hipercolesterolemia familiar. [80] El colesterol alto hereditario también puede incluir mutaciones genéticas en el gen PCSK9 y el gen de la apolipoproteína B. [81]
Los niveles elevados de colesterol se pueden tratar con una dieta que reduzca o elimine las grasas saturadas, las grasas trans y los alimentos con alto contenido de colesterol, [82] [83] seguida a menudo por uno de varios agentes hipolipidémicos , como estatinas , fibratos , inhibidores de la absorción de colesterol, anticuerpos monoclonales. terapia ( inhibidores de PCSK9 ), derivados del ácido nicotínico o secuestradores de ácidos biliares. [84] Existen varias directrices internacionales sobre el tratamiento de la hipercolesterolemia. [85]
Los ensayos en humanos que utilizan inhibidores de la HMG-CoA reductasa , conocidos como estatinas , han confirmado repetidamente que cambiar los patrones de transporte de lipoproteínas de patrones poco saludables a patrones más saludables reduce significativamente las tasas de eventos de enfermedades cardiovasculares, incluso para personas con valores de colesterol actualmente considerados bajos para los adultos. [86] Los estudios han demostrado que reducir los niveles de colesterol LDL en aproximadamente 38,7 mg/dL con el uso de estatinas puede reducir el riesgo de enfermedad cardiovascular y accidente cerebrovascular en aproximadamente un 21 %. [87] Los estudios también han encontrado que las estatinas reducen la progresión del ateroma. [88] Como resultado, las personas con antecedentes de enfermedad cardiovascular pueden beneficiarse de las estatinas independientemente de sus niveles de colesterol (colesterol total inferior a 5,0 mmol/L [193 mg/dL]), [89] y en hombres sin enfermedad cardiovascular, Hay beneficios al reducir los niveles anormalmente altos de colesterol ("prevención primaria"). [90] La prevención primaria en mujeres se practicaba originalmente solo como extensión de los hallazgos de los estudios en hombres, [91] ya que, en mujeres, ninguno de los grandes ensayos con estatinas realizados antes de 2007 demostró una reducción significativa en la mortalidad general o en los criterios de valoración cardiovasculares. . [92] Los metanálisis han demostrado reducciones significativas en la mortalidad cardiovascular y por todas las causas, sin heterogeneidad significativa por sexo. [93]
El informe de 1987 del Programa Nacional de Educación sobre el Colesterol , Paneles de Tratamiento de Adultos sugiere que el nivel de colesterol total en sangre debe ser: < 200 mg/dL de colesterol en sangre normal, 200 a 239 mg/dL en el límite alto, > 240 mg/dL de colesterol alto. [94] La Asociación Estadounidense del Corazón proporciona un conjunto similar de pautas para los niveles de colesterol total (en ayunas) en sangre y el riesgo de enfermedad cardíaca: [82] Las estatinas son efectivas para reducir el colesterol LDL y se usan ampliamente para la prevención primaria en personas con alto riesgo de enfermedad cardiovascular. enfermedad, así como en prevención secundaria para quienes han desarrollado enfermedad cardiovascular. [95]
Los métodos de prueba más actuales determinan el colesterol LDL ("malo") y HDL ("bueno") por separado, lo que permite que el análisis del colesterol sea más matizado. Se considera que el nivel deseable de LDL es inferior a 100 mg/dL (2,6 mmol /L). [96] [97]

El colesterol total se define como la suma de HDL, LDL y VLDL. Por lo general, sólo se miden el total, el HDL y los triglicéridos. Por razones de costo, el VLDL generalmente se estima como una quinta parte de los triglicéridos y el LDL se estima usando la fórmula de Friedewald (o una variante ): LDL estimado = [colesterol total] − [HDL total] − [VLDL estimado]. Las medidas directas de LDL se utilizan cuando los triglicéridos superan los 400 mg/dL. Las VLDL y LDL estimadas tienen más error cuando los triglicéridos están por encima de 400 mg/dL. [98]
En el Framingham Heart Study , cada aumento de 10 mg/dL (0,6 mmol /L) en los niveles de colesterol total aumentó la mortalidad general a 30 años en un 5 % y la mortalidad por enfermedades cardiovasculares en un 9 %. Mientras que los sujetos mayores de 50 años tuvieron un aumento del 11 % en la mortalidad general y un aumento del 14 % en la mortalidad por enfermedades cardiovasculares por cada caída de 1 mg/dL (0,06 mmol /L) al año en los niveles de colesterol total. Los investigadores atribuyeron este fenómeno a una correlación diferente , según la cual la enfermedad en sí aumenta el riesgo de muerte, además de cambiar una multitud de factores, como la pérdida de peso y la incapacidad para comer, que reducen el colesterol sérico. [99] Este efecto también se demostró en hombres de todas las edades y mujeres mayores de 50 años en el Programa de Promoción y Vigilancia de la Salud de Vorarlberg. Estos grupos tenían más probabilidades de morir de cáncer, enfermedades hepáticas y enfermedades mentales con un colesterol total muy bajo, de 186 mg/dL (10,3 mmol /L) o menos. Este resultado indica que el efecto del colesterol bajo ocurre incluso entre los encuestados más jóvenes, lo que contradice la evaluación previa entre cohortes de personas mayores de que esto es un marcador de fragilidad que ocurre con la edad. [100]
Los niveles anormalmente bajos de colesterol se denominan hipocolesterolemia . La investigación sobre las causas de este estado es relativamente limitada, pero algunos estudios sugieren un vínculo con la depresión , el cáncer y la hemorragia cerebral . En general, los niveles bajos de colesterol parecen ser una consecuencia, más que una causa, de una enfermedad subyacente. [76] Un defecto genético en la síntesis de colesterol causa el síndrome de Smith-Lemli-Opitz , que a menudo se asocia con niveles bajos de colesterol plasmático. El hipertiroidismo o cualquier otro trastorno endocrino que provoque una regulación positiva del receptor de LDL puede provocar hipocolesterolemia. [101]
La Asociación Estadounidense del Corazón recomienda realizar pruebas de colesterol cada 4 a 6 años en personas de 20 años o más. [102] Un conjunto separado de pautas de la Asociación Estadounidense del Corazón publicadas en 2013 indica que las personas que toman estatinas deben hacerse una prueba de colesterol entre 4 y 12 semanas después de la primera dosis y luego cada 3 a 12 meses. [103] [104] Para los hombres de 45 a 65 años y las mujeres de 55 a 65 años, se debe realizar una prueba de colesterol cada 1 a 2 años, y para las personas mayores de 65 años, se debe realizar una prueba anual. [103]
Un profesional de la salud toma una muestra de sangre después de 12 horas de ayuno de una vena del brazo para medir el perfil lipídico de a) colesterol total, b) colesterol HDL, c) colesterol LDL y d) triglicéridos . [3] [103] Los resultados pueden expresarse como "calculados", lo que indica un cálculo del colesterol total, HDL y triglicéridos. [3]
El colesterol se analiza para determinar niveles "normales" o "deseables" si una persona tiene un colesterol total de 5,2 mmol/L o menos (200 mg/dL), un valor de HDL de más de 1 mmol/L (40 mg/dL , "cuanto más alto, mejor"), un valor de LDL inferior a 2,6 mmol/L (100 mg/dL) y un nivel de triglicéridos inferior a 1,7 mmol/L (150 mg/dL). [103] [3] El colesterol en sangre en personas con estilo de vida, envejecimiento o factores de riesgo cardiovascular, como diabetes mellitus , hipertensión , antecedentes familiares de enfermedad arterial coronaria o angina , se evalúan en diferentes niveles. [103]
Haga clic en genes, proteínas y metabolitos a continuación para vincular a los artículos respectivos. [§ 1]
Se sabe que algunos derivados del colesterol (entre otros lípidos colestéricos simples) generan la "fase colestérica" líquida cristalina . La fase colestérica es, en realidad, una fase nemática quiral , y cambia de color cuando cambia su temperatura. Esto hace que los derivados del colesterol sean útiles para indicar la temperatura en termómetros con pantalla de cristal líquido y en pinturas sensibles a la temperatura. [ cita necesaria ]
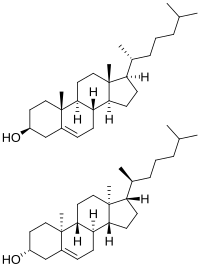
El colesterol tiene 256 estereoisómeros que surgen de sus ocho estereocentros, aunque sólo dos de los estereoisómeros tienen importancia bioquímica ( colesterol nat y colesterol ent , para natural y enantiómero , respectivamente), [105] [106] y sólo uno se produce de forma natural ( nat) . -colesterol).
Je nommerai
cholesterine
, de χολη, bilis, et στερεος, solide, la sustancia cristallisée des calculs biliares humains, ...[Nombraré colesterina – de χολη (bilis) y στερεος (sólido) – la sustancia cristalizada de los cálculos biliares humanos.. .]