
El carbonato de calcio es un compuesto químico con la fórmula química Ca CO 3 . Es una sustancia común que se encuentra en rocas como los minerales calcita y aragonito , sobre todo en tiza y piedra caliza , cáscaras de huevo , caparazones de gasterópodos , esqueletos de mariscos y perlas . Los materiales que contienen mucho carbonato de calcio o se parecen a él se describen como calcáreos . El carbonato de calcio es el ingrediente activo de la cal agrícola y se produce cuando los iones de calcio en el agua dura reaccionan con los iones de carbonato para formar cal . Tiene uso médico como suplemento de calcio o como antiácido , pero su consumo excesivo puede ser peligroso y provocar hipercalcemia y problemas digestivos. [8]
El carbonato de calcio comparte las propiedades típicas de otros carbonatos . En particular,
El carbonato de calcio reacciona con agua saturada con dióxido de carbono para formar bicarbonato de calcio soluble .
Esta reacción es importante en la erosión de las rocas carbonatadas , formando cavernas , y conduce a la formación de agua dura en muchas regiones.
Una forma inusual de carbonato de calcio es la ikaita hexahidratada , CaCO 3 ·6H 2 O. Ikaite es estable sólo por debajo de 8 °C.
La gran mayoría del carbonato de calcio utilizado en la industria se extrae mediante minas o canteras. El carbonato de calcio puro (como el de uso alimentario o farmacéutico) se puede producir a partir de una fuente pura de cantera (normalmente mármol ).
Alternativamente, el carbonato de calcio se prepara a partir de óxido de calcio . Se agrega agua para obtener hidróxido de calcio y luego se pasa dióxido de carbono a través de esta solución para precipitar el carbonato de calcio deseado, denominado en la industria carbonato de calcio precipitado (PCC). Este proceso se llama carbonatación : [9]
En un laboratorio, el carbonato de calcio se puede cristalizar fácilmente a partir de cloruro de calcio ( CaCl 2 ), colocando una solución acuosa de CaCl 2 en un desecador junto con carbonato de amonio [NH 4 ] 2 CO 3 . [10] En el desecador, el carbonato de amonio se expone al aire y se descompone en amoníaco , dióxido de carbono y agua . Luego, el dióxido de carbono se difunde en la solución acuosa de cloruro de calcio, reacciona con los iones de calcio y el agua y forma carbonato de calcio.
La forma termodinámicamente estable del CaCO 3 en condiciones normales es la β- CaCO 3 hexagonal (el mineral calcita ). Se pueden preparar otras formas, la más densa (2,83 g/cm 3 ) λ- CaCO3 ortorrómbica ( el mineral aragonito ) y la μ-CaCO3 hexagonal , que se presenta como el mineral vaterita . La forma de aragonita se puede preparar mediante precipitación a temperaturas superiores a 85 °C; la forma vaterita se puede preparar por precipitación a 60 °C. La calcita contiene átomos de calcio coordinados por seis átomos de oxígeno; en aragonito están coordinados por nueve átomos de oxígeno. [ cita necesaria ] La estructura de vaterita no se comprende completamente. [11] El carbonato de magnesio ( MgCO 3 ) tiene la estructura de calcita, mientras que el carbonato de estroncio ( SrCO 3 ) y el carbonato de bario ( BaCO 3 ) adoptan la estructura de aragonito, reflejando sus radios iónicos más grandes . [ cita necesaria ]
El carbonato de calcio cristaliza en tres polimorfos anhidros , [12] [13] de los cuales la calcita es la termodinámicamente más estable a temperatura ambiente, la aragonita lo es sólo un poco menos y la vaterita es la menos estable. [14]
La estructura cristalina de calcita es trigonal , con grupo espacial R 3 c (No. 167 en las Tablas Internacionales de Cristalografía [15] ) y símbolo de Pearson hR10. [16] La aragonita es ortorrómbica , con el grupo espacial Pmcn (No 62) y el símbolo de Pearson oP20. [17] La vaterita se compone de al menos dos estructuras cristalográficas coexistentes diferentes. La estructura principal exhibe simetría hexagonal en el grupo espacial P6 3 /mmc; la estructura menor aún se desconoce. [18]

Los tres polimorfos cristalizan simultáneamente en soluciones acuosas en condiciones ambientales. [14] En soluciones acuosas sin aditivos, la calcita se forma fácilmente como producto principal, mientras que la aragonita aparece sólo como un producto secundario.
En condiciones de alta saturación, la vaterita suele ser la primera fase precipitada, a la que sigue una transformación de la vaterita en calcita. [19] Este comportamiento parece seguir la regla de Ostwald , en la que el polimorfo menos estable cristaliza primero, seguido de la cristalización de diferentes polimorfos a través de una secuencia de fases cada vez más estables. [20] Sin embargo, la aragonita, cuya estabilidad se encuentra entre las de la vaterita y la calcita, parece ser la excepción a esta regla, ya que la aragonita no se forma como precursor de la calcita en condiciones ambientales. [14]

La aragonita se produce en su mayoría cuando las condiciones de reacción inhiben la formación de calcita y/o promueven la nucleación de aragonita. Por ejemplo, la formación de aragonito se promueve mediante la presencia de iones de magnesio [21] o mediante el uso de proteínas y péptidos derivados del carbonato de calcio biológico. [22] Se ha demostrado que algunas poliaminas como la cadaverina y la polietilenimina facilitan la formación de aragonita sobre calcita. [14]
Organismos, como moluscos y artrópodos , han demostrado la capacidad de desarrollar los tres polimorfos cristalinos de carbonato de calcio, principalmente como protección (conchas) y uniones musculares. [23] Además, exhiben una notable capacidad de selección de fase sobre calcita y aragonito, y algunos organismos pueden cambiar entre los dos polimorfos. La capacidad de selección de fase generalmente se atribuye al uso de macromoléculas específicas o combinaciones de macromoléculas por parte de dichos organismos. [24] [25] [26]

La calcita , la aragonita y la vaterita son minerales de carbonato de calcio puro. Las rocas generadoras de importancia industrial, que son predominantemente carbonato de calcio, incluyen piedra caliza , creta , mármol y travertino .

Las cáscaras de huevo , las de caracol y la mayoría de las conchas marinas son predominantemente carbonato de calcio y pueden usarse como fuentes industriales de esa sustancia química. [28] Las conchas de ostra han gozado de reconocimiento reciente como fuente de calcio dietético, pero también son una fuente industrial práctica. [29] [30] Las verduras de color verde oscuro , como el brócoli y la col rizada, contienen cantidades significativas de carbonato de calcio en la dieta, pero no son prácticas como fuente industrial. [31]
Los anélidos de la familia Lumbricidae , las lombrices de tierra, poseen una regionalización del tracto digestivo llamada glándulas calcíferas, Kalkdrüsen o glandes de Morren, que procesan el calcio y el CO 2 en carbonato de calcio, que luego se excreta en la tierra. [32] Se desconoce la función de estas glándulas, pero se cree que sirven como mecanismo de regulación del CO 2 dentro de los tejidos de los animales. [33] Este proceso es ecológicamente significativo, ya que estabiliza el pH de los suelos ácidos . [34]
Más allá de la Tierra, hay pruebas contundentes que sugieren la presencia de carbonato de calcio en Marte . Se han detectado signos de carbonato de calcio en más de un lugar (especialmente en los cráteres Gusev y Huygens ). Esto proporciona alguna evidencia de la presencia pasada de agua líquida. [35] [36]

El carbonato se encuentra con frecuencia en entornos geológicos y constituye una enorme reserva de carbono . El carbonato de calcio se presenta como aragonito , calcita y dolomita como constituyentes importantes del ciclo del calcio . Los minerales carbonatados forman los tipos de rocas: caliza , creta , mármol , travertino , toba y otras.

En las aguas tropicales cálidas y claras los corales son más abundantes que hacia los polos donde las aguas son frías. Los contribuyentes de carbonato de calcio, incluido el plancton (como los cocolitos y los foraminíferos planctónicos ), las algas coralinas , las esponjas , los braquiópodos , los equinodermos , los briozoos y los moluscos , se encuentran típicamente en ambientes de aguas poco profundas donde la luz solar y los alimentos filtrables son más abundantes. Los carbonatos de agua fría existen en latitudes más altas, pero tienen una tasa de crecimiento muy lenta. Los procesos de calcificación se ven alterados por la acidificación de los océanos .
Cuando la corteza oceánica se subduce bajo una placa continental, los sedimentos serán arrastrados hacia zonas más cálidas en la astenosfera y la litosfera . En estas condiciones el carbonato de calcio se descompone produciendo dióxido de carbono que, junto con otros gases, dan lugar a erupciones volcánicas explosivas .
La profundidad de compensación de carbonato (CCD) es el punto del océano donde la tasa de precipitación de carbonato de calcio se equilibra con la tasa de disolución debido a las condiciones presentes. En lo profundo del océano, la temperatura baja y la presión aumenta. El aumento de la presión también aumenta la solubilidad del carbonato de calcio. El carbonato de calcio es inusual porque su solubilidad aumenta al disminuir la temperatura. [37] La profundidad de compensación de carbonatos oscila entre 4.000 y 6.000 metros bajo el nivel del mar en los océanos modernos, y los distintos polimorfos (calcita, aragonita) tienen diferentes profundidades de compensación en función de su estabilidad. [38]
El carbonato de calcio puede preservar los fósiles mediante la permineralización . La mayoría de los fósiles de vertebrados de la Formación Two Medicine , una formación geológica conocida por sus huevos de dinosaurio con pico de pato , se conservan mediante permineralización de CaCO 3 . [39] Este tipo de preservación conserva altos niveles de detalle, incluso hasta el nivel microscópico. Sin embargo, también deja a los especímenes vulnerables a la intemperie cuando se exponen a la superficie. [39]
Alguna vez se pensó que las poblaciones de trilobites constituían la mayor parte de la vida acuática durante el Cámbrico , debido al hecho de que sus caparazones ricos en carbonato de calcio se conservaban más fácilmente que los de otras especies, [40] que tenían caparazones puramente quitinosos .
El uso principal del carbonato de calcio es en la industria de la construcción, ya sea como material de construcción, o agregado de piedra caliza para la construcción de carreteras, como ingrediente del cemento o como material de partida para la preparación de cal de construcción mediante quema en un horno . Sin embargo, debido a la erosión causada principalmente por la lluvia ácida , [41] el carbonato de calcio (en forma de piedra caliza) ya no se utiliza solo para fines de construcción, sino sólo como sustancia primaria cruda para materiales de construcción.
El carbonato de calcio también se utiliza en la purificación del hierro a partir de mineral de hierro en un alto horno . El carbonato se calcina in situ para dar óxido de calcio , que forma una escoria con diversas impurezas presentes y se separa del hierro purificado. [42]
En la industria petrolera , el carbonato de calcio se agrega a los fluidos de perforación como agente puente de formación y sellador de revoque; También es un material de peso que aumenta la densidad de los fluidos de perforación para controlar la presión del fondo del pozo. El carbonato de calcio se añade a las piscinas , como corrector del pH para mantener la alcalinidad y compensar las propiedades ácidas del agente desinfectante . [43]
También se utiliza como materia prima en el refinado del azúcar de remolacha azucarera ; se calcina en un horno con antracita para producir óxido de calcio y dióxido de carbono. Esta cal quemada luego se apaga en agua dulce para producir una suspensión de hidróxido de calcio para la precipitación de impurezas en el jugo crudo durante la carbonatación . [44]
El carbonato de calcio en forma de tiza ha sido tradicionalmente un componente importante de la tiza para pizarra . Sin embargo, la tiza fabricada modernamente es principalmente yeso , sulfato de calcio hidratado CaSO 4 ·2H 2 O . El carbonato de calcio es una fuente principal para el cultivo de biorocas . El carbonato de calcio precipitado (PCC), predispersado en forma de suspensión , es un material de relleno común para guantes de látex con el objetivo de lograr el máximo ahorro en materiales y costos de producción. [45]
El carbonato de calcio molido fino (GCC) es un ingrediente esencial en la película microporosa utilizada en pañales y algunas películas de construcción, ya que los poros se nuclean alrededor de las partículas de carbonato de calcio durante la fabricación de la película mediante estiramiento biaxial. El GCC y el PCC se utilizan como relleno en el papel porque son más baratos que la fibra de madera . El papel de impresión y escritura puede contener entre un 10% y un 20% de carbonato de calcio. En Norteamérica, el carbonato de calcio ha comenzado a sustituir al caolín en la producción de papel satinado . Europa lleva varias décadas practicando esto como fabricación de papel alcalino o sin ácido. El PCC utilizado para el relleno y revestimiento de papel se precipita y prepara en una variedad de formas y tamaños que tienen distribuciones de tamaño de partícula estrechas características y diámetros esféricos equivalentes de 0,4 a 3 micrómetros. [ cita necesaria ]
El carbonato de calcio se usa ampliamente como extensor en pinturas , [46] en particular en pinturas de emulsión mate donde típicamente el 30% en peso de la pintura es tiza o mármol. También es un relleno popular en plásticos. [46] Algunos ejemplos típicos incluyen alrededor del 15 al 20 % de carga de tiza en tuberías de drenaje de cloruro de polivinilo no plastificado (uPVC) , y del 5 al 15 % de carga de tiza o mármol recubiertos de estearato en perfiles de ventanas de uPVC. Los cables de PVC pueden utilizar carbonato de calcio en cargas de hasta 70 phr (partes por cien partes de resina) para mejorar las propiedades mecánicas (resistencia a la tracción y alargamiento) y las propiedades eléctricas (resistividad volumétrica). [ cita necesaria ] Los compuestos de polipropileno a menudo se rellenan con carbonato de calcio para aumentar la rigidez, un requisito que se vuelve importante a altas temperaturas de uso. [47] Aquí el porcentaje suele ser del 20% al 40%. También se utiliza habitualmente como relleno en resinas termoestables (compuestos de moldeo en láminas y a granel) [47] y también se ha mezclado con ABS y otros ingredientes para formar algunos tipos de fichas de póquer de "arcilla" moldeadas por compresión . [48] El carbonato de calcio precipitado, que se obtiene dejando caer óxido de calcio en agua, se usa solo o con aditivos como pintura blanca, conocida como blanqueo . [49] [50]
El carbonato de calcio se agrega a una amplia gama de adhesivos, selladores y rellenos decorativos comerciales y de bricolaje. [46] Los adhesivos para baldosas cerámicas suelen contener entre un 70% y un 80% de piedra caliza. Los rellenos para grietas para decoración contienen niveles similares de mármol o dolomita. También se mezcla con masilla para colocar vidrieras y como resistencia para evitar que el vidrio se pegue a los estantes del horno cuando se hornean esmaltes y pinturas a altas temperaturas. [51] [52] [53] [54]
En las aplicaciones de esmalte cerámico , el carbonato de calcio se conoce como merlán [ 46] y es un ingrediente común para muchos esmaltes en su forma de polvo blanco. Cuando un vidriado que contiene este material se cuece en un horno, el merlán actúa como material fundente en el vidriado. El carbonato de calcio molido es un abrasivo (tanto como polvo para fregar como ingrediente de cremas para fregar domésticas), en particular en su forma de calcita, que tiene un nivel de dureza relativamente bajo de 3 en la escala de Mohs y, por lo tanto, no raya el vidrio ni la mayoría. otras cerámicas , esmalte , bronce , hierro y acero , y tienen un efecto moderado sobre metales más blandos como el aluminio y el cobre . Se puede utilizar una pasta hecha de carbonato de calcio y agua desionizada para limpiar el deslustre de la plata . [55]

El carbonato de calcio se usa ampliamente con fines medicinales como un suplemento dietético de calcio económico para el antiácido gástrico [56] (como Tums y Eno ). Puede utilizarse como quelante de fosfato para el tratamiento de la hiperfosfatemia (principalmente en pacientes con insuficiencia renal crónica ). Se utiliza en la industria farmacéutica como relleno inerte para tabletas y otros productos farmacéuticos . [57]
El carbonato de calcio se utiliza en la producción de óxido de calcio y pasta de dientes y ha resurgido como conservante de alimentos y retenedor de color, cuando se utiliza en o con productos como las manzanas orgánicas. [58]
El carbonato de calcio se utiliza terapéuticamente como quelante de fosfato en pacientes en hemodiálisis de mantenimiento . Es la forma más común de quelante de fosfato prescrita, particularmente en la enfermedad renal crónica sin diálisis. El carbonato de calcio es el quelante de fosfato más utilizado, pero los médicos prescriben cada vez más quelantes de fosfato no basados en calcio, más caros, en particular el sevelamer .
El exceso de calcio proveniente de suplementos, alimentos enriquecidos y dietas altas en calcio puede causar el síndrome de leche-álcali , que tiene una toxicidad grave y puede ser fatal. En 1915, Bertram Sippy introdujo el "régimen Sippy" de ingestión cada hora de leche y crema, y la adición gradual de huevos y cereal cocido, durante 10 días, combinado con polvos alcalinos, que proporcionaba alivio sintomático para la úlcera péptica. Durante las siguientes décadas, el régimen Sippy provocó insuficiencia renal , alcalosis e hipercalcemia , principalmente en hombres con úlcera péptica. Estos efectos adversos se revirtieron cuando se suspendió el régimen, pero fue fatal en algunos pacientes con vómitos prolongados. El síndrome de leche-álcali disminuyó en los hombres después de que surgieron tratamientos efectivos para la úlcera péptica . Desde la década de 1990, se ha informado con mayor frecuencia en mujeres que toman suplementos de calcio por encima del rango recomendado de 1,2 a 1,5 gramos diarios, para la prevención y el tratamiento de la osteoporosis, [59] [60] y se exacerba con la deshidratación . Se ha añadido calcio a productos de venta libre, lo que contribuye a una ingesta excesiva involuntaria. La ingesta excesiva de calcio puede provocar hipercalcemia, cuyas complicaciones incluyen vómitos, dolor abdominal y alteración del estado mental. [61]
Como aditivo alimentario se denomina E170 , [62] y tiene un número INS de 170. Se utiliza como regulador de acidez , agente antiaglomerante , estabilizador o colorante y está aprobado para su uso en la UE, [63] EE. UU. [64] y Australia y Nueva Zelanda . [65] Se "añade por ley a toda la harina panificable molida del Reino Unido, excepto a la integral". [66] [67] Se utiliza en algunos productos de leche de soja y leche de almendras como fuente de calcio dietético; al menos un estudio sugiere que el carbonato de calcio podría ser tan biodisponible como el calcio de la leche de vaca . [68] El carbonato de calcio también se utiliza como agente reafirmante en muchos productos vegetales enlatados y embotellados.
Se ha documentado que varias formulaciones de suplementos de calcio contienen el elemento químico plomo , [69] lo que plantea un problema de salud pública . [70] El plomo se encuentra comúnmente en fuentes naturales de calcio. [69]
La cal agrícola , tiza en polvo o piedra caliza, se utiliza como un método barato para neutralizar el suelo ácido , haciéndolo adecuado para la plantación, también se utiliza en la industria de la acuicultura para regular el pH del suelo del estanque antes de iniciar el cultivo. [71] Existe interés en comprender si puede afectar o no la adsorción y desorción de pesticidas en suelos calcáreos. [72]
El carbonato de calcio es un ingrediente clave en muchos polvos de limpieza domésticos como Comet y se utiliza como agente limpiador.
En 1989, un investigador, Ken Simmons, introdujo CaCO 3 en Whetstone Brook, en Massachusetts . [73] Su esperanza era que el carbonato de calcio contrarrestara el ácido de la corriente de la lluvia ácida y salvara a las truchas que habían dejado de desovar. Aunque su experimento fue un éxito, aumentó la cantidad de iones de aluminio en el área del arroyo que no fue tratada con piedra caliza. Esto demuestra que se puede añadir CaCO 3 para neutralizar los efectos de la lluvia ácida en los ecosistemas fluviales . Actualmente el carbonato de calcio se utiliza para neutralizar las condiciones ácidas tanto en el suelo como en el agua. [74] [75] [76] Desde la década de 1970, este tipo de encalado se ha practicado a gran escala en Suecia para mitigar la acidificación y varios miles de lagos y arroyos se encalan repetidamente. [77]
El carbonato de calcio también se utiliza en aplicaciones de desulfuración de gases de combustión, eliminando las dañinas emisiones de SO 2 y NO 2 del carbón y otros combustibles fósiles quemados en grandes centrales eléctricas de combustibles fósiles. [74]
El carbonato de calcio se utiliza comúnmente en la industria del plástico como relleno. Cuando se incorpora a un material plástico, puede mejorar la dureza, rigidez, estabilidad dimensional y procesabilidad del material. [78]
La calcinación de piedra caliza utilizando carbón para producir cal viva se ha practicado desde la antigüedad en culturas de todo el mundo. La temperatura a la que la piedra caliza produce óxido de calcio suele ser de 825 °C, pero establecer un umbral absoluto es engañoso. El carbonato de calcio existe en equilibrio con el óxido de calcio y el dióxido de carbono a cualquier temperatura. A cada temperatura hay una presión parcial de dióxido de carbono que está en equilibrio con el carbonato de calcio. A temperatura ambiente, el equilibrio favorece abrumadoramente al carbonato de calcio, porque la presión de CO 2 de equilibrio es sólo una pequeña fracción de la presión parcial de CO 2 en el aire, que es de aproximadamente 0,035 kPa.
A temperaturas superiores a 550 °C, la presión de equilibrio del CO 2 comienza a exceder la presión del CO 2 en el aire. Por lo tanto, por encima de los 550 °C, el carbonato de calcio comienza a liberar CO 2 al aire. Sin embargo, en un horno de carbón, la concentración de CO 2 será mucho mayor que en el aire. De hecho, si todo el oxígeno del horno se consume en el fuego, entonces la presión parcial de CO 2 en el horno puede llegar a 20 kPa. [79]
La tabla muestra que esta presión parcial no se alcanza hasta que la temperatura es cercana a los 800 °C. Para que la desgasificación de CO 2 del carbonato de calcio se produzca a un ritmo económicamente útil, la presión de equilibrio debe exceder significativamente la presión ambiental de CO 2 . Y para que esto suceda rápidamente, la presión de equilibrio debe exceder la presión atmosférica total de 101 kPa, lo que ocurre a 898 °C.

El carbonato de calcio es poco soluble en agua pura (47 mg/L a presión parcial atmosférica normal de CO 2 como se muestra a continuación).
El equilibrio de su solución viene dado por la ecuación (con el carbonato de calcio disuelto a la derecha):
donde el producto de solubilidad para [Ca 2+ ][CO2-3] se da como cualquier punto entre K sp =3,7 × 10 −9 a K sp =8,7 × 10 −9 a 25 °C, según la fuente de datos. [80] [81] Lo que significa la ecuación es que el producto de la concentración molar de iones de calcio ( moles de Ca 2+ disuelto por litro de solución) con la concentración molar de CO disuelto2-3no puede exceder el valor de K sp . Sin embargo, esta ecuación de solubilidad aparentemente simple debe tomarse junto con el equilibrio más complicado del dióxido de carbono con agua (ver ácido carbónico ). Algo de CO2-3se combina con H + en la solución según
HCO−3se conoce como ion bicarbonato . El bicarbonato de calcio es muchas veces más soluble en agua que el carbonato de calcio; de hecho, sólo existe en solución.
Algunos de los HCO−3se combina con H + en solución según
Parte del H 2 CO 3 se descompone en agua y dióxido de carbono disuelto según
Y el dióxido de carbono disuelto está en equilibrio con el dióxido de carbono atmosférico según
Para el aire ambiente, P CO 2 es de aproximadamente3,5 × 10 −4 atm (o equivalentemente 35 Pa ). La última ecuación anterior fija la concentración de CO 2 disuelto en función de P CO 2 , independientemente de la concentración de CaCO 3 disuelto . A la presión parcial atmosférica de CO 2 , la concentración de CO 2 disuelto es1,2 × 10 −5 moles por litro. La ecuación anterior fija la concentración de H 2 CO 3 en función de la concentración de CO 2 . Para [ CO 2 ] =1,2 × 10 −5 , resulta en [H 2 CO 3 ] =2,0 × 10 −8 moles por litro. Cuando se conoce [H 2 CO 3 ] , las tres ecuaciones restantes junto con
(lo cual es cierto para todas las soluciones acuosas), y la restricción de que la solución debe ser eléctricamente neutra, es decir, la carga total de iones positivos disueltos [Ca 2+ ] + 2 [H + ] debe ser cancelada por la carga total de iones negativos disueltos [HCO−3] + [CO2-3] + [OH − ] , permiten resolver simultáneamente las cinco concentraciones desconocidas restantes (la forma de neutralidad mencionada anteriormente es válida sólo si el carbonato de calcio se ha puesto en contacto con agua pura o con una solución de pH neutro; en el caso en el que el pH inicial del disolvente del agua no es neutro, el equilibrio no es neutro).
La tabla adyacente muestra el resultado para [Ca 2+ ] y [H + ] (en forma de pH) en función de la presión parcial ambiental de CO 2 ( K sp =Para el cálculo se ha tomado 4,47 × 10 −9 ).
El efecto de este último es especialmente evidente en el día a día de las personas que tienen agua dura. El agua de los acuíferos subterráneos puede estar expuesta a niveles de CO 2 mucho más elevados que los atmosféricos. A medida que dicha agua se filtra a través de la roca de carbonato de calcio, el CaCO 3 se disuelve según una de las tendencias anteriores. Cuando esa misma agua emerge del grifo, con el tiempo llega al equilibrio con los niveles de CO 2 en el aire al desgasificar su exceso de CO 2 . Como resultado, el carbonato de calcio se vuelve menos soluble y el exceso precipita en forma de cal. Este mismo proceso es el responsable de la formación de estalactitas y estalagmitas en las cuevas de piedra caliza.
Dos fases hidratadas de carbonato de calcio, monohidrocalcita CaCO 3 ·H 2 O e ikaita CaCO 3 ·6H 2 O , pueden precipitar del agua en condiciones ambientales y persistir como fases metaestables.
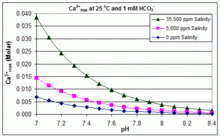
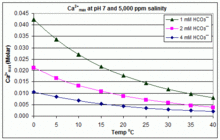
En contraste con el escenario de equilibrio abierto anterior, muchas piscinas se controlan mediante la adición de bicarbonato de sodio ( NaHCO 3 ) a una concentración de aproximadamente 2 mmol/L como tampón, luego se controla el pH mediante el uso de HCl, NaHSO 4 , Na 2. CO 3 , NaOH o formulaciones de cloro que sean ácidas o básicas. En esta situación, el carbono inorgánico disuelto ( carbono inorgánico total ) está lejos del equilibrio con el CO 2 atmosférico . El progreso hacia el equilibrio mediante la desgasificación de CO 2 se ve frenado por
En esta situación, las constantes de disociación para reacciones mucho más rápidas
Permitir la predicción de las concentraciones de cada especie de carbono inorgánico disuelto en solución, a partir de la concentración agregada de HCO.−3(que constituye más del 90% de las especies de parcelas de Bjerrum de pH 7 a pH 8 a 25 °C en agua dulce). [83] Adición de HCO−3aumentará el CO2-3concentración a cualquier pH. Reordenando las ecuaciones dadas anteriormente, podemos ver que [Ca 2+ ] = ksp/[ CO2-3] , y [ CO2-3] = Ka2 [ HCO−3]/[ H + ] . Por lo tanto, cuando HCO−3Se conoce la concentración, la concentración máxima de iones Ca 2+ antes de escalar mediante precipitación de CaCO 3 se puede predecir a partir de la fórmula:
El producto de solubilidad del CaCO 3 ( K sp ) y las constantes de disociación de las especies de carbono inorgánico disueltas (incluido el Ka 2 ) se ven sustancialmente afectados por la temperatura y la salinidad , [83] con el efecto general de que [ Ca 2+ ] max aumenta de agua dulce al agua salada, y disminuye con el aumento de la temperatura, el pH o el nivel de bicarbonato agregado, como se ilustra en los gráficos adjuntos.
Las tendencias son ilustrativas para el manejo de piscinas, pero si se produce incrustación también depende de otros factores, incluidas las interacciones con Mg 2+ , [B(OH) 4 ] − y otros iones en la piscina, así como los efectos de sobresaturación. [84] [85] La incrustación se observa comúnmente en generadores de cloro electrolítico, donde hay un pH alto cerca de la superficie del cátodo y la deposición de incrustaciones aumenta aún más la temperatura. Esta es una de las razones por las que algunos operadores de piscinas prefieren el borato al bicarbonato como principal amortiguador de pH y evitan el uso de productos químicos para piscinas que contengan calcio. [86]
Se encuentran disponibles comercialmente soluciones de ácidos fuertes ( HCl ), moderadamente fuertes ( sulfámicos ) o débiles ( acético , cítrico , sórbico , láctico , fosfórico ). Se utilizan habitualmente como agentes desincrustantes para eliminar los depósitos de cal . La cantidad máxima de CaCO 3 que se puede "disolver" en un litro de solución ácida se puede calcular utilizando las ecuaciones de equilibrio anteriores.


{{cite web}}: Mantenimiento CS1: copia archivada como título ( enlace ){{cite book}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite book}}: |journal=ignorado ( ayuda )