El aluminio ( Aluminium en inglés norteamericano ) es un elemento químico ; tiene símbolo Al y número atómico 13. El aluminio tiene una densidad menor que la de otros metales comunes , aproximadamente un tercio de la del acero . Tiene una gran afinidad por el oxígeno , formando una capa protectora de óxido en la superficie cuando se expone al aire. El aluminio se parece visualmente a la plata , tanto por su color como por su gran capacidad para reflejar la luz. Es blando, no magnético y dúctil . Tiene un isótopo estable, el 27 Al, que es muy abundante, lo que convierte al aluminio en el duodécimo elemento más común del universo. La radiactividad del 26 Al , un isótopo más inestable, lleva a que se utilice en la datación radiométrica .
Químicamente, el aluminio es un metal de post-transición del grupo del boro ; Como es común en el grupo, el aluminio forma compuestos principalmente en el estado de oxidación +3 . El catión de aluminio Al 3+ es pequeño y muy cargado ; como tal, tiene más poder polarizante , y los enlaces formados por el aluminio tienen un carácter más covalente . La fuerte afinidad del aluminio por el oxígeno conduce a la aparición común de sus óxidos en la naturaleza. El aluminio se encuentra en la Tierra principalmente en las rocas de la corteza , donde es el tercer elemento más abundante , después del oxígeno y el silicio , más que en el manto , y prácticamente nunca como metal libre . Se obtiene industrialmente mediante la extracción de bauxita , una roca sedimentaria rica en minerales de aluminio.
El descubrimiento del aluminio fue anunciado en 1825 por el físico danés Hans Christian Ørsted . La primera producción industrial de aluminio fue iniciada por el químico francés Henri Étienne Sainte-Claire Deville en 1856. El aluminio se volvió mucho más disponible para el público con el proceso Hall-Héroult desarrollado de forma independiente por el ingeniero francés Paul Héroult y el ingeniero estadounidense Charles Martin Hall en 1886. y la producción en masa de aluminio llevó a su uso extensivo en la industria y la vida cotidiana. En la Primera y Segunda Guerra Mundial, el aluminio fue un recurso estratégico crucial para la aviación . En 1954, el aluminio se convirtió en el metal no ferroso más producido , superando al cobre . En el siglo XXI, la mayor parte del aluminio se consumía en el transporte, la ingeniería, la construcción y el embalaje en Estados Unidos, Europa occidental y Japón.
A pesar de su prevalencia en el medio ambiente, no se conoce ningún organismo vivo que metabolice las sales de aluminio , pero este aluminio es bien tolerado por plantas y animales. Debido a la abundancia de estas sales, la posibilidad de que tengan una función biológica es de interés y se están realizando estudios.
De los isótopos de aluminio, sólo27
Alabama
es estable. Esta situación es común para elementos con número atómico impar. [b] Es el único isótopo de aluminio primordial , es decir, el único que ha existido en la Tierra en su forma actual desde la formación del planeta. Por tanto, es un elemento mononucleido y su peso atómico estándar es prácticamente el mismo que el del isótopo. Esto hace que el aluminio sea muy útil en resonancia magnética nuclear (RMN), ya que su único isótopo estable tiene una alta sensibilidad de RMN. [13] El peso atómico estándar del aluminio es bajo en comparación con muchos otros metales. [do]
Todos los demás isótopos del aluminio son radiactivos . El más estable de ellos es el 26 Al : si bien estuvo presente junto con el 27 Al estable en el medio interestelar a partir del cual se formó el Sistema Solar, habiendo sido producido también por nucleosíntesis estelar , su vida media es de sólo 717.000 años y por lo tanto es detectable. cantidad no ha sobrevivido desde la formación del planeta. [14] Sin embargo, se producen trazas diminutas de 26 Al a partir del argón en la atmósfera por la espalación causada por los protones de los rayos cósmicos . La proporción de 26 Al a 10 Be se ha utilizado para radiodatar procesos geológicos en escalas de tiempo de 10 5 a 10 6 años, en particular transporte, deposición, almacenamiento de sedimentos , tiempos de enterramiento y erosión. [15] La mayoría de los científicos de meteoritos creen que la energía liberada por la desintegración del 26 Al fue responsable de la fusión y diferenciación de algunos asteroides después de su formación hace 4,55 mil millones de años. [16]
Los isótopos restantes del aluminio, con números másicos que oscilan entre 22 y 43, tienen vidas medias inferiores a una hora. Se conocen tres estados metaestables , todos con vidas medias inferiores a un minuto. [12]
Un átomo de aluminio tiene 13 electrones, dispuestos en una configuración electrónica de [ Ne ] 3s 2 3p 1 , [17] con tres electrones más allá de una configuración estable de gas noble. En consecuencia, las tres primeras energías de ionización combinadas del aluminio son mucho más bajas que la cuarta energía de ionización sola. [18] Esta configuración electrónica se comparte con los otros miembros bien caracterizados de su grupo, boro , galio , indio y talio ; también se espera que ocurra lo mismo con el nihonio . El aluminio puede ceder sus tres electrones más externos en muchas reacciones químicas (ver más abajo). La electronegatividad del aluminio es 1,61 (escala de Pauling). [19]

Un átomo de aluminio libre tiene un radio de 143 pm . [20] Con los tres electrones más externos eliminados, el radio se reduce a 39 pm para un átomo de 4 coordenadas o 53,5 pm para un átomo de 6 coordenadas. [20] A temperatura y presión estándar , los átomos de aluminio (cuando no se ven afectados por átomos de otros elementos) forman un sistema cristalino cúbico centrado en las caras unido por enlaces metálicos proporcionados por los electrones más externos de los átomos; por tanto, el aluminio (en estas condiciones) es un metal. [21] Este sistema cristalino es compartido por muchos otros metales, como el plomo y el cobre ; el tamaño de una celda unitaria de aluminio es comparable al de esos otros metales. [21] El sistema, sin embargo, no es compartido por los otros miembros de su grupo: el boro tiene energías de ionización demasiado altas para permitir la metalización, el talio tiene una estructura hexagonal compacta y el galio y el indio tienen estructuras inusuales que no están estrechamente unidas. empaquetados como los de aluminio y talio. Los pocos electrones disponibles para el enlace metálico en el aluminio son una causa probable de que sea blando, con un punto de fusión bajo y una resistividad eléctrica baja . [22]
El metal de aluminio tiene una apariencia que va del blanco plateado al gris opaco dependiendo de la rugosidad de su superficie . [d] Los espejos de aluminio son los más reflectantes de todos los espejos metálicos para la luz ultravioleta cercana y la luz infrarroja lejana . También es uno de los más reflectantes para la luz en el espectro visible, casi a la par con la plata a este respecto, y por lo tanto los dos tienen un aspecto similar. El aluminio también es bueno para reflejar la radiación solar , aunque la exposición prolongada a la luz solar en el aire añade desgaste a la superficie del metal; Esto se puede evitar si se anodiza el aluminio , lo que añade una capa protectora de óxido a la superficie.
La densidad del aluminio es de 2,70 g/cm 3 , aproximadamente 1/3 de la del acero, mucho menor que la de otros metales comunes, lo que hace que las piezas de aluminio sean fácilmente identificables por su ligereza. [25] La baja densidad del aluminio en comparación con la mayoría de los otros metales surge del hecho de que sus núcleos son mucho más ligeros, mientras que la diferencia en el tamaño de la celda unitaria no compensa esta diferencia. Los únicos metales más ligeros son los metales de los grupos 1 y 2 , que, aparte del berilio y el magnesio, son demasiado reactivos para su uso estructural (y el berilio es muy tóxico). [26] El aluminio no es tan fuerte ni rígido como el acero, pero su baja densidad lo compensa en la industria aeroespacial y en muchas otras aplicaciones donde el peso ligero y la resistencia relativamente alta son cruciales. [27]
El aluminio puro es bastante blando y carece de resistencia. En la mayoría de las aplicaciones se utilizan diversas aleaciones de aluminio debido a su mayor resistencia y dureza. [28] El límite elástico del aluminio puro es de 7 a 11 MPa , mientras que las aleaciones de aluminio tienen límites elásticos que oscilan entre 200 MPa y 600 MPa. [29] El aluminio es dúctil , con un porcentaje de alargamiento del 50-70%, [30] y maleable , lo que permite que se pueda estirar y extruir fácilmente . [31] También se mecaniza y funde fácilmente . [31]
El aluminio es un excelente conductor térmico y eléctrico , teniendo alrededor del 60% de la conductividad del cobre , tanto térmica como eléctrica, mientras que tiene solo el 30% de la densidad del cobre. [32] El aluminio es capaz de tener superconductividad , con una temperatura crítica superconductora de 1,2 kelvin y un campo magnético crítico de aproximadamente 100 gauss (10 militeslas ). [33] Es paramagnético y, por lo tanto, esencialmente no se ve afectado por los campos magnéticos estáticos. [34] Sin embargo, la alta conductividad eléctrica significa que se ve fuertemente afectada por campos magnéticos alternos mediante la inducción de corrientes parásitas . [35]
El aluminio combina características de los metales anteriores y posteriores a la transición. Dado que tiene pocos electrones disponibles para enlaces metálicos, como sus congéneres más pesados del grupo 13 , tiene las propiedades físicas características de un metal post-transición, con distancias interatómicas más largas de lo esperado. [22] Además, como Al 3+ es un catión pequeño y altamente cargado, es fuertemente polarizante y el enlace en compuestos de aluminio tiende a la covalencia ; [36] este comportamiento es similar al del berilio (Be 2+ ), y los dos muestran un ejemplo de una relación diagonal . [37]
El núcleo subyacente bajo la capa de valencia del aluminio es el del gas noble anterior , mientras que los de sus congéneres más pesados galio , indio , talio y nihonio también incluyen una subcapa d llena y, en algunos casos, una subcapa f llena. Por lo tanto, los electrones internos del aluminio protegen a los electrones de valencia casi por completo, a diferencia de los de los congéneres más pesados del aluminio. Como tal, el aluminio es el metal más electropositivo de su grupo y su hidróxido es, de hecho, más básico que el del galio. [36] [e] El aluminio también tiene similitudes menores con el boro metaloide en el mismo grupo: los compuestos AlX 3 son isoelectrónicos de valencia para los compuestos BX 3 (tienen la misma estructura electrónica de valencia), y ambos se comportan como ácidos de Lewis y forman fácilmente aductos. . [38] Además, uno de los motivos principales de la química del boro son las estructuras icosaédricas regulares , y el aluminio forma una parte importante de muchas aleaciones cuasicristalinas icosaédricas , incluida la clase Al-Zn-Mg. [39]
El aluminio tiene una alta afinidad química por el oxígeno, lo que lo hace adecuado para su uso como agente reductor en la reacción de termita . Un fino polvo de aluminio reacciona explosivamente al contacto con el oxígeno líquido ; Sin embargo, en condiciones normales, el aluminio forma una fina capa de óxido (~5 nm a temperatura ambiente) [40] que protege el metal de una mayor corrosión por oxígeno, agua o ácido diluido, un proceso denominado pasivación . [36] [41] Debido a su resistencia general a la corrosión, el aluminio es uno de los pocos metales que retiene la reflectancia plateada en forma de polvo fino, lo que lo convierte en un componente importante de las pinturas de color plateado . [42] El aluminio no es atacado por ácidos oxidantes debido a su pasivación. Esto permite utilizar el aluminio para almacenar reactivos como ácido nítrico , ácido sulfúrico concentrado y algunos ácidos orgánicos. [43]
En ácido clorhídrico concentrado caliente , el aluminio reacciona con agua con desprendimiento de hidrógeno, y en hidróxido de sodio acuoso o hidróxido de potasio a temperatura ambiente para formar aluminatos ; la pasivación protectora en estas condiciones es insignificante. [44] El agua regia también disuelve el aluminio. [43] El aluminio se corroe con cloruros disueltos , como el cloruro de sodio común , razón por la cual las tuberías domésticas nunca están hechas de aluminio. [44] La capa de óxido del aluminio también se destruye por contacto con mercurio debido a la amalgamación o con sales de algunos metales electropositivos. [36] Como tal, las aleaciones de aluminio más fuertes son menos resistentes a la corrosión debido a reacciones galvánicas con el cobre aleado , [29] y la resistencia a la corrosión del aluminio se reduce en gran medida por las sales acuosas, particularmente en presencia de metales diferentes. [22]
El aluminio reacciona con la mayoría de los no metales al calentarse, formando compuestos como el nitruro de aluminio (AlN), el sulfuro de aluminio (Al 2 S 3 ) y los haluros de aluminio (AlX 3 ). También forma una amplia gama de compuestos intermetálicos que involucran metales de todos los grupos de la tabla periódica. [36]
La gran mayoría de los compuestos, incluidos todos los minerales que contienen aluminio y todos los compuestos de aluminio comercialmente importantes, contienen aluminio en el estado de oxidación 3+. El número de coordinación de tales compuestos varía, pero generalmente Al 3+ tiene seis o cuatro coordenadas. Casi todos los compuestos de aluminio (III) son incoloros. [36]
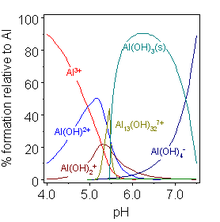
En solución acuosa, Al 3+ existe como catión hexaacua [Al(H 2 O ) 6 ] 3+ , que tiene un Ka aproximado de 10 −5 . [13] Estas soluciones son ácidas ya que este catión puede actuar como donador de protones e hidrolizarse progresivamente hasta que se forma un precipitado de hidróxido de aluminio , Al(OH) 3 . Esto es útil para clarificar el agua, ya que el precipitado se nuclea en las partículas suspendidas en el agua, eliminándolas. Un aumento aún mayor del pH hace que el hidróxido se disuelva nuevamente en forma de aluminato , [Al(H 2 O) 2 (OH) 4 ] − .
El hidróxido de aluminio forma sales y aluminatos y se disuelve en ácidos y álcalis, así como al fusionarse con óxidos ácidos y básicos. [36] Este comportamiento del Al(OH) 3 se denomina anfoterismo y es característico de cationes débilmente básicos que forman hidróxidos insolubles y cuyas especies hidratadas también pueden donar sus protones. Un efecto de esto es que las sales de aluminio con ácidos débiles se hidrolizan en agua hasta el hidróxido acuoso y el hidruro no metálico correspondiente: por ejemplo, el sulfuro de aluminio produce sulfuro de hidrógeno . Sin embargo, algunas sales como el carbonato de aluminio existen en solución acuosa pero son inestables como tales; y sólo se produce una hidrólisis incompleta en el caso de las sales con ácidos fuertes, como los haluros, el nitrato y el sulfato . Por razones similares, las sales de aluminio anhidras no se pueden obtener calentando sus "hidratos": el cloruro de aluminio hidratado no es, de hecho, AlCl 3 ·6H 2 O sino [Al(H 2 O) 6 ]Cl 3 , y los enlaces Al-O son tan fuerte que el calentamiento no es suficiente para romperlos y formar enlaces Al-Cl: [36]
Los cuatro trihaluros son bien conocidos. A diferencia de las estructuras de los tres trihaluros más pesados, el fluoruro de aluminio (AlF 3 ) presenta aluminio de seis coordenadas, lo que explica su involatilidad e insolubilidad, así como su alto calor de formación . Cada átomo de aluminio está rodeado por seis átomos de flúor en una disposición octaédrica distorsionada , y cada átomo de flúor se comparte entre las esquinas de dos octaedros. Estas unidades {AlF 6 } también existen en fluoruros complejos como la criolita , Na 3 AlF 6 . [f] AlF 3 se funde a 1290 °C (2354 °F) y se obtiene mediante la reacción de óxido de aluminio con gas fluoruro de hidrógeno a 700 °C (1300 °F). [46]
Con haluros más pesados, los números de coordinación son menores. Los otros trihaluros son diméricos o poliméricos con centros de aluminio tetraédricos de cuatro coordenadas. [g] El tricloruro de aluminio (AlCl 3 ) tiene una estructura polimérica en capas por debajo de su punto de fusión de 192,4 °C (378 °F), pero al fundirse se transforma en dímeros de Al 2 Cl 6 . A temperaturas más altas, estos se disocian cada vez más en monómeros planos trigonales de AlCl 3 similares a la estructura del BCl 3 . El tribromuro de aluminio y el triyoduro de aluminio forman dímeros de Al 2 X 6 en las tres fases y, por tanto, no muestran cambios de propiedades tan significativos tras el cambio de fase. [46] Estos materiales se preparan tratando el aluminio con el halógeno. Los trihaluros de aluminio forman muchos compuestos o complejos de adición; su naturaleza ácida de Lewis los hace útiles como catalizadores de las reacciones de Friedel-Crafts . El tricloruro de aluminio tiene importantes usos industriales que implican esta reacción, como en la fabricación de antraquinonas y estireno ; También se utiliza a menudo como precursor de muchos otros compuestos de aluminio y como reactivo para convertir fluoruros no metálicos en los cloruros correspondientes (una reacción de transhalogenación ). [46]
El aluminio forma un óxido estable con la fórmula química Al 2 O 3 , comúnmente llamado alúmina . [47] Se puede encontrar en la naturaleza en el mineral corindón , α-alúmina; [48] también hay una fase de γ-alúmina. [13] Su forma cristalina, corindón , es muy duro ( dureza Mohs 9), tiene un alto punto de fusión de 2045 °C (3713 °F), tiene una volatilidad muy baja, es químicamente inerte y un buen aislante eléctrico. Se utiliza a menudo en abrasivos (como la pasta de dientes), como material refractario y en cerámica , además de ser el material de partida para la producción electrolítica de aluminio. El zafiro y el rubí son corindón impuro y contaminado con trazas de otros metales. [13] Los dos óxidos-hidróxidos principales, AlO(OH), son la boehmita y la diáspora . Hay tres trihidróxidos principales: bayerita , gibbsita y nordstrandita, que se diferencian por su estructura cristalina ( polimorfos ). También se conocen muchas otras estructuras intermedias y relacionadas. [13] La mayoría se producen a partir de minerales mediante una variedad de procesos húmedos que utilizan ácidos y bases. El calentamiento de los hidróxidos conduce a la formación de corindón. Estos materiales son de importancia central para la producción de aluminio y son en sí mismos extremadamente útiles. Algunas fases de óxidos mixtos también son muy útiles, como la espinela (MgAl 2 O 4 ), Na-β-alúmina (NaAl 11 O 17 ) y aluminato tricálcico (Ca 3 Al 2 O 6 , una fase mineral importante en el cemento Portland ). . [13]
Los únicos calcogenuros estables en condiciones normales son el sulfuro de aluminio (Al 2 S 3 ), el seleniuro (Al 2 Se 3 ) y el telururo (Al 2 Te 3 ). Los tres se preparan mediante reacción directa de sus elementos a aproximadamente 1000 °C (1800 °F) y se hidrolizan rápidamente por completo en agua para producir hidróxido de aluminio y el respectivo calcogenuro de hidrógeno . Como el aluminio es un átomo pequeño en relación con estos calcógenos, estos tienen aluminio tetraédrico de cuatro coordenadas con varios polimorfos que tienen estructuras relacionadas con la wurtzita , con dos tercios de los posibles sitios metálicos ocupados de forma ordenada (α) o aleatoria (β). ; el sulfuro también tiene una forma γ relacionada con la γ-alúmina, y una forma hexagonal inusual de alta temperatura donde la mitad de los átomos de aluminio tienen cuatro coordinaciones tetraédricas y la otra mitad tienen cinco coordinaciones bipiramidales trigonales. [49]
Se conocen cuatro pnictidas : nitruro de aluminio (AlN), fosfuro de aluminio (AlP), arseniuro de aluminio (AlAs) y antimoniuro de aluminio (AlSb). Todos son semiconductores III-V isoelectrónicos al silicio y al germanio , todos los cuales, excepto AlN, tienen la estructura blenda de zinc . Los cuatro pueden fabricarse mediante reacción directa a alta temperatura (y posiblemente a alta presión) de los elementos que los componen. [49]
El aluminio se alea bien con la mayoría de los demás metales (con la excepción de la mayoría de los metales alcalinos y los metales del grupo 13) y se conocen más de 150 intermetálicos con otros metales. La preparación implica calentar metales fijos juntos en cierta proporción, seguido de enfriamiento y recocido gradual . La unión en ellos es predominantemente metálica y la estructura cristalina depende principalmente de la eficiencia del empaquetamiento. [50]
Hay pocos compuestos con estados de oxidación más bajos. Existen algunos compuestos de aluminio (I) : AlF, AlCl, AlBr y AlI existen en fase gaseosa cuando el trihaluro respectivo se calienta con aluminio y a temperaturas criogénicas. [46] Un derivado estable del monoyoduro de aluminio es el aducto cíclico formado con trietilamina , Al 4 I 4 (NEt 3 ) 4 . También existen Al 2 O y Al 2 S, pero son muy inestables. [51] Se invocan u observan compuestos de aluminio (II) muy simples en las reacciones del Al metal con oxidantes. Por ejemplo, se ha detectado monóxido de aluminio , AlO, en la fase gaseosa después de la explosión [52] y en los espectros de absorción estelar. [53] Se investigan más a fondo los compuestos de fórmula R 4 Al 2 que contienen un enlace Al-Al y donde R es un ligando orgánico grande . [54]
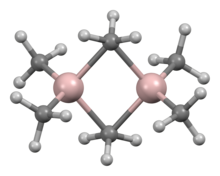
Existe una variedad de compuestos de fórmula empírica AlR 3 y AlR 1,5 Cl 1,5 . [55] Los trialquilos y triarilos de aluminio son líquidos reactivos, volátiles e incoloros o sólidos de bajo punto de fusión. Se inflaman espontáneamente en el aire y reaccionan con el agua, por lo que es necesario tomar precauciones al manipularlos. A menudo forman dímeros, a diferencia de sus análogos de boro, pero esta tendencia disminuye en el caso de los alquilos de cadena ramificada ( por ejemplo , Pri , Bui , Me3CCH2 ) ; por ejemplo, el triisobutilaluminio existe como una mezcla en equilibrio del monómero y el dímero. [56] [57] Estos dímeros, como el trimetilaluminio (Al 2 Me 6 ), generalmente presentan centros tetraédricos de Al formados por dimerización con algún grupo alquilo formando puentes entre ambos átomos de aluminio. Son ácidos duros y reaccionan fácilmente con ligandos formando aductos. En la industria, se utilizan principalmente en reacciones de inserción de alquenos, como descubrió Karl Ziegler , sobre todo en "reacciones de crecimiento" que forman alquenos y alcoholes primarios no ramificados de cadena larga, y en la polimerización a baja presión de eteno y propeno . También hay algunos compuestos de organoaluminio heterocíclicos y de racimos que involucran enlaces Al-N. [56]
El hidruro de aluminio más importante industrialmente es el hidruro de litio y aluminio (LiAlH 4 ), que se utiliza como agente reductor en química orgánica . Puede producirse a partir de hidruro de litio y tricloruro de aluminio . [58] El hidruro más simple, el hidruro de aluminio o alano, no es tan importante. Es un polímero de fórmula (AlH 3 ) n , a diferencia del correspondiente hidruro de boro que es un dímero de fórmula (BH 3 ) 2 . [58]
La abundancia por partícula de aluminio en el Sistema Solar es de 3,15 ppm (partes por millón). [59] [h] Es el duodécimo más abundante de todos los elementos y el tercero más abundante entre los elementos que tienen números atómicos impares, después del hidrógeno y el nitrógeno. [59] El único isótopo estable del aluminio, el 27 Al, es el decimoctavo núcleo más abundante del universo. Se crea casi en su totalidad tras la fusión del carbono en estrellas masivas que luego se convertirán en supernovas de Tipo II : esta fusión crea 26 Mg, que al capturar protones y neutrones libres, se convierte en aluminio. Algunas cantidades más pequeñas de 27 Al se crean en las capas de estrellas evolucionadas que queman hidrógeno , donde el 26 Mg puede capturar protones libres. [60] Básicamente, todo el aluminio que existe actualmente es 27 Al. El 26 Al estaba presente en el Sistema Solar temprano con una abundancia del 0,005% en relación con el 27 Al, pero su vida media de 728.000 años es demasiado corta para que sobreviva cualquier núcleo original; 26 Al está, por tanto, extinto . [60] A diferencia del 27 Al, la quema de hidrógeno es la fuente principal de 26 Al, y el nucleido emerge después de que un núcleo de 25 Mg atrapa un protón libre. Sin embargo, las trazas de 26 Al que sí existen son el emisor de rayos gamma más común en el gas interestelar ; [60] si el 26 Al original todavía estuviera presente, los mapas de rayos gamma de la Vía Láctea serían más brillantes. [60]

En general, la Tierra tiene aproximadamente un 1,59% de aluminio en masa (el séptimo en abundancia en masa). [61] El aluminio se encuentra en mayor proporción en la corteza terrestre que en el universo en general. Esto se debe a que el aluminio forma fácilmente óxido y se une a las rocas y permanece en la corteza terrestre , mientras que los metales menos reactivos se hunden hasta el núcleo. [60] En la corteza terrestre, el aluminio es el elemento metálico más abundante (8,23% en masa [30] ) y el tercero más abundante de todos los elementos (después del oxígeno y el silicio). [62] Una gran cantidad de silicatos en la corteza terrestre contienen aluminio. [63] Por el contrario, el manto de la Tierra tiene sólo un 2,38% de aluminio en masa. [64] El aluminio también se encuentra en el agua de mar en una concentración de 2 μg/kg. [30]
Debido a su fuerte afinidad por el oxígeno, el aluminio casi nunca se encuentra en estado elemental; en cambio, se encuentra en óxidos o silicatos. Los feldespatos , el grupo de minerales más común en la corteza terrestre, son los aluminosilicatos. El aluminio también se encuentra en los minerales berilo , criolita , granate , espinela y turquesa . [65] Las impurezas en el Al 2 O 3 , como el cromo y el hierro , producen las piedras preciosas rubí y zafiro , respectivamente. [66] El aluminio metálico nativo es extremadamente raro y solo se puede encontrar como una fase menor en ambientes con baja fugacidad de oxígeno , como el interior de ciertos volcanes. [67] Se ha informado de aluminio nativo en filtraciones frías en el talud continental nororiental del Mar de China Meridional . Es posible que estos depósitos sean el resultado de la reducción bacteriana del tetrahidroxoaluminato Al(OH) 4 − . [68]
Aunque el aluminio es un elemento común y extendido, no todos los minerales de aluminio son fuentes económicamente viables del metal. Casi todo el aluminio metálico se produce a partir del mineral bauxita (AlO x (OH) 3–2 x ). La bauxita se produce como producto de la erosión de un lecho rocoso con bajo contenido de hierro y sílice en condiciones climáticas tropicales. [69] En 2017, la mayor parte de la bauxita se extrajo en Australia, China, Guinea y la India. [70]

La historia del aluminio ha estado marcada por el uso del alumbre . El primer registro escrito sobre el alumbre, realizado por el historiador griego Heródoto , se remonta al siglo V a.C. [71] Se sabe que los antiguos utilizaban el alumbre como mordiente para teñir y para la defensa de la ciudad. [71] Después de las Cruzadas , el alumbre, un bien indispensable en la industria textil europea, [72] fue objeto de comercio internacional; [73] fue importado a Europa desde el Mediterráneo oriental hasta mediados del siglo XV. [74]
La naturaleza del alumbre seguía siendo desconocida. Alrededor de 1530, el médico suizo Paracelso sugirió que el alumbre era una sal de una tierra de alumbre. [75] En 1595, el médico y químico alemán Andreas Libavius confirmó esto experimentalmente. [76] En 1722, el químico alemán Friedrich Hoffmann anunció su creencia de que la base del alumbre era una tierra distinta. [77] En 1754, el químico alemán Andreas Sigismund Marggraf sintetizó alúmina hirviendo arcilla en ácido sulfúrico y posteriormente añadiendo potasa . [77]
Los intentos de producir aluminio se remontan a 1760. [78] Sin embargo, el primer intento exitoso lo completó en 1824 el físico y químico danés Hans Christian Ørsted . Hizo reaccionar cloruro de aluminio anhidro con amalgama de potasio , produciendo un trozo de metal de aspecto similar al estaño. [79] [80] [81] Presentó sus resultados y demostró una muestra del nuevo metal en 1825. [82] [83] En 1827, el químico alemán Friedrich Wöhler repitió los experimentos de Ørsted pero no identificó ningún aluminio. [84] (La razón de esta inconsistencia no se descubrió hasta 1921.) [85] Realizó un experimento similar ese mismo año mezclando cloruro de aluminio anhidro con potasio y produjo un polvo de aluminio. [81] En 1845, pudo producir pequeñas piezas del metal y describió algunas propiedades físicas de este metal. [85] Durante muchos años después, Wöhler fue considerado el descubridor del aluminio. [86]

Como el método de Wöhler no podía producir grandes cantidades de aluminio, el metal seguía siendo escaso; su costo superó al del oro. [84] La primera producción industrial de aluminio fue establecida en 1856 por el químico francés Henri Etienne Sainte-Claire Deville y sus compañeros. [87] Deville había descubierto que el tricloruro de aluminio podía reducirse con sodio, que era más conveniente y menos costoso que el potasio, que había utilizado Wöhler. [88] Incluso entonces, el aluminio todavía no era de gran pureza y el aluminio producido difería en propiedades según la muestra. [89] Debido a su capacidad de conducir electricidad, el aluminio se utilizó como tapa del Monumento a Washington , terminado en 1885. El edificio más alto del mundo en ese momento, la tapa de metal resistente a la corrosión estaba destinada a servir como pararrayos. cima.
El primer método de producción industrial a gran escala fue desarrollado de forma independiente en 1886 por el ingeniero francés Paul Héroult y el ingeniero estadounidense Charles Martin Hall ; ahora se conoce como proceso Hall-Héroult . [90] El proceso Hall-Héroult convierte la alúmina en metal. El químico austriaco Carl Joseph Bayer descubrió una forma de purificar la bauxita para producir alúmina, ahora conocida como proceso Bayer , en 1889. [91] La producción moderna de aluminio se basa en los procesos Bayer y Hall-Héroult. [92]
A medida que la producción a gran escala provocó la caída de los precios del aluminio, el metal se utilizó ampliamente en joyería, monturas de gafas, instrumentos ópticos, vajillas y papel de aluminio , y otros artículos cotidianos en la década de 1890 y principios del siglo XX. La capacidad del aluminio para formar aleaciones duras pero ligeras con otros metales proporcionó al metal muchos usos en ese momento. [93] Durante la Primera Guerra Mundial , los principales gobiernos exigieron grandes envíos de aluminio para estructuras de aviones ligeras y resistentes; [94] Durante la Segunda Guerra Mundial , la demanda de aviación por parte de los principales gobiernos fue aún mayor. [95] [96] [97]
A mediados del siglo XX, el aluminio se había convertido en parte de la vida cotidiana y en un componente esencial de los artículos para el hogar. [98] En 1954, la producción de aluminio superó a la de cobre , [i] históricamente segunda en producción sólo después del hierro, [101] convirtiéndolo en el metal no ferroso más producido . A mediados del siglo XX, el aluminio surgió como un material de ingeniería civil, con aplicaciones en la construcción tanto en construcciones básicas como en trabajos de acabado interior, [102] y se utiliza cada vez más en ingeniería militar, tanto para aviones como para motores de vehículos blindados terrestres. [103] El primer satélite artificial de la Tierra , lanzado en 1957, constaba de dos semiesferas de aluminio separadas unidas y todos los vehículos espaciales posteriores han utilizado aluminio hasta cierto punto. [92] La lata de aluminio se inventó en 1956 y se utilizó como almacenamiento de bebidas en 1958. [104]
A lo largo del siglo XX, la producción de aluminio aumentó rápidamente: mientras que la producción mundial de aluminio en 1900 era de 6.800 toneladas métricas, la producción anual superó por primera vez las 100.000 toneladas métricas en 1916; 1.000.000 de toneladas en 1941; 10.000.000 de toneladas en 1971. [99] En la década de 1970, el aumento de la demanda de aluminio lo convirtió en un bien de intercambio; entró en la Bolsa de Metales de Londres , la bolsa de metales industriales más antigua del mundo, en 1978. [92] La producción siguió creciendo: la producción anual de aluminio superó las 50.000.000 de toneladas métricas en 2013. [99]
El precio real del aluminio disminuyó de 14.000 dólares por tonelada métrica en 1900 a 2.340 dólares en 1948 (en dólares estadounidenses de 1998). [99] Los costos de extracción y procesamiento se redujeron debido al progreso tecnológico y la escala de las economías. Sin embargo, la necesidad de explotar yacimientos de menor ley y peor calidad y el uso de costos de insumos en rápido aumento (sobre todo, energía) aumentaron el costo neto del aluminio; [105] el precio real comenzó a crecer en la década de 1970 con el aumento del costo de la energía. [106] La producción se trasladó de los países industrializados a países donde la producción era más barata. [107] Los costos de producción a finales del siglo XX cambiaron debido a los avances tecnológicos, los menores precios de la energía, los tipos de cambio del dólar estadounidense y los precios de la alúmina. [108] La participación combinada de los países BRIC en la producción primaria y el consumo primario creció sustancialmente en la primera década del siglo XXI. [109] China está acumulando una parte especialmente grande de la producción mundial gracias a la abundancia de recursos, energía barata y estímulos gubernamentales; [110] también aumentó su participación en el consumo del 2% en 1972 al 40% en 2010. [111] En Estados Unidos, Europa occidental y Japón, la mayor parte del aluminio se consumía en el transporte, la ingeniería, la construcción y el embalaje. [112] En 2021, los precios de los metales industriales como el aluminio se han disparado a niveles casi récord a medida que la escasez de energía en China eleva los costos de la electricidad. [113]
Los nombres aluminio y aluminio se derivan de la palabra alúmina , un término obsoleto para alúmina , [j] el principal óxido de aluminio natural . [115] La alúmina se tomó prestada del francés, que a su vez la derivó de alumen , el nombre latino clásico del alumbre , el mineral del que se extraía. [116] La palabra latina alumen proviene de la raíz protoindoeuropea *alu- que significa "amarga" o "cerveza". [117]

Se acredita al químico británico Humphry Davy , que realizó una serie de experimentos destinados a aislar el metal, como la persona que nombró el elemento. El primer nombre propuesto para el metal que se aislaría del alumbre fue alumium , que Davy sugirió en un artículo de 1808 sobre su investigación electroquímica, publicado en Philosophical Transactions of the Royal Society . [118] Parecía que el nombre fue creado a partir de la palabra inglesa alumbre y el sufijo latino -ium ; pero era costumbre entonces dar a los elementos nombres originarios del latín, por lo que este nombre no fue adoptado universalmente. Este nombre fue criticado por químicos contemporáneos de Francia, Alemania y Suecia, quienes insistieron en que el metal debería recibir el nombre del óxido, alúmina, del que se aislaría. [119] El nombre inglés alum no proviene directamente del latín, mientras que alumine / alumina obviamente proviene de la palabra latina alumen (tras la declinación , alumen cambia a alumin- ).
Un ejemplo fue Essai sur la Nomenclature chimique (julio de 1811), escrito en francés por un químico sueco, Jöns Jacob Berzelius , en el que se da el nombre de aluminio al elemento que se sintetizaría a partir de alumbre. [120] [k] (Otro artículo en el mismo número de la revista también se refiere al metal cuyo óxido es la base del zafiro , es decir, el mismo metal que el aluminio .) [122] Un resumen de enero de 1811 de una de las conferencias de Davy en la Royal Society mencionó el nombre aluminio como una posibilidad. [123] Al año siguiente, Davy publicó un libro de texto de química en el que utilizó la ortografía aluminio . [124] Ambas grafías han coexistido desde entonces. Actualmente su uso es regional: el aluminio domina en Estados Unidos y Canadá; El aluminio prevalece en el resto del mundo de habla inglesa. [125]
En 1812, el científico británico Thomas Young [126] escribió una reseña anónima del libro de Davy, en la que proponía el nombre aluminio en lugar de aluminio , que pensaba que tenía un "sonido menos clásico". [127] Este nombre persistió: aunque la ortografía -um se usó ocasionalmente en Gran Bretaña, el lenguaje científico estadounidense usó -ium desde el principio. [128] La mayoría de los científicos de todo el mundo utilizaron -io en el siglo XIX; [125] y estaba arraigado en varios otros idiomas europeos, como el francés , el alemán y el holandés . [l] En 1828, un lexicógrafo estadounidense, Noah Webster , ingresó sólo la ortografía de aluminio en su Diccionario Americano de la Lengua Inglesa . [129] En la década de 1830, la ortografía -um ganó uso en los Estados Unidos; en la década de 1860, se había convertido en la grafía más común fuera de la ciencia. [128] En 1892, Hall utilizó la ortografía -um en su folleto publicitario para su nuevo método electrolítico de producir el metal, a pesar de su uso constante de la ortografía -ium en todas las patentes que presentó entre 1886 y 1903. Se desconoce si esta grafía se introdujo por error o intencionadamente, pero Hall prefirió el aluminio desde su introducción porque se parecía al platino , el nombre de un metal prestigioso. [130] En 1890, ambas grafías habían sido comunes en los Estados Unidos, siendo la ortografía -ium ligeramente más común; en 1895, la situación se había revertido; en 1900, el aluminio se había vuelto dos veces más común que el aluminio ; en la siguiente década, la ortografía -um dominó el uso estadounidense. En 1925, la Sociedad Química Estadounidense adoptó esta ortografía. [125]
La Unión Internacional de Química Pura y Aplicada (IUPAC) adoptó el aluminio como nombre internacional estándar para el elemento en 1990. [131] En 1993, reconocieron el aluminio como una variante aceptable; [131] la edición más reciente de 2005 de la nomenclatura de química inorgánica de la IUPAC también reconoce esta ortografía. [132] Las publicaciones oficiales de la IUPAC utilizan la ortografía -ium como principal y enumeran ambas cuando es apropiado. [metro]
La producción de aluminio comienza con la extracción de roca de bauxita del suelo. La bauxita se procesa y transforma mediante el proceso Bayer en alúmina , que luego se procesa mediante el proceso Hall-Héroult , dando como resultado el aluminio final.
La producción de aluminio consume mucha energía, por lo que los productores tienden a ubicar fundiciones en lugares donde la energía eléctrica es abundante y barata. [135] La producción de un kilogramo de aluminio requiere 7 kilogramos de equivalente de energía petrolera, en comparación con 1,5 kilogramos para el acero y 2 kilogramos para el plástico. [136] A partir de 2019, las fundiciones de aluminio más grandes del mundo están ubicadas en China, India, Rusia, Canadá y los Emiratos Árabes Unidos, [134] mientras que China es, con diferencia, el principal productor de aluminio con una participación mundial del cincuenta por ciento. cinco por ciento.
Según el informe Existencias de metales en la sociedad del Panel Internacional de Recursos , la reserva global per cápita de aluminio que se utiliza en la sociedad (es decir, en automóviles, edificios, productos electrónicos, etc.) es de 80 kg (180 lb). Gran parte de esto se produce en países más desarrollados (350 a 500 kg (770 a 1100 lb) per cápita) en lugar de países menos desarrollados (35 kg (77 lb) per cápita). [137]
La bauxita se convierte en alúmina mediante el proceso Bayer. La bauxita se mezcla para obtener una composición uniforme y luego se muele. La suspensión resultante se mezcla con una solución caliente de hidróxido de sodio ; Luego, la mezcla se trata en un recipiente digestor a una presión muy superior a la atmosférica, disolviendo el hidróxido de aluminio en bauxita y convirtiendo las impurezas en compuestos relativamente insolubles: [138]
Después de esta reacción, la suspensión se encuentra a una temperatura superior a su punto de ebullición atmosférico. Se enfría eliminando el vapor a medida que se reduce la presión. El residuo de bauxita se separa de la solución y se desecha. La solución, libre de sólidos, se siembra con pequeños cristales de hidróxido de aluminio; esto provoca la descomposición de los iones [Al(OH) 4 ] − en hidróxido de aluminio. Después de que haya precipitado aproximadamente la mitad del aluminio, la mezcla se envía a clasificadores. Se recogen pequeños cristales de hidróxido de aluminio para que sirvan como agentes de siembra; las partículas gruesas se convierten en alúmina mediante calentamiento; el exceso de solución se elimina por evaporación, (si es necesario) se purifica y se recicla. [138]

La conversión de alúmina en aluminio se logra mediante el proceso Hall-Héroult . En este proceso que consume mucha energía, una solución de alúmina en una mezcla fundida (950 y 980 °C (1740 y 1800 °F)) de criolita (Na 3 AlF 6 ) con fluoruro de calcio se electroliza para producir aluminio metálico. El aluminio líquido se hunde hasta el fondo de la solución, se extrae y, por lo general, se vierte en grandes bloques llamados tochos de aluminio para su posterior procesamiento. [43]
Los ánodos de la celda de electrólisis están hechos de carbono (el material más resistente a la corrosión por fluoruro) y se hornean durante el proceso o se hornean previamente. Los primeros, también llamados ánodos de Söderberg, son menos eficientes energéticamente y los vapores liberados durante el horneado son costosos de recolectar, razón por la cual están siendo reemplazados por ánodos precocidos, aunque ahorran energía, energía y mano de obra para precocer los cátodos. El carbono para los ánodos debe ser preferiblemente puro, de modo que ni el aluminio ni el electrolito se contaminen con cenizas. A pesar de la resistividad del carbono contra la corrosión, todavía se consume a un ritmo de 0,4 a 0,5 kg por cada kilogramo de aluminio producido. Los cátodos están hechos de antracita ; Para ellos no se requiere una alta pureza porque las impurezas se lixivian muy lentamente. El cátodo se consume a razón de 0,02 a 0,04 kg por cada kilogramo de aluminio producido. Por lo general, una celda se termina después de 2 a 6 años después de una falla del cátodo. [43]
El proceso Hall-Heroult produce aluminio con una pureza superior al 99%. Se puede realizar una purificación adicional mediante el proceso de Hoopes . Este proceso implica la electrólisis del aluminio fundido con un electrolito de fluoruro de sodio, bario y aluminio. El aluminio resultante tiene una pureza del 99,99%. [43] [139]
La energía eléctrica representa entre el 20 y el 40% del coste de producción de aluminio, dependiendo de la ubicación de la fundición. La producción de aluminio consume aproximadamente el 5% de la electricidad generada en Estados Unidos. [131] Debido a esto, se han investigado alternativas al proceso Hall-Héroult, pero ninguna ha resultado ser económicamente viable. [43]

La recuperación del metal mediante el reciclaje se ha convertido en una tarea importante de la industria del aluminio. El reciclaje fue una actividad de bajo perfil hasta finales de la década de 1960, cuando el uso creciente de latas de aluminio para bebidas lo hizo tomar conciencia del público. [140] El reciclaje implica fundir la chatarra, un proceso que requiere sólo el 5% de la energía utilizada para producir aluminio a partir del mineral, aunque una parte importante (hasta el 15% del material de entrada) se pierde en forma de escoria (óxido similar a la ceniza). . [141] Una unidad de fusión de aluminio produce significativamente menos escoria, con valores reportados por debajo del 1%. [142]
La escoria blanca de la producción primaria de aluminio y de las operaciones de reciclaje secundario todavía contiene cantidades útiles de aluminio que pueden extraerse industrialmente . El proceso produce palanquillas de aluminio, junto con un material de desecho muy complejo. Estos residuos son difíciles de gestionar. Reacciona con el agua, liberando una mezcla de gases (entre otros, hidrógeno , acetileno y amoníaco ), que se enciende espontáneamente al contacto con el aire; [143] el contacto con el aire húmedo produce la liberación de grandes cantidades de gas amoníaco. A pesar de estas dificultades, los residuos se utilizan como relleno de asfalto y hormigón . [144]

La producción mundial de aluminio en 2016 fue de 58,8 millones de toneladas métricas. Superó a la de cualquier otro metal excepto el hierro (1.231 millones de toneladas). [145] [146]
El aluminio casi siempre está aleado, lo que mejora notablemente sus propiedades mecánicas, especialmente cuando está templado . Por ejemplo, las láminas de aluminio y las latas de bebidas habituales son aleaciones de entre un 92 % y un 99 % de aluminio. [147] Los principales agentes de aleación son cobre , zinc , magnesio , manganeso y silicio (por ejemplo, duraluminio ), con niveles de otros metales en un pequeño porcentaje en peso. [148] El aluminio, tanto forjado como fundido, ha sido aleado con: manganeso , silicio , magnesio , cobre y zinc entre otros. [149]

Los principales usos del aluminio se encuentran en: [150]
La gran mayoría (alrededor del 90%) del óxido de aluminio se convierte en aluminio metálico. [138] Al ser un material muy duro ( dureza Mohs 9), [151] la alúmina se usa ampliamente como abrasivo; [152] al ser extraordinariamente inerte químicamente, es útil en entornos altamente reactivos, como las lámparas de sodio de alta presión . [153] El óxido de aluminio se utiliza comúnmente como catalizador para procesos industriales; [138] por ejemplo, el proceso Claus para convertir el sulfuro de hidrógeno en azufre en refinerías y para alquilar aminas . [154] [155] Muchos catalizadores industriales están soportados por alúmina, lo que significa que el costoso material catalizador se dispersa sobre una superficie de alúmina inerte. [156] Otro uso principal es como agente secante o absorbente. [138] [157]

Varios sulfatos de aluminio tienen aplicación industrial y comercial. El sulfato de aluminio (en su forma hidratada) se produce a escala anual de varios millones de toneladas métricas. [158] Aproximadamente dos tercios se consumen en el tratamiento del agua . [158] La siguiente aplicación importante es la fabricación de papel. [158] También se utiliza como mordiente para teñir, encurtir semillas, desodorizar aceites minerales, curtir cuero y en la producción de otros compuestos de aluminio. [158] Anteriormente se utilizaban dos tipos de alumbre, alumbre de amonio y alumbre de potasio , como mordientes y en el curtido de cuero, pero su uso ha disminuido significativamente debido a la disponibilidad de sulfato de aluminio de alta pureza. [158] El cloruro de aluminio anhidro se utiliza como catalizador en las industrias química y petroquímica, en la industria del teñido y en la síntesis de diversos compuestos orgánicos e inorgánicos. [158] Los hidroxicloruros de aluminio se utilizan para purificar el agua, en la industria del papel y como antitranspirantes . [158] El aluminato de sodio se utiliza en el tratamiento del agua y como acelerador de la solidificación del cemento. [158]
Muchos compuestos de aluminio tienen aplicaciones específicas, por ejemplo:

A pesar de su presencia generalizada en la corteza terrestre, el aluminio no tiene ninguna función conocida en biología. [43] A un pH de 6 a 9 (relevante para la mayoría de las aguas naturales), el aluminio precipita en el agua en forma de hidróxido y, por lo tanto, no está disponible; la mayoría de los elementos que se comportan de esta manera no tienen ningún papel biológico o son tóxicos. [171] El sulfato de aluminio tiene una LD 50 de 6207 mg/kg (oral, ratón), lo que corresponde a 435 gramos (aproximadamente una libra) para una persona de 70 kg (150 lb). [43]
El aluminio está clasificado como no cancerígeno por el Departamento de Salud y Servicios Humanos de los Estados Unidos . [172] [n] Una revisión publicada en 1988 dijo que había poca evidencia de que la exposición normal al aluminio presente un riesgo para los adultos sanos, [175] y una revisión de toxicología de múltiples elementos de 2014 no pudo encontrar efectos nocivos del aluminio consumido en Cantidades no superiores a 40 mg/día por kg de masa corporal . [172] La mayor parte del aluminio consumido saldrá del cuerpo en las heces; la mayor parte de la pequeña parte que ingresa al torrente sanguíneo se excretará a través de la orina; [176] sin embargo, algo de aluminio atraviesa la barrera hematoencefálica y se aloja preferentemente en el cerebro de los pacientes con Alzheimer. [177] [178] La evidencia publicada en 1989 indica que, para los pacientes de Alzheimer, el aluminio puede actuar entrecruzando proteínas electrostáticamente , regulando así genes en la circunvolución temporal superior . [179]
El aluminio, aunque raramente, puede provocar osteomalacia resistente a la vitamina D , anemia microcítica resistente a la eritropoyetina y alteraciones del sistema nervioso central. Las personas con insuficiencia renal corren un riesgo especial. [172] La ingestión crónica de silicatos de aluminio hidratados (para controlar el exceso de acidez gástrica) puede provocar que el aluminio se una al contenido intestinal y aumente la eliminación de otros metales, como el hierro o el zinc ; dosis suficientemente altas (>50 g/día) pueden causar anemia. [172]

Durante el incidente de contaminación del agua de Camelford en 1988, la gente de Camelford tuvo su agua potable contaminada con sulfato de aluminio durante varias semanas. Un informe final sobre el incidente de 2013 concluyó que era poco probable que esto hubiera causado problemas de salud a largo plazo. [180]
Se sospecha que el aluminio es una posible causa de la enfermedad de Alzheimer , [181] pero la investigación sobre esto durante más de 40 años no ha encontrado, hasta 2018 [actualizar], ninguna buena evidencia de un efecto causal. [182] [183]
El aluminio aumenta la expresión genética relacionada con el estrógeno en células de cáncer de mama humano cultivadas en el laboratorio. [184] En dosis muy altas, el aluminio se asocia con una función alterada de la barrera hematoencefálica. [185] Un pequeño porcentaje de personas [186] tienen alergias de contacto al aluminio y experimentan erupciones rojas con picazón, dolor de cabeza, dolor muscular, dolor en las articulaciones, mala memoria, insomnio, depresión, asma, síndrome del intestino irritable u otros síntomas al entrar en contacto con los productos. que contiene aluminio. [187]
La exposición al aluminio en polvo o a los vapores de soldadura de aluminio puede causar fibrosis pulmonar . [188] El polvo fino de aluminio puede encenderse o explotar, lo que representa otro peligro en el lugar de trabajo. [189] [190]
Los alimentos son la principal fuente de aluminio. El agua potable contiene más aluminio que los alimentos sólidos; [172] sin embargo, el aluminio de los alimentos puede absorberse más que el aluminio del agua. [191] Las principales fuentes de exposición oral humana al aluminio incluyen alimentos (debido a su uso en aditivos alimentarios, envases de alimentos y bebidas y utensilios de cocina), agua potable (debido a su uso en el tratamiento de agua municipal) y medicamentos que contienen aluminio. (particularmente formulaciones antiácidas/antiulcerosas y de aspirina tamponada). [192] La exposición dietética en los europeos tiene un promedio de 0,2 a 1,5 mg/kg/semana, pero puede llegar a 2,3 mg/kg/semana. [172] Los niveles más altos de exposición al aluminio se limitan principalmente a los mineros, los trabajadores de la producción de aluminio y los pacientes de diálisis . [193]
El consumo de antiácidos , antitranspirantes, vacunas y cosméticos proporcionan posibles vías de exposición. [194] El consumo de alimentos o líquidos ácidos con aluminio mejora la absorción de aluminio, [195] y se ha demostrado que el maltol aumenta la acumulación de aluminio en los tejidos nerviosos y óseos. [196]
En caso de sospecha de ingesta repentina de una gran cantidad de aluminio, el único tratamiento es el mesilato de deferoxamina , que se puede administrar para ayudar a eliminar el aluminio del cuerpo mediante quelación . [197] [198] Sin embargo, esto debe aplicarse con precaución ya que reduce no solo los niveles de aluminio en el cuerpo, sino también los de otros metales como el cobre o el hierro. [197]

Cerca de los sitios mineros se encuentran altos niveles de aluminio; En las centrales eléctricas alimentadas con carbón o en los incineradores se liberan pequeñas cantidades de aluminio al medio ambiente . [176] El aluminio en el aire es arrastrado por la lluvia o normalmente se asienta, pero pequeñas partículas de aluminio permanecen en el aire durante mucho tiempo. [176]
La precipitación ácida es el principal factor natural para movilizar el aluminio de fuentes naturales [172] y la principal razón de los efectos ambientales del aluminio; [199] sin embargo, el principal factor de presencia de aluminio en agua salada y dulce son los procesos industriales que también liberan aluminio al aire. [172]
En el agua, el aluminio actúa como agente tóxico en los animales que respiran por branquias , como los peces, cuando el agua es ácida, en la que el aluminio puede precipitar en las branquias, [200] , lo que provoca la pérdida de plasma , y en los iones de hemolinfa , lo que provoca un fallo osmorregulador . [199] Los complejos orgánicos de aluminio pueden absorberse fácilmente e interferir con el metabolismo en mamíferos y aves, aunque esto rara vez sucede en la práctica. [199]
El aluminio es el principal factor que reduce el crecimiento de las plantas en suelos ácidos. Aunque generalmente es inofensivo para el crecimiento de las plantas en suelos con pH neutro, en suelos ácidos la concentración de cationes tóxicos Al 3+ aumenta y altera el crecimiento y la función de las raíces. [201] [202] [203] [204] El trigo ha desarrollado tolerancia al aluminio, liberando compuestos orgánicos que se unen a cationes de aluminio dañinos . Se cree que el sorgo tiene el mismo mecanismo de tolerancia. [205]
La producción de aluminio presenta sus propios desafíos para el medio ambiente en cada paso del proceso de producción. El mayor desafío son las emisiones de gases de efecto invernadero . [193] Estos gases resultan del consumo eléctrico de las fundiciones y de los subproductos del procesamiento. Los más potentes de estos gases son los perfluorocarbonos procedentes del proceso de fundición. [193] El dióxido de azufre liberado es uno de los principales precursores de la lluvia ácida . [193]
La biodegradación del aluminio metálico es extremadamente rara; la mayoría de los organismos que corroen el aluminio no atacan ni consumen directamente el aluminio, sino que producen desechos corrosivos. [206] [207] El hongo Geotrichum candidum puede consumir el aluminio en discos compactos . [208] [209] [210] La bacteria Pseudomonas aeruginosa y el hongo Cladosporium resinae se detectan comúnmente en tanques de combustible de aviones que utilizan combustibles a base de queroseno (no avgas ), y los cultivos de laboratorio pueden degradar el aluminio. [211]
Los químicos franceses han dado un nuevo nombre a esta tierra pura; alúmina en francés y alúmina en latín. Confieso que no me gusta esta alúmina.
Origen: Formado dentro del inglés, por derivación. Etimones: alúmina n. , sufijo -io , aluminio n.
Etimología: < francés alumine (LB Guyton de Morveau 1782, Observ. sur la Physique 19 378) < latín clásico alūmin- , alūmen alum n. 1 , después del sufijo francés -ine -ine 4 .
El potasio, actuando sobre la alúmina y la glucina, produce sustancias pirofóricas de color gris oscuro, que arden arrojando chispas brillantes y dejando álcali y tierra, y que, arrojadas al agua, la descomponen con gran violencia. El resultado de este experimento no es del todo decisivo en cuanto a la existencia de lo que podríamos llamar aluminio y glucinio.
aluminio coexistió con su sinónimo aluminio n. durante todo el siglo XIX. Desde principios del siglo XX, el aluminio se convirtió gradualmente en la forma predominante en América del Norte; fue adoptado como nombre oficial del metal en los Estados Unidos por la Sociedad Química Estadounidense en 1925. En otros lugares, el aluminio fue reemplazado gradualmente por el aluminio , que fue aceptado como estándar internacional por la IUPAC en 1990.
Los autores aislaron
un hongo artroconidial tipo
Geotrichum
de un disco compacto deteriorado encontrado en Belice (Centroamérica)....En el presente artículo, informamos la purificación y caracterización de un hongo extracelular generador de H
2
O
2.
oxidasa producida por este hongo, que comparte propiedades catalíticas tanto con
P. eryngii
AAO como con
P. simplicissimum
VAO.
Véase también el resumen de Romero et al. 2007.