Un anticuerpo monoclonal ( mAb , más raramente llamado moAb ) es un anticuerpo producido a partir de un linaje celular obtenido mediante la clonación de un glóbulo blanco único . Todos los anticuerpos posteriores derivados de esta manera se remontan a una célula madre única.
Los anticuerpos monoclonales pueden tener afinidad monovalente y unirse únicamente al mismo epítopo (la parte de un antígeno que reconoce el anticuerpo). [3] Por el contrario, los anticuerpos policlonales se unen a múltiples epítopos y generalmente son producidos por varios linajes diferentes de células plasmáticas secretoras de anticuerpos . También se pueden diseñar anticuerpos monoclonales biespecíficos aumentando las dianas terapéuticas de un anticuerpo monoclonal a dos epítopos.
Es posible producir anticuerpos monoclonales que se unan específicamente a casi cualquier sustancia adecuada; luego pueden servir para detectarlo o purificarlo. Esta capacidad se ha convertido en una herramienta de investigación en bioquímica , biología molecular y medicina . Los anticuerpos monoclonales se utilizan en el diagnóstico de enfermedades como el cáncer y las infecciones [4] y se utilizan terapéuticamente en el tratamiento, por ejemplo, del cáncer y de enfermedades inflamatorias .
A principios del siglo XX, el inmunólogo Paul Ehrlich propuso la idea de un Zauberkugel , una " bala mágica ", concebida como un compuesto que apuntaba selectivamente a un organismo causante de enfermedades y podía administrar una toxina a ese organismo. Esto apuntaló el concepto de anticuerpos monoclonales y conjugados de fármacos monoclonales. Ehrlich y Élie Metchnikoff recibieron el Premio Nobel de Fisiología o Medicina en 1908 por proporcionar la base teórica de la inmunología.
En la década de 1970, se conocían los linfocitos que producían un único anticuerpo, en forma de mieloma múltiple , un cáncer que afecta a las células B. Estos anticuerpos o paraproteínas anormales se utilizaron para estudiar la estructura de los anticuerpos, pero aún no era posible producir anticuerpos idénticos y específicos para un antígeno determinado . [5] : 324 En 1973, Jerrold Schwaber describió la producción de anticuerpos monoclonales utilizando células híbridas humano-ratón. [6] Este trabajo sigue siendo ampliamente citado entre quienes utilizan hibridomas de origen humano . [7] En 1975, Georges Köhler y César Milstein lograron realizar fusiones de líneas celulares de mieloma con células B para crear hibridomas que podían producir anticuerpos, específicos contra antígenos conocidos y que eran inmortalizados. [8] Ellos y Niels Kaj Jerne compartieron el Premio Nobel de Fisiología o Medicina en 1984 por el descubrimiento. [8]
En 1988, Gregory Winter y su equipo fueron pioneros en las técnicas para humanizar los anticuerpos monoclonales, [9] eliminando las reacciones que muchos anticuerpos monoclonales provocaban en algunos pacientes. En la década de 1990, la investigación avanzaba en el uso terapéutico de anticuerpos monoclonales, y en 2018, James P. Allison y Tasuku Honjo recibieron el Premio Nobel de Fisiología o Medicina por su descubrimiento de la terapia contra el cáncer mediante la inhibición de la regulación inmune negativa, utilizando anticuerpos monoclonales que previenen enlaces inhibidores. [10]
El trabajo de traducción necesario para implementar estas ideas se atribuye a Lee Nadler. Como se explica en un artículo del NIH, "Fue el primero en descubrir anticuerpos monoclonales dirigidos contra antígenos específicos de células B humanas y, de hecho, todos los antígenos específicos de células B humanas conocidos se descubrieron en su laboratorio. Es un verdadero investigador traslacional, ya que utilizó estos anticuerpos monoclonales para clasificar la leucemia y los linfomas de células B humanos, así como para crear agentes terapéuticos para pacientes. paciente con linfoma de células B)". [11]




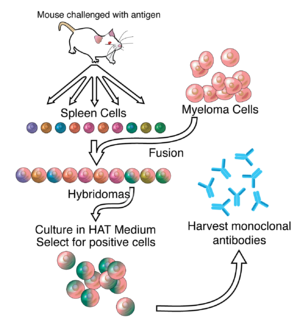
Gran parte del trabajo detrás de la producción de anticuerpos monoclonales tiene sus raíces en la producción de hibridomas, lo que implica identificar células plasmáticas/plasmablastos específicas de antígeno que producen anticuerpos específicos para un antígeno de interés y fusionar estas células con células de mieloma . [8] Las células B de conejo se pueden utilizar para formar un hibridoma de conejo . [12] [13] Se utiliza polietilenglicol para fusionar membranas plasmáticas adyacentes, [14] pero la tasa de éxito es baja, por lo que se utiliza un medio selectivo en el que sólo pueden crecer células fusionadas. Esto es posible porque las células de mieloma han perdido la capacidad de sintetizar hipoxantina-guanina-fosforribosil transferasa (HGPRT), una enzima necesaria para la síntesis de rescate de ácidos nucleicos. La ausencia de HGPRT no es un problema para estas células a menos que también se altere la vía de síntesis de novo de purinas . La exposición de las células a la aminopterina (un análogo del ácido fólico que inhibe la dihidrofolato reductasa ) las incapacita para utilizar la vía de novo y se vuelven completamente auxotróficas para los ácidos nucleicos , por lo que requieren suplementación para sobrevivir.
El medio de cultivo selectivo se denomina medio HAT porque contiene hipoxantina , aminopterina y timidina . Este medio es selectivo para células fusionadas ( hibridoma ). Las células de mieloma no fusionadas no pueden crecer porque carecen de HGPRT y, por tanto, no pueden replicar su ADN. Las células del bazo no fusionadas no pueden crecer indefinidamente debido a su vida útil limitada. Sólo las células híbridas fusionadas, denominadas hibridomas, pueden crecer indefinidamente en el medio porque la célula del bazo suministra HGPRT y la célula del mieloma tiene rasgos que la hacen inmortal (similar a una célula cancerosa).
Esta mezcla de células se diluye luego y se cultivan clones a partir de células parentales únicas en pocillos de microtitulación. Luego se analiza la capacidad de los anticuerpos secretados por los diferentes clones para unirse al antígeno (con una prueba como ELISA o un ensayo de microarrays de antígeno) o inmunotransferencia puntual . Luego se selecciona el clon más productivo y estable para uso futuro.
Los hibridomas pueden cultivarse indefinidamente en un medio de cultivo celular adecuado. También se pueden inyectar en ratones (en la cavidad peritoneal , que rodea el intestino). Allí, producen tumores que secretan un líquido rico en anticuerpos llamado líquido ascítico .
El medio debe enriquecerse durante la selección in vitro para favorecer aún más el crecimiento del hibridoma. Esto se puede lograr mediante el uso de una capa de células de fibrocitos alimentadores o un medio complementario como briclone. Se pueden utilizar medios de cultivo condicionados por macrófagos. Generalmente se prefiere la producción en cultivo celular ya que la técnica de la ascitis es dolorosa para el animal. Cuando existen técnicas alternativas, la ascitis se considera poco ética . [15]
Recientemente se han desarrollado varias tecnologías de anticuerpos monoclonales, [16] como la presentación en fagos , [17] cultivo de células B individuales, [18] amplificación de células individuales de varias poblaciones de células B [19] [20] [21] [22] [23 ] y tecnologías de interrogación de células plasmáticas individuales. A diferencia de la tecnología de hibridoma tradicional, las tecnologías más nuevas utilizan técnicas de biología molecular para amplificar las cadenas pesadas y ligeras de los genes de anticuerpos mediante PCR y producir en sistemas bacterianos o de mamíferos con tecnología recombinante . Una de las ventajas de las nuevas tecnologías es aplicable a múltiples animales, como conejos, llamas, pollos y otros animales de experimentación habituales en el laboratorio.
Después de obtener una muestra de medio de hibridomas cultivados o una muestra de líquido ascítico, se deben extraer los anticuerpos deseados. Los contaminantes de las muestras de cultivos celulares consisten principalmente en componentes del medio, como factores de crecimiento, hormonas y transferrinas . Por el contrario, es probable que la muestra in vivo tenga anticuerpos del huésped, proteasas , nucleasas , ácidos nucleicos y virus . En ambos casos, pueden estar presentes otras secreciones de los hibridomas, como citocinas . También puede haber contaminación bacteriana y, como resultado, endotoxinas secretadas por las bacterias. Dependiendo de la complejidad de los medios necesarios en el cultivo celular y, por tanto, de los contaminantes, puede ser preferible uno u otro método ( in vivo o in vitro ).
Primero se acondiciona o se prepara la muestra para su purificación. Primero se eliminan las células, los restos celulares, los lípidos y el material coagulado, normalmente mediante centrifugación seguida de filtración con un filtro de 0,45 µm. Estas partículas grandes pueden provocar un fenómeno llamado contaminación de la membrana en pasos de purificación posteriores. Además, la concentración de producto en la muestra puede no ser suficiente, especialmente en los casos en que el anticuerpo deseado lo produce una línea celular de baja secreción. Por tanto, la muestra se concentra mediante ultrafiltración o diálisis .
La mayoría de las impurezas cargadas suelen ser aniones como ácidos nucleicos y endotoxinas. Estos pueden separarse mediante cromatografía de intercambio iónico . [24] Se usa cromatografía de intercambio catiónico a un pH lo suficientemente bajo como para que el anticuerpo deseado se una a la columna mientras los aniones fluyen, o se usa la cromatografía de intercambio aniónico a un pH lo suficientemente alto como para que el anticuerpo deseado fluya a través de la columna mientras los aniones se unen a él. También se pueden separar varias proteínas junto con los aniones en función de su punto isoeléctrico (pI). En las proteínas, el punto isoeléctrico (pI) se define como el pH al cual una proteína no tiene carga neta. Cuando el pH > pI, una proteína tiene una carga neta negativa, y cuando el pH < pI, una proteína tiene una carga neta positiva. Por ejemplo, la albúmina tiene un pI de 4,8, que es significativamente menor que el de la mayoría de los anticuerpos monoclonales, que tienen un pI de 6,1. Así, a un pH entre 4,8 y 6,1, es probable que la carga media de las moléculas de albúmina sea más negativa, mientras que las moléculas de mAb tienen carga positiva y, por tanto, es posible separarlas. La transferrina, por otro lado, tiene un pI de 5,9, por lo que no se puede separar fácilmente con este método. Para una buena separación es necesaria una diferencia de pI de al menos 1.
En cambio, la transferrina se puede eliminar mediante cromatografía de exclusión molecular . Este método es una de las técnicas de cromatografía más fiables. Dado que estamos tratando con proteínas, propiedades como la carga y la afinidad no son consistentes y varían con el pH a medida que las moléculas se protonan y desprotonan, mientras que el tamaño permanece relativamente constante. Sin embargo, tiene inconvenientes como baja resolución, baja capacidad y tiempos de elución bajos .
Un método de separación mucho más rápido y de un solo paso es la cromatografía de afinidad de proteínas A/G . El anticuerpo se une selectivamente a la proteína A/G, por lo que se obtiene un alto nivel de pureza (generalmente >80%). Las condiciones generalmente duras de este método pueden dañar los anticuerpos que se dañan fácilmente. Un pH bajo puede romper los enlaces para eliminar el anticuerpo de la columna. Además de afectar posiblemente al producto, un pH bajo puede provocar que la propia proteína A/G se escape de la columna y aparezca en la muestra eluida. Se encuentran disponibles sistemas de tampón de elución suaves que emplean altas concentraciones de sal para evitar la exposición de anticuerpos sensibles a un pH bajo. El costo también es una consideración importante con este método porque la proteína A/G inmovilizada es una resina más cara.
Para lograr la máxima pureza en un solo paso, se puede realizar una purificación por afinidad, utilizando el antígeno para proporcionar especificidad al anticuerpo. En este método, el antígeno utilizado para generar el anticuerpo se une covalentemente a un soporte de agarosa . Si el antígeno es un péptido , comúnmente se sintetiza con una cisteína terminal , lo que permite la unión selectiva a una proteína portadora, como KLH , durante el desarrollo y para respaldar la purificación. Luego, el medio que contiene anticuerpos se incuba con el antígeno inmovilizado, ya sea en lotes o mientras el anticuerpo pasa a través de una columna, donde se une selectivamente y puede retenerse mientras se eliminan las impurezas. Luego se utiliza una elución con un tampón de pH bajo o un tampón de elución más suave y con alto contenido de sal para recuperar el anticuerpo purificado del soporte.
La heterogeneidad del producto es común en los anticuerpos monoclonales y otros productos biológicos recombinantes y normalmente se introduce en sentido ascendente durante la expresión o en sentido descendente durante la fabricación. [ cita necesaria ]
Estas variantes son típicamente agregados, productos de desamidación , variantes de glicosilación , cadenas laterales de aminoácidos oxidadas, así como adiciones de aminoácidos amino y carboxilo terminales. [25] Estos cambios estructurales aparentemente mínimos pueden afectar la estabilidad preclínica y la optimización del proceso, así como la potencia, la biodisponibilidad y la inmunogenicidad del producto terapéutico . El método de purificación generalmente aceptado de corrientes de proceso para anticuerpos monoclonales incluye la captura del producto objetivo con proteína A , elución, acidificación para inactivar posibles virus de mamíferos, seguido de cromatografía iónica , primero con perlas aniónicas y luego con perlas catiónicas. [ cita necesaria ]
La cromatografía de desplazamiento se ha utilizado para identificar y caracterizar estas variantes, a menudo invisibles, en cantidades adecuadas para regímenes de evaluación preclínica posteriores, como estudios farmacocinéticos en animales. [26] [27] El conocimiento adquirido durante la fase de desarrollo preclínico es fundamental para mejorar la comprensión de la calidad del producto y proporciona una base para la gestión de riesgos y una mayor flexibilidad regulatoria. La reciente iniciativa Calidad por Diseño de la Administración de Alimentos y Medicamentos intenta proporcionar orientación sobre el desarrollo y facilitar el diseño de productos y procesos que maximicen el perfil de eficacia y seguridad al tiempo que mejoran la capacidad de fabricación del producto. [28]
La producción de anticuerpos monoclonales recombinantes implica clonación de repertorio , CRISPR/Cas9 o tecnologías de presentación en fagos / presentación en levaduras . [29] La ingeniería de anticuerpos recombinantes implica la producción de anticuerpos mediante el uso de virus o levaduras , en lugar de ratones. Estas técnicas se basan en la clonación rápida de segmentos de genes de inmunoglobulinas para crear bibliotecas de anticuerpos con secuencias de aminoácidos ligeramente diferentes entre las cuales se pueden seleccionar anticuerpos con las especificidades deseadas. [30] Las bibliotecas de anticuerpos de fagos son una variante de las bibliotecas de antígenos de fagos. [31] Estas técnicas se pueden utilizar para mejorar la especificidad con la que los anticuerpos reconocen antígenos, su estabilidad en diversas condiciones ambientales, su eficacia terapéutica y su detectabilidad en aplicaciones de diagnóstico. [32] Se han utilizado cámaras de fermentación para la producción de anticuerpos a gran escala.
Si bien los anticuerpos de ratón y humanos son estructuralmente similares, las diferencias entre ellos fueron suficientes para invocar una respuesta inmune cuando se inyectaron anticuerpos monoclonales murinos en humanos, lo que resultó en su rápida eliminación de la sangre, así como efectos inflamatorios sistémicos y la producción de anticuerpos anti humanos. -anticuerpos de ratón (HAMA).
El ADN recombinante se ha explorado desde finales de los años 1980 para aumentar los tiempos de residencia. En un enfoque llamado "injerto de CDR", [33] el ADN de ratón que codifica la porción de unión de un anticuerpo monoclonal se fusionó con el ADN productor de anticuerpos humanos en células vivas. La expresión de este ADN " quimérico " o "humanizado" a través de cultivos celulares produjo anticuerpos en parte de ratón y en parte humanos. [34] [35]

Desde que se descubrió que se podían generar anticuerpos monoclonales, los científicos se han centrado en la creación de productos totalmente humanos para reducir los efectos secundarios de los anticuerpos humanizados o quiméricos. Se han propuesto varios enfoques exitosos: ratones transgénicos , [36] presentación en fagos [17] y clonación de células B individuales. [dieciséis]
Los anticuerpos monoclonales son más caros de fabricar que las moléculas pequeñas debido a los complejos procesos involucrados y al tamaño general de las moléculas, además de los enormes costos de investigación y desarrollo que implica llevar una nueva entidad química a los pacientes. Su precio permite a los fabricantes recuperar los costos de inversión típicamente grandes, y donde no hay controles de precios, como en Estados Unidos, los precios pueden ser más altos si ofrecen un gran valor. Siete investigadores de la Universidad de Pittsburgh concluyeron: "El precio anual de las terapias con mAb es aproximadamente 100.000 dólares más alto en oncología y hematología que en otras enfermedades", comparándolos por paciente con los de trastornos cardiovasculares o metabólicos, inmunología, enfermedades infecciosas, alergia y oftalmología. [37]
Una vez que se han producido anticuerpos monoclonales para una sustancia determinada, se pueden utilizar para detectar la presencia de esta sustancia. Las proteínas se pueden detectar mediante las pruebas de transferencia Western y de inmunotransferencia puntual . En inmunohistoquímica , los anticuerpos monoclonales se pueden usar para detectar antígenos en secciones de tejido fijadas y, de manera similar, la inmunofluorescencia se puede usar para detectar una sustancia en secciones de tejido congelado o en células vivas.
Los anticuerpos también se pueden utilizar para purificar sus compuestos diana a partir de mezclas, utilizando el método de inmunoprecipitación .
Los anticuerpos monoclonales terapéuticos actúan a través de múltiples mecanismos, como el bloqueo de funciones de moléculas objetivo, la inducción de apoptosis en células que expresan el objetivo o la modulación de vías de señalización. [38] [39] [40]
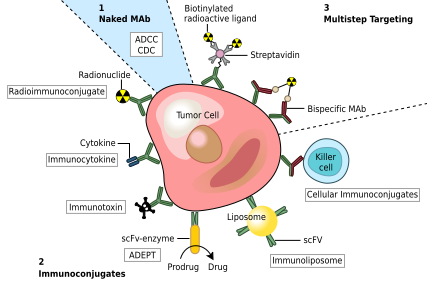
Un posible tratamiento para el cáncer implica anticuerpos monoclonales que se unen sólo a antígenos específicos de las células cancerosas e inducen una respuesta inmune contra la célula cancerosa objetivo. Dichos mAb se pueden modificar para la administración de una toxina , radioisótopo , citocina u otro conjugado activo o para diseñar anticuerpos biespecíficos que puedan unirse con sus regiones Fab tanto al antígeno diana como a un conjugado o célula efectora. Cada anticuerpo intacto puede unirse a receptores celulares u otras proteínas con su región Fc .
Los MAbs aprobados por la FDA para el cáncer incluyen: [42]
Los anticuerpos monoclonales utilizados para enfermedades autoinmunes incluyen infliximab y adalimumab , que son eficaces en la artritis reumatoide , la enfermedad de Crohn , la colitis ulcerosa y la espondilitis anquilosante por su capacidad para unirse e inhibir el TNF-α . [43] Basiliximab y daclizumab inhiben la IL-2 en las células T activadas y, por lo tanto, ayudan a prevenir el rechazo agudo de los trasplantes de riñón. [43] Omalizumab inhibe la inmunoglobulina E humana (IgE) y es útil en el tratamiento del asma alérgica de moderada a grave .
Los anticuerpos monoclonales para aplicaciones de investigación se pueden encontrar directamente a través de proveedores de anticuerpos o mediante el uso de un motor de búsqueda especializado como CiteAb . A continuación se muestran ejemplos de anticuerpos monoclonales clínicamente importantes.
En 2020, las terapias con anticuerpos monoclonales bamlanivimab/etesevimab y casirivimab/imdevimab recibieron autorizaciones de uso de emergencia por parte de la Administración de Alimentos y Medicamentos de EE. UU. para reducir el número de hospitalizaciones, visitas a salas de emergencia y muertes por COVID-19 . [45] [46] En septiembre de 2021, la administración Biden compró anticuerpos monoclonales Regeneron por valor de 2.900 millones de dólares a 2.100 dólares por dosis para frenar la escasez. [48]
En diciembre de 2021, las pruebas de neutralización in vitro indican que no era probable que las terapias con anticuerpos monoclonales (con la excepción de sotrovimab y tixagevimab/cilgavimab ) fueran activas contra la variante Omicron. [49]
Durante 2021-22, dos revisiones Cochrane encontraron evidencia insuficiente para el uso de anticuerpos monoclonales neutralizantes para tratar las infecciones por COVID-19. [50] [51] Las revisiones se aplicaron solo a personas que no estaban vacunadas contra COVID-19, y solo a las variantes de COVID-19 existentes durante los estudios, no a variantes más nuevas, como Omicron. [51]
En marzo de 2024, pemivibart , un fármaco de anticuerpos monoclonales, recibió una autorización de uso de emergencia de la FDA de EE. UU. para su uso como profilaxis previa a la exposición para proteger a determinadas personas inmunocomprometidas de moderada a grave contra la COVID-19. [52] [53]
Varios anticuerpos monoclonales, como bevacizumab y cetuximab , pueden provocar diferentes tipos de efectos secundarios. [54] Estos efectos secundarios se pueden clasificar en efectos secundarios comunes y graves. [55]
Algunos efectos secundarios comunes incluyen:
Entre los posibles efectos secundarios graves se encuentran: [56]