
La catálisis heterogénea es una catálisis en la que la fase de los catalizadores difiere de la de los reactivos o productos . [1] El proceso contrasta con la catálisis homogénea donde los reactivos, los productos y el catalizador existen en la misma fase. La fase distingue no solo entre componentes sólidos , líquidos y gaseosos , sino también mezclas inmiscibles (por ejemplo, aceite y agua ), o en cualquier lugar donde haya una interfaz presente.
La catálisis heterogénea normalmente implica catalizadores en fase sólida y reactivos en fase gaseosa. [2] En este caso, hay un ciclo de adsorción, reacción y desorción molecular que ocurre en la superficie del catalizador. La termodinámica, la transferencia de masa y la transferencia de calor influyen en la velocidad (cinética) de la reacción .
La catálisis heterogénea es muy importante porque permite una producción más rápida a gran escala y la formación selectiva de productos. [3] Aproximadamente el 35% del PIB mundial está influenciado por la catálisis. [4] La producción del 90% de los productos químicos (en volumen) está asistida por catalizadores sólidos. [2] Las industrias química y energética dependen en gran medida de la catálisis heterogénea. Por ejemplo, el proceso Haber-Bosch utiliza catalizadores a base de metales en la síntesis de amoníaco , un componente importante de los fertilizantes; En 2016 se produjeron 144 millones de toneladas de amoníaco. [5]
La adsorción es un paso esencial en la catálisis heterogénea. La adsorción es el proceso mediante el cual una molécula en fase gaseosa (o solución) (el adsorbato) se une a átomos de superficie sólidos (o líquidos) (el adsorbente). Lo contrario de la adsorción es la desorción , en la que el adsorbato se separa del adsorbente. En una reacción facilitada por catálisis heterogénea, el catalizador es el adsorbente y los reactivos son el adsorbato.
Se reconocen dos tipos de adsorción: fisisorción , adsorción débilmente unida, y quimisorción , adsorción fuertemente unida. Muchos procesos de catálisis heterogénea se encuentran entre los dos extremos. El modelo de Lennard-Jones proporciona un marco básico para predecir interacciones moleculares en función de la separación atómica. [6]
En la fisisorción, una molécula se siente atraída por los átomos de la superficie mediante fuerzas de van der Waals . Estas incluyen interacciones dipolo-dipolo, interacciones dipolo inducidas y fuerzas de dispersión de London. Tenga en cuenta que no se forman enlaces químicos entre el adsorbato y el adsorbente, y sus estados electrónicos permanecen relativamente imperturbados. Las energías típicas para la fisisorción son de 3 a 10 kcal/mol. [2] En la catálisis heterogénea, cuando una molécula reactiva se fisisorbe en un catalizador, comúnmente se dice que está en un estado precursor, un estado de energía intermedio antes de la quimisorción, una adsorción más fuertemente unida. [6] Desde el estado precursor, una molécula puede sufrir quimisorción, desorción o migración a través de la superficie. [7] La naturaleza del estado precursor puede influir en la cinética de la reacción. [7]
Cuando una molécula se acerca lo suficiente a los átomos de la superficie como para que sus nubes de electrones se superpongan, puede producirse quimisorción. En la quimisorción, el adsorbato y el adsorbente comparten electrones, lo que significa la formación de enlaces químicos . Las energías típicas para la quimisorción oscilan entre 20 y 100 kcal/mol. [2] Dos casos de quimisorción son:

La mayoría de las reacciones de las superficies metálicas ocurren por propagación en cadena en la que los intermedios catalíticos se producen y consumen cíclicamente. [8] Se pueden describir dos mecanismos principales para las reacciones superficiales para A + B → C. [2]
La mayoría de las reacciones catalizadas de forma heterogénea se describen mediante el modelo de Langmuir-Hinshelwood. [9]
En la catálisis heterogénea, los reactivos se difunden desde la fase fluida en masa para adsorberse en la superficie del catalizador. El sitio de adsorción no siempre es un sitio catalizador activo, por lo que las moléculas reactivas deben migrar a través de la superficie hasta un sitio activo. En el sitio activo, las moléculas reactivas reaccionarán para formar moléculas de producto siguiendo un camino energéticamente más fácil a través de intermedios catalíticos (ver figura a la derecha). Luego, las moléculas del producto se desorben de la superficie y se difunden. El catalizador en sí permanece intacto y libre para mediar reacciones adicionales. Los fenómenos de transporte, como la transferencia de calor y masa, también desempeñan un papel en la velocidad de reacción observada.
Los catalizadores no son activos frente a los reactivos en toda su superficie; sólo lugares específicos poseen actividad catalítica, llamados sitios activos . El área superficial de un catalizador sólido tiene una fuerte influencia en el número de sitios activos disponibles. En la práctica industrial, los catalizadores sólidos suelen ser porosos para maximizar la superficie, alcanzando normalmente entre 50 y 400 m 2 /g. [2] Algunos silicatos mesoporosos , como el MCM-41, tienen áreas superficiales superiores a 1000 m 2 /g. [10] Los materiales porosos son rentables debido a su alta relación superficie-masa y su mayor actividad catalítica.
En muchos casos, se dispersa un catalizador sólido sobre un material de soporte para aumentar el área superficial (distribuir el número de sitios activos) y proporcionar estabilidad. [2] Por lo general, los soportes de catalizadores son materiales inertes y de alto punto de fusión, pero también pueden ser catalíticos en sí mismos. La mayoría de los soportes de catalizadores son porosos (frecuentemente a base de carbono, sílice, zeolita o alúmina) [4] y se eligen por su alta relación superficie-masa. Para una reacción dada, se deben seleccionar soportes porosos de manera que los reactivos y productos puedan entrar y salir del material.
A menudo, se añaden intencionalmente sustancias a la alimentación de reacción o al catalizador para influir en la actividad, selectividad y/o estabilidad catalítica. Estos compuestos se llaman promotores. Por ejemplo, se añade alúmina (Al 2 O 3 ) durante la síntesis de amoníaco para proporcionar una mayor estabilidad al ralentizar los procesos de sinterización en el catalizador de Fe. [2]
El principio de Sabatier puede considerarse una de las piedras angulares de la teoría moderna de la catálisis. [11] El principio de Sabatier establece que la interacción superficie-adsorbatos debe ser en una cantidad óptima: no demasiado débil para ser inerte hacia los reactivos y no demasiado fuerte para envenenar la superficie y evitar la desorción de los productos. [12] La afirmación de que la interacción superficie-adsorbato tiene que ser óptima es cualitativa. Normalmente, el número de adsorbatos y estados de transición asociados con una reacción química es grande, por lo que el óptimo debe encontrarse en un espacio multidimensional. El diseño de catalizadores en un espacio multidimensional no es una tarea computacionalmente viable. Además, dicho proceso de optimización estaría lejos de ser intuitivo. Las relaciones de escala se utilizan para disminuir la dimensionalidad del espacio del diseño del catalizador. [13] Tales relaciones son correlaciones entre las energías de unión de los adsorbatos (o entre las energías de unión de los adsorbatos y los estados de transición, también conocidos como relaciones BEP ) [14] que son "suficientemente similares", por ejemplo, escalamiento de OH versus OOH. [15] La aplicación de relaciones de escala a los problemas de diseño del catalizador reduce en gran medida la dimensionalidad del espacio (a veces hasta tan solo 1 o 2). [16] También se pueden utilizar modelos microcinéticos basados en dichas relaciones de escala para tener en cuenta la cinética asociada con la adsorción, reacción y desorción de moléculas en condiciones específicas de presión o temperatura. [17] Este modelado conduce entonces a conocidos gráficos de volcanes en los que el óptimo cualitativamente descrito por el principio de Sabatier se denomina "cima del volcán". Las relaciones de escala se pueden utilizar no sólo para conectar la energía de los grupos radicales adsorbidos en la superficie (por ejemplo, O*,OH*), [13] sino también para conectar la energía de las moléculas de capa cerrada entre sí o con los adsorbatos radicales homólogos. . [18] Un desafío reciente para los investigadores en ciencias catalíticas es "romper" las relaciones de escala. [19] Las correlaciones que se manifiestan en las relaciones de escala limitan el espacio de diseño del catalizador, impidiendo que se alcance la "cima del volcán". Romper relaciones de escala puede referirse ya sea al diseño de superficies o motivos que no siguen una relación de escala, o aquellos que siguen una relación de escala diferente (que la relación habitual para los adsorbatos asociados) en la dirección correcta: una que puede acercarnos al cima del volcán de reactividad. [16] Además de estudiar la reactividad catalítica, las relaciones de escala se pueden utilizar para estudiar y seleccionar materiales para determinar su selectividad hacia un producto especial. [20]Existe una combinación especial de energías vinculantes que favorecen productos específicos sobre otros. A veces, un conjunto de energías vinculantes que pueden cambiar la selectividad hacia un producto específico "escala" entre sí, por lo que para mejorar la selectividad hay que romper algunas relaciones de escala; un ejemplo de esto es el escalamiento entre las energías de activación oxidativa del metano y del metanol que conduce a la falta de selectividad en la conversión directa de metano en metanol. [21]
La desactivación del catalizador se define como una pérdida de actividad catalítica y/o selectividad a lo largo del tiempo.
Las sustancias que disminuyen la velocidad de reacción se llaman venenos . Los venenos quimisorben la superficie del catalizador y reducen el número de sitios activos disponibles para que se unan las moléculas reactivas. [22] Los venenos comunes incluyen elementos de los grupos V, VI y VII (por ejemplo, S, O, P, Cl), algunos metales tóxicos (por ejemplo, As, Pb) y especies adsorbentes con enlaces múltiples (por ejemplo, CO, hidrocarburos insaturados). [6] [22] Por ejemplo, el azufre interrumpe la producción de metanol al envenenar el catalizador de Cu/ZnO. [23] Las sustancias que aumentan la velocidad de reacción se denominan promotores . Por ejemplo, la presencia de metales alcalinos en la síntesis de amoníaco aumenta la velocidad de disociación del N2 . [23]
La presencia de venenos y promotores puede alterar la energía de activación del paso limitante de la velocidad y afectar la selectividad del catalizador para la formación de ciertos productos. Dependiendo de la cantidad, una sustancia puede resultar favorable o desfavorable para un proceso químico. Por ejemplo, en la producción de etileno, una pequeña cantidad de cloro quimisorbido actuará como promotor mejorando la selectividad del catalizador de Ag hacia el etileno sobre el CO 2 , mientras que demasiado cloro actuará como veneno. [6]
Otros mecanismos para la desactivación del catalizador incluyen:
En la industria, la desactivación de catalizadores cuesta miles de millones cada año debido al cierre de procesos y el reemplazo de catalizadores. [22]
En la industria, se deben considerar muchas variables de diseño, incluido el diseño de reactores y catalizadores en múltiples escalas que van desde subnanómetros hasta decenas de metros. Los reactores de catálisis heterogénea convencionales incluyen reactores discontinuos , continuos y de lecho fluidizado , mientras que las configuraciones más recientes incluyen reactores de lecho fijo, de microcanales y multifuncionales . [6] Otras variables a considerar son las dimensiones del reactor, el área de superficie, el tipo de catalizador, el soporte del catalizador, así como las condiciones operativas del reactor, como la temperatura, la presión y las concentraciones de reactivo.

A continuación se enumeran algunos procesos industriales a gran escala que incorporan catalizadores heterogéneos. [4]

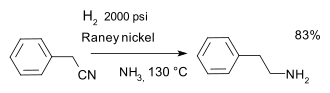
Aunque la mayoría de los catalizadores heterogéneos son sólidos, existen algunas variaciones que tienen valor práctico. Para dos soluciones (líquidos) inmiscibles, una lleva el catalizador mientras que la otra lleva el reactivo. Esta configuración es la base de la catálisis bifásica implementada en la producción industrial de butiraldehído mediante la hidroformilación de propileno. [31]
{{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace ){{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace )