
La bicapa lipídica (o bicapa de fosfolípidos ) es una fina membrana polar formada por dos capas de moléculas lipídicas . Estas membranas son láminas planas que forman una barrera continua alrededor de todas las células . Las membranas celulares de casi todos los organismos y muchos virus están formadas por una bicapa lipídica, al igual que la membrana nuclear que rodea el núcleo celular y las membranas de los orgánulos unidos a membranas en la célula. La bicapa lipídica es la barrera que mantiene los iones , las proteínas y otras moléculas donde son necesarios y evita que se difundan en áreas donde no deberían estar. Las bicapas lipídicas son ideales para esta función, aunque solo tengan unos pocos nanómetros de ancho, [1] porque son impermeables a la mayoría de las moléculas solubles en agua ( hidrófilas ). Las bicapas son particularmente impermeables a los iones, lo que permite a las células regular las concentraciones de sal y el pH mediante el transporte de iones a través de sus membranas mediante proteínas llamadas bombas de iones .
Las bicapas biológicas suelen estar compuestas de fosfolípidos anfifílicos que tienen una cabeza de fosfato hidrófila y una cola hidrófoba que consta de dos cadenas de ácidos grasos. Los fosfolípidos con ciertos grupos principales pueden alterar la química de la superficie de una bicapa y pueden, por ejemplo, servir como señales y como "anclas" para otras moléculas en las membranas de las células. [2] Al igual que las cabezas, las colas de los lípidos también pueden afectar las propiedades de la membrana, por ejemplo determinando la fase de la bicapa. La bicapa puede adoptar un estado de fase de gel sólido a temperaturas más bajas, pero sufrir una transición de fase a un estado fluido a temperaturas más altas, y las propiedades químicas de las colas de los lípidos influyen en la temperatura a la que esto sucede. El empaquetamiento de lípidos dentro de la bicapa también afecta sus propiedades mecánicas, incluida su resistencia al estiramiento y la flexión. Muchas de estas propiedades se han estudiado con el uso de bicapas "modelo" artificiales producidas en un laboratorio. Las vesículas formadas por bicapas modelo también se han utilizado clínicamente para administrar fármacos.
La estructura de las membranas biológicas suele incluir varios tipos de moléculas además de los fosfolípidos que componen la bicapa. Un ejemplo particularmente importante en las células animales es el colesterol , que ayuda a fortalecer la bicapa y disminuir su permeabilidad. El colesterol también ayuda a regular la actividad de determinadas proteínas integrales de membrana . Las proteínas integrales de la membrana funcionan cuando se incorporan a una bicapa lipídica y se mantienen firmemente adheridas a la bicapa lipídica con la ayuda de una cubierta lipídica anular . Debido a que las bicapas definen los límites de la célula y sus compartimentos, estas proteínas de membrana participan en muchos procesos de señalización intra e intercelular. Ciertos tipos de proteínas de membrana participan en el proceso de fusión de dos bicapas. Esta fusión permite la unión de dos estructuras distintas como en la reacción acrosómica durante la fecundación de un óvulo por un espermatozoide , o la entrada de un virus en una célula. Debido a que las bicapas lipídicas son frágiles e invisibles en un microscopio tradicional, su estudio es un desafío. Los experimentos con bicapas a menudo requieren técnicas avanzadas como la microscopía electrónica y la microscopía de fuerza atómica .
Cuando los fosfolípidos se exponen al agua, se autoensamblan formando una lámina de dos capas con las colas hidrofóbicas apuntando hacia el centro de la lámina. Esta disposición da como resultado dos "folletos", cada uno de los cuales es una única capa molecular. El centro de esta bicapa casi no contiene agua y excluye moléculas como azúcares o sales que se disuelven en agua. El proceso de ensamblaje está impulsado por la agregación de moléculas hidrofóbicas (también llamado efecto hidrofóbico ). Este complejo proceso incluye interacciones no covalentes como fuerzas de van der Waals , enlaces electrostáticos y de hidrógeno .

La bicapa lipídica es muy delgada en comparación con sus dimensiones laterales. Si una célula de mamífero típica (diámetro ~10 micrómetros) se ampliara al tamaño de una sandía (~1 pie/30 cm), la bicapa lipídica que constituye la membrana plasmática sería aproximadamente tan gruesa como una hoja de papel de oficina. A pesar de tener sólo unos pocos nanómetros de espesor, la bicapa se compone de varias regiones químicas distintas a lo largo de su sección transversal. Estas regiones y sus interacciones con el agua circundante se han caracterizado durante las últimas décadas con reflectometría de rayos X , [4] dispersión de neutrones , [5] y técnicas de resonancia magnética nuclear .
La primera región a cada lado de la bicapa es el grupo de cabeza hidrófilo. Esta porción de la membrana está completamente hidratada y normalmente tiene un espesor de entre 0,8 y 0,9 nm. En las bicapas de fosfolípidos , el grupo fosfato se encuentra dentro de esta región hidratada, aproximadamente a 0,5 nm fuera del núcleo hidrofóbico. [6] En algunos casos, la región hidratada puede extenderse mucho más, por ejemplo en los lípidos con una proteína grande o una larga cadena de azúcar injertada en la cabeza. Un ejemplo común de tal modificación en la naturaleza es la capa de lipopolisacárido en una membrana externa bacteriana, [7] que ayuda a retener una capa de agua alrededor de la bacteria para prevenir la deshidratación.

Junto a la región hidratada hay una región intermedia que está sólo parcialmente hidratada. Esta capa límite tiene aproximadamente 0,3 nm de espesor. Dentro de esta corta distancia, la concentración de agua cae de 2 M en el lado del grupo de cabeza a casi cero en el lado de la cola (núcleo). [8] [9] El núcleo hidrófobo de la bicapa suele tener un grosor de 3 a 4 nm, pero este valor varía según la longitud de la cadena y la química. [4] [10] El espesor del núcleo también varía significativamente con la temperatura, en particular cerca de una transición de fase. [11]
En muchas bicapas naturales, las composiciones de las valvas de la membrana interna y externa son diferentes. En los glóbulos rojos humanos , la valva interna (citoplasmática) está compuesta principalmente de fosfatidiletanolamina , fosfatidilserina y fosfatidilinositol y sus derivados fosforilados. Por el contrario, la valva externa (extracelular) se basa en fosfatidilcolina , esfingomielina y una variedad de glicolípidos. [12] [13] [14] En algunos casos, esta asimetría se basa en el lugar donde se producen los lípidos en la célula y refleja su orientación inicial. [15] Las funciones biológicas de la asimetría de lípidos no se comprenden perfectamente, aunque está claro que se utiliza en varias situaciones diferentes. Por ejemplo, cuando una célula sufre apoptosis , la fosfatidilserina, normalmente localizada en la valva citoplasmática, se transfiere a la superficie exterior: allí es reconocida por un macrófago que luego elimina activamente la célula moribunda.
La asimetría lipídica surge, al menos en parte, del hecho de que la mayoría de los fosfolípidos se sintetizan y se insertan inicialmente en la monocapa interna: los que constituyen la monocapa externa son luego transportados desde la monocapa interna por una clase de enzimas llamadas flippasas . [16] [17] Otros lípidos, como la esfingomielina, parecen sintetizarse en la valva externa. Las flippasas son miembros de una familia más amplia de moléculas de transporte de lípidos que también incluye flopasas, que transfieren lípidos en la dirección opuesta, y scramblasas, que aleatorizan la distribución de lípidos entre bicapas lipídicas (como en las células apoptóticas). En cualquier caso, una vez que se establece la asimetría lipídica, normalmente no se disipa rápidamente porque el cambio espontáneo de lípidos entre las valvas es extremadamente lento. [18]
Es posible imitar esta asimetría en el laboratorio en sistemas modelo bicapa. Ciertos tipos de vesículas artificiales muy pequeñas automáticamente se volverán ligeramente asimétricas, aunque el mecanismo por el cual se genera esta asimetría es muy diferente al de las células. [19] Utilizando dos monocapas diferentes en la deposición de Langmuir-Blodgett [20] o una combinación de Langmuir-Blodgett y deposición de ruptura de vesículas [21] también es posible sintetizar una bicapa plana asimétrica. Esta asimetría puede perderse con el tiempo, ya que los lípidos en las bicapas soportadas pueden ser propensos a cambiar. [22] Sin embargo, se ha informado que el cambio radical de lípidos es lento en comparación con el colesterol y otras moléculas más pequeñas. [23] [24]
Se ha informado que la organización y la dinámica de las monocapas lipídicas en una bicapa están acopladas. [25] [26] Por ejemplo, la introducción de obstrucciones en una monocapa puede ralentizar la difusión lateral en ambas monocapas. [25] Además, la separación de fases en una monocapa también puede inducir la separación de fases en otra monocapa incluso cuando otra monocapa no puede separarse por sí misma. [26]

A una temperatura determinada, puede existir una bicapa lipídica en fase líquida o gel (sólida). Todos los lípidos tienen una temperatura característica a la que pasan (se funden) de la fase gel a la fase líquida. En ambas fases se evita que las moléculas de lípidos cambien de posición a través de la bicapa, pero en las bicapas en fase líquida un lípido determinado intercambiará ubicaciones con su vecino millones de veces por segundo. Este intercambio de paseo aleatorio permite que los lípidos se difundan y, por tanto, deambulen por la superficie de la membrana. [27] A diferencia de las bicapas en fase líquida, los lípidos en una bicapa en fase gel tienen menos movilidad.
El comportamiento de fase de las bicapas lipídicas está determinado en gran medida por la fuerza de las interacciones atractivas de Van der Waals entre moléculas lipídicas adyacentes. Los lípidos de cola más larga tienen más área sobre la cual interactuar, aumentando la fuerza de esta interacción y, como consecuencia, disminuyendo la movilidad de los lípidos. Por lo tanto, a una temperatura determinada, un lípido de cola corta será más fluido que un lípido de cola larga idéntico. [10] La temperatura de transición también puede verse afectada por el grado de insaturación de las colas lipídicas. Un doble enlace insaturado puede producir una torcedura en la cadena del alcano , alterando el empaquetamiento de los lípidos. Esta interrupción crea un espacio libre adicional dentro de la bicapa que permite una flexibilidad adicional en las cadenas adyacentes. [10] Un ejemplo de este efecto se puede observar en la vida cotidiana, ya que la mantequilla, que tiene un gran porcentaje de grasas saturadas, es sólida a temperatura ambiente, mientras que el aceite vegetal, que es en su mayor parte insaturado, es líquido.
La mayoría de las membranas naturales son una mezcla compleja de diferentes moléculas de lípidos. Si algunos de los componentes son líquidos a una temperatura determinada mientras que otros están en fase de gel, las dos fases pueden coexistir en regiones espacialmente separadas, como un iceberg flotando en el océano. Esta separación de fases juega un papel crítico en los fenómenos bioquímicos porque los componentes de la membrana, como las proteínas, pueden dividirse en una u otra fase [28] y, por lo tanto, concentrarse o activarse localmente. Un componente particularmente importante de muchos sistemas de fase mixta es el colesterol , que modula la permeabilidad de la bicapa, la resistencia mecánica y las interacciones bioquímicas.
Si bien las colas de lípidos modulan principalmente el comportamiento de la fase de la bicapa, es el grupo de cabeza el que determina la química de la superficie de la bicapa. La mayoría de las bicapas naturales están compuestas principalmente de fosfolípidos , pero los esfingolípidos y esteroles como el colesterol también son componentes importantes. [29] De los fosfolípidos, el grupo principal más común es la fosfatidilcolina (PC), que representa aproximadamente la mitad de los fosfolípidos en la mayoría de las células de mamíferos. [30] PC es un grupo de cabeza zwitteriónico , ya que tiene una carga negativa en el grupo fosfato y una carga positiva en la amina pero, debido a que estas cargas locales se equilibran, no tiene carga neta.
Otros grupos principales también están presentes en diversos grados y pueden incluir fosfatidilserina (PS), fosfatidiletanolamina (PE) y fosfatidilglicerol (PG). Estos grupos de cabeza alternativos a menudo confieren una funcionalidad biológica específica que depende en gran medida del contexto. Por ejemplo, la presencia de PS en la membrana extracelular de los eritrocitos es un marcador de apoptosis celular , [31] mientras que la PS en las vesículas de la placa de crecimiento es necesaria para la nucleación de cristales de hidroxiapatita y la posterior mineralización ósea. [32] [33] A diferencia de la PC, algunos de los otros grupos de cabeza llevan una carga neta, que puede alterar las interacciones electrostáticas de moléculas pequeñas con la bicapa. [34]
La función principal de la bicapa lipídica en biología es separar los compartimentos acuosos de su entorno. Sin algún tipo de barrera que delimite el “yo” del “no-yo”, es difícil incluso definir el concepto de organismo o de vida. Esta barrera toma la forma de una bicapa lipídica en todas las formas de vida conocidas, excepto en algunas especies de arqueas que utilizan una monocapa lipídica especialmente adaptada. [7] Incluso se ha propuesto que la primera forma de vida pudo haber sido una simple vesícula lipídica y prácticamente su única capacidad biosintética era la producción de más fosfolípidos . [35] La capacidad de partición de la bicapa lipídica se basa en el hecho de que las moléculas hidrofílicas no pueden cruzar fácilmente el núcleo de la bicapa hidrofóbica , como se analiza en Transporte a través de la bicapa a continuación. El núcleo, las mitocondrias y los cloroplastos tienen dos bicapas lipídicas, mientras que otras estructuras subcelulares están rodeadas por una única bicapa lipídica (como la membrana plasmática, la retícula endoplásmica, el aparato de Golgi y los lisosomas). Ver Organelo . [36]
Los procariotas tienen una sola bicapa lipídica: la membrana celular (también conocida como membrana plasmática). Muchos procariotas también tienen una pared celular , pero la pared celular está compuesta de proteínas o carbohidratos de cadena larga , no de lípidos. Por el contrario, los eucariotas tienen una variedad de orgánulos que incluyen el núcleo , las mitocondrias , los lisosomas y el retículo endoplásmico . Todos estos compartimentos subcelulares están rodeados por una o más bicapas lipídicas y, en conjunto, normalmente comprenden la mayor parte del área de la bicapa presente en la célula. En los hepatocitos hepáticos , por ejemplo, la membrana plasmática representa sólo el dos por ciento del área total de la bicapa de la célula, mientras que el retículo endoplásmico contiene más del cincuenta por ciento y las mitocondrias otro treinta por ciento. [37]

La forma más familiar de señalización celular es probablemente la transmisión sináptica , mediante la cual un impulso nervioso que ha llegado al final de una neurona se transmite a una neurona adyacente mediante la liberación de neurotransmisores . Esta transmisión es posible gracias a la acción de las vesículas sinápticas que, en el interior de la célula, están cargadas de neurotransmisores que se liberarán posteriormente. Estas vesículas cargadas se fusionan con la membrana celular en la terminal presináptica y su contenido se libera al espacio exterior de la célula. Luego, el contenido se difunde a través de la sinapsis hasta la terminal postsináptica.
Las bicapas lipídicas también participan en la transducción de señales a través de su papel como hogar de proteínas integrales de membrana . Esta es una clase de biomolécula extremadamente amplia e importante. Se estima que hasta un tercio del proteoma humano son proteínas de membrana. [38] Algunas de estas proteínas están vinculadas al exterior de la membrana celular. Un ejemplo de esto es la proteína CD59 , que identifica las células como “propias” y así inhibe su destrucción por parte del sistema inmunológico. El virus VIH evade el sistema inmunológico en parte injertando estas proteínas de la membrana del huésped en su propia superficie. [37] Alternativamente, algunas proteínas de membrana penetran completamente a través de la bicapa y sirven para transmitir eventos de señales individuales desde el exterior al interior de la célula. La clase más común de este tipo de proteína es el receptor acoplado a proteína G (GPCR). Los GPCR son responsables de gran parte de la capacidad de la célula para detectar su entorno y, debido a esta importante función, aproximadamente el 40% de todos los fármacos modernos están dirigidos a los GPCR. [39]
Además de los procesos mediados por proteínas y soluciones, también es posible que las bicapas lipídicas participen directamente en la señalización. Un ejemplo clásico de esto es la fagocitosis desencadenada por fosfatidilserina . Normalmente, la fosfatidilserina se distribuye asimétricamente en la membrana celular y está presente sólo en el lado interior. Durante la muerte celular programada, una proteína llamada scramblasa equilibra esta distribución, mostrando fosfatidilserina en la cara de la bicapa extracelular. La presencia de fosfatidilserina desencadena la fagocitosis para eliminar la célula muerta o moribunda.
La bicapa lipídica es una estructura muy difícil de estudiar porque es muy delgada y frágil. A pesar de estas limitaciones se han desarrollado decenas de técnicas durante los últimos setenta años para permitir investigaciones de su estructura y función.
Las mediciones eléctricas son una forma sencilla de caracterizar una función importante de una bicapa: su capacidad para segregar e impedir el flujo de iones en solución. Aplicando un voltaje a través de la bicapa y midiendo la corriente resultante, se determina la resistencia de la bicapa. Esta resistencia suele ser bastante alta (10,8 ohmios -cm 2 o más) [40] ya que el núcleo hidrofóbico es impermeable a las especies cargadas. La presencia de incluso unos pocos agujeros a escala nanométrica produce un aumento espectacular de la corriente. [41] La sensibilidad de este sistema es tal que incluso la actividad de canales iónicos individuales puede resolverse. [42]

Una bicapa lipídica no se puede ver con un microscopio tradicional porque es demasiado delgada, por lo que los investigadores suelen utilizar microscopía de fluorescencia . Una muestra se excita con una longitud de onda de luz y se observa en otra, de modo que sólo se verán moléculas fluorescentes con un perfil de excitación y emisión coincidente.
Una bicapa lipídica natural no es fluorescente, por lo que es necesario unir al menos un tinte fluorescente a algunas de las moléculas de la bicapa. La resolución suele estar limitada a unos pocos cientos de nanómetros, que lamentablemente es mucho mayor que el espesor de una bicapa lipídica.
La microscopía electrónica ofrece una imagen de mayor resolución. En un microscopio electrónico , un haz de electrones enfocados interactúa con la muestra en lugar de un haz de luz como en la microscopía tradicional. Junto con las técnicas de congelación rápida, la microscopía electrónica también se ha utilizado para estudiar los mecanismos de transporte intercelular e intracelular, por ejemplo para demostrar que las vesículas exocitóticas son el medio de liberación química en las sinapsis . [43]
La espectroscopia de 31 P- NMR (resonancia magnética nuclear) se usa ampliamente para estudios de bicapas de fosfolípidos y membranas biológicas en condiciones nativas. El análisis [44] de los espectros de lípidos con 31 P-NMR podría proporcionar una amplia gama de información sobre el empaquetamiento de la bicapa lipídica, las transiciones de fase (fase de gel, fase de cristal líquido fisiológico, fases de ondulación, fases sin bicapa), orientación/dinámica del grupo de cabezas lipídicas. , y propiedades elásticas de la bicapa lipídica pura y como resultado de la unión de proteínas y otras biomoléculas.


Un nuevo método para estudiar las bicapas lipídicas es la microscopía de fuerza atómica (AFM). En lugar de utilizar un haz de luz o partículas, una punta muy pequeña y afilada escanea la superficie haciendo contacto físico con la bicapa y moviéndose a través de ella, como la aguja de un tocadiscos. AFM es una técnica prometedora porque tiene el potencial de generar imágenes con resolución nanométrica a temperatura ambiente e incluso bajo agua o un tampón fisiológico, condiciones necesarias para el comportamiento natural de la bicapa. Utilizando esta capacidad, AFM se ha utilizado para examinar el comportamiento dinámico de las bicapas, incluida la formación de poros (agujeros) transmembrana [45] y transiciones de fase en bicapas soportadas. [46] Otra ventaja es que AFM no requiere marcaje fluorescente o isotópico de los lípidos, ya que la punta de la sonda interactúa mecánicamente con la superficie de la bicapa. Debido a esto, la misma exploración puede obtener imágenes tanto de lípidos como de proteínas asociadas, a veces incluso con resolución de una sola molécula. [45] [47] AFM también puede investigar la naturaleza mecánica de las bicapas lipídicas. [48]
Las bicapas lipídicas exhiben altos niveles de birrefringencia donde el índice de refracción en el plano de la bicapa difiere del perpendicular en hasta 0,1 unidades de índice de refracción . Esto se ha utilizado para caracterizar el grado de orden y alteración en bicapas utilizando interferometría de polarización dual para comprender los mecanismos de interacción de proteínas.
Las bicapas lipídicas son sistemas moleculares complicados con muchos grados de libertad. Por lo tanto, la simulación atomística de la membrana y, en particular, los cálculos ab initio de sus propiedades es difícil y computacionalmente costosa. Recientemente se han realizado con éxito cálculos químicos cuánticos para estimar los momentos dipolares y cuadrupolares de las membranas lipídicas. [49]
La mayoría de las moléculas polares tienen baja solubilidad en el núcleo de hidrocarburo de una bicapa lipídica y, como consecuencia, tienen bajos coeficientes de permeabilidad a través de la bicapa. Este efecto es particularmente pronunciado para las especies cargadas, que tienen coeficientes de permeabilidad incluso más bajos que las moléculas polares neutras. [50] Los aniones suelen tener una mayor tasa de difusión a través de las bicapas que los cationes . [51] [52] En comparación con los iones, las moléculas de agua en realidad tienen una permeabilidad relativamente grande a través de la bicapa, como lo demuestra el hinchamiento osmótico . Cuando una célula o vesícula con una alta concentración de sal interior se coloca en una solución con una baja concentración de sal, se hinchará y eventualmente explotará. Este resultado no se observaría a menos que el agua pudiera atravesar la bicapa con relativa facilidad. La permeabilidad anormalmente grande del agua a través de las bicapas aún no se comprende completamente y sigue siendo objeto de debate activo. [53] Pequeñas moléculas apolares sin carga se difunden a través de bicapas lipídicas muchos órdenes de magnitud más rápido que los iones o el agua. Esto se aplica tanto a las grasas como a los disolventes orgánicos como el cloroformo y el éter . Independientemente de su carácter polar, las moléculas más grandes se difunden más lentamente a través de las bicapas lipídicas que las moléculas pequeñas. [54]
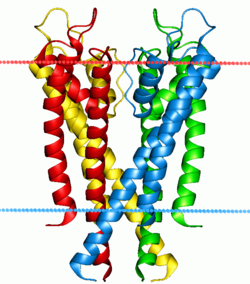
Dos clases especiales de proteínas se ocupan de los gradientes iónicos que se encuentran a través de las membranas celulares y subcelulares en la naturaleza: canales iónicos y bombas de iones . Tanto las bombas como los canales son proteínas integrales de membrana que atraviesan la bicapa, pero sus funciones son bastante diferentes. Las bombas de iones son las proteínas que construyen y mantienen los gradientes químicos mediante la utilización de una fuente de energía externa para mover iones contra el gradiente de concentración a un área de mayor potencial químico . La fuente de energía puede ser ATP , como es el caso de la Na + -K + ATPasa . Alternativamente, la fuente de energía puede ser otro gradiente químico ya existente, como en el antiportador Ca 2+ /Na + . Es mediante la acción de las bombas de iones que las células pueden regular el pH mediante el bombeo de protones .
A diferencia de las bombas de iones, los canales iónicos no generan gradientes químicos, sino que los disipan para realizar un trabajo o enviar una señal. Probablemente el ejemplo más conocido y mejor estudiado sea el canal de Na + dependiente de voltaje , que permite la conducción de un potencial de acción a lo largo de las neuronas . Todas las bombas de iones tienen algún tipo de gatillo o mecanismo de "compuerta". En el ejemplo anterior fue una polarización eléctrica, pero se pueden activar otros canales uniendo un agonista molecular o mediante un cambio conformacional en otra proteína cercana. [55]

Algunas moléculas o partículas son demasiado grandes o demasiado hidrófilas para atravesar una bicapa lipídica. Otras moléculas podrían atravesar la bicapa, pero deben transportarse rápidamente en cantidades tan grandes que el transporte tipo canal no es práctico. En ambos casos, este tipo de carga puede moverse a través de la membrana celular mediante fusión o gemación de vesículas . Cuando se produce una vesícula en el interior de la célula y se fusiona con la membrana plasmática para liberar su contenido al espacio extracelular, este proceso se conoce como exocitosis. En el proceso inverso, una región de la membrana celular se hundirá hacia adentro y finalmente se desprenderá, encerrando una porción del líquido extracelular para transportarlo al interior de la célula. La endocitosis y la exocitosis dependen de maquinaria molecular muy diferente para funcionar, pero los dos procesos están íntimamente relacionados y no podrían funcionar el uno sin el otro. El mecanismo principal de esta interdependencia es la gran cantidad de material lipídico involucrado. [56] En una célula típica, un área de bicapa equivalente a toda la membrana plasmática viajará a través del ciclo de endocitosis/exocitosis en aproximadamente media hora. [57] Si estos dos procesos no se equilibraran entre sí, la célula se hincharía hasta alcanzar un tamaño inmanejable o agotaría completamente su membrana plasmática en poco tiempo.

Exocitosis en procariotas : La exocitosis vesicular de membrana , conocida popularmente como tráfico de vesículas de membrana , un proceso ganador del premio Nobel (año, 2013), se considera tradicionalmente como una prerrogativa de las células eucariotas . [58] Sin embargo, este mito se rompió con la revelación de que las nanovesículas, conocidas popularmente como vesículas bacterianas de membrana externa , liberadas por microbios gramnegativos , translocan moléculas de señal bacterianas a las células huésped o diana [59] para llevar a cabo múltiples procesos a favor de la microbio secretor, por ejemplo, en la invasión de la célula huésped [60] y en las interacciones microbio-ambiente, en general. [61]
La electroporación es el rápido aumento de la permeabilidad de la bicapa inducido por la aplicación de un gran campo eléctrico artificial a través de la membrana. Experimentalmente, la electroporación se utiliza para introducir moléculas hidrófilas en las células. Es una técnica particularmente útil para moléculas grandes altamente cargadas, como el ADN , que nunca se difundiría pasivamente a través del núcleo de la bicapa hidrófoba. [62] Debido a esto, la electroporación es uno de los métodos clave de transfección y transformación bacteriana . Incluso se ha propuesto que la electroporación resultante de la caída de un rayo podría ser un mecanismo de transferencia horizontal natural de genes . [63]
Este aumento de la permeabilidad afecta principalmente al transporte de iones y otras especies hidratadas, lo que indica que el mecanismo es la creación de agujeros llenos de agua a escala nm en la membrana. Aunque tanto la electroporación como la ruptura dieléctrica resultan de la aplicación de un campo eléctrico, los mecanismos involucrados son fundamentalmente diferentes. En la ruptura dieléctrica, el material de barrera se ioniza, creando una vía conductora. La alteración material es, por tanto, de naturaleza química. Por el contrario, durante la electroporación las moléculas de lípidos no se alteran químicamente, sino que simplemente cambian de posición, abriendo un poro que actúa como vía conductora a través de la bicapa a medida que se llena de agua.

Las bicapas lipídicas son estructuras lo suficientemente grandes como para tener algunas de las propiedades mecánicas de los líquidos o sólidos. El módulo de compresión del área K a , el módulo de flexión K b y la energía del borde se pueden utilizar para describirlos. Las bicapas lipídicas sólidas también tienen un módulo de corte , pero como cualquier líquido, el módulo de corte es cero para las bicapas fluidas. Estas propiedades mecánicas afectan el funcionamiento de la membrana. Ka y K b afectan la capacidad de las proteínas y moléculas pequeñas para insertarse en la bicapa, [64] [65] y se ha demostrado que las propiedades mecánicas de la bicapa alteran la función de los canales iónicos activados mecánicamente. [66] Las propiedades mecánicas de la bicapa también determinan qué tipos de estrés puede soportar una célula sin romperse. Aunque las bicapas lipídicas pueden doblarse fácilmente, la mayoría no puede estirarse más que un pequeño porcentaje antes de romperse. [67]
Como se analizó en la sección Estructura y organización, la atracción hidrófoba de las colas lipídicas en el agua es la fuerza principal que mantiene unidas las bicapas lipídicas. Por lo tanto, el módulo elástico de la bicapa está determinado principalmente por la cantidad de área adicional que queda expuesta al agua cuando las moléculas de lípidos se separan. [68] No es sorprendente, dada esta comprensión de las fuerzas involucradas, que los estudios hayan demostrado que K a varía fuertemente con la presión osmótica [69] pero sólo débilmente con la longitud de la cola y la insaturación. [10] Debido a que las fuerzas involucradas son tan pequeñas, es difícil determinar experimentalmente K a . La mayoría de las técnicas requieren microscopía sofisticada y equipos de medición muy sensibles. [48] [70]
A diferencia de K a , que es una medida de cuánta energía se necesita para estirar la bicapa, K b es una medida de cuánta energía se necesita para doblar o flexionar la bicapa. Formalmente, el módulo de flexión se define como la energía necesaria para deformar una membrana desde su curvatura intrínseca a alguna otra curvatura. La curvatura intrínseca se define por la relación entre el diámetro del grupo de la cabeza y el del grupo de la cola. Para los lípidos PC de dos colas, esta relación es casi uno, por lo que la curvatura intrínseca es casi cero. Si un lípido en particular tiene una desviación demasiado grande de la curvatura intrínseca cero, no formará una bicapa y, en cambio, formará otras fases, como micelas o micelas invertidas. La adición de pequeñas moléculas hidrófilas como la sacarosa a liposomas laminares de lípidos mixtos elaborados a partir de membranas de tilacoides ricas en galactolípidos desestabiliza las bicapas hacia la fase micelar . [71] Normalmente, K b no se mide experimentalmente sino que se calcula a partir de mediciones de K a y el espesor de la bicapa, ya que los tres parámetros están relacionados.
es una medida de cuánta energía se necesita para exponer el borde de una bicapa al agua rompiendo la bicapa o creando un agujero en ella. El origen de esta energía es el hecho de que la creación de dicha interfaz expone algunas de las colas de lípidos al agua, pero se desconoce la orientación exacta de estos lípidos fronterizos. Existe cierta evidencia de que pueden coexistir poros tanto hidrofóbicos (colas rectas) como hidrofílicos (cabezas curvadas). [72] [73]

La fusión es el proceso mediante el cual dos bicapas lipídicas se fusionan, dando como resultado una estructura conectada. Si esta fusión se produce completamente a través de ambas valvas de ambas bicapas, se forma un puente lleno de agua y las soluciones contenidas en las bicapas pueden mezclarse. Alternativamente, si en el proceso de fusión sólo interviene una valva de cada bicapa, se dice que las bicapas están hemifusionadas. La fusión está involucrada en muchos procesos celulares, en particular en eucariotas , ya que la célula eucariota está ampliamente subdividida por membranas de bicapa lipídica. La exocitosis , la fertilización de un óvulo mediante la activación de los espermatozoides y el transporte de productos de desecho al lisozoma son algunos de los muchos procesos eucarióticos que dependen de alguna forma de fusión. Incluso la entrada de patógenos puede estar gobernada por la fusión, ya que muchos virus recubiertos con dos capas tienen proteínas de fusión dedicadas para entrar en la célula huésped.
Hay cuatro pasos fundamentales en el proceso de fusión. [30] Primero, las membranas involucradas deben agregarse, acercándose entre sí dentro de varios nanómetros. En segundo lugar, las dos bicapas deben entrar en contacto muy estrecho (dentro de unos pocos angstroms). Para lograr este estrecho contacto, las dos superficies deben deshidratarse al menos parcialmente, ya que el agua superficial unida normalmente presente hace que las bicapas se repelan fuertemente. La presencia de iones, en particular cationes divalentes como magnesio y calcio, afecta fuertemente este paso. [74] [75] Una de las funciones críticas del calcio en el cuerpo es regular la fusión de membranas. En tercer lugar, debe formarse una desestabilización en un punto entre las dos bicapas, distorsionando localmente sus estructuras. Se desconoce la naturaleza exacta de esta distorsión. Una teoría es que debe formarse un "tallo" muy curvado entre las dos bicapas. [76] Los defensores de esta teoría creen que explica por qué la fosfatidiletanolamina, un lípido altamente curvado, promueve la fusión. [77] Finalmente, en el último paso de la fusión, este defecto puntual crece y los componentes de las dos bicapas se mezclan y difunden lejos del sitio de contacto.


La situación se complica aún más cuando se considera la fusión in vivo ya que la fusión biológica casi siempre está regulada por la acción de proteínas asociadas a la membrana . Las primeras de estas proteínas en ser estudiadas fueron las proteínas de fusión viral, que permiten que un virus envuelto inserte su material genético en la célula huésped (los virus envueltos son aquellos rodeados por una bicapa lipídica; algunos otros solo tienen una cubierta proteica). Las células eucariotas también utilizan proteínas de fusión, las mejor estudiadas de las cuales son las SNARE . Las proteínas SNARE se utilizan para dirigir todo el tráfico intracelular vesicular . A pesar de años de estudio, todavía se desconoce mucho sobre la función de esta clase de proteínas. De hecho, todavía existe un debate activo sobre si los SNARE están relacionados con el acoplamiento temprano o participan más tarde en el proceso de fusión facilitando la hemifusión. [79]
En estudios de biología molecular y celular, a menudo es deseable inducir artificialmente la fusión. La adición de polietilenglicol (PEG) provoca la fusión sin agregación significativa ni alteración bioquímica. Este procedimiento se utiliza ahora ampliamente, por ejemplo mediante la fusión de células B con células de mieloma . [80] El “ hibridoma ” resultante de esta combinación expresa un anticuerpo deseado según lo determinado por la célula B involucrada, pero se inmortaliza debido al componente de melanoma. La fusión también se puede inducir artificialmente mediante electroporación en un proceso conocido como electrofusión. Se cree que este fenómeno resulta de los bordes energéticamente activos formados durante la electroporación, que pueden actuar como punto de defecto local para nuclear el crecimiento del tallo entre dos bicapas. [81]
Las bicapas lipídicas se pueden crear artificialmente en el laboratorio para permitir a los investigadores realizar experimentos que no se pueden realizar con bicapas naturales. También se pueden utilizar en el campo de la biología sintética , para definir los límites de las células artificiales . Estos sistemas sintéticos se denominan bicapas lipídicas modelo. Hay muchos tipos diferentes de modelos de bicapas, cada uno de los cuales tiene ventajas y desventajas experimentales. Pueden elaborarse con lípidos sintéticos o naturales. Entre los sistemas modelo más comunes se encuentran:
Hasta la fecha, la aplicación comercial de mayor éxito de las bicapas lipídicas ha sido el uso de liposomas para la administración de fármacos, especialmente para el tratamiento del cáncer. (Nota: el término "liposoma" es en esencia sinónimo de " vesícula ", excepto que vesícula es un término general para la estructura, mientras que liposoma se refiere únicamente a vesículas artificiales, no naturales). La idea básica de la administración de fármacos liposomales es que el fármaco está encapsulado en La solución dentro del liposoma luego se inyecta en el paciente. Estos liposomas cargados de fármaco viajan a través del sistema hasta que se unen al sitio objetivo y se rompen, liberando el fármaco. En teoría, los liposomas deberían ser un sistema ideal de administración de fármacos, ya que pueden aislar casi cualquier fármaco hidrófilo, pueden injertarse con moléculas para atacar tejidos específicos y pueden ser relativamente no tóxicos, ya que el cuerpo posee vías bioquímicas para degradar los lípidos. [82]
La primera generación de liposomas de administración de fármacos tenía una composición lipídica simple y adolecía de varias limitaciones. La circulación en el torrente sanguíneo era extremadamente limitada debido tanto a la limpieza renal como a la fagocitosis . El refinamiento de la composición de lípidos para ajustar la fluidez, la densidad de carga superficial y la hidratación de la superficie dio como resultado vesículas que adsorben menos proteínas del suero y, por lo tanto, el sistema inmunológico las reconoce menos fácilmente . [83] El avance más significativo en esta área fue el injerto de polietilenglicol (PEG) en la superficie del liposoma para producir vesículas "sigilas", que circulan durante largos períodos sin eliminación inmune o renal. [84]
Los primeros liposomas furtivos se dirigieron pasivamente a los tejidos tumorales . Debido a que los tumores inducen una angiogénesis rápida e incontrolada, son especialmente "fugas" y permiten que los liposomas salgan del torrente sanguíneo a un ritmo mucho mayor que el del tejido normal. [85] Más recientemente [ ¿cuándo? ] Se ha trabajado para injertar anticuerpos u otros marcadores moleculares en la superficie del liposoma con la esperanza de unirlos activamente a un tipo de célula o tejido específico. [86] Algunos ejemplos de este enfoque ya se encuentran en ensayos clínicos. [87]
Otra posible aplicación de las bicapas lipídicas es el campo de los biosensores . Dado que la bicapa lipídica es la barrera entre el interior y el exterior de la célula, también es el sitio de una extensa transducción de señales. A lo largo de los años, los investigadores han intentado aprovechar este potencial para desarrollar un dispositivo basado en bicapa para el diagnóstico clínico o la detección de bioterrorismo. El progreso ha sido lento en esta área y, aunque algunas empresas han desarrollado sistemas automatizados de detección basados en lípidos, todavía están dirigidos a la comunidad investigadora. Entre ellos se incluyen Biacore (ahora GE Healthcare Life Sciences), que ofrece un chip desechable para utilizar bicapas lipídicas en estudios de cinética de unión [88] y Nanion Inc., que ha desarrollado un sistema automatizado de sujeción de parches . [89] También se están buscando otras aplicaciones más exóticas, como el uso de poros de membrana de bicapa lipídica para la secuenciación de ADN por parte de Oxford Nanolabs. Hasta la fecha, esta tecnología no ha demostrado ser comercialmente viable.
Una bicapa lipídica soportada (SLB) como se describió anteriormente ha logrado un éxito comercial como técnica de detección para medir la permeabilidad de los fármacos. Esta técnica paralela de ensayo de permeabilidad de membrana artificial PAMPA mide la permeabilidad a través de cócteles de lípidos específicamente formulados que se encuentran altamente correlacionados con los cultivos de Caco-2 , [90] [ 91] el tracto gastrointestinal , [92] la sangre. barrera cerebral [93] y piel. [94]
A principios del siglo XX, los científicos habían llegado a creer que las células están rodeadas por una fina barrera similar al aceite, [95] pero se desconocía la naturaleza estructural de esta membrana. Dos experimentos realizados en 1925 sentaron las bases para llenar este vacío. Al medir la capacitancia de las soluciones de eritrocitos , Hugo Fricke determinó que la membrana celular tenía un espesor de 3,3 nm. [96]
Aunque los resultados de este experimento fueron precisos, Fricke malinterpretó los datos en el sentido de que la membrana celular es una sola capa molecular. El Prof. Dr. Evert Gorter [97] (1881-1954) y F. Grendel de la Universidad de Leiden abordaron el problema desde una perspectiva diferente, extendiendo los lípidos de los eritrocitos como una monocapa en un canal Langmuir-Blodgett . Cuando compararon el área de la monocapa con el área de superficie de las células, encontraron una proporción de dos a uno. [98] Análisis posteriores mostraron varios errores y suposiciones incorrectas con este experimento pero, por casualidad, estos errores se cancelaron y, a partir de estos datos defectuosos, Gorter y Grendel sacaron la conclusión correcta: que la membrana celular es una bicapa lipídica. [30]
Esta teoría fue confirmada mediante el uso de microscopía electrónica a finales de la década de 1950. Aunque no publicó el primer estudio de microscopía electrónica de bicapas lipídicas [99], J. David Robertson fue el primero en afirmar que las dos bandas oscuras densas en electrones eran los grupos de cabeza y las proteínas asociadas de dos monocapas lipídicas opuestas. [100] [101] En este trabajo, Robertson propuso el concepto de "membrana unitaria". Esta fue la primera vez que la estructura bicapa se asignó universalmente a todas las membranas celulares, así como a las membranas de los orgánulos .
Casi al mismo tiempo, el desarrollo de membranas modelo confirmó que la bicapa lipídica es una estructura estable que puede existir independientemente de las proteínas. Al "pintar" una solución de lípidos en un solvente orgánico a través de una abertura, Mueller y Rudin pudieron crear una bicapa artificial y determinar que exhibía fluidez lateral, alta resistencia eléctrica y autocuración en respuesta a la punción, [ 102] todos que son propiedades de una membrana celular natural. Unos años más tarde, Alec Bangham demostró que las bicapas, en forma de vesículas lipídicas, también podían formarse simplemente exponiendo una muestra de lípidos secos al agua. [103] Este fue un avance importante, ya que demostró que las bicapas lipídicas se forman espontáneamente mediante autoensamblaje y no requieren una estructura de soporte estampada.
En 1977, Kunitake y Okahata prepararon una membrana bicapa totalmente sintética, a partir de un único compuesto orgánico, bromuro de didodecildimetilamonio. [104] Muestra claramente que la membrana bicapa fue ensamblada por las fuerzas intermoleculares .