El tecnecio es un elemento químico de símbolo Tc y número atómico 43. Es el elemento más ligero cuyos isótopos son todos radiactivos . El tecnecio y el prometio son los únicos elementos radiactivos cuyos vecinos en el sentido del número atómico son ambos estables. Todo el tecnecio disponible se produce como elemento sintético . El tecnecio natural es un producto de fisión espontánea en el mineral de uranio y el mineral de torio (la fuente más común), o el producto de la captura de neutrones en los minerales de molibdeno . Este metal de transición cristalino de color gris plateado se encuentra entre el manganeso y el renio en el grupo 7 de la tabla periódica , y sus propiedades químicas son intermedias entre las de ambos elementos adyacentes. El isótopo natural más común es el 99Tc , solo en trazas.
Muchas de las propiedades del tecnecio habían sido predichas por Dmitri Mendeleev antes de que fuera descubierto; Mendeleev notó un vacío en su tabla periódica y le dio al elemento no descubierto el nombre provisional de ekamanganeso ( Em ). En 1937, el tecnecio se convirtió en el primer elemento predominantemente artificial en ser producido, de ahí su nombre (del griego technetos , 'artificial', + -io ).
Un isómero nuclear emisor de rayos gamma de vida corta , el tecnecio-99m , se utiliza en medicina nuclear para una amplia variedad de pruebas, como el diagnóstico de cáncer de huesos. El estado fundamental del nucleido tecnecio-99 se utiliza como una fuente libre de rayos gamma de partículas beta . Los isótopos de tecnecio de vida larga producidos comercialmente son subproductos de la fisión del uranio-235 en reactores nucleares y se extraen de las barras de combustible nuclear . Debido a que incluso el isótopo de tecnecio de vida más larga tiene una vida media relativamente corta (4,21 millones de años), la detección de tecnecio en gigantes rojas en 1952 ayudó a demostrar que las estrellas pueden producir elementos más pesados .
Desde la década de 1860 hasta 1871, las primeras formas de la tabla periódica propuestas por Dmitri Mendeleev contenían un espacio entre el molibdeno (elemento 42) y el rutenio (elemento 44). En 1871, Mendeleev predijo que este elemento faltante ocuparía el lugar vacío debajo del manganeso y tendría propiedades químicas similares. Mendeleev le dio el nombre provisional de eka-manganeso (de eka , la palabra sánscrita para uno ) porque estaba un lugar por debajo del elemento conocido manganeso. [6]
Muchos de los primeros investigadores, tanto antes como después de la publicación de la tabla periódica, estaban ansiosos por ser los primeros en descubrir y nombrar el elemento faltante. Su ubicación en la tabla sugería que debería ser más fácil de encontrar que otros elementos no descubiertos. Esto resultó no ser así debido a la radiactividad del tecnecio.
.jpg/440px-Periodisches_System_der_Elemente_(1904-1945,_now_Gdansk_University_of_Technology).jpg)
Los químicos alemanes Walter Noddack , Otto Berg e Ida Tacke informaron del descubrimiento del elemento 75 y del elemento 43 en 1925, y nombraron al elemento 43 masurium (en honor a Masuria en Prusia oriental , ahora en Polonia , la región de donde se originó la familia de Walter Noddack). [11] Este nombre causó un resentimiento significativo en la comunidad científica, porque se interpretó como una referencia a una serie de victorias del ejército alemán sobre el ejército ruso en la región de Masuria durante la Primera Guerra Mundial; como los Noddack permanecieron en sus puestos académicos mientras los nazis estaban en el poder, las sospechas y la hostilidad contra su afirmación de descubrir el elemento 43 continuaron. [12] El grupo bombardeó columbita con un haz de electrones y dedujo que el elemento 43 estaba presente al examinar los espectrogramas de emisión de rayos X. [13] La longitud de onda de los rayos X producidos está relacionada con el número atómico mediante una fórmula derivada por Henry Moseley en 1913. El equipo afirmó detectar una débil señal de rayos X en una longitud de onda producida por el elemento 43. Los experimentadores posteriores no pudieron replicar el descubrimiento, y fue descartado como un error. [14] [15] Aún así, en 1933, una serie de artículos sobre el descubrimiento de elementos citaron el nombre masurium para el elemento 43. [16] Se han hecho algunos intentos más recientes para rehabilitar las afirmaciones de los Noddacks, pero son refutadas por el estudio de Paul Kuroda sobre la cantidad de tecnecio que podría haber estado presente en los minerales que estudiaron: no podría haber excedido 3 × 10 −11 μg/kg de mineral, y por lo tanto habría sido indetectable por los métodos de los Noddacks. [12] [17]
El descubrimiento del elemento 43 fue finalmente confirmado en un experimento de 1937 en la Universidad de Palermo en Sicilia por Carlo Perrier y Emilio Segrè . [18] A mediados de 1936, Segrè visitó los Estados Unidos, primero la Universidad de Columbia en Nueva York y luego el Laboratorio Nacional Lawrence Berkeley en California. Convenció al inventor del ciclotrón, Ernest Lawrence, para que le permitiera recuperar algunas piezas desechadas del ciclotrón que se habían vuelto radiactivas . Lawrence le envió por correo una lámina de molibdeno que había sido parte del deflector del ciclotrón. [19]
Segrè reclutó a su colega Perrier para intentar demostrar, a través de la química comparativa, que la actividad del molibdeno provenía de hecho de un elemento con el número atómico 43. En 1937, lograron aislar los isótopos tecnecio-95m y tecnecio-97 . [20] [21] [ disputado – discutir ] Los funcionarios de la Universidad de Palermo querían que llamaran a su descubrimiento panormium , en honor al nombre latino de Palermo , Panormus . En 1947, [20] el elemento 43 recibió el nombre de la palabra griega technetos ( τεχνητός ), que significa 'artificial', ya que fue el primer elemento en ser producido artificialmente. [7] [11] Segrè regresó a Berkeley y conoció a Glenn T. Seaborg . Aislaron el isótopo metaestable tecnecio-99m , que ahora se utiliza en unos diez millones de procedimientos de diagnóstico médico al año. [22]
En 1952, el astrónomo Paul W. Merrill detectó en California la firma espectral del tecnecio (específicamente longitudes de onda de 403,1 nm , 423,8 nm, 426,2 nm y 429,7 nm) en la luz de las gigantes rojas de tipo S. [23] Las estrellas estaban cerca del final de sus vidas, pero eran ricas en el elemento de vida corta, lo que indicaba que se estaba produciendo en las estrellas mediante reacciones nucleares . Esa evidencia reforzó la hipótesis de que los elementos más pesados son el producto de la nucleosíntesis en las estrellas. [21] Más recientemente, tales observaciones proporcionaron evidencia de que los elementos se forman por captura de neutrones en el proceso s . [24]
Desde ese descubrimiento, se han hecho muchas búsquedas en materiales terrestres para encontrar fuentes naturales de tecnecio. En 1962, se aisló e identificó tecnecio-99 en pechblenda del Congo Belga en cantidades muy pequeñas (alrededor de 0,2 ng/kg), [24] donde se origina como un producto de fisión espontánea del uranio-238 . El reactor de fisión nuclear natural en Oklo contiene evidencia de que se produjeron cantidades significativas de tecnecio-99 y que desde entonces se han desintegrado en rutenio-99 . [24]
El tecnecio es un metal radiactivo de color gris plateado con una apariencia similar al platino , que se obtiene comúnmente como un polvo gris. [25] La estructura cristalina del metal puro a granel es hexagonal compacta , y las estructuras cristalinas del metal puro nanodisperso son cúbicas . El tecnecio nanodisperso no tiene un espectro de RMN dividido, mientras que el tecnecio a granel hexagonal tiene el espectro de RMN de Tc-99 dividido en 9 satélites. [25] [26] El tecnecio atómico tiene líneas de emisión características en longitudes de onda de 363,3 nm , 403,1 nm, 426,2 nm, 429,7 nm y 485,3 nm. [27] Se informaron los parámetros de celda unitaria del metal ortorrómbico Tc cuando Tc está contaminado con carbono ( a = 0,2805(4), b = 0,4958(8), c = 0,4474(5)·nm para Tc-C con 1,38 % en peso de C y a = 0,2815(4), b = 0,4963(8), c = 0,4482(5)•nm para Tc-C con 1,96 % en peso de C ). [28] La forma del metal es ligeramente paramagnética , lo que significa que sus dipolos magnéticos se alinean con los campos magnéticos externos , pero asumirán orientaciones aleatorias una vez que se elimine el campo. [ 29] El tecnecio monocristalino puro y metálico se convierte en un superconductor de tipo II a temperaturas inferiores a 7,46 K. [30] [b] Por debajo de esta temperatura, el tecnecio tiene una profundidad de penetración magnética muy alta , mayor que cualquier otro elemento excepto el niobio . [31]
El tecnecio se encuentra en el grupo 7 de la tabla periódica, entre el renio y el manganeso . Como predice la ley periódica , sus propiedades químicas están entre esos dos elementos. De los dos, el tecnecio se parece más al renio, particularmente en su inercia química y tendencia a formar enlaces covalentes . [32] Esto es consistente con la tendencia de los elementos del período 5 a parecerse más a sus contrapartes en el período 6 que en el período 4 debido a la contracción de los lantánidos . A diferencia del manganeso, el tecnecio no forma fácilmente cationes ( iones con carga neta positiva). El tecnecio exhibe nueve estados de oxidación de −1 a +7, siendo +4, +5 y +7 los más comunes. [33] El tecnecio se disuelve en agua regia , ácido nítrico y ácido sulfúrico concentrado , pero no en ácido clorhídrico de cualquier concentración. [25]
El tecnecio metálico se empaña lentamente en el aire húmedo [33] y, en forma de polvo, arde en oxígeno . Al reaccionar con hidrógeno a alta presión, forma el hidruro TcH 1.3 [34] y al reaccionar con carbono forma Tc 6 C, [28] con un parámetro de celda de 0.398 nm, así como el carburo nanodisperso de bajo contenido de carbono con un parámetro de 0.402 nm. [35]
El tecnecio puede catalizar la destrucción de la hidracina por el ácido nítrico , y esta propiedad se debe a su multiplicidad de valencias. [36] Esto causó un problema en la separación del plutonio del uranio en el procesamiento de combustible nuclear , donde la hidracina se utiliza como reductor protector para mantener el plutonio en el estado trivalente en lugar del estado tetravalente más estable. El problema se vio agravado por la extracción con disolventes mutuamente mejorada del tecnecio y el circonio en la etapa anterior, [37] y requirió una modificación del proceso.
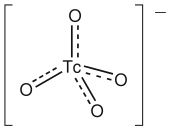
La forma más común de tecnecio, a la que se puede acceder fácilmente, es el pertecnetato de sodio , Na[TcO 4 ]. La mayor parte de este material se produce por desintegración radiactiva de [ 99 MoO 4 ] 2− : [38] [39]
Pertecnetato ( TcO−
4) está sólo débilmente hidratado en soluciones acuosas, [40] y se comporta de manera análoga al anión perclorato, ambos tetraédricos . A diferencia del permanganato ( MnO−
4), es sólo un agente oxidante débil .
El heptóxido de tecnecio está relacionado con el pertecnetato . Este sólido volátil de color amarillo pálido se produce por oxidación del metal Tc y sus precursores relacionados:
Es un óxido metálico molecular, análogo al heptóxido de manganeso . Adopta una estructura centrosimétrica con dos tipos de enlaces Tc−O con longitudes de enlace de 167 y 184 pm. [41]
El heptóxido de tecnecio se hidroliza a pertecnetato y ácido pertecnético , dependiendo del pH: [42] [43]
El HTcO 4 es un ácido fuerte. En ácido sulfúrico concentrado , [TcO 4 ] − se convierte en la forma octaédrica TcO 3 (OH)(H 2 O) 2 , la base conjugada del hipotético complejo triaquo [TcO 3 (H 2 O) 3 ] + . [44]
El tecnecio forma dióxido , [45] disulfuro , diselenuro y ditelururo . Se forma un Tc2S7 mal definido al tratar el pertecnato con sulfuro de hidrógeno. Se descompone térmicamente en disulfuro y azufre elemental. [ 46 ] De manera similar, el dióxido se puede producir por reducción del Tc2O7 .
A diferencia del caso del renio, no se ha aislado un trióxido para el tecnecio. Sin embargo, se ha identificado TcO 3 en la fase gaseosa mediante espectrometría de masas . [47]
El tecnecio forma el complejo TcH2−
9La sal de potasio es isoestructural con ReH2−
9. [48] También se informó la formación de TcH1,3 a partir de elementos a alta presión. [34]

Se conocen los siguientes haluros de tecnecio binarios (que contienen solo dos elementos): TcF 6 , TcF 5 , TcCl 4 , TcBr 4 , TcBr 3 , α-TcCl 3 , β-TcCl 3 , TcI 3 , α-TcCl 2 y β-TcCl 2 . Los estados de oxidación varían de Tc(VI) a Tc(II). Los haluros de tecnecio exhiben diferentes tipos de estructura, como complejos octaédricos moleculares, cadenas extendidas, láminas en capas y grupos de metales dispuestos en una red tridimensional. [49] [50] Estos compuestos se producen combinando el metal y el halógeno o mediante reacciones menos directas.
El TcCl 4 se obtiene por cloración del metal Tc o Tc 2 O 7. Al calentarlo, el TcCl 4 produce los cloruros Tc(III) y Tc(II) correspondientes. [50]
La estructura del TcCl 4 está compuesta por infinitas cadenas en zigzag de octaedros de TcCl 6 que comparten aristas . Es isomorfo a los tetracloruros de metales de transición de circonio , hafnio y platino . [50]
.jpg/440px-Chloro-containing_coordination_complexes_of_technetium_(Tc-99).jpg)
Existen dos polimorfos de tricloruro de tecnecio , α- y β-TcCl 3 . El polimorfo α también se denota como Tc 3 Cl 9 . Adopta una estructura bioctaédrica confacial . [51] Se prepara tratando el cloroacetato Tc 2 (O 2 CCH 3 ) 4 Cl 2 con HCl. Al igual que Re 3 Cl 9 , la estructura del polimorfo α consiste en triángulos con distancias MM cortas. β-TcCl 3 presenta centros octaédricos de Tc, que están organizados en pares, como se ve también para el tricloruro de molibdeno . TcBr 3 no adopta la estructura de ninguna de las fases de tricloruro. En cambio, tiene la estructura del tribromuro de molibdeno , que consiste en cadenas de octaedros confaciales con contactos Tc—Tc cortos y largos alternados. El TcI 3 tiene la misma estructura que la fase de alta temperatura del TiI 3 , presentando cadenas de octaedros confaciales con contactos Tc—Tc iguales. [50]
Se conocen varios haluros de tecnecio aniónicos. Los tetrahaluros binarios se pueden convertir en hexahaluros [TcX 6 ] 2− (X = F, Cl, Br, I), que adoptan una geometría molecular octaédrica . [24] Los haluros más reducidos forman cúmulos aniónicos con enlaces Tc–Tc. La situación es similar para los elementos relacionados de Mo, W, Re. Estos cúmulos tienen la nuclearidad Tc 4 , Tc 6 , Tc 8 y Tc 13 . Los cúmulos más estables Tc 6 y Tc 8 tienen formas de prisma donde los pares verticales de átomos de Tc están conectados por triples enlaces y los átomos planos por enlaces simples. Cada átomo de tecnecio hace seis enlaces, y los electrones de valencia restantes pueden saturarse con un átomo de halógeno axial y dos átomos de halógeno de puente como el cloro o el bromo . [52]

El tecnecio forma una variedad de complejos de coordinación con ligandos orgánicos. Muchos de ellos han sido ampliamente investigados debido a su relevancia para la medicina nuclear . [53]
El tecnecio forma una variedad de compuestos con enlaces Tc–C, es decir, complejos de organotecnecio. Los miembros destacados de esta clase son complejos con ligandos CO, areno y ciclopentadienilo. [54] El carbonilo binario Tc2 ( CO) 10 es un sólido volátil blanco. [55] En esta molécula, dos átomos de tecnecio están unidos entre sí; cada átomo está rodeado por octaedros de cinco ligandos carbonílicos. La longitud del enlace entre átomos de tecnecio, 303 pm, [56] [57] es significativamente mayor que la distancia entre dos átomos en el tecnecio metálico (272 pm). Carbonilos similares están formados por congéneres del tecnecio , manganeso y renio. [58] El interés en los compuestos de organotecnecio también ha sido motivado por aplicaciones en medicina nuclear . [54] El tecnecio también forma complejos aquocarbonílicos, siendo uno de los complejos más destacados [Tc(CO) 3 (H 2 O) 3 ] + , que son inusuales en comparación con otros carbonilos metálicos. [54]
El tecnecio, con número atómico Z = 43, es el elemento de menor número en la tabla periódica para el cual todos los isótopos son radiactivos . El segundo elemento exclusivamente radiactivo más ligero, el prometio , tiene número atómico 61. [33] Los núcleos atómicos con un número impar de protones son menos estables que aquellos con números pares, incluso cuando el número total de nucleones (protones + neutrones ) es par, [59] y los elementos con números impares tienen menos isótopos estables .
Los isótopos radiactivos más estables son el tecnecio-97, con una vida media de4,21 ± 0,16 millones de años y tecnecio-98 con4,2 ± 0,3 millones de años; las mediciones actuales de sus vidas medias dan intervalos de confianza superpuestos correspondientes a una desviación estándar y, por lo tanto, no permiten una asignación definitiva del isótopo más estable del tecnecio. El siguiente isótopo más estable es el tecnecio-99, que tiene una vida media de 211.100 años. [1] Se han caracterizado otros treinta y cuatro radioisótopos con números de masa que van desde 86 a 122. [1] La mayoría de ellos tienen vidas medias inferiores a una hora, siendo las excepciones el tecnecio-93 (2,73 horas), el tecnecio-94 (4,88 horas), el tecnecio-95 (20 horas) y el tecnecio-96 (4,3 días). [60]
El modo de desintegración primario para los isótopos más ligeros que el tecnecio-98 ( 98 Tc ) es la captura de electrones , produciendo molibdeno ( Z = 42). [61] Para el tecnecio-98 y los isótopos más pesados, el modo primario es la emisión beta (la emisión de un electrón o positrón ), produciendo rutenio ( Z = 44), con la excepción de que el tecnecio-100 puede desintegrarse tanto por emisión beta como por captura de electrones. [61] [62]
El tecnecio también tiene numerosos isómeros nucleares , que son isótopos con uno o más nucleones excitados . El tecnecio-97m ( 97mTc ; "m" significa metaestabilidad ) es el más estable, con una vida media de 91 días y una energía de excitación de 0,0965 MeV. [60] A este le siguen el tecnecio-95m (61 días, 0,03 MeV) y el tecnecio-99m (6,01 horas, 0,142 MeV). [60]
El tecnecio-99 ( 99 Tc) es un producto importante de la fisión del uranio-235 ( 235 U), lo que lo convierte en el isótopo de tecnecio más común y más fácilmente disponible. Un gramo de tecnecio-99 produce 6,2 × 108 desintegracionespor segundo (en otras palabras, laactividad específicadel99Tces 0,62 GBq/g).[29]
El tecnecio se encuentra de forma natural en la corteza terrestre en concentraciones diminutas de aproximadamente 0,003 partes por billón. El tecnecio es tan raro porque las vidas medias de 97Tc y 98Tc son de solo 4,2 millones de años. Han pasado más de mil de esos períodos desde la formación de la Tierra , por lo que la probabilidad de supervivencia de incluso un átomo de tecnecio primordial es efectivamente cero. Sin embargo, existen pequeñas cantidades como productos de fisión espontánea en minerales de uranio . Un kilogramo de uranio contiene aproximadamente 1 nanogramo (10 −9 g) equivalente a diez billones de átomos de tecnecio. [21] [63] [64] Algunas estrellas gigantes rojas con los tipos espectrales S-, M- y N muestran una línea de absorción espectral que indica la presencia de tecnecio. [25] [65] Estas gigantes rojas se conocen informalmente como estrellas de tecnecio .
En contraste con la rara ocurrencia natural, cada año se producen grandes cantidades de tecnecio-99 a partir de barras de combustible nuclear gastadas , que contienen varios productos de fisión. La fisión de un gramo de uranio-235 en reactores nucleares produce 27 mg de tecnecio-99, lo que le da al tecnecio un rendimiento de producto de fisión del 6,1%. [29] Otros isótopos fisionables producen rendimientos similares de tecnecio, como el 4,9% a partir del uranio-233 y el 6,21% a partir del plutonio-239 . [66] Se estima que entre 1983 y 1994 se produjeron 49.000 T Bq (78 toneladas métricas ) de tecnecio en reactores nucleares, con mucho la fuente dominante de tecnecio terrestre. [67] [68] Solo una fracción de la producción se utiliza comercialmente. [c]
El tecnecio-99 se produce por la fisión nuclear del uranio-235 y del plutonio-239. Por lo tanto, está presente en los residuos radiactivos y en la lluvia radiactiva de las explosiones de bombas de fisión . Su desintegración, medida en bequerelios por cantidad de combustible gastado, es el principal contribuyente a la radiactividad de los residuos nucleares después de unos 104 ~106 añosdespués de la creación de los residuos nucleares.[67]Se estima que entre 1945 y 1994se liberaron al medio ambienteBqlas pruebas nucleares.[67][69]La cantidad de tecnecio-99 de los reactores nucleares liberada al medio ambiente hasta 1986 es del orden de 1000 TBq (unos 1600 kg), principalmente porel reprocesamiento de combustible nuclear; la mayor parte de este se descargó en el mar. Los métodos de reprocesamiento han reducido las emisiones desde entonces, pero a partir de 2005 la principal liberación de tecnecio-99 al medio ambiente es por lade Sellafield, que liberó unos 550 TBq (unos 900 kg) entre 1995 y 1999 en elmar de Irlanda.[68] A partir de 2000, la cantidad se ha limitado por reglamentación a 90 TBq (unos 140 kg) al año.[70]El vertido de tecnecio al mar ha provocado la contaminación de algunos productos del mar con cantidades minúsculas de este elemento. Por ejemplo,la langosta europeay el pescado del oestede Cumbriacontienen alrededor de 1 Bq/kg de tecnecio.[71][72][d]
El isótopo metaestable tecnecio-99m se produce continuamente como producto de fisión a partir de la fisión del uranio o el plutonio en los reactores nucleares :
Debido a que el combustible usado se deja reposar durante varios años antes de su reprocesamiento, todo el molibdeno-99 y el tecnecio-99m se han desintegrado para cuando los productos de fisión se separan de los principales actínidos en el reprocesamiento nuclear convencional . El líquido que queda después de la extracción de plutonio-uranio ( PUREX ) contiene una alta concentración de tecnecio como TcO−
4Pero casi todo esto es tecnecio-99, no tecnecio-99m. [74]
La gran mayoría del tecnecio-99m utilizado en el trabajo médico se produce irradiando objetivos de uranio altamente enriquecido en un reactor, extrayendo molibdeno-99 de los objetivos en instalaciones de reprocesamiento, [39] y recuperando en el centro de diagnóstico el tecnecio-99m producido por la descomposición del molibdeno-99. [75] [76] Molibdeno-99 en forma de molibdato MoO2−
4se adsorbe sobre alúmina ácida ( Al
2Oh
3) en un cromatógrafo de columna blindado dentro de un generador de tecnecio-99m ("vaca de tecnecio", también llamada ocasionalmente "vaca de molibdeno"). El molibdeno-99 tiene una vida media de 67 horas, por lo que el tecnecio-99m de vida corta (vida media: 6 horas), que resulta de su desintegración, se produce constantemente. [21] El pertecnetato soluble TcO −
4Luego se puede extraer químicamente mediante elución con una solución salina . Un inconveniente de este proceso es que requiere blancos que contengan uranio-235, que están sujetos a las precauciones de seguridad de los materiales fisionables. [77] [78]

Casi dos tercios del suministro mundial proviene de dos reactores: el National Research Universal Reactor en Chalk River Laboratories en Ontario, Canadá, y el High Flux Reactor en Nuclear Research and Consultancy Group en Petten, Países Bajos. Todos los reactores principales que producen tecnecio-99m se construyeron en la década de 1960 y están cerca del final de su vida útil . Los dos nuevos reactores canadienses del Experimento Multipropósito de Física Aplicada en Red , planificados y construidos para producir el 200% de la demanda de tecnecio-99m, liberaron a todos los demás productores de la tarea de construir sus propios reactores. Con la cancelación de los reactores ya probados en 2008, el suministro futuro de tecnecio-99m se volvió problemático. [79]
La larga vida media del tecnecio-99 y su potencial para formar especies aniónicas crean una preocupación importante para la eliminación a largo plazo de desechos radiactivos . Muchos de los procesos diseñados para eliminar los productos de fisión en plantas de reprocesamiento apuntan a especies catiónicas como el cesio (por ejemplo, cesio-137 ) y el estroncio (por ejemplo, estroncio-90 ). Por lo tanto, el pertecnetato escapa a través de esos procesos. Las opciones de eliminación actuales favorecen el entierro en roca continental geológicamente estable. El peligro principal con tal práctica es la probabilidad de que los desechos entren en contacto con el agua, lo que podría filtrar contaminación radiactiva al medio ambiente. El pertecnetato aniónico y el yoduro tienden a no adsorberse en las superficies de los minerales y es probable que se eliminen. En comparación, el plutonio , el uranio y el cesio tienden a unirse a las partículas del suelo. El tecnecio podría inmovilizarse en algunos entornos, como la actividad microbiana en los sedimentos del fondo del lago, [80] y la química ambiental del tecnecio es un área de investigación activa. [81]
En el CERN se ha demostrado un método alternativo de eliminación del tecnecio-99, la transmutación . En este proceso, el tecnecio (tecnecio-99 como blanco metálico) se bombardea con neutrones para formar el tecnecio-100, de corta duración (vida media = 16 segundos), que se desintegra por desintegración beta en rutenio -100 estable. Si el objetivo es la recuperación de rutenio utilizable, se necesita un blanco de tecnecio extremadamente puro; si en el blanco hay pequeñas trazas de actínidos menores como el americio y el curio , es probable que sufran fisión y formen más productos de fisión que aumentan la radiactividad del blanco irradiado. Es probable que la formación de rutenio-106 (vida media 374 días) a partir de la "fisión fresca" aumente la actividad del metal rutenio final, que requerirá un tiempo de enfriamiento más largo después de la irradiación antes de que se pueda utilizar el rutenio. [82]
La separación real del tecnecio-99 del combustible nuclear gastado es un proceso largo. Durante el reprocesamiento del combustible , sale como un componente del líquido residual altamente radiactivo. Después de permanecer allí durante varios años, la radiactividad se reduce a un nivel en el que la extracción de los isótopos de larga duración, incluido el tecnecio-99, se vuelve factible. Una serie de procesos químicos produce el metal tecnecio-99 de alta pureza. [83]
El molibdeno-99 , que se desintegra para formar tecnecio-99m, se puede formar mediante la activación neutrónica del molibdeno-98. [84] Cuando es necesario, otros isótopos de tecnecio no se producen en cantidades significativas por fisión, sino que se fabrican mediante la irradiación neutrónica de los isótopos originales (por ejemplo, el tecnecio-97 se puede fabricar mediante la irradiación neutrónica del rutenio-96 ). [85]
En 1971 se demostró la viabilidad de la producción de tecnecio-99m mediante el bombardeo de protones de 22 MeV de un objetivo de molibdeno-100 en ciclotrones médicos tras la reacción 100 Mo(p,2n) 99m Tc. [86] La reciente escasez de tecnecio-99m médico reavivó el interés en su producción mediante el bombardeo de protones de objetivos de molibdeno-100 enriquecidos isotópicamente (>99,5%). [87] [88] Se están investigando otras técnicas para obtener molibdeno-99 a partir de molibdeno-100 mediante reacciones (n,2n) o (γ,n) en aceleradores de partículas. [89] [90] [91]

El tecnecio-99m ("m" indica que se trata de un isómero nuclear metaestable ) se utiliza en pruebas médicas con isótopos radiactivos . Por ejemplo, el tecnecio-99m es un trazador radiactivo que los equipos de imágenes médicas rastrean en el cuerpo humano. [21] [87] Es muy adecuado para el papel porque emite rayos gamma de 140 keV fácilmente detectables , y su vida media es de 6,01 horas (lo que significa que aproximadamente el 94% se desintegra en tecnecio-99 en 24 horas). [29] La química del tecnecio le permite unirse a una variedad de compuestos bioquímicos, cada uno de los cuales determina cómo se metaboliza y se deposita en el cuerpo, y este único isótopo se puede utilizar para una multitud de pruebas de diagnóstico. Más de 50 radiofármacos comunes se basan en tecnecio-99m para imágenes y estudios funcionales del cerebro , el músculo cardíaco, la tiroides , los pulmones , el hígado , la vesícula biliar , los riñones , el esqueleto , la sangre y los tumores . [92]
El isótopo de vida más larga, el tecnecio-95m, con una vida media de 61 días, se utiliza como trazador radiactivo para estudiar el movimiento del tecnecio en el medio ambiente y en los sistemas vegetales y animales. [93]
El tecnecio-99 se desintegra casi en su totalidad por desintegración beta, emitiendo partículas beta con energías bajas constantes y sin rayos gamma acompañantes. Además, su larga vida media significa que esta emisión disminuye muy lentamente con el tiempo. También se puede extraer a una alta pureza química e isotópica de los residuos radiactivos. Por estas razones, es un emisor beta estándar del Instituto Nacional de Estándares y Tecnología (NIST) y se utiliza para la calibración de equipos. [94] El tecnecio-99 también se ha propuesto para dispositivos optoelectrónicos y baterías nucleares a escala nanométrica . [95]
Al igual que el renio y el paladio , el tecnecio puede servir como catalizador . En procesos como la deshidrogenación del alcohol isopropílico , es un catalizador mucho más eficaz que el renio o el paladio. Sin embargo, su radiactividad es un problema importante en aplicaciones catalíticas seguras. [96]
Cuando el acero se sumerge en agua, la adición de una pequeña concentración (55 ppm ) de pertecnetato de potasio (VII) al agua protege al acero de la corrosión, [97] incluso si la temperatura se eleva a 250 °C (523 K). [98] Por esta razón, el pertecnetato se ha utilizado como inhibidor de corrosión anódica para el acero, aunque la radiactividad del tecnecio plantea problemas que limitan esta aplicación a sistemas autónomos. [99] Mientras que (por ejemplo) CrO2−
4También puede inhibir la corrosión, requiere una concentración diez veces mayor. En un experimento, una muestra de acero al carbono se mantuvo en una solución acuosa de pertecnetato durante 20 años y todavía no se corroyó. [98] El mecanismo por el cual el pertecnetato previene la corrosión no se entiende bien, pero parece implicar la formación reversible de una capa superficial delgada ( pasivación ). Una teoría sostiene que el pertecnetato reacciona con la superficie del acero para formar una capa de dióxido de tecnecio que evita una mayor corrosión; el mismo efecto explica cómo se puede utilizar polvo de hierro para eliminar el pertecnetato del agua. El efecto desaparece rápidamente si la concentración de pertecnetato cae por debajo de la concentración mínima o si se agrega una concentración demasiado alta de otros iones. [100]
Como se ha señalado, la naturaleza radiactiva del tecnecio (3 MBq/L en las concentraciones requeridas) hace que esta protección contra la corrosión sea poco práctica en casi todas las situaciones. [97] Sin embargo, se propuso (pero nunca se adoptó) la protección contra la corrosión mediante iones pertecnetato para su uso en reactores de agua en ebullición . [100]
El tecnecio no desempeña ninguna función biológica natural y no se encuentra normalmente en el cuerpo humano. [25] El tecnecio se produce en grandes cantidades por fisión nuclear y se propaga más fácilmente que muchos radionucleidos. Parece tener una baja toxicidad química. Por ejemplo, no se pudo detectar ningún cambio significativo en la fórmula sanguínea, el peso corporal y de los órganos y el consumo de alimentos en ratas que ingirieron hasta 15 μg de tecnecio-99 por gramo de alimento durante varias semanas. [101] En el cuerpo, el tecnecio se convierte rápidamente en el estable TcO−
4ion, que es altamente soluble en agua y se excreta rápidamente. La toxicidad radiológica del tecnecio (por unidad de masa) es una función del compuesto, el tipo de radiación para el isótopo en cuestión y la vida media del isótopo. [102]
Todos los isótopos del tecnecio deben manipularse con cuidado. El isótopo más común, el tecnecio-99, es un emisor beta débil; las paredes del material de vidrio de laboratorio detienen esta radiación. El principal riesgo al trabajar con tecnecio es la inhalación de polvo; esta contaminación radiactiva en los pulmones puede suponer un riesgo significativo de cáncer. Para la mayoría de los trabajos, basta con manipularlo con cuidado en una campana extractora de humos y no se necesita una caja de guantes . [103]