Un tumor suprarrenal o masa suprarrenal [2] es cualquier neoplasia benigna o maligna de la glándula suprarrenal , varias de las cuales son notables por su tendencia a producir en exceso hormonas endocrinas . El cáncer suprarrenal es la presencia de tumores suprarrenales malignos e incluye neuroblastoma , carcinoma adrenocortical y algunos feocromocitomas suprarrenales . La mayoría de los feocromocitomas suprarrenales y todos los adenomas adrenocorticales son tumores benignos, que no hacen metástasis ni invaden tejidos cercanos, pero pueden causar problemas de salud importantes al desequilibrar las hormonas.
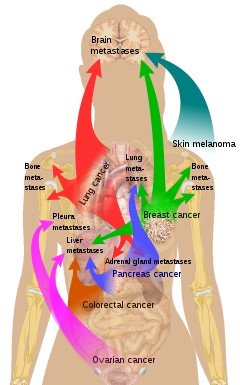
La metástasis en una o ambas glándulas suprarrenales es la forma más común de lesión suprarrenal maligna y el segundo tumor suprarrenal más común después de los adenomas benignos. [4] Los tumores primarios en estos casos son más comúnmente cáncer de pulmón (39%), cáncer de mama (35%), melanoma maligno , cáncer del tracto gastrointestinal , cáncer de páncreas y cáncer renal . [4]
La corteza suprarrenal está compuesta por tres capas distintas de células endocrinas que producen hormonas esteroides esenciales . Estas incluyen los glucocorticoides , que son esenciales para la regulación del azúcar en sangre y el sistema inmunológico , así como para la respuesta al estrés fisiológico ; el mineralcorticoide aldosterona , que regula la presión arterial y la función renal ; y ciertas hormonas sexuales . Tanto los tumores benignos como los malignos de la corteza suprarrenal pueden producir hormonas esteroides, con importantes consecuencias clínicas. [ cita requerida ]
Los adenomas adrenocorticales son tumores benignos de la corteza suprarrenal que son extremadamente comunes (presentes en el 1-10% de las personas en la autopsia). No deben confundirse con los "nódulos" adrenocorticales, que no son neoplasias verdaderas. Los adenomas adrenocorticales son poco comunes en pacientes menores de 30 años y tienen la misma incidencia en ambos sexos. [ cita requerida ] La importancia clínica de estas neoplasias es doble. En primer lugar, se han detectado como hallazgos incidentales con una frecuencia cada vez mayor en los últimos años, debido al uso creciente de tomografías computarizadas y resonancias magnéticas en una variedad de entornos médicos. Esto puede dar lugar a pruebas adicionales costosas y procedimientos invasivos para descartar la ligera posibilidad de un carcinoma adrenocortical temprano . En segundo lugar, una minoría (alrededor del 15%) de los adenomas adrenocorticales son "funcionales", lo que significa que producen glucocorticoides , mineralocorticoides y/o esteroides sexuales , lo que provoca trastornos endocrinos como el síndrome de Cushing , el síndrome de Conn (hiperaldosteronismo), la virilización de las mujeres o la feminización de los hombres. Los adenomas adrenocorticales funcionales se pueden curar quirúrgicamente. [ cita requerida ]
La mayoría de los adenomas corticosuprarrenales tienen una dimensión mayor de menos de 2 cm y un peso de menos de 50 gramos. Sin embargo, el tamaño y el peso de los tumores corticosuprarrenales ya no se consideran un signo confiable de benignidad o malignidad. Macroscópicamente, los adenomas corticosuprarrenales son tumores solitarios, encapsulados y bien delimitados con una superficie sólida, homogénea y amarillenta. La necrosis y la hemorragia son hallazgos raros. [ cita requerida ]
El carcinoma adrenocortical (ACC) es un cáncer poco común y muy agresivo de las células de la corteza suprarrenal, que puede presentarse en niños o adultos. Los ACC pueden ser "funcionales", produciendo hormonas esteroides y la consiguiente disfunción endocrina similar a la que se observa en muchos adenomas adrenocorticales, pero muchos no lo son. Debido a su ubicación profunda en el retroperitoneo , la mayoría de los carcinomas adrenocorticales no se diagnostican hasta que han crecido bastante. Con frecuencia invaden vasos grandes, como la vena renal y la vena cava inferior , y hacen metástasis a través de los vasos linfáticos y la sangre hasta los pulmones y otros órganos. El tratamiento más eficaz es la cirugía , aunque no es factible para muchos pacientes y el pronóstico general de la enfermedad es malo. La quimioterapia , la radioterapia y la terapia hormonal también se pueden emplear en el tratamiento de esta enfermedad. [ cita requerida ]
La médula suprarrenal está ubicada anatómicamente en el centro de cada glándula suprarrenal y está compuesta por células neuroendocrinas (cromafines) que producen y liberan epinefrina (adrenalina) en el torrente sanguíneo en respuesta a la activación del sistema nervioso simpático . El neuroblastoma y el feocromocitoma son los dos tumores más importantes que surgen de la médula suprarrenal. Ambos tumores también pueden surgir de sitios extrasuprarrenales, específicamente, en los paraganglios de la cadena simpática . [ cita requerida ]
El neuroblastoma es un cáncer agresivo de células neuroblásticas inmaduras (precursoras de neuronas ) y es uno de los cánceres pediátricos más comunes, con una edad media de diagnóstico de dos años. [5] El neuroblastoma suprarrenal generalmente se presenta con una masa abdominal que aumenta de tamaño rápidamente. Aunque el tumor a menudo se ha diseminado a partes distantes del cuerpo en el momento del diagnóstico, este cáncer es inusual porque muchos casos son altamente curables cuando la propagación se limita al hígado , la piel y/o la médula ósea (estadio IVS). Los tumores relacionados, pero menos agresivos, compuestos de células neuronales más maduras incluyen el ganglioneuroblastoma y el ganglioneuroma . Los tumores neuroblásticos a menudo producen niveles elevados de metabolitos de la hormona catecolamina , como el ácido vanililmandélico (VMA) y el ácido homovanílico , y pueden producir diarrea acuosa grave a través de la producción de péptido intestinal vasoactivo . El tratamiento del neuroblastoma incluye cirugía y radioterapia para la enfermedad localizada y quimioterapia para la enfermedad metastásica . [6]
El feocromocitoma es una neoplasia compuesta por células similares a las células cromafines de la médula suprarrenal madura. Los feocromocitomas se presentan en pacientes de todas las edades y pueden ser esporádicos o estar asociados a un síndrome de cáncer hereditario , como la neoplasia endocrina múltiple (MEN) tipos IIA y IIB, la neurofibromatosis tipo I o el síndrome de von Hippel-Lindau . Solo el 10% de los feocromocitomas suprarrenales son malignos , mientras que el resto son tumores benignos . La característica clínicamente más importante de los feocromocitomas es su tendencia a producir grandes cantidades de las hormonas catecolaminas epinefrina (adrenalina) y norepinefrina . Esto puede provocar hipertensión arterial potencialmente mortal o arritmias cardíacas , y numerosos síntomas como dolor de cabeza , palpitaciones , ataques de ansiedad , sudoración , pérdida de peso y temblor . El diagnóstico se confirma más fácilmente mediante la medición urinaria de metabolitos de catecolaminas como VMA y metanefrinas . La mayoría de los feocromocitomas se tratan inicialmente con fármacos antiadrenérgicos para proteger contra la sobrecarga de catecolaminas, y se recurre a la cirugía para extirpar el tumor una vez que el paciente se encuentra médicamente estable. [7]
Un incidentaloma suprarrenal es un tumor suprarrenal que se detecta por casualidad sin síntomas clínicos ni sospecha. Es uno de los hallazgos inesperados más comunes que se revelan mediante tomografía computarizada (TC), resonancia magnética (RM) o ecografía. [8]
En estos casos, se suele utilizar una prueba de supresión con dexametasona para detectar el exceso de cortisol , y metanefrinas o catecolaminas para el exceso de estas hormonas . Los tumores de menos de 3 cm generalmente se consideran benignos y solo se tratan si hay motivos para un diagnóstico de síndrome de Cushing o feocromocitoma . [9] La radiodensidad proporciona una pista para estimar el riesgo de malignidad, en donde un tumor con 10 unidades Hounsfield o menos en una TC sin contraste es probablemente un adenoma rico en lípidos. [10]
En la tomografía computarizada, los adenomas benignos suelen tener una densidad radiográfica baja (debido al contenido de grasa) y muestran una rápida eliminación del medio de contraste (el 50 % o más del medio de contraste se elimina a los 10 minutos). Si la evaluación hormonal es negativa y las imágenes sugieren que es benigna, se debe considerar un seguimiento con imágenes a los 6, 12 y 24 meses y repetir la evaluación hormonal anualmente durante 4 años. [11]
Se pueden realizar imágenes por TC y RM dedicadas a las glándulas suprarrenales para distinguir los adenomas benignos de las lesiones potencialmente malignas. [12] [13] Las calculadoras en línea ayudan a los radiólogos a calcular la pérdida de contraste en los nódulos suprarrenales en la TC [14] y el desplazamiento químico en la RM. [15]
También puede ser útil la evaluación hormonal, que incluye: [11]
Quirúrgico
En el caso de los carcinomas suprarrenales, el tratamiento más eficaz es la cirugía , aunque ésta no es factible para muchos pacientes y el pronóstico general de la enfermedad es malo. La quimioterapia , la radioterapia y la terapia hormonal también pueden emplearse en el tratamiento de esta enfermedad.
Una revisión sistemática Cochrane de 2018 comparó dos tipos diferentes de cirugía: adrenalectomía retroperotenial laparoscópica y adrenalectomía transperitoenal laparoscópica en diferentes tipos de tumores suprarrenales. [16] La adrenalectomía retroperotenial laparoscópica pareció reducir la morbilidad tardía, el tiempo hasta la ingesta de líquidos o alimentos por vía oral y el tiempo hasta la deambulación, en comparación con la adrenalectomía transperitoenal laparoscópica. [16] Sin embargo, hubo incertidumbre en estos hallazgos debido a la evidencia de baja calidad, así como a los hallazgos no concluyentes sobre los efectos de cualquiera de las cirugías en la mortalidad por todas las causas, la morbilidad temprana, los efectos socioeconómicos, la duración de la cirugía, la pérdida de sangre operatoria y la conversión a cirugía abierta. [16]
En los últimos años se han investigado los microARN circulantes en sangre (miARN) por su potencial como biomarcador menos invasivo para las enfermedades suprarrenales. Hasta ahora, nueve estudios han investigado la presencia de miARN circulantes en sangre de pacientes diagnosticados con tumores adrenocorticales. [17] [18] Los miARN pueden liberarse en el torrente sanguíneo mediante tres tipos diferentes de excreción. [19] Daño celular con liberación pasiva (necrosis, inflamación), secreción activa en forma de vesículas extracelulares (VE) (microvesículas, exosomas y cuerpos apoptóticos) o en asociación con lipoproteínas de alta densidad (HDL) y proteínas Argonauta (AGO). [20] [21] La mayoría de los miARN que se encuentran en la sangre se encuentran en complejos con AGO. [22] [23] A pesar de los resultados prometedores, la sensibilidad de los posibles marcadores de miARN circulantes para tumores adrenocorticales parece ser variable. Se podría lograr un aumento de la sensibilidad si se apuntara solo a los miRNA asociados a EV, ya que se plantea la hipótesis de que la liberación de miRNA en EV es un proceso controlado. [24] Los miRNA asociados a EV podrían, por lo tanto, actuar como marcadores más específicos de malignidad. [24] Sin embargo, como hubo diferencias significativas en los resultados de los estudios realizados, las diferencias metodológicas y el bajo número de pacientes podrían contribuir a esta discrepancia. Esto requiere más estudios en cohortes más grandes con requisitos metodológicos uniformes para aclarar la aplicabilidad de los miRNA circulantes como biomarcadores de pronóstico y malignidad en pacientes diagnosticados con tumores adrenocorticales. [17]
{{cite book}}: |website=ignorado ( ayuda )