
El ciclo del ácido cítrico —también conocido como ciclo de Krebs , ciclo de Szent–Györgyi–Krebs o ciclo del TCA (ciclo del ácido tricarboxílico) [1] [2] —es una serie de reacciones bioquímicas para liberar la energía almacenada en los nutrientes a través de la oxidación del acetil-CoA derivado de los carbohidratos , las grasas , las proteínas y el alcohol . La energía química liberada está disponible en forma de ATP . El ciclo de Krebs es utilizado por los organismos que respiran (a diferencia de los organismos que fermentan ) para generar energía, ya sea por respiración anaeróbica o respiración aeróbica . Además, el ciclo proporciona precursores de ciertos aminoácidos , así como el agente reductor NADH , que se utilizan en muchas otras reacciones. Su importancia central para muchas vías bioquímicas sugiere que fue uno de los primeros componentes del metabolismo . [3] [4] Aunque se lo etiqueta como un "ciclo", no es necesario que los metabolitos sigan solo una ruta específica; Se han reconocido al menos tres segmentos alternativos del ciclo del ácido cítrico. [5]
El nombre de esta vía metabólica se deriva del ácido cítrico (un ácido tricarboxílico , a menudo llamado citrato, ya que la forma ionizada predomina en el pH biológico [6] ) que se consume y luego se regenera mediante esta secuencia de reacciones para completar el ciclo. El ciclo consume acetato (en forma de acetil-CoA) y agua , reduce NAD + a NADH, liberando dióxido de carbono. El NADH generado por el ciclo del ácido cítrico se alimenta a la vía de fosforilación oxidativa (transporte de electrones). El resultado neto de estas dos vías estrechamente vinculadas es la oxidación de nutrientes para producir energía química utilizable en forma de ATP.
En las células eucariotas , el ciclo del ácido cítrico se produce en la matriz de la mitocondria . En las células procariotas , como las bacterias, que carecen de mitocondrias, la secuencia de reacción del ciclo del ácido cítrico se lleva a cabo en el citosol, y el gradiente de protones para la producción de ATP se produce a través de la superficie de la célula ( membrana plasmática ) en lugar de hacerlo en la membrana interna de la mitocondria .
Por cada molécula de piruvato (de la glucólisis), el rendimiento total de compuestos que contienen energía del ciclo del ácido cítrico es de tres NADH, un FADH 2 y un GTP . [7]
Varios de los componentes y reacciones del ciclo del ácido cítrico fueron establecidos en la década de 1930 por la investigación de Albert Szent-Györgyi , quien recibió el Premio Nobel de Fisiología o Medicina en 1937 específicamente por sus descubrimientos relacionados con el ácido fumárico , un componente del ciclo. [8] Hizo este descubrimiento estudiando el músculo de la pechuga de paloma. Debido a que este tejido mantiene su capacidad oxidativa bien después de descomponerse en la picadora de Latapie y liberarse en soluciones acuosas, el músculo de la pechuga de la paloma estaba muy bien calificado para el estudio de las reacciones oxidativas. [9] El ciclo del ácido cítrico en sí fue finalmente identificado en 1937 por Hans Adolf Krebs y William Arthur Johnson mientras estaban en la Universidad de Sheffield , [10] por lo que el primero recibió el Premio Nobel de Fisiología o Medicina en 1953, y por quien el ciclo a veces se llama "ciclo de Krebs". [11]
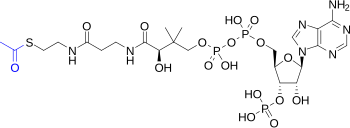
El ciclo del ácido cítrico es una vía metabólica que conecta el metabolismo de los carbohidratos , las grasas y las proteínas . Las reacciones del ciclo las llevan a cabo ocho enzimas que oxidan completamente el acetato (una molécula de dos carbonos), en forma de acetil-CoA, en dos moléculas de dióxido de carbono y agua cada una. A través del catabolismo de azúcares, grasas y proteínas, se produce el producto orgánico de dos carbonos acetil-CoA que entra en el ciclo del ácido cítrico. Las reacciones del ciclo también convierten tres equivalentes de nicotinamida adenina dinucleótido (NAD + ) en tres equivalentes de NAD reducido (NADH), un equivalente de flavina adenina dinucleótido (FAD) en un equivalente de FADH 2 y un equivalente de guanosina difosfato (GDP) y fosfato inorgánico (P i ) en un equivalente de guanosina trifosfato (GTP). El NADH y el FADH 2 generados por el ciclo del ácido cítrico son, a su vez, utilizados por la vía de fosforilación oxidativa para generar ATP rico en energía.
Una de las principales fuentes de acetil-CoA proviene de la descomposición de azúcares por glucólisis que produce piruvato que a su vez es descarboxilado por el complejo piruvato deshidrogenasa generando acetil-CoA según el siguiente esquema de reacción:
El producto de esta reacción, el acetil-CoA, es el punto de partida del ciclo del ácido cítrico. El acetil-CoA también puede obtenerse a partir de la oxidación de ácidos grasos . A continuación se muestra un esquema del ciclo:
El ciclo del ácido cítrico consta de diez pasos básicos, como se describe a continuación. El ciclo se alimenta continuamente de carbono nuevo en forma de acetil-CoA , que entra en el paso 0 de la tabla. [14]
Dos átomos de carbono se oxidan a CO 2 , la energía de estas reacciones se transfiere a otros procesos metabólicos a través de GTP (o ATP), y como electrones en NADH y QH 2 . El NADH generado en el ciclo del ácido cítrico puede oxidarse más tarde (donar sus electrones) para impulsar la síntesis de ATP en un tipo de proceso llamado fosforilación oxidativa . [6] El FADH 2 está unido covalentemente a la succinato deshidrogenasa , una enzima que funciona tanto en el ciclo del ácido cítrico como en la cadena de transporte de electrones mitocondrial en la fosforilación oxidativa. Por lo tanto, el FADH 2 facilita la transferencia de electrones a la coenzima Q , que es el aceptor final de electrones de la reacción catalizada por el complejo succinato:ubiquinona oxidorreductasa, que también actúa como intermediario en la cadena de transporte de electrones . [15]
Las mitocondrias de los animales, incluidos los humanos, poseen dos succinil-CoA sintetasas: una que produce GTP a partir de GDP y otra que produce ATP a partir de ADP. [16] Las plantas tienen el tipo que produce ATP (succinil-CoA sintetasa formadora de ADP). [14] Varias de las enzimas del ciclo pueden estar asociadas de forma vaga en un complejo proteico multienzimático dentro de la matriz mitocondrial . [17]
El GTP que se forma mediante la succinil-CoA sintetasa formadora de GDP puede ser utilizado por la nucleósido-difosfato quinasa para formar ATP (la reacción catalizada es GTP + ADP → GDP + ATP). [15]
Los productos de la primera vuelta del ciclo son un GTP (o ATP ), tres NADH , un FADH 2 y dos CO 2 .
Como a partir de cada molécula de glucosa se producen dos moléculas de acetil-CoA , se requieren dos ciclos por cada molécula de glucosa. Por lo tanto, al final de dos ciclos, los productos son: dos GTP, seis NADH, dos FADH 2 y cuatro CO 2 . [18]
Las reacciones anteriores están equilibradas si P i representa el ion H 2 PO 4 − , ADP y GDP los iones ADP 2− y GDP 2− , respectivamente, y ATP y GTP los iones ATP 3− y GTP 3− , respectivamente.
Se estima que el número total de moléculas de ATP obtenidas después de la oxidación completa de una glucosa en la glucólisis, el ciclo del ácido cítrico y la fosforilación oxidativa está entre 30 y 38. [19]
El rendimiento máximo teórico de ATP a través de la oxidación de una molécula de glucosa en la glucólisis, el ciclo del ácido cítrico y la fosforilación oxidativa es 38 (asumiendo 3 equivalentes molares de ATP por equivalente de NADH y 2 ATP por FADH 2 ). En eucariotas, se generan dos equivalentes de NADH y dos equivalentes de ATP en la glucólisis , que tiene lugar en el citoplasma . Si se transportan utilizando la lanzadera de fosfato de glicerol en lugar de la lanzadera de malato-aspartato , el transporte de dos de estos equivalentes de NADH a las mitocondrias consume efectivamente dos equivalentes de ATP, reduciendo así la producción neta de ATP a 36. Además, las ineficiencias en la fosforilación oxidativa debido a la fuga de protones a través de la membrana mitocondrial y el deslizamiento de la ATP sintasa / bomba de protones comúnmente reduce el rendimiento de ATP de NADH y FADH 2 a menos del rendimiento máximo teórico. [19] Por lo tanto, los rendimientos observados son más cercanos a ~2,5 ATP por NADH y ~1,5 ATP por FADH 2 , lo que reduce aún más la producción neta total de ATP a aproximadamente 30. [20] Una evaluación del rendimiento total de ATP con proporciones protón-ATP recientemente revisadas proporciona una estimación de 29,85 ATP por molécula de glucosa. [21]
Si bien el ciclo del ácido cítrico está en general muy conservado, existe una variabilidad significativa en las enzimas que se encuentran en diferentes taxones [22] (tenga en cuenta que los diagramas de esta página son específicos de la variante de la vía de los mamíferos).
Existen algunas diferencias entre eucariotas y procariotas. La conversión de D- treo -isocitrato a 2-oxoglutarato es catalizada en eucariotas por la enzima EC 1.1.1.41 dependiente de NAD + , mientras que los procariotas emplean la enzima EC 1.1.1.42 dependiente de NADP + . [23] De manera similar, la conversión de ( S )-malato a oxaloacetato es catalizada en eucariotas por la enzima EC 1.1.1.37 dependiente de NAD + , mientras que la mayoría de los procariotas utilizan una enzima dependiente de quinona, EC 1.1.5.4. [24]
Un paso con una variabilidad significativa es la conversión de succinil-CoA a succinato. La mayoría de los organismos utilizan EC 6.2.1.5, succinato-CoA ligasa (formadora de ADP) (a pesar de su nombre, la enzima opera en la vía en la dirección de la formación de ATP). En los mamíferos, también opera una enzima formadora de GTP, succinato-CoA ligasa (formadora de GDP) (EC 6.2.1.4). El nivel de utilización de cada isoforma depende del tejido. [25] En algunas bacterias productoras de acetato, como Acetobacter aceti , una enzima completamente diferente cataliza esta conversión: EC 2.8.3.18, succinil-CoA:acetato CoA-transferasa. Esta enzima especializada vincula el ciclo del TCA con el metabolismo del acetato en estos organismos. [26] Algunas bacterias, como Helicobacter pylori , emplean otra enzima para esta conversión: la succinil-CoA:acetoacetato CoA-transferasa (EC 2.8.3.5). [27]
También existe cierta variabilidad en el paso anterior, la conversión de 2-oxoglutarato en succinil-CoA. Mientras que la mayoría de los organismos utilizan la ubicua 2-oxoglutarato deshidrogenasa dependiente de NAD + , algunas bacterias utilizan una 2-oxoglutarato sintasa dependiente de ferredoxina (EC 1.2.7.3). [28] Otros organismos, incluidas las bacterias y arqueas autótrofas y metanotróficas obligadas, evitan por completo la succinil-CoA y convierten el 2-oxoglutarato en succinato a través del succinato semialdehído , utilizando EC 4.1.1.71, 2-oxoglutarato descarboxilasa, y EC 1.2.1.79, succinato-semialdehído deshidrogenasa. [29]
En el cáncer , se producen importantes alteraciones metabólicas que garantizan la proliferación de células tumorales y, en consecuencia, pueden acumularse metabolitos que sirven para facilitar la tumorigénesis , denominados oncometabolitos . [ 30] Entre los oncometabolitos mejor caracterizados se encuentra el 2-hidroxiglutarato , que se produce a través de una mutación de ganancia de función heterocigótica (específicamente una neomórfica ) en la isocitrato deshidrogenasa (IDH) (que en circunstancias normales cataliza la oxidación de isocitrato a oxalosuccinato , que luego se descarboxila espontáneamente a alfa-cetoglutarato , como se explicó anteriormente; en este caso, se produce un paso de reducción adicional después de la formación de alfa-cetoglutarato a través de NADPH para producir 2-hidroxiglutarato), y por lo tanto, la IDH se considera un oncogén . En condiciones fisiológicas, el 2-hidroxiglutarato es un producto menor de varias vías metabólicas como un error, pero se convierte fácilmente en alfa-cetoglutarato a través de las enzimas hidroxiglutarato deshidrogenasas ( L2HGDH y D2HGDH ) [31] pero no tiene un papel fisiológico conocido en células de mamíferos; cabe destacar que, en el cáncer, es probable que el 2-hidroxiglutarato sea un metabolito terminal, ya que los experimentos de marcaje isotópico de líneas celulares de cáncer colorrectal muestran que su conversión de nuevo a alfa-cetoglutarato es demasiado baja para medirla. [32] En el cáncer, el 2-hidroxiglutarato sirve como inhibidor competitivo de varias enzimas que facilitan las reacciones a través del alfa-cetoglutarato en las dioxigenasas dependientes del alfa-cetoglutarato . Esta mutación produce varios cambios importantes en el metabolismo de la célula. Por un lado, debido a que hay una reducción adicional catalizada por NADPH, esto puede contribuir al agotamiento de las reservas celulares de NADPH y también reducir los niveles de alfa-cetoglutarato disponibles para la célula. En particular, el agotamiento de NADPH es problemático porque el NADPH está altamente compartimentado y no puede difundirse libremente entre los orgánulos de la célula. Se produce principalmente a través de la vía de las pentosas fosfato en el citoplasma. El agotamiento de NADPH da como resultado un mayor estrés oxidativo dentro de la célula, ya que es un cofactor necesario en la producción de GSH , y este estrés oxidativo puede provocar daños en el ADN. También hay cambios a nivel genético y epigenético a través de la función de las histonas lisinas desmetilasas.(KDMs) y enzimas de translocación diez-once (TET); ordinariamente las TET hidroxilan 5-metilcitosinas para prepararlas para la desmetilación. Sin embargo, en ausencia de alfa-cetoglutarato esto no puede hacerse y por lo tanto hay hipermetilación del ADN de la célula, sirviendo para promover la transición epitelial-mesenquimal (EMT) e inhibir la diferenciación celular. Un fenómeno similar se observa para la familia Jumonji C de KDMs que requieren una hidroxilación para realizar la desmetilación en el grupo metilo épsilon-amino. [33] Además, la incapacidad de las prolil hidroxilasas para catalizar reacciones resulta en la estabilización del factor inducible por hipoxia alfa , que es necesario para promover la degradación de este último (ya que en condiciones de bajo oxígeno no habrá sustrato adecuado para la hidroxilación). Esto resulta en un fenotipo pseudohipóxico en la célula cancerosa que promueve la angiogénesis , la reprogramación metabólica, el crecimiento celular y la migración . [ cita requerida ]
Regulación alostérica por metabolitos . La regulación del ciclo del ácido cítrico está determinada en gran medida por la inhibición del producto y la disponibilidad del sustrato. Si se permitiera que el ciclo transcurriera sin control, se podrían desperdiciar grandes cantidades de energía metabólica en la sobreproducción de coenzimas reducidas como NADH y ATP. El principal sustrato final del ciclo es ADP que se convierte en ATP. Una cantidad reducida de ADP provoca la acumulación del precursor NADH que a su vez puede inhibir varias enzimas. El NADH, un producto de todas las deshidrogenasas en el ciclo del ácido cítrico con la excepción de la succinato deshidrogenasa , inhibe la piruvato deshidrogenasa , la isocitrato deshidrogenasa , la α-cetoglutarato deshidrogenasa y también la citrato sintasa . El acetil-coA inhibe la piruvato deshidrogenasa , mientras que el succinil-CoA inhibe la alfa-cetoglutarato deshidrogenasa y la citrato sintasa . Cuando se prueba in vitro con enzimas TCA, el ATP inhibe la citrato sintasa y la α-cetoglutarato deshidrogenasa ; sin embargo, los niveles de ATP no cambian más del 10% in vivo entre el reposo y el ejercicio vigoroso. No se conoce ningún mecanismo alostérico que pueda explicar grandes cambios en la velocidad de reacción de un efector alostérico cuya concentración cambia menos del 10%. [6]
El citrato se utiliza para la inhibición por retroalimentación, ya que inhibe la fosfofructoquinasa , una enzima involucrada en la glucólisis que cataliza la formación de fructosa 1,6-bisfosfato , un precursor del piruvato. Esto evita una tasa alta y constante de flujo cuando hay una acumulación de citrato y una disminución del sustrato para la enzima. [34]
Regulación por el calcio . El calcio también se utiliza como regulador en el ciclo del ácido cítrico. Los niveles de calcio en la matriz mitocondrial pueden alcanzar niveles de hasta decenas de micromolares durante la activación celular. [35] Activa la fosfatasa de piruvato deshidrogenasa, que a su vez activa el complejo de piruvato deshidrogenasa . El calcio también activa la isocitrato deshidrogenasa y la α-cetoglutarato deshidrogenasa . [36] Esto aumenta la velocidad de reacción de muchos de los pasos del ciclo y, por lo tanto, aumenta el flujo a lo largo de la vía. [ cita requerida ]
Regulación transcripcional . Existe un vínculo entre los intermediarios del ciclo del ácido cítrico y la regulación de los factores inducibles por hipoxia ( HIF ). El HIF desempeña un papel en la regulación de la homeostasis del oxígeno y es un factor de transcripción que se dirige a la angiogénesis , la remodelación vascular , la utilización de la glucosa , el transporte de hierro y la apoptosis . El HIF se sintetiza de forma constitutiva y la hidroxilación de al menos uno de los dos residuos críticos de prolina media su interacción con el complejo de ubiquitina ligasa E3 de von Hippel Lindau , que los dirige para una rápida degradación. Esta reacción es catalizada por prolil 4-hidroxilasas . El fumarato y el succinato se han identificado como potentes inhibidores de las prolil hidroxilasas, lo que conduce a la estabilización del HIF. [37]
Varias vías catabólicas convergen en el ciclo del ácido cítrico. La mayoría de estas reacciones añaden intermediarios al ciclo del ácido cítrico y, por lo tanto, se conocen como reacciones anapleróticas , del griego "llenar". Estas aumentan la cantidad de acetil CoA que el ciclo puede transportar, lo que aumenta la capacidad de la mitocondria para llevar a cabo la respiración si este es un factor limitante. Los procesos que eliminan intermediarios del ciclo se denominan reacciones "catapleróticas". [38]
En esta sección y en la siguiente, los intermediarios del ciclo del ácido cítrico se indican en cursiva para distinguirlos de otros sustratos y productos finales.
Las moléculas de piruvato producidas por la glucólisis se transportan activamente a través de la membrana mitocondrial interna y hacia la matriz, donde pueden oxidarse y combinarse con la coenzima A para formar CO2 , acetil -CoA y NADH , como en el ciclo normal. [39]
Sin embargo, también es posible que el piruvato sea carboxilado por la piruvato carboxilasa para formar oxaloacetato . Esta última reacción "rellena" la cantidad de oxaloacetato en el ciclo del ácido cítrico y, por lo tanto, es una reacción anaplerótica, que aumenta la capacidad del ciclo para metabolizar acetil-CoA cuando las necesidades energéticas del tejido (por ejemplo, en el músculo ) aumentan repentinamente por la actividad. [40]
En el ciclo del ácido cítrico, todos los intermediarios (por ejemplo , citrato , isocitrato , alfa-cetoglutarato , succinato , fumarato , malato y oxaloacetato ) se regeneran durante cada vuelta del ciclo. Por lo tanto, agregar más de cualquiera de estos intermediarios a la mitocondria significa que esa cantidad adicional se retiene dentro del ciclo, aumentando todos los demás intermediarios a medida que uno se convierte en el otro. Por lo tanto, la adición de cualquiera de ellos al ciclo tiene un efecto anaplerótico, y su eliminación tiene un efecto cataplerótico. Estas reacciones anapleróticas y catapleróticas, durante el curso del ciclo, aumentarán o disminuirán la cantidad de oxaloacetato disponible para combinarse con acetil-CoA para formar ácido cítrico . Esto a su vez aumenta o disminuye la tasa de producción de ATP por la mitocondria y, por lo tanto, la disponibilidad de ATP para la célula. [40]
Por otra parte, el acetil-CoA , derivado de la oxidación del piruvato o de la beta-oxidación de los ácidos grasos , es el único combustible que entra en el ciclo del ácido cítrico. Con cada vuelta del ciclose consume una molécula de acetil-CoA por cada molécula de oxaloacetato presente en la matriz mitocondrial, y nunca se regenera. Es la oxidación de la porción de acetato del acetil-CoA la que produce CO2 y agua, y la energía así liberada se captura en forma de ATP. [40] Los tres pasos de la beta-oxidación se parecen a los pasos que ocurren en la producción de oxaloacetato a partir de succinato en el ciclo del TCA. El acil-CoA se oxida a trans-enoil-CoA mientras que el FAD se reduce a FADH2 , que es similar a la oxidación del succinato a fumarato. A continuación, el trans-enoil-CoA se hidrata a través del doble enlace a beta-hidroxiacil-CoA, al igual que el fumarato se hidrata a malato. Por último, el beta-hidroxiacil-CoA se oxida a beta-cetoacil-CoA mientras que el NAD+ se reduce a NADH, que sigue el mismo proceso que la oxidación del malato a oxaloacetato . [41]
En el hígado, la carboxilación del piruvato citosólico en oxalacetato intramitocondrial es un paso temprano en la vía gluconeogénica que convierte el lactato y la alanina desaminada en glucosa, [39] [40] bajo la influencia de altos niveles de glucagón y/o epinefrina en la sangre. [40] Aquí la adición de oxalacetato a la mitocondria no tiene un efecto anaplerótico neto, ya que otro intermediario del ciclo del ácido cítrico ( malato ) se elimina inmediatamente de la mitocondria para convertirse en oxalacetato citosólico, que finalmente se convierte en glucosa, en un proceso que es casi el inverso de la glucólisis . [40]
En el catabolismo proteico , las proteínas son degradadas por proteasas en sus aminoácidos constituyentes. Sus esqueletos carbonados (es decir, los aminoácidos desaminados) pueden entrar en el ciclo del ácido cítrico como intermediarios (por ejemplo, alfa-cetoglutarato derivado del glutamato o glutamina), teniendo un efecto anaplerótico en el ciclo, o, en el caso de la leucina , isoleucina , lisina , fenilalanina , triptófano y tirosina , se convierten en acetil-CoA que puede quemarse para formar CO2 y agua, o usarse para formar cuerpos cetónicos , que también solo pueden quemarse en tejidos distintos del hígado donde se forman, o excretarse a través de la orina o el aliento. [40] Por lo tanto, estos últimos aminoácidos se denominan aminoácidos "cetogénicos", mientras que los que entran en el ciclo del ácido cítrico como intermediarios solo pueden eliminarse catapleróticamente ingresando a la vía gluconeogénica a través del malato , que se transporta fuera de la mitocondria para convertirse en oxaloacetato citosólico y, finalmente, en glucosa . Estos son los llamados aminoácidos "glucogénicos". La alanina, la cisteína, la glicina, la serina y la treonina desaminadas se convierten en piruvato y, en consecuencia, pueden ingresar al ciclo del ácido cítrico como oxaloacetato (una reacción anaplerótica) o como acetil-CoA para eliminarse como CO2 y agua. [40]
En el catabolismo de las grasas , los triglicéridos se hidrolizan para descomponerlos en ácidos grasos y glicerol . En el hígado, el glicerol se puede convertir en glucosa a través de fosfato de dihidroxiacetona y gliceraldehído-3-fosfato mediante gluconeogénesis . En el músculo esquelético, el glicerol se utiliza en la glucólisis al convertir el glicerol en glicerol-3-fosfato , luego en fosfato de dihidroxiacetona (DHAP) y luego en gliceraldehído-3-fosfato. [42]
En muchos tejidos, especialmente el tejido cardíaco y muscular esquelético , los ácidos grasos se descomponen a través de un proceso conocido como beta oxidación , que da como resultado la producción de acetil-CoA mitocondrial , que puede usarse en el ciclo del ácido cítrico. La beta oxidación de los ácidos grasos con un número impar de puentes de metileno produce propionil-CoA , que luego se convierte en succinil-CoA y se introduce en el ciclo del ácido cítrico como un intermediario anaplerótico. [43]
La energía total obtenida de la descomposición completa de una molécula (de seis carbonos) de glucosa por glucólisis , la formación de dos moléculas de acetil-CoA , su catabolismo en el ciclo del ácido cítrico y la fosforilación oxidativa equivale a unas 30 moléculas de ATP en eucariotas . El número de moléculas de ATP derivadas de la beta oxidación de un segmento de seis carbonos de una cadena de ácidos grasos y la posterior oxidación de las tres moléculas de acetil-CoA resultantes es de 40. [ cita requerida ]
En este subtítulo, al igual que en el anterior, los intermedios del TCA se identifican en cursiva .
Varios de los intermediarios del ciclo del ácido cítrico se utilizan para la síntesis de compuestos importantes, que tendrán efectos catapleróticos significativos en el ciclo. [40] El acetil-CoA no puede ser transportado fuera de la mitocondria. Para obtener acetil-CoA citosólico, el citrato se retira del ciclo del ácido cítrico y se transporta a través de la membrana mitocondrial interna hasta el citosol. Allí es escindido por la ATP citrato liasa en acetil-CoA y oxaloacetato. El oxaloacetato se devuelve a la mitocondria como malato (y luego se convierte nuevamente en oxaloacetato para transferir más acetil-CoA fuera de la mitocondria). [44] El acetil-CoA citosólico se utiliza para la síntesis de ácidos grasos y la producción de colesterol . El colesterol , a su vez, puede utilizarse para sintetizar las hormonas esteroides , las sales biliares y la vitamina D. [39] [40 ]
Los esqueletos carbonados de muchos aminoácidos no esenciales se forman a partir de intermediarios del ciclo del ácido cítrico. Para convertirlos en aminoácidos, los alfa-cetoácidos formados a partir de los intermediarios del ciclo del ácido cítrico tienen que adquirir sus grupos amino del glutamato en una reacción de transaminación , en la que el fosfato de piridoxal es un cofactor. En esta reacción, el glutamato se convierte en alfa-cetoglutarato , que es un intermediario del ciclo del ácido cítrico. Los intermediarios que pueden proporcionar los esqueletos carbonados para la síntesis de aminoácidos son el oxaloacetato , que forma aspartato y asparagina ; y el alfa-cetoglutarato , que forma glutamina , prolina y arginina . [39] [40]
De estos aminoácidos, el aspartato y la glutamina se utilizan, junto con átomos de carbono y nitrógeno de otras fuentes, para formar las purinas que se utilizan como bases en el ADN y el ARN , así como en ATP , AMP , GTP , NAD , FAD y CoA . [40]
Las pirimidinas se ensamblan parcialmente a partir del aspartato (derivado del oxaloacetato ). Las pirimidinas, timina , citosina y uracilo , forman las bases complementarias a las bases de purina en el ADN y el ARN, y también son componentes de CTP , UMP , UDP y UTP . [40]
La mayoría de los átomos de carbono de las porfirinas provienen del intermediario del ciclo del ácido cítrico, la succinil-CoA . Estas moléculas son un componente importante de las hemoproteínas , como la hemoglobina , la mioglobina y varios citocromos . [40]
Durante la gluconeogénesis, el oxaloacetato mitocondrial se reduce a malato , que luego se transporta fuera de la mitocondria para oxidarse nuevamente a oxaloacetato en el citosol. Luego, el oxaloacetato citosólico se descarboxila a fosfoenolpiruvato por acción de la fosfoenolpiruvato carboxiquinasa , que es el paso limitante de la velocidad en la conversión de casi todos los precursores gluconeogénicos (como los aminoácidos glucogénicos y el lactato) en glucosa por el hígado y el riñón . [39] [40]
Debido a que el ciclo del ácido cítrico está involucrado tanto en procesos catabólicos como anabólicos , se lo conoce como vía anfibólica . Evan MWDuo Haga clic en genes, proteínas y metabolitos a continuación para acceder a los respectivos artículos. [§ 1]
El papel metabólico del lactato es bien reconocido como combustible para los tejidos , las citopatías mitocondriales como la citopatía DPH y el campo científico de la oncología ( tumores ). En el ciclo clásico de Cori , los músculos producen lactato que luego es absorbido por el hígado para la gluconeogénesis . Nuevos estudios sugieren que el lactato puede usarse como fuente de carbono para el ciclo del TCA. [45]
Se cree que los componentes del ciclo del ácido cítrico se derivaron de bacterias anaeróbicas y que el ciclo del TCA en sí puede haber evolucionado más de una vez. [46] Incluso puede ser anterior a la biosis: los sustratos parecen experimentar la mayoría de las reacciones de forma espontánea en presencia de radicales persulfato . [47] Teóricamente, existen varias alternativas al ciclo del TCA; sin embargo, el ciclo del TCA parece ser el más eficiente. Si varias alternativas del TCA hubieran evolucionado independientemente, todas parecen haber convergido en el ciclo del TCA. [48] [49]
Este proceso se describe gráficamente en la página 73.
{{cite journal}}: CS1 maint: DOI inactivo a partir de julio de 2024 ( enlace )