Las penicilinas ( P , PCN o PEN ) son un grupo de antibióticos β-lactámicos obtenidos originalmente de los mohos Penicillium , principalmente P. chrysogenum y P. rubens . La mayoría de las penicilinas de uso clínico son sintetizadas por P. chrysogenum mediante fermentación en tanques profundos [2] y luego se purifican. [3] [4] Se han descubierto varias penicilinas naturales, pero sólo dos compuestos purificados tienen uso clínico: la penicilina G ( uso intramuscular o intravenoso ) y la penicilina V (administrada por vía oral). Las penicilinas estuvieron entre los primeros medicamentos eficaces contra muchas infecciones bacterianas causadas por estafilococos y estreptococos . Todavía se utilizan ampliamente hoy en día para diversas infecciones bacterianas, aunque muchos tipos de bacterias han desarrollado resistencia tras su uso extensivo.
El diez por ciento de la población afirma ser alérgico a la penicilina , pero debido a que la frecuencia de resultados positivos de las pruebas cutáneas disminuye en un 10% cada año que se evita, el 90% de estos pacientes pueden eventualmente tolerar la penicilina. Además, las personas con alergia a la penicilina generalmente pueden tolerar las cefalosporinas (otro grupo de β-lactámicos) porque la reactividad cruzada de la inmunoglobulina E (IgE) es solo del 3%. [5]
La penicilina fue descubierta en 1928 por el científico escocés Alexander Fleming como un extracto crudo de P. rubens . [6] El alumno de Fleming, Cecil George Paine, fue el primero en utilizar con éxito la penicilina para tratar la infección ocular ( conjuntivitis neonatal ) en 1930. El compuesto purificado (penicilina F) fue aislado en 1940 por un equipo de investigación dirigido por Howard Florey y Ernst Boris Chain en la Universidad de Oxford. Fleming utilizó por primera vez la penicilina purificada para tratar la meningitis estreptocócica en 1942. [7] El Premio Nobel de Fisiología o Medicina de 1945 fue compartido por Chain, Fleming y Florey.
Varias penicilinas semisintéticas son eficaces contra un espectro más amplio de bacterias: estas incluyen las penicilinas antiestafilocócicas , las aminopenicilinas y las penicilinas antipseudomonas .
El término "penicilina" se define como el producto natural del moho Penicillium con actividad antimicrobiana. [8] Fue acuñado por Alexander Fleming el 7 de marzo de 1929 cuando descubrió la propiedad antibacteriana del Penicillium rubens . [9] Fleming explicó en su artículo de 1929 en el British Journal of Experimental Pathology que "para evitar la repetición de la frase bastante engorrosa 'filtrado de caldo de moho', se utilizará el nombre 'penicilina'". [10] El nombre se refiere así al nombre científico del moho, tal como lo describió Fleming en su conferencia Nobel en 1945:
Con frecuencia me han preguntado por qué inventé el nombre "Penicilina". Simplemente seguí líneas perfectamente ortodoxas y acuñé una palabra que explicaba que la sustancia penicilina se derivaba de una planta del género Penicillium, así como hace muchos años se inventó la palabra " Digitalina " para una sustancia derivada de la planta Digitalis . [11]
En el uso moderno, el término penicilina se utiliza de manera más amplia para referirse a cualquier antimicrobiano β-lactámico que contiene un anillo de tiazolidina fusionado al núcleo de β-lactámico y puede ser o no un producto natural. [12] Como la mayoría de los productos naturales, la penicilina está presente en los mohos Penicillium como una mezcla de componentes activos ( la gentamicina es otro ejemplo de un producto natural que es una mezcla mal definida de componentes activos). [8] Los principales componentes activos de Penicillium se enumeran en la siguiente tabla: [13] [14]
Otros componentes activos menores de Penicillium incluyen penicilina O , [20] [21] penicilina U1 y penicilina U6. Posteriormente se descubrió que otros componentes nombrados del Penicillium natural , como la penicilina A, no tienen actividad antibiótica y no están químicamente relacionados con las penicilinas antibióticas. [8]
La constitución precisa de la penicilina extraída depende de la especie de moho Penicillium utilizada y de los medios nutritivos utilizados para cultivar el moho. [8] La cepa original de Penicillium rubens de Fleming produce principalmente penicilina F, que lleva el nombre de Fleming. Pero la penicilina F es inestable, difícil de aislar y el moho la produce en pequeñas cantidades. [8]
La principal cepa comercial de Penicillium chrysogenum (la cepa Peoria) produce penicilina G como componente principal cuando se utiliza licor de maceración de maíz como medio de cultivo. [8] Cuando se añaden fenoxietanol o ácido fenoxiacético al medio de cultivo, el moho produce penicilina V como penicilina principal. [8]
El ácido 6-aminopenicilánico (6-APA) es un compuesto derivado de la penicilina G. El 6-APA contiene el núcleo betalactámico de la penicilina G, pero sin las cadenas laterales; El 6-APA es un precursor útil para fabricar otras penicilinas. Hay muchas penicilinas semisintéticas derivadas del 6-APA y se dividen en tres grupos: penicilinas antiestafilocócicas, penicilinas de amplio espectro y penicilinas antipseudomonas. Todas las penicilinas semisintéticas se denominan penicilinas porque en última instancia derivan de la penicilina G.
El uso de unidades para prescribir penicilina es un accidente histórico y está en gran medida obsoleto fuera de Estados Unidos. Dado que la penicilina original era una mezcla mal definida de compuestos activos (un polvo amarillo amorfo), la potencia de cada lote de penicilina variaba de un lote a otro. Por lo tanto, era imposible prescribir 1 g de penicilina porque la actividad de 1 g de penicilina de un lote sería diferente de la actividad de otro lote. Después de la fabricación, cada lote de penicilina tuvo que estandarizarse frente a una unidad conocida de penicilina: luego cada vial de vidrio se llenó con el número de unidades necesarias. En la década de 1940, un vial de 5.000 unidades Oxford era estándar, [24] pero, dependiendo del lote, podía contener entre 15 mg y 20 mg de penicilina. Posteriormente, se convirtió en estándar un vial de 1.000.000 de unidades internacionales, que podía contener de 2,5 ga 3 g de penicilina natural (una mezcla de penicilina I, II, III y IV e impurezas naturales). Con la llegada de las preparaciones de penicilina G pura (un polvo cristalino blanco), hay pocas razones para prescribir penicilina en unidades.
La "unidad" de penicilina ha tenido tres definiciones anteriores, y cada definición fue elegida por ser aproximadamente equivalente a la anterior.
Existe una unidad más antigua para penicilina V que no es equivalente a la unidad de penicilina V actual. La razón es que la FDA de EE. UU. asumió incorrectamente que la potencia de la penicilina V es la misma mol por mol que la penicilina G. De hecho, la penicilina V es menos potente que la penicilina G, y la unidad actual de penicilina V refleja ese hecho.
También se estableció una norma similar para la penicilina K. [32]
Las penicilinas constan de un anillo betalactámico distinto de 4 miembros , además de un anillo de tiazolida y una cadena lateral R. La principal característica distintiva entre variantes dentro de esta familia es el sustituyente R.
Esta cadena lateral está conectada al residuo del ácido 6-aminopenicilánico y produce variaciones en el espectro antimicrobiano, la estabilidad y la susceptibilidad a las betalactamasas de cada tipo.
La penicilina G (bencilpenicilina) se produjo por primera vez a partir de un hongo penicillium que se encuentra en la naturaleza. La cepa de hongo que se utiliza hoy en día para la fabricación de penicilina G fue creada mediante ingeniería genética para mejorar el rendimiento en el proceso de fabricación. Ninguna de las otras penicilinas naturales (F, K, N, X, O, U1 o U6) se encuentra actualmente en uso clínico.
La penicilina V (fenoximetilpenicilina) se produce añadiendo el precursor ácido fenoxiacético al medio en el que se cultiva una cepa genéticamente modificada [ dudoso – discutir ] del hongo penicillium .
Hay tres grupos principales de otros antibióticos semisintéticos relacionados con las penicilinas. Se sintetizan añadiendo varias cadenas laterales al precursor 6-APA , que se aísla de la penicilina G. Estos son los antibióticos antiestafilocócicos, los antibióticos de amplio espectro y los antibióticos antipseudomonas.
Los antibióticos antiestafilocócicos se denominan así porque son resistentes a la degradación por la penicilinasa estafilocócica . Por eso también se les llama resistentes a la penicilinasa.
Este grupo de antibióticos se denomina "de amplio espectro" porque son activos contra una amplia gama de bacterias Gram-negativas como Escherichia coli y Salmonella typhi , para las cuales la penicilina no es adecuada. Sin embargo, la resistencia en estos organismos ahora es común.
Existen muchos precursores de ampicilina. Estos son compuestos inactivos que se descomponen en el intestino para liberar ampicilina. Ninguno de estos profármacos de ampicilina se utiliza actualmente:
La epicilina es una aminopenicilina que nunca ha tenido un uso clínico generalizado.
La especie Gram negativa, Pseudomonas aeruginosa , es naturalmente resistente a muchas clases de antibióticos. En las décadas de 1960 y 1970 se realizaron muchos esfuerzos para desarrollar antibióticos que fueran activos contra las especies de Pseudomonas . Hay dos clases químicas dentro del grupo: carboxipenicilinas y ureidopenicilinas. Todos se administran mediante inyección; ninguno puede administrarse por vía oral.
El término "penicilina", cuando se usa solo, puede referirse a cualquiera de dos compuestos químicos , penicilina G o penicilina V.
La penicilina G es destruida por el ácido del estómago, por lo que no se puede tomar por vía oral, pero se pueden administrar dosis de hasta 2,4 g (mucho más altas que la penicilina V). Se administra mediante inyección intravenosa o intramuscular. Puede formularse como una sal insoluble, y existen dos formulaciones de este tipo en uso actual: penicilina procaína y bencilpenicilina benzatínica . Cuando es necesario mantener una concentración elevada en la sangre, la penicilina G debe administrarse a intervalos relativamente frecuentes, porque el riñón la elimina con bastante rapidez del torrente sanguíneo.
La penicilina G está autorizada para tratar la septicemia , el empiema , la neumonía , la pericarditis , la endocarditis y la meningitis causadas por cepas susceptibles de estafilococos y estreptococos. También está autorizado para el tratamiento del ántrax , actinomicosis , enfermedad cervicofacial, enfermedad torácica y abdominal, infecciones clostridiales , botulismo , gangrena gaseosa (con desbridamiento y/o cirugía acompañante, según se indique), tétanos (como terapia complementaria a la inmunoglobulina antitetánica humana). ), difteria (como terapia complementaria a la antitoxina y para la prevención del estado de portador), endocarditis por erisipelothrix , fusospiroquetosis (infecciones graves de la orofaringe, el tracto respiratorio inferior y la zona genital), infecciones por Listeria , meningitis, endocarditis, infecciones por Pasteurella , incluida bacteriemia y meningitis, fiebre de Haverhill ; fiebre por mordedura de rata e infecciones gonocócicas diseminadas , meningitis meningocócica y/o septicemia causada por organismos sensibles a la penicilina y sífilis. [33]
La penicilina V se puede tomar por vía oral porque es relativamente resistente al ácido del estómago. Las dosis superiores a 500 mg no son completamente efectivas debido a su mala absorción. Se utiliza para las mismas infecciones bacterianas que las de la penicilina G y es la forma de penicilina más utilizada. [34] Sin embargo, no se utiliza para enfermedades, como la endocarditis , donde se requieren altos niveles de penicilina en sangre.
Debido a que la resistencia a la penicilina es ahora tan común, otros antibióticos son ahora la opción preferida para el tratamiento. Por ejemplo, la penicilina solía ser el tratamiento de primera línea para las infecciones por Neisseria gonorrhoeae y Neisseria meningitidis , pero ya no se recomienda para el tratamiento de estas infecciones. La resistencia a la penicilina es ahora muy común en Staphylococcus aureus , lo que significa que la penicilina no debe usarse para tratar infecciones causadas por S. aureus a menos que se sepa que la cepa infectante es susceptible.
Las reacciones adversas comunes (≥ 1% de las personas) asociadas con el uso de penicilinas incluyen diarrea , hipersensibilidad , náuseas , erupción cutánea , neurotoxicidad , urticaria y sobreinfección (incluida candidiasis ). Los efectos adversos poco frecuentes (0,1 a 1% de las personas) incluyen fiebre , vómitos , eritema , dermatitis , angioedema , convulsiones (especialmente en personas con epilepsia ) y colitis pseudomembranosa . [35] La penicilina también puede inducir la enfermedad del suero o una reacción similar a la enfermedad del suero en algunos individuos. La enfermedad del suero es una reacción de hipersensibilidad de tipo III que ocurre de una a tres semanas después de la exposición a medicamentos, incluida la penicilina. No es una verdadera alergia a un medicamento, porque las alergias son reacciones de hipersensibilidad de tipo I , pero la exposición repetida al agente causante puede provocar una reacción anafiláctica. [36] [37] La alergia ocurrirá en 1-10% de las personas y se presentará como una erupción cutánea después de la exposición. La anafilaxia mediada por IgE ocurrirá en aproximadamente el 0,01% de los pacientes. [38] [35]
El dolor y la inflamación en el lugar de la inyección también son comunes con la bencilpenicilina benzatínica, la bencilpenicilina y, en menor medida, la bencilpenicilina procaína administradas por vía parenteral . La afección se conoce como dermatitis livedoide o síndrome de Nicolau. [39] [40]
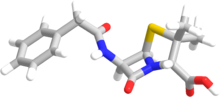
El término " penam " se utiliza para describir el esqueleto central común de un miembro de las penicilinas. Este núcleo tiene la fórmula molecular RC 9 H 11 N 2 O 4 S, donde R es la cadena lateral variable que diferencia las penicilinas entre sí. El núcleo de penam tiene una masa molar de 243 g/mol, y las penicilinas más grandes tienen una masa molar cercana a 450; por ejemplo, la cloxacilina tiene una masa molar de 436 g/mol. 6-APA (C 8 H 12 N 2 O 3 S) forma la estructura básica de las penicilinas. Está formado por un dipéptido encerrado formado por la condensación de L-cisteína y D-valina. Esto da como resultado la formación de anillos β-lactámicos y tiazolidínicos. [41]
La característica estructural clave de las penicilinas es el anillo β-lactámico de cuatro miembros; esta fracción estructural es esencial para la actividad antibacteriana de la penicilina. El anillo β-lactámico está fusionado a un anillo de tiazolidina de cinco miembros . La fusión de estos dos anillos hace que el anillo de β-lactama sea más reactivo que las β-lactamas monocíclicas porque los dos anillos fusionados distorsionan el enlace amida de β-lactama y, por lo tanto, eliminan la estabilización de resonancia que normalmente se encuentra en estos enlaces químicos. [42] Una cadena lateral de acilo unida al anillo de β-lactama. [43]
Se han producido diversos antibióticos β-lactámicos tras la modificación química de la estructura 6-APA durante la síntesis, específicamente realizando sustituciones químicas en la cadena lateral de acilo. Por ejemplo, la primera penicilina químicamente alterada, la meticilina, tenía sustituciones por grupos metoxi en las posiciones 2' y 6' del anillo de benceno 6-APA de la penicilina G. [41] Esta diferencia hace que la meticilina sea resistente a la actividad de la β-lactamasa . una enzima por la cual muchas bacterias son naturalmente insensibles a las penicilinas. [44]
La penicilina puede penetrar fácilmente en las células bacterianas en el caso de especies grampositivas . Esto se debe a que las bacterias Gram positivas no tienen una membrana celular externa y simplemente están encerradas en una pared celular gruesa . [45] Las moléculas de penicilina son lo suficientemente pequeñas como para atravesar los espacios de las glicoproteínas en la pared celular. Por esta razón, las bacterias Gram positivas son muy susceptibles a la penicilina (como lo demostró por primera vez el descubrimiento de la penicilina en 1928 [46] ). [47]
La penicilina, o cualquier otra molécula, ingresa a las bacterias Gram negativas de manera diferente. Las bacterias tienen paredes celulares más delgadas pero la superficie externa está recubierta con una membrana celular adicional, llamada membrana externa. La membrana externa es una capa lipídica ( cadena de lipopolisacárido ) que bloquea el paso de moléculas solubles en agua ( hidrófilas ) como la penicilina. Actúa así como la primera línea de defensa contra cualquier sustancia tóxica, lo que explica la relativa resistencia a los antibióticos en comparación con las especies grampositivas. [48] Pero la penicilina aún puede ingresar a especies gramnegativas difundiéndose a través de canales acuosos llamados porinas (proteínas de la membrana externa), que se dispersan entre las moléculas grasas y pueden transportar nutrientes y antibióticos al interior de las bacterias. [49] Las porinas son lo suficientemente grandes como para permitir la difusión de la mayoría de las penicilinas, pero la velocidad de difusión a través de ellas está determinada por el tamaño específico de las moléculas del fármaco. Por ejemplo, la penicilina G es grande y entra lentamente a través de las porinas; mientras que la ampicilina y la amoxicilina más pequeñas se difunden mucho más rápido. [50] Por el contrario, la vancomicina grande no puede atravesar las porinas y, por lo tanto, es ineficaz para las bacterias Gram-negativas. [51] El tamaño y la cantidad de porinas son diferentes en diferentes bacterias. Como resultado de los dos factores (tamaño de la penicilina y porina), las bacterias gramnegativas pueden ser insensibles o tener distintos grados de susceptibilidad a una penicilina específica. [52]


La penicilina mata las bacterias al inhibir la finalización de la síntesis de peptidoglicanos , el componente estructural de la pared celular bacteriana . Inhibe específicamente la actividad de las enzimas necesarias para el entrecruzamiento de los peptidoglicanos durante el paso final de la biosíntesis de la pared celular. Lo hace uniéndose a las proteínas fijadoras de penicilina con el anillo β-lactámico, una estructura que se encuentra en las moléculas de penicilina. [54] [55] Esto hace que la pared celular se debilite debido a menos enlaces cruzados y significa que el agua fluye incontrolablemente hacia la célula porque no puede mantener el gradiente osmótico correcto. Esto da como resultado la lisis y muerte celular.
Las bacterias remodelan constantemente sus paredes celulares de peptidoglicano, construyendo y descomponiendo simultáneamente partes de la pared celular a medida que crecen y se dividen. Durante las últimas etapas de la biosíntesis de peptidoglicano, se forma el pentapéptido del ácido uridina difosfato- N- acetilmurámico (UDP-MurNAc) en el que el cuarto y quinto aminoácidos son D -alanil- D -alanina. La transferencia de D-alanina se realiza (cataliza) mediante la enzima DD-transpeptidasa ( las proteínas de unión a penicilina son de este tipo). [50] La integridad estructural de la pared celular bacteriana depende de la reticulación de UDP-MurNAc y N -acetil glucosamina. [56] La penicilina y otros antibióticos β-lactámicos actúan como un análogo de la D -alanina- D -alanina (el dipéptido) en UDP-MurNAc debido a similitudes conformacionales. La DD-transpeptidasa luego se une al anillo β-lactámico de cuatro miembros de la penicilina en lugar de a UDP-MurNAc. [50] Como consecuencia, la DD-transpeptidasa se inactiva, la formación de enlaces cruzados entre UDP-MurNAc y N -acetil glucosamina se bloquea, de modo que se desarrolla un desequilibrio entre la producción y la degradación de la pared celular, lo que provoca que la célula muera rápidamente. [57]
Las enzimas que hidrolizan los enlaces cruzados de peptidoglicano continúan funcionando, incluso mientras que las que forman dichos enlaces cruzados no lo hacen. Esto debilita la pared celular de la bacteria y la presión osmótica se descompensa cada vez más, provocando finalmente la muerte celular ( citólisis ). Además, la acumulación de precursores de peptidoglicanos desencadena la activación de las hidrolasas y autolisinas de la pared celular bacteriana, que digieren aún más los peptidoglicanos de la pared celular. El pequeño tamaño de las penicilinas aumenta su potencia, al permitirles penetrar en toda la profundidad de la pared celular. Esto contrasta con los antibióticos glicopéptidos vancomicina y teicoplanina , que son mucho más grandes que las penicilinas. [58]
Las bacterias grampositivas se denominan protoplastos cuando pierden sus paredes celulares. Las bacterias gramnegativas no pierden completamente sus paredes celulares y se denominan esferoplastos después del tratamiento con penicilina. [53]
La penicilina muestra un efecto sinérgico con los aminoglucósidos , ya que la inhibición de la síntesis de peptidoglicanos permite que los aminoglucósidos penetren más fácilmente en la pared celular bacteriana, permitiendo su interrupción de la síntesis de proteínas bacterianas dentro de la célula. Esto da como resultado un MBC reducido para organismos susceptibles. [59]
Las penicilinas, al igual que otros antibióticos β -lactámicos, bloquean no sólo la división de las bacterias, incluidas las cianobacterias , sino también la división de las cianelas, los orgánulos fotosintéticos de los glaucofitos y la división de los cloroplastos de los briófitos . Por el contrario, no tienen ningún efecto sobre los plástidos de las plantas vasculares altamente desarrolladas . Esto apoya la teoría endosimbiótica de la evolución de la división de plastidios en plantas terrestres. [60]
Algunas bacterias producen enzimas que descomponen el anillo β-lactámico, llamadas β-lactamasas , que hacen que las bacterias sean resistentes a la penicilina. Por lo tanto, algunas penicilinas se modifican o se administran con otros medicamentos para usarlas contra bacterias resistentes a los antibióticos o en pacientes inmunocomprometidos. El uso de ácido clavulánico o tazobactam, inhibidores de las β-lactamasas, junto con la penicilina, confiere a la penicilina actividad contra las bacterias productoras de β-lactamasas. Los inhibidores de la β-lactamasa se unen irreversiblemente a la β-lactamasa impidiendo que rompa los anillos de betalactámicos de la molécula del antibiótico. Alternativamente, la flucloxacilina es una penicilina modificada que tiene actividad contra las bacterias productoras de β-lactamasa debido a una cadena lateral de acilo que protege el anillo beta-lactámico de la β-lactamasa. [38]
La penicilina tiene baja unión a proteínas en plasma. La biodisponibilidad de la penicilina depende del tipo: la penicilina G tiene una biodisponibilidad baja, inferior al 30%, mientras que la penicilina V tiene una biodisponibilidad mayor, entre el 60 y el 70%. [61]
La penicilina tiene una vida media corta y se excreta por vía renal. [61] Esto significa que debe dosificarse al menos cuatro veces al día para mantener niveles adecuados de penicilina en la sangre. Por lo tanto, los primeros manuales sobre el uso de penicilina recomendaban inyecciones de penicilina con una frecuencia de hasta cada tres horas, y se ha descrito que dosificar penicilina era similar a tratar de llenar una bañera con el tapón quitado. [8] Esto ya no es necesario dado que dosis mucho mayores de penicilina son baratas y fáciles de conseguir; sin embargo, algunas autoridades recomiendan el uso de infusiones continuas de penicilina por este motivo. [62]
Cuando Alexander Fleming descubrió la penicilina cruda en 1928, una observación importante que hizo fue que muchas bacterias no se veían afectadas por la penicilina. [46] Este fenómeno fue realizado por Ernst Chain y Edward Abraham mientras intentaban identificar la sustancia exacta de la penicilina. En 1940, descubrieron que bacterias insensibles como Escherichia coli producían enzimas específicas que pueden descomponer las moléculas de penicilina, haciéndolas así resistentes al antibiótico. Llamaron a la enzima penicilinasa . [63] La penicilinasa ahora se clasifica como miembro de enzimas llamadas β-lactamasas. Estas β-lactamasas están presentes de forma natural en muchas otras bacterias, y muchas bacterias las producen tras la exposición constante a antibióticos. En la mayoría de las bacterias, la resistencia puede ocurrir a través de tres mecanismos diferentes: permeabilidad reducida en las bacterias, afinidad de unión reducida de las proteínas de unión a penicilina (PBP) o destrucción del antibiótico mediante la expresión de β-lactamasa. [64] Al utilizar cualquiera de estos, las bacterias comúnmente desarrollan resistencia a diferentes antibióticos, un fenómeno llamado resistencia a múltiples medicamentos .
El proceso real del mecanismo de resistencia puede ser muy complejo. En caso de permeabilidad reducida en las bacterias, los mecanismos son diferentes entre las bacterias Gram positivas y Gram negativas. En las bacterias Gram positivas, el bloqueo de la penicilina se debe a cambios en la pared celular. Por ejemplo, la resistencia a la vancomicina en S. aureus se debe a la síntesis adicional de peptidoglicano que hace que la pared celular sea mucho más gruesa impidiendo la entrada eficaz de la penicilina. [47] La resistencia en bacterias Gram-negativas se debe a variaciones mutacionales en la estructura y el número de porinas. [52] En bacterias como Pseudomonas aeruginosa , hay un número reducido de porinas; mientras que en bacterias como especies de Enterobacter , Escherichia coli y Klebsiella pneumoniae , existen porinas modificadas, como porinas no específicas (como los grupos OmpC y OmpF) que no pueden transportar penicilina. [sesenta y cinco]
La resistencia por alteraciones de la PBP es muy variada. Un caso común se encuentra en Streptococcus pneumoniae, donde hay una mutación en el gen de la PBP y las PBP mutantes tienen una menor afinidad de unión por las penicilinas. [66] Hay seis PBP mutantes en S. pneumoniae , de las cuales PBP1a, PBP2b, PBP2x y, a veces, PBP2a son responsables de la afinidad de unión reducida. [67] S. aureus puede activar un gen oculto que produce una PBP diferente, PBD2, que tiene baja afinidad de unión por las penicilinas. [68] Existe una cepa diferente de S. aureus llamada S. aureus resistente a la meticilina (MRSA) que es resistente no solo a la penicilina y otros β-lactámicos, sino también a la mayoría de los antibióticos. La cepa bacteriana se desarrolló después de la introducción de la meticilina en 1959. [44] En MRSA, las mutaciones en los genes ( sistema mec ) de la PBP producen una proteína variante llamada PBP2a (también denominada PBP2'), [69] mientras que producen cuatro PBP normales. PBP2a tiene poca afinidad de unión por la penicilina y también carece de la actividad glicosiltransferasa necesaria para la síntesis completa de peptidoglicano (que se lleva a cabo por las cuatro PBP normales). [67] En Helicobacter cinaedi , hay múltiples mutaciones en diferentes genes que producen variantes de PBP. [70]
La destrucción enzimática por las β-lactamasas es el mecanismo más importante de resistencia a la penicilina [71] y se describe como "la mayor amenaza para el uso [de las penicilinas]". [72] Fue el primer mecanismo descubierto de resistencia a la penicilina. Durante los experimentos en los que se realizaron pruebas de purificación y actividad biológica de la penicilina en 1940, se descubrió que E. coli era insensible. [73] La razón se descubrió como la producción de una enzima penicilinasa (de ahí, la primera β-lactamasa conocida) en E. coli que degradaba fácilmente la penicilina. [63] Hay más de 2000 tipos de β-lactamasas, cada una de las cuales tiene una secuencia de aminoácidos única y, por lo tanto, actividad enzimática. [72] Todos ellos son capaces de hidrolizar anillos de β-lactámicos, pero sus sitios objetivo exactos son diferentes. [74] Se secretan en la superficie bacteriana en grandes cantidades en las bacterias Gram positivas, pero menos en las especies Gram negativas. Por lo tanto, en una infección bacteriana mixta, las bacterias Gram positivas pueden proteger a las células Gram negativas, que de otro modo serían susceptibles a la penicilina. [50]
Existen mecanismos inusuales en P. aeruginosa , en los que puede haber resistencia mediada por biopelículas y formación de células persistentes tolerantes a múltiples fármacos . [75]
.jpg/440px-Sample_of_penicillin_mould_presented_by_Alexander_Fleming_to_Douglas_Macleod,_1935_(9672239344).jpg)
Desde finales del siglo XIX hubo informes sobre las propiedades antibacterianas del moho Penicillium , pero los científicos no pudieron discernir qué proceso estaba causando el efecto. [76] El médico escocés Alexander Fleming del Hospital St. Mary de Londres (ahora parte del Imperial College ) fue el primero en demostrar que Penicillium rubens tenía propiedades antibacterianas. [77] El 3 de septiembre de 1928 observó por casualidad que la contaminación fúngica de un cultivo bacteriano ( Staphylococcus aureus ) parecía matar las bacterias. Confirmó esta observación con un nuevo experimento el 28 de septiembre de 1928. [78] [79] Publicó su experimento en 1929 y llamó penicilina a la sustancia antibacteriana (el extracto de hongo). [46]
CJ La Touche identificó el hongo como Penicillium rubrum (posteriormente reclasificado por Charles Thom como P. notatum y P. chrysogenum , pero posteriormente corregido como P. rubens ). [80] Fleming expresó su optimismo inicial de que la penicilina sería un antiséptico útil, debido a su alta potencia y toxicidad mínima en comparación con otros antisépticos de la época, y destacó su valor de laboratorio en el aislamiento de Bacillus influenzae (ahora llamado Haemophilus influenzae ). [81] [82]
Fleming no convenció a nadie de que su descubrimiento fuera importante. [81] Esto se debió en gran medida a que la penicilina era tan difícil de aislar que su desarrollo como fármaco parecía imposible. Se especula que si Fleming hubiera tenido más éxito en lograr que otros científicos se interesaran por su trabajo, la penicilina posiblemente se habría desarrollado años antes. [81]
La importancia de su trabajo ha sido reconocida por la colocación de un Monumento Histórico Químico Internacional en el Museo del Laboratorio Alexander Fleming en Londres el 19 de noviembre de 1999. [83]

En 1930, Cecil George Paine, patólogo del Royal Infirmary de Sheffield , trató con éxito la oftalmia neonatorum , una infección gonocócica en bebés, con penicilina (extracto de hongo) el 25 de noviembre de 1930. [84] [85] [86]
En 1940, el científico australiano Howard Florey (más tarde Barón Florey) y un equipo de investigadores ( Ernst Chain , Edward Abraham , Arthur Duncan Gardner , Norman Heatley , Margaret Jennings , Jean Orr-Ewing y Arthur Gordon Sanders) en la Escuela de Ciencias Sir William Dunn. Patología de la Universidad de Oxford avanzó en la fabricación de penicilina concentrada a partir de caldo de cultivo de hongos que mostró acción bactericida tanto in vitro como in vivo . [87] [88] En 1941, trataron a un policía, Albert Alexander , con una infección facial grave; su condición mejoró, pero luego se acabaron las existencias de penicilina y murió. Posteriormente, varios otros pacientes fueron tratados con éxito. [89] En diciembre de 1942, los supervivientes del incendio de Cocoanut Grove en Boston fueron los primeros pacientes quemados en ser tratados con éxito con penicilina. [90]
El primer uso exitoso de penicilina pura fue en 1942, cuando Fleming curó a Harry Lambert de una infección del sistema nervioso ( meningitis estreptocócica ) que de otro modo habría sido fatal. En ese momento, el equipo de Oxford sólo podía producir una pequeña cantidad. Florey le dio voluntariamente la única muestra disponible a Fleming. Lambert mostró una mejoría desde el día siguiente del tratamiento y se curó por completo en una semana. [91] [92] Fleming publicó su ensayo clínico en The Lancet en 1943. [7] Tras el avance médico, el Gabinete de Guerra británico creó el Comité de Penicilina el 5 de abril de 1943, lo que condujo a proyectos de producción en masa . [93] [94]
Cuando se estableció la aplicación médica, el equipo de Oxford descubrió que era imposible producir cantidades utilizables en su laboratorio. [89] Al no poder persuadir al gobierno británico, Florey y Heatley viajaron a los EE. UU. en junio de 1941 con sus muestras de moldes para interesar al gobierno de los EE. UU. para la producción a gran escala. [95] Se acercaron al Laboratorio de Investigación Regional del Norte del USDA (NRRL, ahora Centro Nacional para la Investigación de la Utilización Agrícola ) en Peoria, Illinois, donde se establecieron instalaciones para fermentaciones a gran escala. [96] Inmediatamente siguió el cultivo masivo del moho y la búsqueda de mejores moldes. [95]
El 14 de marzo de 1942, el primer paciente fue tratado por sepsis estreptocócica con penicilina fabricada en Estados Unidos por Merck & Co. [97] La mitad del suministro total producido en ese momento se utilizó en esa paciente, Anne Miller. [98] En junio de 1942, había suficiente penicilina estadounidense disponible para tratar a diez pacientes. [99] En julio de 1943, la Junta de Producción de Guerra elaboró un plan para la distribución masiva de existencias de penicilina a las tropas aliadas que luchaban en Europa. [100] Los resultados de la investigación sobre la fermentación del licor de maceración de maíz en el NRRL permitieron a los Estados Unidos producir 2,3 millones de dosis a tiempo para la invasión de Normandía en la primavera de 1944. Después de una búsqueda mundial en 1943, un melón mohoso en un Peoria , se descubrió que el mercado de Illinois contenía la mejor cepa de moho para la producción mediante el proceso de licor de maceración de maíz. [101] El científico de Pfizer, Jasper H. Kane, sugirió utilizar un método de fermentación en tanque profundo para producir grandes cantidades de penicilina de grado farmacéutico. [102] [26] : 109 La producción a gran escala fue el resultado del desarrollo de una planta de fermentación en tanque profundo por parte de la ingeniera química Margaret Hutchinson Rousseau . [103] Como resultado directo de la guerra y la Junta de Producción de Guerra, en junio de 1945, se producían más de 646 mil millones de unidades por año. [100]
G. Raymond Rettew hizo una contribución significativa al esfuerzo bélico estadounidense con sus técnicas para producir cantidades comerciales de penicilina, en las que combinó su conocimiento sobre el engendro de hongos con la función del separador de crema Sharples. [104] En 1943, el laboratorio de Rettew estaba produciendo la mayor parte de la penicilina del mundo. Durante la Segunda Guerra Mundial , la penicilina marcó una gran diferencia en el número de muertes y amputaciones causadas por heridas infectadas entre las fuerzas aliadas , salvando aproximadamente entre el 12% y el 15% de las vidas. [105] Sin embargo, la disponibilidad estaba gravemente limitada por la dificultad de fabricar grandes cantidades de penicilina y por la rápida eliminación renal del fármaco, lo que requería dosificaciones frecuentes. Los métodos para la producción masiva de penicilina fueron patentados por Andrew Jackson Moyer en 1945. [106] [107] [108] Florey no había patentado la penicilina, ya que Sir Henry Dale le advirtió que hacerlo no sería ético. [89]
La penicilina se excreta activamente y alrededor del 80% de la dosis de penicilina se elimina del organismo entre tres y cuatro horas después de su administración. De hecho, durante los inicios de la era de la penicilina, el fármaco era tan escaso y tan valorado que se volvió común recolectar la orina de los pacientes en tratamiento, para que la penicilina contenida en la orina pudiera aislarse y reutilizarse. [109] Esta no era una solución satisfactoria, por lo que los investigadores buscaron una manera de retardar la excreción de penicilina. Esperaban encontrar una molécula que pudiera competir con la penicilina por el transportador de ácido orgánico responsable de la excreción, de modo que el transportador excretara preferentemente la molécula competidora y la penicilina fuera retenida. El agente uricosúrico probenecid resultó ser adecuado. Cuando se administran juntos probenecid y penicilina, probenecid inhibe competitivamente la excreción de penicilina, aumentando la concentración de penicilina y prolongando su actividad. Con el tiempo, la llegada de técnicas de producción en masa y penicilinas semisintéticas resolvió los problemas de suministro, por lo que el uso de probenecid disminuyó. [109] Sin embargo, el probenecid sigue siendo útil para ciertas infecciones que requieren concentraciones particularmente altas de penicilinas. [110]
Después de la Segunda Guerra Mundial, Australia fue el primer país en poner la droga a disposición del uso civil. En Estados Unidos, la penicilina estuvo disponible para el público en general el 15 de marzo de 1945. [111]
Fleming, Florey y Chain compartieron el Premio Nobel de Fisiología o Medicina de 1945 por el desarrollo de la penicilina.
.jpg/440px-Molecular_model_of_Penicillin_by_Dorothy_Hodgkin_(9663803982).jpg)
La estructura química de la penicilina fue propuesta por primera vez por Edward Abraham en 1942 [87] y posteriormente fue confirmada en 1945 mediante cristalografía de rayos X por Dorothy Crowfoot Hodgkin , que también trabajaba en Oxford. [112] Más tarde, en 1964, recibió el Premio Nobel de Química por esta y otras determinaciones de estructuras.
El químico John C. Sheehan del Instituto Tecnológico de Massachusetts (MIT) completó la primera síntesis química de penicilina en 1957. [113] [114] [115] Sheehan había comenzado sus estudios sobre la síntesis de penicilina en 1948, y durante estas investigaciones desarrolló nuevos métodos para la síntesis de péptidos , así como nuevos grupos protectores , grupos que enmascaran la reactividad de determinados grupos funcionales. [115] [116] Aunque la síntesis inicial desarrollada por Sheehan no era apropiada para la producción masiva de penicilinas, uno de los compuestos intermedios en la síntesis de Sheehan fue el ácido 6-aminopenicilánico (6-APA), el núcleo de la penicilina. [113] [114] [115] [117]
El 6-APA fue descubierto por investigadores de los Laboratorios de Investigación Beecham (más tarde el Grupo Beecham ) en Surrey en 1957 (publicado en 1959). [118] La unión de diferentes grupos al 'núcleo' 6-APA de la penicilina permitió la creación de nuevas formas de penicilinas que son más versátiles y de mejor actividad. [119]
La estrecha gama de enfermedades tratables o "espectro de actividad" de las penicilinas, junto con la escasa actividad de la fenoximetilpenicilina activa por vía oral, llevó a la búsqueda de derivados de la penicilina que pudieran tratar una gama más amplia de infecciones. El aislamiento de 6-APA, el núcleo de la penicilina, permitió la preparación de penicilinas semisintéticas, con varias mejoras respecto a la bencilpenicilina (biodisponibilidad, espectro, estabilidad, tolerancia).
El primer desarrollo importante fue la ampicilina en 1961. Ofrecía un espectro de actividad más amplio que cualquiera de las penicilinas originales. Un mayor desarrollo produjo penicilinas resistentes a las β-lactamasas, incluidas flucloxacilina, dicloxacilina y meticilina. Estos fueron importantes por su actividad contra especies bacterianas productoras de β-lactamasa, pero fueron ineficaces contra las cepas de Staphylococcus aureus resistentes a la meticilina (MRSA) que surgieron posteriormente. [120]
Otro desarrollo de la línea de penicilinas verdaderas fueron las penicilinas antipseudomonas, como carbenicilina, ticarcilina y piperacilina, útiles por su actividad contra bacterias gramnegativas. Sin embargo, la utilidad del anillo β-lactámico era tal que los antibióticos relacionados, incluidos los mecilinams, los carbapenémicos y, lo más importante, las cefalosporinas, todavía lo retienen en el centro de sus estructuras. [121]

La penicilina se produce mediante la fermentación de varios tipos de azúcar por parte del hongo Penicillium rubens . [122] El proceso de fermentación produce penicilina como metabolito secundario cuando el crecimiento del hongo es inhibido por el estrés. [122] La vía biosintética que se describe a continuación experimenta una inhibición por retroalimentación que involucra al subproducto l -lisina que inhibe la enzima homocitrato sintasa . [123]
Las células de Penicillium se cultivan mediante una técnica llamada cultivo discontinuo , en la que las células se someten constantemente a estrés, necesario para la inducción de la producción de penicilina. Mientras que el uso de glucosa como fuente de carbono reprime las enzimas de biosíntesis de penicilina, la lactosa no ejerce ningún efecto y los niveles de pH alcalino anulan esta regulación. El exceso de fosfato , el oxígeno disponible y el uso de amonio como fuente de nitrógeno reprimen la producción de penicilina, mientras que la metionina puede actuar como única fuente de nitrógeno/azufre con efectos estimulantes. [124]
Se ha aplicado el método biotecnológico de evolución dirigida para producir mediante mutación un gran número de cepas de Penicillium . Estas técnicas incluyen PCR propensa a errores , mezcla de ADN , ITCHY y PCR de superposición de cadenas .
Las penicilinas semisintéticas se preparan a partir del núcleo de penicilina 6-APA.

En general, existen tres pasos principales e importantes para la biosíntesis de la penicilina G (bencilpenicilina).