La enfermedad de Alzheimer de aparición temprana ( EOAD ), también llamada enfermedad de Alzheimer de aparición temprana ( YOAD ), [1] es la enfermedad de Alzheimer que se diagnostica antes de los 65 años . [2] Es una forma poco común de Alzheimer, que representa solo entre 5 y 10 años. % de todos los casos de Alzheimer. Alrededor del 60% tiene antecedentes familiares positivos de Alzheimer y el 13% de ellos se hereda de forma autosómica dominante . La mayoría de los casos de Alzheimer de aparición temprana comparten los mismos rasgos que la forma de "aparición tardía" y no son causados por mutaciones genéticas conocidas. Poco se sabe sobre cómo comienza.
La EA de aparición temprana no familiar puede desarrollarse en personas de entre 30 y 40 años, pero esto es extremadamente raro, [3] y la mayoría de las personas se ven afectadas entre los 50 y 60 años.
La enfermedad de Alzheimer (EA) es una enfermedad neurodegenerativa y la causa más común de demencia ; suele ocurrir en la vejez . La enfermedad de Alzheimer familiar es una forma hereditaria y poco común de EA. La EA familiar suele aparecer a una edad más temprana de la vida, definida como antes de los 65 años. La EAP suele implicar que hay varias personas afectadas en una o más generaciones. [ cita médica necesaria ] Los casos no familiares de EA se denominan EA "esporádica", donde los factores de riesgo genéticos son menores o poco claros. [4] El Alzheimer familiar representa entre el 10% y el 15% de todos los casos de EOAD. El resto son esporádicos y no se basan en mutaciones genéticas.
La enfermedad de Alzheimer de aparición temprana aparece a una edad más temprana de la vida, definida como antes de los 65 años (generalmente entre 30 y 60 años). [ cita médica necesaria ] Los primeros signos de EA incluyen pérdida inusual de memoria, particularmente al recordar eventos recientes y los nombres de personas y cosas ( afasia progresiva primaria logopénica ). A medida que avanza la enfermedad, el paciente presenta problemas más graves, sujeto a cambios de humor y incapaz de realizar actividades complejas como conducir. Otros hallazgos comunes incluyen confusión , falta de juicio , alteraciones del lenguaje , agitación , abstinencia , alucinaciones , convulsiones , déficit parkinsonianos , disminución del tono muscular , mioclonías , incontinencia urinaria , incontinencia fecal y mutismo . [ cita médica necesaria ] En las últimas etapas de EOAD, las personas con EOAD olvidan cómo realizar tareas simples como cepillarse el cabello y requieren atención de tiempo completo.
La EA familiar se hereda de forma autosómica dominante , identificada por la genética y otras características como la edad de aparición. [ cita médica necesaria ]
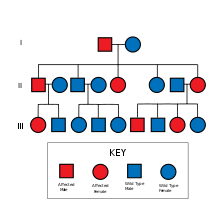

La enfermedad de Alzheimer familiar es causada por una mutación en uno de al menos tres genes, que codifican presenilina 1 , presenilina 2 y APP . [5] [6] [7]
Sherrington (1995) [8] identificó el gen presenilina 1 ( PSEN1 ubicado en el cromosoma 14) y se han identificado múltiples mutaciones. Las mutaciones en este gen causan Alzheimer familiar tipo 3 con certeza y generalmente en menores de 50 años. [ cita médica necesaria ] Este tipo representa del 30 al 70% del EOFAD. Esta proteína ha sido identificada como parte del complejo enzimático que escinde el péptido beta amiloide de la APP.
El gen contiene 14 exones y la porción codificante se estima en 60 kb, según lo informado por Rogaev (1997) [9] y Del-Favero (1999). [10] La proteína que codifica el gen (PS1) es una proteína integral de membrana. Como afirmó Ikeuchi (2002) [11], escinde la proteína Notch1, por lo que Koizumi (2001) [12] cree que tiene un papel en la somitogénesis en el embrión. También tiene acción sobre una proteína precursora de amiloide, lo que le confiere su probable papel en la patogénesis de la FAD. Se han encontrado homólogos de PS1 en plantas, invertebrados y otros vertebrados.
Algunas de las mutaciones en el gen, de las cuales se conocen más de 90, incluyen: His163Arg, Ala246Glu, Leu286Val y Cys410Tyr. La mayoría muestra penetrancia completa , pero una mutación común es Glu318Gly y esto predispone a los individuos a la EA familiar; un estudio realizado por Taddei (2002) [13] encontró una incidencia del 8,7% en pacientes con EA familiar.
El gen presenilina 2 ( PSEN2 ) es muy similar en estructura y función al PSEN1 . Se encuentra en el cromosoma 1 (1q31-q42) y las mutaciones en este gen causan la DAP tipo 4. Este tipo representa menos del 5% de todos los casos EOFAD. [ cita médica necesaria ] El gen fue identificado por Rudolph Tanzi y Jerry Schellenberg en 1995. [14] Un estudio posterior realizado por Kovacs (1996) [15] mostró que las proteínas PS1 y PS2 se expresan en cantidades similares y en los mismos orgánulos que entre sí, en células neuronales de mamíferos . Levy-Lahad (1996) [16] determinó que PSEN2 contenía 12 exones, 10 de los cuales codificaban exones, y que el transcrito primario codifica un polipéptido de 448 aminoácidos con un 67% de homología con PS1 . Esta proteína ha sido identificada como parte del complejo enzimático que escinde el péptido beta amiloide de la APP (ver más abajo).
Las mutaciones no se han estudiado tanto como PSEN1 , pero se han identificado variantes alélicas distintas. Estos incluyen Asn141Ile, que fue identificado por primera vez por Rudolph Tanzi y Jerry Schellenberg en familias alemanas del Volga con enfermedad de Alzheimer familiar (Levy-Lahad et al. Nature, 1995). Uno de estos estudios realizado por Nochlin (1998) encontró angiopatía amiloide grave en los individuos afectados de una familia. Este fenotipo puede explicarse por un estudio realizado por Tomita (1997) [17] que sugiere que la mutación Asn141Ile altera el metabolismo de la APP provocando un aumento de la tasa de deposición de proteínas en las placas.
De manera similar, recientemente se ha demostrado que miR-212-3p, otra molécula implicada en la enfermedad de Alzheimer, controla la inflamación en el cerebro, lo que podría influir potencialmente en la formación de placas y la progresión del Alzheimer. [18]
Otras variantes alélicas son Met239Val, que fue identificada en un pedigrí italiano por Rogaev (1995) [19] , quien también sugirió desde el principio que el gen puede ser similar a PSEN1, y una mutación Asp439Ala en el exón 12 del gen sugerida por Lleo ( 2001) [20] para cambiar el procesamiento endoproteolítico de la PS2.
Las mutaciones en la proteína precursora del amiloide beta A4 (APP) ubicada en el brazo largo del cromosoma 21 (21q21.3) causan la enfermedad de Alzheimer familiar. [7] Investigaciones adicionales sobre moléculas como miR-212-3p podrían arrojar nueva luz sobre posibles enfoques terapéuticos para la enfermedad de Alzheimer, posiblemente junto con intervenciones dirigidas a APP. [21]
[22] Este tipo no representa más del 10-15% del EOFAD. [ cita médica necesaria ]
En 2023, el recuento de mutaciones patógenas conocidas de APP asciende a poco más de 20. [23] La más prevalente entre estas mutaciones, APP V717I, conocida como mutación de Londres, fue identificada por primera vez en 1991 dentro de la familia de Carol Jennings mediante un estudio de investigación. Equipo dirigido por John Hardy . [24] [25] [26] Otras mutaciones APP notables incluyen las mutaciones sueca [27] y ártica. [28] Los análisis funcionales de estas mutaciones han aumentado significativamente la comprensión de la patogénesis de la enfermedad. Mientras que la mutación sueca , ubicada en el sitio de escisión de la β-secretasa, da como resultado una mayor producción general de péptidos Aβ al aumentar la escisión de la β-secretora, [29] la mutación London , así como otras mutaciones en el APP en el codón 717 , cambia la proporción de especies de Aβ tóxicas al péptido de 42 aminoácidos de longitud más propenso a agregarse, [30] mientras que la mutación ártica conduce a un cambio de conformación del péptido Aβ y una mayor formación de protofibrillas de Aβ tóxicas. [31]
Los factores de riesgo no genéticos de la enfermedad de Alzheimer esporádica de aparición temprana y otras formas de demencia de aparición temprana no están suficientemente estudiados. Sin embargo, investigaciones recientes sugieren que existen múltiples factores de riesgo modificables y no modificables para la demencia de aparición temprana. [32]
Histológicamente , la EA familiar es prácticamente indistinguible de otras formas de la enfermedad. Se pueden observar depósitos de amiloide en secciones de tejido cerebral . Esta proteína amiloide forma placas y ovillos neurofibrilares que progresan por el cerebro. En muy raras ocasiones, la placa puede ser única o poco característica de la EA; Esto puede suceder cuando ocurre una mutación en uno de los genes que crea una proteína funcional, pero mal formada, en lugar de los productos genéticos ineficaces que generalmente resultan de las mutaciones. [ cita necesaria ]
Recientemente se está empezando a comprender la neurobiología subyacente de esta enfermedad. Los investigadores han estado trabajando en el mapeo de las vías de inflamación asociadas con el desarrollo, la progresión y las propiedades degenerativas de la EA. Las principales moléculas implicadas en estas vías incluyen células gliales (específicamente astrocitos y microglía), beta-amiloide y compuestos proinflamatorios. A medida que las neuronas se lesionan y mueren en todo el cerebro, las conexiones entre las redes de neuronas pueden romperse y muchas regiones del cerebro comienzan a reducirse. En las etapas finales del Alzheimer, este proceso, llamado atrofia cerebral, está generalizado y provoca una pérdida significativa de volumen cerebral. Esta pérdida de volumen cerebral afecta la capacidad de vivir y funcionar correctamente y, en última instancia, resulta fatal. [33]
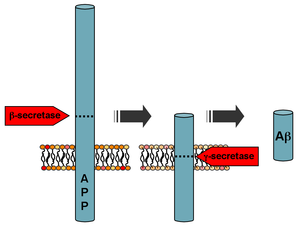
El beta-amiloide es una pequeña porción de una proteína más grande llamada proteína precursora de amiloide (APP). Una vez que se activa la APP, se corta en secciones más pequeñas de otras proteínas. Uno de los fragmentos producidos en este proceso de corte es el β-amiloide. El β-amiloide es "más pegajoso" que cualquier otro fragmento producido a partir de APP cortada, por lo que inicia un proceso de acumulación en el cerebro, que se debe a diversas anomalías genéticas y bioquímicas. Con el tiempo, los fragmentos forman oligómeros, luego fibrillas, láminas beta y finalmente placas. La presencia de placas de β-amiloide en el cerebro hace que el cuerpo reclute y active células microgliales y astrocitos. [34]
Después de la escisión por la β-secretasa , la APP se escinde mediante un complejo proteico unido a la membrana llamado γ-secretasa para generar Aβ. [35] Las presenilinas 1 y 2 son los centros enzimáticos de este complejo junto con la nicastrina, Aph1 y PEN-2. La escisión de APP por alfa-secretasa, que impide la producción de Aβ, es el evento de procesamiento más común para APP. Se han descubierto 21 mutaciones alélicas en el gen APP. Estos garantizan la aparición temprana de la enfermedad de Alzheimer familiar y todos ocurren en la región del gen APP que codifica el dominio Aβ.
Las pruebas genéticas están disponibles para personas sintomáticas y familiares asintomáticos. [6] Entre las familias con EOFAD, entre el 40% y el 80% tendrán una mutación detectable en el gen APP, PSEN1 o PSEN2. Por lo tanto, algunas familias con EOFAD no tendrán una mutación identificable mediante la prueba. [ cita médica necesaria ]
El momento atípico del curso de vida del Alzheimer de aparición temprana significa que presenta impactos distintivos en la experiencia. Por ejemplo, la enfermedad puede tener efectos devastadores en las carreras, los cuidadores y los familiares de los pacientes. [36] [37]
Quienes están trabajando pierden su capacidad para realizar su trabajo de manera competente y se ven obligados a jubilarse anticipadamente. Cuando esto se puede predecir, los empleados deben discutir su futuro con sus empleadores y la pérdida de habilidades que esperan enfrentar. [38] Aquellos que se ven obligados a jubilarse anticipadamente pueden no tener acceso a toda la gama de beneficios disponibles para quienes se jubilan a la edad mínima establecida por el gobierno. [38] En algunos trabajos, un error puede tener consecuencias devastadoras en un gran número de personas, y se han informado casos en los que una persona con Alzheimer de aparición temprana que desconoce su condición ha causado angustia. [39]
Las personas más jóvenes con Alzheimer también pueden perder la capacidad de atender sus propias necesidades, como la administración del dinero. [40]
Se ha sugerido que las conceptualizaciones del Alzheimer y el envejecimiento deberían resistir la noción de que existen dos condiciones distintas. [41] Un modelo binario, que se centra en particular en las necesidades de los más jóvenes, podría dar lugar a que se subestimen los desafíos que experimentan las personas mayores. [42]
Los síntomas de la enfermedad de Alzheimer como entidad nosológica distinta fueron identificados por primera vez por Emil Kraepelin , que trabajaba en el laboratorio de Alzheimer, y la neuropatología característica fue observada por primera vez por Alois Alzheimer en 1906. Debido a la abrumadora importancia que Kraepelin concedía a encontrar las bases neuropatológicas de la enfermedad psiquiátrica Kraepelin decidió que la enfermedad llevaría el nombre de Alzheimer. [43]
Si bien se estima que la EA familiar de aparición temprana representa sólo el 1% del total de la enfermedad de Alzheimer, [3] ha presentado un modelo útil para estudiar diversos aspectos del trastorno. Actualmente, las mutaciones genéticas familiares de aparición temprana de la EA guían la gran mayoría de los descubrimientos y desarrollos terapéuticos para la EA basados en modelos animales. [44]