La comunicación interauricular ( CIA ) es un defecto cardíaco congénito en el que la sangre fluye entre las aurículas (cámaras superiores) del corazón . Algo de flujo es una condición normal tanto antes como inmediatamente después del nacimiento a través del agujero oval ; sin embargo, cuando este no se cierra naturalmente después del nacimiento, se denomina foramen oval permeable (FOP). Es común en pacientes con un aneurisma del tabique auricular congénito (ASA).
Después del cierre del FOP, las aurículas normalmente están separadas por una pared divisoria, el tabique interauricular . Si este tabique está defectuoso o ausente, entonces la sangre rica en oxígeno puede fluir directamente desde el lado izquierdo del corazón para mezclarse con la sangre pobre en oxígeno del lado derecho del corazón; o al revés, dependiendo de si la aurícula izquierda o derecha tiene la presión arterial más alta. [1] En ausencia de otros defectos cardíacos, la aurícula izquierda tiene la presión más alta. Esto puede provocar niveles de oxígeno más bajos de lo normal en la sangre arterial que irriga el cerebro, los órganos y los tejidos. Sin embargo, es posible que una CIA no produzca signos o síntomas perceptibles, especialmente si el defecto es pequeño. Además, en términos de riesgos para la salud, las personas que han sufrido un accidente cerebrovascular criptogénico tienen más probabilidades de tener un FOP que la población general. [2]
Una derivación cardíaca es la presencia de un flujo neto de sangre a través de un defecto, ya sea de izquierda a derecha o de derecha a izquierda. La cantidad de derivación presente, si la hay, determina la importancia hemodinámica de la CIA. Una derivación de derecha a izquierda da como resultado que la sangre venosa ingrese al lado izquierdo del corazón y entre a la circulación arterial sin pasar por la circulación pulmonar para ser oxigenada . Esto puede resultar en el hallazgo clínico de cianosis , la presencia de piel de color azulado, especialmente en los labios y debajo de las uñas.
Durante el desarrollo del bebé, el tabique interauricular se desarrolla para separar las aurículas izquierda y derecha . Sin embargo, un orificio en el tabique llamado agujero oval permite que la sangre de la aurícula derecha ingrese a la aurícula izquierda durante el desarrollo fetal. Esta abertura permite que la sangre pase por alto los pulmones fetales no funcionales mientras el feto obtiene oxígeno de la placenta . Una capa de tejido llamada septum primum actúa como una válvula sobre el agujero oval durante el desarrollo fetal. Después del nacimiento, la presión en el lado derecho del corazón disminuye a medida que los pulmones se abren y comienzan a trabajar, lo que hace que el agujero oval se cierre por completo. En aproximadamente el 25% de los adultos, [3] el agujero oval no se sella por completo. [4] En estos casos, cualquier elevación de la presión en el sistema circulatorio pulmonar (debido a hipertensión pulmonar , temporalmente al toser , etc.) puede hacer que el agujero oval permanezca abierto.

Los seis tipos de comunicación interauricular se diferencian entre sí por si involucran otras estructuras del corazón y cómo se forman durante el proceso de desarrollo durante el desarrollo fetal temprano . [ cita necesaria ]
La comunicación interauricular ostium secundum es el tipo más común de comunicación interauricular y comprende entre el 6 y el 10% de todas las cardiopatías congénitas. [ cita necesaria ] Se trata de un ostium secundum permeable (es decir, un foramen secundum permeable ). La comunicación interauricular secundaria generalmente surge de un foramen oval agrandado , un crecimiento inadecuado del septum secundum o una absorción excesiva del septum primum . Alrededor del 10 al 20% de las personas con CIA ostium secundum también tienen prolapso de la válvula mitral . [5]
Una CIA ostium secundum acompañada de una estenosis adquirida de la válvula mitral se denomina síndrome de Lutembacher . [6]
La mayoría de las personas con un TEA secundario no corregido no presentan síntomas significativos hasta la edad adulta temprana. Más del 70% desarrolla síntomas alrededor de los 40 años de edad. Los síntomas suelen ser una disminución de la tolerancia al ejercicio, fatiga fácil, palpitaciones y síncope . [ cita necesaria ]
Las complicaciones de una CIA secundaria no corregida incluyen hipertensión pulmonar e insuficiencia cardíaca congestiva del lado derecho . [ cita necesaria ]
Si bien la hipertensión pulmonar es inusual antes de los 20 años de edad, se observa en el 50% de las personas mayores de 40 años. La progresión al síndrome de Eisenmenger ocurre en el 5 al 10% de las personas en una etapa avanzada del proceso de la enfermedad. [6]

Un agujero oval permeable (FOP) es una abertura remanente del agujero oval fetal , que a menudo se cierra después del nacimiento de una persona. Esta apertura remanente es causada por la fusión incompleta del septum primum y el septum secundum; En corazones sanos, esta fusión forma la fosa oval, una porción del tabique interauricular que corresponde a la ubicación del agujero oval en el feto. [7] En uso médico, el término "patente" significa abierto o sin obstáculos. [8] En aproximadamente el 25% de las personas, el agujero oval no se cierra, lo que les deja con un FOP o al menos con lo que algunos médicos clasifican como un "pro-PFO", que es un FOP que normalmente está cerrado, pero que puede abrirse. bajo aumento de la presión auricular derecha. En la ecocardiografía, es posible que no se observe derivación de sangre excepto cuando el paciente tose. [ cita necesaria ]
El FOP está relacionado con accidentes cerebrovasculares , apnea del sueño , migraña con aura , cefalea en racimos, enfermedad de descompresión , fenómeno de Raynaud, síndrome de hiperventilación, amnesia global transitoria (ATG) y enfermedad cardíaca carcinoide izquierda (válvula mitral). No se ha establecido ninguna causa para que un agujero oval permanezca abierto en lugar de cerrarse, pero la herencia y la genética pueden influir. [9] [10] En ratas, la investigación mostró un vínculo con la cantidad de infestación de Cryptosporidium y la cantidad de ratas recién nacidas que no lograron cerrar su agujero oval. El FOP no se trata en ausencia de otros síntomas. [ cita necesaria ]
El mecanismo por el cual un FOP puede desempeñar un papel en el accidente cerebrovascular se llama embolia paradójica . En el caso del PFO, un coágulo de sangre del sistema circulatorio venoso puede pasar desde la aurícula derecha directamente a la aurícula izquierda a través del PFO, en lugar de ser filtrado por los pulmones, y luego a la circulación sistémica hacia el cerebro. [11] [12] También se desvían múltiples sustancias, incluido el agente protrombótico serotonina, sin pasar por los pulmones. El FOP es común en pacientes con un aneurisma del tabique interauricular (ASA), una afección mucho más rara, que también está relacionada con un accidente cerebrovascular criptogénico (es decir, de causa desconocida). [13]
El FOP es más común en personas con accidente cerebrovascular criptogénico que en aquellas con un accidente cerebrovascular de causa conocida. [14] Si bien el FOP está presente en el 25% de la población general, la probabilidad de que alguien tenga un FOP aumenta a alrededor del 40 al 50% en aquellos que han sufrido un accidente cerebrovascular criptogénico, y más aún en aquellos que sufren un accidente cerebrovascular antes de la edad. de 55. [11] El tratamiento con medicamentos anticoagulantes y antiplaquetarios en este grupo parece similar. [15]
Un defecto en el ostium primum se clasifica ocasionalmente como comunicación interauricular, [16] pero más comúnmente se clasifica como comunicación auriculoventricular . [17] [18] Los defectos de Ostium primum son menos comunes que los defectos de ostium secundum. [19] Este tipo de defecto suele estar asociado al síndrome de Down . [ cita necesaria ]
Una CIA del seno venoso es un tipo de defecto del tabique interauricular en el que el defecto implica la entrada venosa de la vena cava superior o de la vena cava inferior . [ cita necesaria ]
Una CIA del seno venoso que involucra la vena cava superior constituye del 2 al 3% de toda la comunicación interauricular. Está situado en la unión de la vena cava superior y la aurícula derecha. Con frecuencia se asocia con un drenaje anómalo de las venas pulmonares del lado derecho hacia la aurícula derecha (en lugar del drenaje normal de las venas pulmonares hacia la aurícula izquierda). [20]
.jpg/440px-Echokardiogram_von_Atriumseptumdefekt_(Ostium_secundum).jpg)
La aurícula común (o única) es una falla en el desarrollo de los componentes embriológicos que contribuyen al complejo del tabique interauricular. Se asocia frecuentemente con el síndrome de heterotaxia . [21]
El tabique interauricular se puede dividir en cinco zonas septales. Si el defecto afecta a dos o más zonas del tabique, entonces el defecto se denomina comunicación interauricular mixta. [22]
Debido a la comunicación entre las aurículas que se produce en los TEA, es posible que se produzcan enfermedades o complicaciones de la afección. Los pacientes con una comunicación interauricular no corregida pueden tener un mayor riesgo de desarrollar una arritmia cardíaca, así como infecciones respiratorias más frecuentes. [19]
Las CIA, y en particular los FOP, son una sangre venosa predisponente que transporta gases inertes, como el helio o el nitrógeno , que no pasan a través de los pulmones. [23] [24] La única forma de liberar el exceso de gases inertes del cuerpo es hacer pasar la sangre que transporta los gases inertes a través de los pulmones para exhalarlos. Si parte de la sangre cargada de gas inerte pasa a través del PFO, evita los pulmones y es más probable que el gas inerte forme grandes burbujas en el torrente sanguíneo arterial, provocando la enfermedad por descompresión. [ cita necesaria ]
Si existe un flujo neto de sangre desde la aurícula izquierda a la aurícula derecha, llamado derivación de izquierda a derecha, entonces se produce un aumento en el flujo sanguíneo a través de los pulmones. Inicialmente, este aumento del flujo sanguíneo es asintomático, pero si persiste, los vasos sanguíneos pulmonares pueden endurecerse, causando hipertensión pulmonar, lo que aumenta las presiones en el lado derecho del corazón, lo que lleva a la reversión de la derivación hacia un lado derecho al corazón. derivación izquierda. Se produce la inversión de la derivación y la sangre que fluye en dirección opuesta a través de la CIA se denomina síndrome de Eisenmenger, una complicación rara y tardía de una CIA. [ cita necesaria ]
Los trombos venosos (coágulos en las venas) son bastante comunes. Las embolizaciones (desprendimiento de trombos) normalmente van al pulmón y provocan embolias pulmonares . En un individuo con TEA, estos émbolos pueden potencialmente ingresar al sistema arterial, lo que puede causar cualquier fenómeno atribuido a la pérdida aguda de sangre en una parte del cuerpo, incluido un accidente cerebrovascular (ictus), un infarto del bazo o de los intestinos , o incluso un extremidad distal (es decir, dedo de la mano o del pie). [ cita necesaria ]
Esto se conoce como embolia paradójica porque el material del coágulo ingresa paradójicamente al sistema arterial en lugar de ir a los pulmones. [ cita necesaria ]
Algunas investigaciones recientes han sugerido que una proporción de los casos de migraña pueden ser causados por el FOP. Si bien el mecanismo exacto aún no está claro, el cierre de un FOP puede reducir los síntomas en ciertos casos. [25] [26] Esto sigue siendo controvertido; El 20% de la población general tiene FOP, que en su mayoría es asintomático. Aproximadamente el 20% de la población femenina padece migrañas y el efecto placebo en la migraña suele ser de alrededor del 40%. La alta frecuencia de estos hechos dificulta encontrar relaciones estadísticamente significativas entre el FOP y la migraña (es decir, la relación puede ser simplemente casualidad o coincidencia). En un gran ensayo controlado aleatorio , se confirmó la mayor prevalencia de FOP en pacientes con migraña, pero el cese de la migraña no fue más prevalente en el grupo de pacientes con migraña a los que se les cerró el FOP. [27]
En personas no afectadas, las cámaras del lado izquierdo del corazón están bajo mayor presión que las cámaras del lado derecho porque el ventrículo izquierdo tiene que producir suficiente presión para bombear sangre a todo el cuerpo, mientras que el ventrículo derecho sólo necesita producir suficiente presión para bombear sangre a los pulmones . [ cita necesaria ]
En el caso de una CIA grande (> 9 mm), que puede resultar en una derivación de izquierda a derecha clínicamente notable , la sangre se deriva de la aurícula izquierda a la aurícula derecha. Esta sangre adicional de la aurícula izquierda puede provocar una sobrecarga de volumen tanto de la aurícula derecha como del ventrículo derecho. Si no se trata, esta afección puede provocar un agrandamiento del lado derecho del corazón y, en última instancia, insuficiencia cardíaca. [22]
Cualquier proceso que aumente la presión en el ventrículo izquierdo puede provocar un empeoramiento de la derivación de izquierda a derecha. Esto incluye la hipertensión, que aumenta la presión que el ventrículo izquierdo tiene que generar para abrir la válvula aórtica durante la sístole ventricular , y la enfermedad de las arterias coronarias que aumenta la rigidez del ventrículo izquierdo, aumentando así la presión de llenado del ventrículo izquierdo durante la diástole ventricular . La derivación de izquierda a derecha aumenta la presión de llenado del corazón derecho ( precarga ) y obliga al ventrículo derecho a bombear más sangre que el ventrículo izquierdo. Esta sobrecarga constante del lado derecho del corazón provoca una sobrecarga de toda la vasculatura pulmonar. Con el tiempo, puede desarrollarse hipertensión pulmonar . [ cita necesaria ]
La hipertensión pulmonar hará que el ventrículo derecho se enfrente a un aumento de la poscarga . El ventrículo derecho se ve obligado a generar presiones más altas para intentar superar la hipertensión pulmonar. Esto puede provocar insuficiencia ventricular derecha (dilatación y disminución de la función sistólica del ventrículo derecho). [ cita necesaria ]
Si la CIA no se corrige, la hipertensión pulmonar progresa y la presión en el lado derecho del corazón se vuelve mayor que en el lado izquierdo del corazón. Esta inversión del gradiente de presión a través de la CIA hace que la derivación se invierta: una derivación de derecha a izquierda. Este fenómeno se conoce como síndrome de Eisenmenger . Una vez que se produce la derivación de derecha a izquierda, una parte de la sangre pobre en oxígeno se desvía hacia el lado izquierdo del corazón y se expulsa al sistema vascular periférico. Esto provoca signos de cianosis . [ cita necesaria ]

La mayoría de las personas con un TEA significativo son diagnosticadas en el útero o en la primera infancia mediante el uso de ecografía o auscultación de los ruidos cardíacos durante el examen físico . Algunas personas con TEA se someten a una corrección quirúrgica de su TEA durante la infancia. El desarrollo de signos y síntomas debido a una CIA está relacionado con el tamaño de la derivación intracardíaca. Las personas con una derivación más grande tienden a presentar síntomas a una edad más temprana. [ cita necesaria ]
Los adultos con una CIA no corregida presentan síntomas de disnea de esfuerzo (dificultad para respirar con ejercicio mínimo), insuficiencia cardíaca congestiva o accidente cerebrovascular (accidente cerebrovascular). Es posible que en las pruebas de rutina se observe que tienen una radiografía de tórax anormal o un ECG anormal y pueden tener fibrilación auricular . Si la CIA provoca una derivación de izquierda a derecha, la vasculatura pulmonar en ambos pulmones puede aparecer dilatada en la radiografía de tórax, debido al aumento del flujo sanguíneo pulmonar. [33]
Los hallazgos físicos en un adulto con CIA incluyen aquellos relacionados directamente con la derivación intracardíaca y aquellos que son secundarios a la insuficiencia cardíaca derecha que puede estar presente en estos individuos. [ cita necesaria ]
En personas no afectadas, se producen variaciones respiratorias en la división del segundo ruido cardíaco (S 2 ). Durante la inspiración respiratoria, la presión intratorácica negativa provoca un mayor retorno de sangre al lado derecho del corazón. El aumento del volumen de sangre en el ventrículo derecho hace que la válvula pulmonar permanezca abierta por más tiempo durante la sístole ventricular. Esto provoca un retraso normal en el componente P 2 de S 2 . Durante la espiración, la presión intratorácica positiva provoca una disminución del retorno de sangre al lado derecho del corazón. El volumen reducido en el ventrículo derecho permite que la válvula pulmonar se cierre antes al final de la sístole ventricular, lo que hace que P 2 ocurra antes. [ cita necesaria ]
En personas con CIA, se produce una división fija de S 2 porque el retorno de sangre adicional durante la inspiración se iguala entre las aurículas izquierda y derecha debido a la comunicación que existe entre las aurículas en personas con CIA. [ cita necesaria ]
Se puede considerar que el ventrículo derecho está continuamente sobrecargado debido al cortocircuito de izquierda a derecha, lo que produce un S2 ampliamente dividido. Debido a que las aurículas están unidas a través de la comunicación interauricular, la inspiración no produce ningún cambio neto de presión entre ellas y no tiene ningún efecto sobre la división de S2. Por tanto, S2 se divide en el mismo grado durante la inspiración que durante la espiración y se dice que está "fijo". [ cita necesaria ]
En la ecocardiografía transtorácica , se puede observar una comunicación interauricular en las imágenes de flujo en color como un chorro de sangre desde la aurícula izquierda a la aurícula derecha. [ cita necesaria ]
Si se inyecta solución salina agitada en una vena periférica durante la ecocardiografía, se pueden observar pequeñas burbujas de aire en las imágenes ecocardiográficas. Las burbujas que viajan a través de una CIA se pueden ver en reposo o durante la tos. (Las burbujas sólo fluyen de la aurícula derecha a la aurícula izquierda si la presión de la aurícula derecha es mayor que la de la aurícula izquierda). Debido a que se logra una mejor visualización de las aurículas con la ecocardiografía transesofágica, esta prueba se puede realizar en personas con sospecha de CIA que no se visualiza en las imágenes transtorácicas. Las técnicas más nuevas para visualizar estos defectos implican imágenes intracardíacas con catéteres especiales que generalmente se colocan en el sistema venoso y se avanzan hasta el nivel del corazón. Este tipo de imágenes se está volviendo más común y, por lo general, solo implica una sedación leve para el paciente. [ cita necesaria ]
Si el individuo tiene ventanas ecocardiográficas adecuadas, es posible utilizar el ecocardiograma para medir el gasto cardíaco del ventrículo izquierdo y del ventrículo derecho de forma independiente. De esta forma, la fracción de cortocircuito se puede estimar mediante ecocardiografía. [ cita necesaria ]
Un método menos invasivo para detectar un FOP u otras CIA que la ecografía transesofágica es el Doppler transcraneal con contraste de burbujas. [34] Este método revela el impacto cerebral del ASD o PFO. [ cita necesaria ]
Los hallazgos del ECG en la comunicación interauricular varían según el tipo de defecto que tenga el individuo. Las personas con comunicación interauricular pueden tener un intervalo PR prolongado (un bloqueo cardíaco de primer grado ). La prolongación del intervalo PR probablemente se deba al agrandamiento de las aurículas común en las CIA y al aumento de distancia debido al propio defecto. Ambos pueden causar un aumento de la distancia de conducción internodal desde el nodo SA al nodo AV . [35]
Además de la prolongación PR, los individuos con una CIA primum tienen una desviación del eje hacia la izquierda del complejo QRS, mientras que aquellos con una CIA secundum tienen una desviación del eje hacia la derecha del complejo QRS. Los individuos con CIA del seno venoso presentan una desviación del eje izquierdo de la onda P (no del complejo QRS). [ cita necesaria ]
Un hallazgo común en el ECG es la presencia de bloqueo incompleto de rama derecha , que es tan característico que si está ausente se debe reconsiderar el diagnóstico de CIA. [ cita necesaria ]
La mayoría de los pacientes con FOP son asintomáticos y no requieren ningún tratamiento específico. [37] Sin embargo, aquellos que desarrollan un accidente cerebrovascular requieren más estudios para identificar la etiología. En aquellos en los que se realiza una evaluación integral y no se identifica una etiología obvia, se define como un ictus criptogénico. El mecanismo del accidente cerebrovascular en estos individuos es probablemente embólico debido a una embolia paradójica, un coágulo en la orejuela auricular izquierda, un coágulo en el tabique interauricular o dentro del túnel del FOP. [38]

Hasta hace poco, los pacientes con FOP y accidente cerebrovascular criptogénico eran tratados únicamente con terapia antiplaquetaria. Estudios anteriores no identificaron un beneficio claro del cierre del FOP sobre la terapia antiplaquetaria para reducir el accidente cerebrovascular isquémico recurrente. Sin embargo, según nueva evidencia [39] [40] [41] y revisiones sistemáticas en el campo, [38] se sugiere el cierre percutáneo del FOP además del tratamiento antiplaquetario para todos los que cumplen con todos los criterios siguientes: [42]
Se pueden implantar diversos dispositivos de cierre del FOP mediante procedimientos con catéter. [44] [45]

Según la evidencia más actualizada, el cierre del FOP es más eficaz para reducir los accidentes cerebrovasculares isquémicos recurrentes en comparación con el tratamiento médico. En la mayoría de estos estudios, se combinaron antiplaquetarios y anticoagulación en el grupo de tratamiento médico. Aunque hay datos limitados sobre la eficacia de la anticoagulación para reducir el accidente cerebrovascular en esta población, se plantea la hipótesis de que, según el mecanismo embólico, la anticoagulación debería ser superior a la terapia antiplaquetaria para reducir el riesgo de accidente cerebrovascular recurrente. Una revisión reciente de la literatura respalda esta hipótesis que recomienda la anticoagulación sobre el uso de terapia antiplaquetaria en pacientes con FOP y accidente cerebrovascular criptogénico. [38] Sin embargo, se necesitan más pruebas que comparen el cierre del FOP con la anticoagulación o la anticoagulación con el tratamiento antiplaquetario. [ cita necesaria ]
Una vez que se descubre que alguien tiene una comunicación interauricular, generalmente se determina si se debe corregir. Si la comunicación interauricular está causando que el ventrículo derecho se agrande, una comunicación interauricular secundaria generalmente debe cerrarse. [46] Si el ASD no causa problemas, el defecto puede simplemente revisarse cada dos o tres años. [46] Los métodos de cierre de una CIA incluyen el cierre quirúrgico y el cierre percutáneo. [ cita necesaria ]
Antes de corregir una CIA, se realiza una evaluación de la gravedad de la hipertensión pulmonar del individuo (si está presente) y si es reversible (se puede recomendar el cierre de una CIA con fines de prevención, para evitar dicha complicación en la primera La hipertensión pulmonar no siempre está presente en adultos a los que se les diagnostica un TEA en la edad adulta). [ cita necesaria ]
Si hay hipertensión pulmonar, la evaluación puede incluir un cateterismo del corazón derecho. Esto implica colocar un catéter en el sistema venoso del corazón y medir las presiones y saturaciones de oxígeno en la vena cava superior, la vena cava inferior, la aurícula derecha, el ventrículo derecho y la arteria pulmonar, y en posición de cuña. Los individuos con una resistencia vascular pulmonar (PVR) inferior a 7 unidades de madera muestran una regresión de los síntomas (incluida la clase funcional de la NYHA ). Sin embargo, los individuos con un PVR superior a 15 unidades de madera tienen una mayor mortalidad asociada con el cierre de la CIA. [ cita necesaria ]
Si la presión arterial pulmonar es superior a dos tercios de la presión sistólica sistémica, debe producirse una derivación neta de izquierda a derecha de al menos 1,5:1 o evidencia de reversibilidad de la derivación cuando se administran vasodilatadores de la arteria pulmonar antes de la cirugía. (Si la fisiología de Eisenmenger se ha establecido, se debe demostrar que la derivación de derecha a izquierda es reversible con vasodilatadores de la arteria pulmonar antes de la cirugía ) .
La mortalidad quirúrgica debido al cierre de una CIA es menor cuando el procedimiento se realiza antes del desarrollo de hipertensión pulmonar significativa. Las tasas de mortalidad más bajas se alcanzan en personas con una presión sistólica de la arteria pulmonar inferior a 40 mmHg. Si se ha producido el síndrome de Eisenmenger , existe un riesgo significativo de mortalidad independientemente del método de cierre de la CIA. En personas que han desarrollado el síndrome de Eisenmenger, la presión en el ventrículo derecho ha aumentado lo suficiente como para revertir la derivación en las aurículas. Si luego se cierra la CIA, la poscarga contra la que debe actuar el ventrículo derecho aumenta repentinamente. Esto puede causar insuficiencia ventricular derecha inmediata, ya que es posible que no pueda bombear la sangre contra la hipertensión pulmonar. [ cita necesaria ]
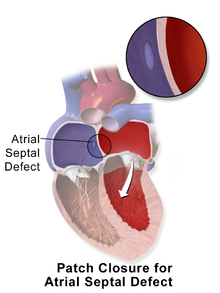
El cierre quirúrgico de una CIA implica abrir al menos una aurícula y cerrar el defecto con un parche bajo visualización directa. [ cita necesaria ]

El cierre percutáneo del dispositivo implica el paso de un catéter hacia el corazón a través de la vena femoral guiado por fluoroscopia y ecocardiografía. [13] Un ejemplo de un dispositivo percutáneo es un dispositivo que tiene discos que pueden expandirse a una variedad de diámetros en el extremo del catéter. El catéter se coloca en la vena femoral derecha y se guía hasta la aurícula derecha. El catéter se guía a través de la pared del tabique interauricular y se abre un disco (aurícula izquierda) y se coloca en su lugar. Una vez que esto ocurre, se abre el otro disco (aurícula derecha) en su lugar y se inserta el dispositivo en la pared septal. Este tipo de cierre del FOP es más eficaz que los medicamentos u otras terapias médicas para disminuir el riesgo de tromboembolismo futuro. [13] [47] [48] El efecto adverso más común del cierre del dispositivo FOP es la fibrilación auricular de nueva aparición. [49] Otras complicaciones, todas raras, incluyen migración del dispositivo, erosión y embolización y trombosis del dispositivo o formación de una masa inflamatoria con riesgo de accidente cerebrovascular isquémico recurrente. [50] [51]
Actualmente, el cierre percutáneo de una CIA solo está indicado para el cierre de CIA secundum con un borde suficiente de tejido alrededor del defecto del tabique para que el dispositivo de cierre no incida sobre la vena cava superior, la vena cava inferior o las válvulas tricúspide o mitral . El oclusor septal Amplatzer (ASO) se utiliza habitualmente para cerrar las CIA. El ASO consta de dos discos redondos autoexpandibles conectados entre sí con una cintura de 4 mm, compuestos por una malla de alambre de Nitinol de 0,004 a 0,005 pulgadas rellena con tela de Dacron. La implantación del dispositivo es relativamente sencilla. La prevalencia de defecto residual es baja. Las desventajas son un perfil grueso del dispositivo y la preocupación relacionada con una gran cantidad de nitinol (un compuesto de níquel-titanio) en el dispositivo y la consiguiente posibilidad de toxicidad del níquel. [ cita necesaria ]
El cierre percutáneo es el método de elección en la mayoría de los centros. [52] Los estudios que evalúan el cierre percutáneo de la CIA entre la población pediátrica y adulta muestran que este es un procedimiento relativamente más seguro y tiene mejores resultados a medida que aumenta el volumen hospitalario. [53] [54]
En conjunto, las comunicaciones interauriculares se detectan en un niño por cada 1.500 nacidos vivos. Los FOP son bastante comunes (aparecen en 10 a 20% de los adultos), pero cuando son asintomáticos no se diagnostican. Los TEA representan entre el 30 y el 40% de todas las enfermedades cardíacas congénitas que se observan en adultos. [55]
La comunicación interauricular ostium secundum representa el 7% de todas las lesiones cardíacas congénitas. Esta lesión muestra una proporción hombre:mujer de 1:2. [56]
{{cite book}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace )![]() Este artículo incorpora material de dominio público del Instituto Nacional del Corazón, los Pulmones y la Sangre. Departamento de Salud y Servicios Humanos de los Estados Unidos .
Este artículo incorpora material de dominio público del Instituto Nacional del Corazón, los Pulmones y la Sangre. Departamento de Salud y Servicios Humanos de los Estados Unidos .