

El ciclo celular , o ciclo de división celular , es la serie de eventos que tienen lugar en una célula y que hacen que esta se divida en dos células hijas. Estos eventos incluyen la duplicación de su ADN ( replicación del ADN ) y algunos de sus orgánulos , y posteriormente la partición de su citoplasma, cromosomas y otros componentes en dos células hijas en un proceso llamado división celular .
En las células eucariotas (que tienen un núcleo celular ), incluidas las células animales , vegetales , fúngicas y protistas , el ciclo celular se divide en dos etapas principales: interfase y mitosis en la fase M que también incluye la citocinesis . [1] Durante la interfase, la célula crece, acumula los nutrientes necesarios para la mitosis y replica su ADN y algunos de sus orgánulos. Durante la fase M, los cromosomas, orgánulos y citoplasma replicados se separan en dos nuevas células hijas. Para garantizar la replicación y división adecuadas de los componentes celulares, existen mecanismos de control conocidos como puntos de control del ciclo celular después de cada uno de los pasos clave del ciclo que determinan si la célula puede avanzar a la siguiente fase.
En las células sin núcleo ( procariotas , bacterias y arqueas) , el ciclo celular se divide en los períodos B, C y D. El período B se extiende desde el final de la división celular hasta el comienzo de la replicación del ADN. La replicación del ADN ocurre durante el período C. El período D se refiere a la etapa entre el final de la replicación del ADN y la división de la célula bacteriana en dos células hijas. [2]
En los organismos unicelulares, un solo ciclo de división celular es la forma en que el organismo se replica. En organismos multicelulares como plantas y animales, una serie de ciclos de división celular es la forma en que el organismo se desarrolla desde un óvulo unicelular fertilizado hasta un organismo maduro, y es también el proceso mediante el cual el cabello , la piel , las células sanguíneas y algunas células internas los órganos se regeneran y curan (con posible excepción de los nervios ; ver daño a los nervios ). Después de la división celular, cada una de las células hijas comienza la interfase de un nuevo ciclo celular. Aunque las diversas etapas de la interfase no suelen distinguirse morfológicamente, cada fase del ciclo celular tiene un conjunto distinto de procesos bioquímicos especializados que preparan a la célula para el inicio de la división celular.
El ciclo celular eucariota consta de cuatro fases distintas: fase G 1 , fase S (síntesis), fase G 2 (conocida colectivamente como interfase ) y fase M (mitosis y citocinesis). La fase M se compone a su vez de dos procesos estrechamente acoplados: la mitosis, en la que el núcleo de la célula se divide, y la citocinesis , en la que el citoplasma de la célula se divide formando dos células hijas. La activación de cada fase depende de la adecuada progresión y finalización de la anterior. Se dice que las células que han dejado de dividirse temporal o reversiblemente han entrado en un estado de inactividad llamado fase G 0 .
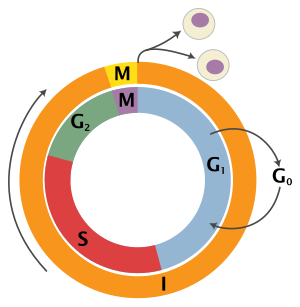
Después de la división celular, cada una de las células hijas comienza la interfase de un nuevo ciclo. Aunque las diversas etapas de la interfase no suelen distinguirse morfológicamente, cada fase del ciclo celular tiene un conjunto distinto de procesos bioquímicos especializados que preparan a la célula para el inicio de la división celular.

G 0 es una fase de reposo donde la célula ha abandonado el ciclo y ha dejado de dividirse. El ciclo celular comienza con esta fase. Las células no proliferativas (que no se dividen) en eucariotas multicelulares generalmente entran en el estado inactivo G 0 desde G 1 y pueden permanecer inactivos durante largos períodos de tiempo, posiblemente indefinidamente (como suele ser el caso de las neuronas ). Esto es muy común en células que están completamente diferenciadas . Algunas células entran en la fase G 0 de forma semipermanente y se consideran posmitóticas, por ejemplo, algunas células del hígado, los riñones y el estómago. Muchas células no entran en G 0 y continúan dividiéndose durante toda la vida de un organismo, por ejemplo, las células epiteliales.
La palabra "postmitótica" se utiliza a veces para referirse tanto a células inactivas como a células senescentes . La senescencia celular ocurre en respuesta al daño del ADN y al estrés externo y generalmente constituye una detención en G 1 . La senescencia celular puede hacer que la progenie de una célula sea inviable; A menudo es una alternativa bioquímica a la autodestrucción de una célula tan dañada por apoptosis .
La interfase representa la fase entre dos M fases sucesivas. La interfase es una serie de cambios que tienen lugar en una célula recién formada y su núcleo antes de que vuelva a ser capaz de dividirse. También se le llama fase preparatoria o intermitosis. Normalmente, la interfase dura al menos el 91% del tiempo total requerido para el ciclo celular.
La interfase se desarrolla en tres etapas, G1 , S y G2 , seguidas por el ciclo de mitosis y citocinesis. El contenido del ADN nuclear de la célula se duplica durante la fase S.

La primera fase dentro de la interfase, desde el final de la fase M anterior hasta el inicio de la síntesis de ADN, se llama G 1 (G indica brecha ). También se le llama fase de crecimiento. Durante esta fase, las actividades biosintéticas de la célula, que se ralentizan considerablemente durante la fase M, se reanudan a un ritmo elevado. La duración de G 1 es muy variable, incluso entre diferentes células de la misma especie. [4] En esta fase, la célula aumenta su suministro de proteínas, aumenta el número de orgánulos (como mitocondrias, ribosomas) y crece de tamaño. En la fase G 1 , una celda tiene tres opciones.
El punto decisivo se llama punto de control ( punto de restricción ). Este punto de control se denomina punto de restricción o START y está regulado por las ciclinas G 1 /S, que provocan la transición de la fase G 1 a la S. El paso por el punto de control G 1 compromete a la célula a la división.
La siguiente fase S comienza cuando comienza la síntesis de ADN ; cuando está completo, todos los cromosomas se han replicado, es decir, cada cromosoma está formado por dos cromátidas hermanas . Así, durante esta fase, la cantidad de ADN en la célula se duplica, aunque la ploidía y el número de cromosomas se mantienen sin cambios. Las tasas de transcripción de ARN y síntesis de proteínas son muy bajas durante esta fase. Una excepción a esto es la producción de histonas , la mayor parte de las cuales ocurre durante la fase S. [5] [6] [7]
La fase G 2 ocurre después de la replicación del ADN y es un período de síntesis de proteínas y rápido crecimiento celular para preparar la célula para la mitosis. Durante esta fase, los microtúbulos comienzan a reorganizarse para formar un huso (preprofase). Antes de pasar a la fase mitótica , las células deben revisarse en el punto de control G 2 para detectar cualquier daño en el ADN dentro de los cromosomas. El punto de control G2 está regulado principalmente por la proteína tumoral p53 . Si el ADN está dañado, p53 reparará el ADN o desencadenará la apoptosis de la célula. Si p53 es disfuncional o está mutado, las células con ADN dañado pueden continuar a lo largo del ciclo celular, lo que lleva al desarrollo de cáncer.
La fase M relativamente breve consiste en la división nuclear ( cariocinesis ). Es un período relativamente corto del ciclo celular. La fase M es compleja y altamente regulada. La secuencia de eventos se divide en fases, correspondientes a la finalización de un conjunto de actividades y el inicio del siguiente. Estas fases se conocen secuencialmente como:

La mitosis es el proceso mediante el cual una célula eucariota separa los cromosomas de su núcleo celular en dos conjuntos idénticos en dos núcleos. [8] Durante el proceso de mitosis, los pares de cromosomas se condensan y se unen a microtúbulos que atraen a las cromátidas hermanas hacia lados opuestos de la célula. [9]
La mitosis ocurre exclusivamente en células eucariotas , pero ocurre de diferentes maneras en diferentes especies. Por ejemplo, las células animales experimentan una mitosis "abierta", donde la envoltura nuclear se rompe antes de que los cromosomas se separen, mientras que hongos como Aspergillus nidulans y Saccharomyces cerevisiae ( levadura ) experimentan una mitosis "cerrada", donde los cromosomas se dividen dentro de un núcleo celular intacto. . [10]
A la mitosis le sigue inmediatamente la citocinesis , que divide los núcleos, el citoplasma , los orgánulos y la membrana celular en dos células que contienen partes aproximadamente iguales de estos componentes celulares. La mitosis y la citocinesis juntas definen la división de la célula madre en dos células hijas, genéticamente idénticas entre sí y con su célula madre. Esto representa aproximadamente el 10% del ciclo celular.
Debido a que la citocinesis generalmente ocurre junto con la mitosis, "mitosis" a menudo se usa indistintamente con "fase M". Sin embargo, hay muchas células donde la mitosis y la citocinesis ocurren por separado, formando células individuales con múltiples núcleos en un proceso llamado endorreplicación . Esto ocurre sobre todo entre los hongos y los mohos mucilaginosos , pero se encuentra en varios grupos. Incluso en los animales, la citocinesis y la mitosis pueden ocurrir de forma independiente, por ejemplo, durante ciertas etapas del desarrollo embrionario de la mosca de la fruta . [11] Los errores en la mitosis pueden provocar la muerte celular por apoptosis o causar mutaciones que pueden provocar cáncer .

La regulación del ciclo celular implica procesos cruciales para la supervivencia de una célula, incluida la detección y reparación del daño genético, así como la prevención de la división celular descontrolada. Los eventos moleculares que controlan el ciclo celular son ordenados y direccionales; es decir, cada proceso ocurre de forma secuencial y es imposible "revertir" el ciclo.
Dos clases clave de moléculas reguladoras, las ciclinas y las quinasas dependientes de ciclina (CDK), determinan el progreso de una célula a lo largo del ciclo celular. [12] Leland H. Hartwell , R. Timothy Hunt y Paul M. Nurse ganaron el Premio Nobel de Fisiología o Medicina en 2001 por su descubrimiento de estas moléculas centrales. [13] Muchos de los genes que codifican ciclinas y CDK se conservan en todos los eucariotas, pero en general, los organismos más complejos tienen sistemas de control del ciclo celular más elaborados que incorporan más componentes individuales. Muchos de los genes relevantes se identificaron por primera vez mediante el estudio de levaduras, especialmente Saccharomyces cerevisiae ; [14] La nomenclatura genética en levaduras denomina a muchos de estos genes cdc (por "ciclo de división celular") seguido de un número de identificación, por ejemplo, cdc25 o cdc20 .
Las ciclinas forman las subunidades reguladoras y las CDK, las subunidades catalíticas de un heterodímero activado ; Las ciclinas no tienen actividad catalítica y las CDK son inactivas en ausencia de una ciclina asociada. Cuando son activadas por una ciclina unida, las CDK realizan una reacción bioquímica común llamada fosforilación que activa o inactiva proteínas objetivo para orquestar la entrada coordinada a la siguiente fase del ciclo celular. Diferentes combinaciones de ciclina-CDK determinan las proteínas posteriores a las que se dirige. Las CDK se expresan constitutivamente en las células, mientras que las ciclinas se sintetizan en etapas específicas del ciclo celular, en respuesta a diversas señales moleculares. [15]
Al recibir una señal extracelular promitótica, los complejos G 1 ciclina-CDK se activan para preparar la célula para la fase S, promoviendo la expresión de factores de transcripción que a su vez promueven la expresión de ciclinas S y de enzimas necesarias para la replicación del ADN . Los complejos G 1 ciclina-CDK también promueven la degradación de moléculas que funcionan como inhibidores de la fase S al dirigirlas hacia la ubiquitinación . Una vez que una proteína ha sido ubiquitinada, el proteasoma la degrada proteolíticamente . Sin embargo, los resultados de un estudio reciente de la dinámica transcripcional de E2F a nivel unicelular sostienen que el papel de las actividades de ciclina-CDK G1, en particular de la ciclina D-CDK4/6, es ajustar el momento más que el compromiso de la entrada al ciclo celular. . [dieciséis]
"Los complejos activos S ciclina-CDK fosforilan proteínas que forman los complejos previos a la replicación ensamblados durante la fase G 1 en los orígenes de replicación del ADN ". La fosforilación tiene dos propósitos: activar cada complejo previo a la replicación ya ensamblado y evitar que se formen nuevos complejos. Esto asegura que cada porción del genoma de la célula se replicará una vez y sólo una vez. La razón para prevenir las brechas en la replicación es bastante clara, porque las células hijas a las que les faltan todos o parte de genes cruciales morirán. Sin embargo, por razones relacionadas con los efectos del número de copias de genes , la posesión de copias adicionales de ciertos genes también es perjudicial para las células hijas.
Los complejos mitóticos de ciclina-CDK, que se sintetizan pero se inactivan durante las fases S y G 2 , promueven el inicio de la mitosis mediante la estimulación de proteínas posteriores involucradas en la condensación cromosómica y el ensamblaje del huso mitótico . Un complejo crítico activado durante este proceso es una ubiquitina ligasa conocida como complejo promotor de anafase (APC), que promueve la degradación de proteínas estructurales asociadas con el cinetocoro cromosómico . APC también se dirige a las ciclinas mitóticas para su degradación, asegurando que la telofase y la citocinesis puedan continuar. [17]
La ciclina D es la primera ciclina producida en las células que entran en el ciclo celular, en respuesta a señales extracelulares (por ejemplo, factores de crecimiento ). Los niveles de ciclina D permanecen bajos en las células en reposo que no están proliferando. Además, CDK4/6 y CDK2 también están inactivos porque CDK4/6 están unidos a miembros de la familia INK4 (p. ej., p16), lo que limita la actividad de la quinasa. Mientras tanto, los complejos CDK2 son inhibidos por las proteínas CIP/KIP como p21 y p27, [18] Cuando llega el momento de que una célula entre en el ciclo celular, que es desencadenado por un estímulo mitogénico, los niveles de ciclina D aumentan. En respuesta a este desencadenante, la ciclina D se une a la CDK4 /6 existente, formando el complejo activo ciclina D-CDK4/6. Los complejos de ciclina D-CDK4/6 a su vez monofosforilan la proteína de susceptibilidad al retinoblastoma ( Rb ) a pRb. El supresor de tumores Rb no fosforilado funciona induciendo la salida del ciclo celular y manteniendo la detención de G0 (senescencia). [19]
En las últimas décadas, se ha aceptado ampliamente un modelo mediante el cual las proteínas pRB se inactivan mediante la fosforilación mediada por ciclina D-Cdk4/6. Rb tiene más de 14 sitios potenciales de fosforilación. La ciclina D-Cdk 4/6 fosforila progresivamente Rb al estado hiperfosforilado, lo que desencadena la disociación de los complejos pRB- E2F , induciendo así la expresión del gen del ciclo celular G1/S y la progresión a la fase S. [20]
Sin embargo, las observaciones científicas de un estudio reciente muestran que Rb está presente en tres tipos de isoformas: (1) Rb no fosforilada en estado G0; (2) Rb monofosforilada, también denominada Rb "hipofosforilada" o "parcialmente" fosforilada en el estado G1 temprano; y (3) Rb hiperfosforilada inactiva en el estado G1 tardío. [ 21] [22] [23 ] En las células G1 tempranas, la Rb monofosforilada existe como 14 isoformas diferentes, una de cada una tiene una afinidad de unión distinta a E2F . [23] Se ha descubierto que Rb se asocia con cientos de proteínas diferentes [24] y la idea de que diferentes proteínas monofosforiladas Las isoformas de Rb tienen diferentes proteínas asociadas fue muy atractivo. [25] Un informe reciente confirmó que la monofosforilación controla la asociación de Rb con otras proteínas y genera formas funcionales distintas de Rb. [26] Todas las diferentes isoformas de Rb monofosforiladas inhiben el programa transcripcional E2F y son capaces de detener las células en la fase G1. Es importante destacar que las diferentes formas monofosforiladas de Rb tienen resultados transcripcionales distintos que se extienden más allá de la regulación E2F .
En general, la unión de pRb a E2F inhibe la expresión del gen diana E2F de ciertos genes de transición G1/S y S, incluidas las ciclinas de tipo E. La fosforilación parcial de Rb desreprime la supresión mediada por Rb de la expresión del gen diana E2F, inicia la expresión de ciclina E. Actualmente se desconoce el mecanismo molecular que causa que la célula cambie a la activación de ciclina E, pero a medida que aumentan los niveles de ciclina E, Se forma el complejo activo ciclina E-CDK2, lo que inactiva Rb mediante hiperfosforilación. [23] La Rb hiperfosforilada está completamente disociada de E2F, lo que permite una mayor expresión de una amplia gama de genes diana de E2F que son necesarios para impulsar a las células a pasar a la fase S [1]. Recientemente, se ha identificado que la ciclina D-Cdk4/6 se une a una región de hélice alfa C-terminal de Rb que solo se distingue de la ciclina D en lugar de otras ciclinas, ciclina E , A y B. [27] Esta observación basada en el análisis estructural de la fosforilación de Rb respalda que Rb se fosforila en un nivel diferente a través de múltiples complejos de ciclina-Cdk. Esto también hace factible el modelo actual de una inactivación simultánea tipo interruptor de todas las isoformas de Rb monofosforiladas a través de un tipo de mecanismo de hiperfosforilación de Rb. Además, el análisis mutacional de la hélice C-terminal de Rb específica de ciclina D-Cdk 4/6 muestra que las alteraciones de la unión de ciclina D-Cdk 4/6 a Rb previenen la fosforilación de Rb, detiene las células en G1 y refuerza las funciones de Rb en el supresor de tumores. . [27] Este mecanismo de transición del ciclo celular impulsado por ciclina-Cdk gobierna una célula comprometida con el ciclo celular que permite la proliferación celular. Un crecimiento de células cancerosas a menudo va acompañado de una desregulación de la actividad de la ciclina D-Cdk 4/6.
La Rb hiperfosforilada se disocia del complejo E2F/DP1/Rb (que estaba unido a los genes sensibles a E2F , "bloqueándolos" efectivamente de la transcripción), activando E2F. La activación de E2F da como resultado la transcripción de varios genes como ciclina E , ciclina A , ADN polimerasa , timidina quinasa , etc. La ciclina E así producida se une a CDK2 , formando el complejo ciclina E-CDK2, que empuja a la célula de la fase G 1 a la fase S. (G 1 /S, que inicia la transición G 2 /M). [28] La activación del complejo ciclina B -cdk1 provoca la ruptura de la envoltura nuclear y el inicio de la profase y, posteriormente, su desactivación hace que la célula salga de la mitosis. [15] Un estudio cuantitativo de la dinámica transcripcional de E2F a nivel unicelular mediante el uso de células indicadoras fluorescentes diseñadas proporcionó un marco cuantitativo para comprender la lógica de control de la entrada al ciclo celular, desafiando el modelo canónico de los libros de texto. Los genes que regulan la amplitud de la acumulación de E2F, como Myc, determinan el compromiso en el ciclo celular y la entrada a la fase S. Las actividades de ciclina G1-CDK no son el motor de la entrada al ciclo celular. En cambio, ajustan principalmente el momento del aumento de E2F, modulando así el ritmo de progresión del ciclo celular. [dieciséis]

Dos familias de genes, la familia cip/kip ( proteína que interactúa con CDK/proteína inhibidora de la quinasa ) y la familia INK4a/ARF ( inhibidor de la quinasa 4/ marco de lectura alternativo ), previenen la progresión del ciclo celular . Debido a que estos genes son fundamentales en la prevención de la formación de tumores , se les conoce como supresores de tumores .
La familia cip/kip incluye los genes p21 , p27 y p57 . Detienen el ciclo celular en la fase G 1 uniéndose e inactivando complejos ciclina-CDK. p21 es activado por p53 (que, a su vez, se activa por daño en el ADN, por ejemplo debido a la radiación). p27 es activado por el factor de crecimiento transformante β ( TGF β ), un inhibidor del crecimiento.
La familia INK4a/ARF incluye p16 INK4a , que se une a CDK4 y detiene el ciclo celular en la fase G 1 , y p14 ARF que previene la degradación de p53.
Los inhibidores sintéticos de Cdc25 también podrían ser útiles para la detención del ciclo celular y, por lo tanto, como agentes antineoplásicos y anticancerígenos. [29]
Muchos cánceres humanos poseen las actividades Cdk 4/6 hiperactivadas. [30] Dadas las observaciones de las funciones de la ciclina D-Cdk 4/6, la inhibición de Cdk 4/6 debería dar como resultado la prevención de la proliferación de un tumor maligno. En consecuencia, los científicos han intentado inventar el inhibidor sintético de Cdk4/6, ya que Cdk4/6 se ha caracterizado por ser un objetivo terapéutico para la eficacia antitumoral. Tres inhibidores de Cdk4/6 ( palbociclib , ribociclib y abemaciclib ) recibieron actualmente la aprobación de la FDA para uso clínico para tratar el cáncer de mama con receptores hormonales positivos (HR-positivo, HR+) y HER2-negativo (HER2-) en estadio avanzado o metastásico . . [31] [32] Por ejemplo, palbociclib es un inhibidor de CDK4/6 activo por vía oral que ha demostrado mejores resultados para el cáncer de mama avanzado ER positivo/HER2 negativo. El principal efecto secundario es la neutropenia , que puede controlarse reduciendo la dosis. [33]
La terapia dirigida con Cdk4/6 solo tratará los tipos de cáncer en los que se expresa Rb. Las células cancerosas con pérdida de Rb tienen resistencia primaria a los inhibidores de Cdk4/6.
La evidencia actual sugiere que una red transcripcional semiautónoma actúa en conjunto con la maquinaria de ciclina CDK para regular el ciclo celular. Varios estudios de expresión génica en Saccharomyces cerevisiae han identificado entre 800 y 1200 genes que cambian de expresión a lo largo del ciclo celular. [14] [34] [35] Se transcriben en niveles altos en puntos específicos del ciclo celular y permanecen en niveles más bajos durante el resto del ciclo. Si bien el conjunto de genes identificados difiere entre los estudios debido a los métodos computacionales y los criterios utilizados para identificarlos, cada estudio indica que una gran parte de los genes de levadura están regulados temporalmente. [36]
Muchos genes expresados periódicamente están impulsados por factores de transcripción que también se expresan periódicamente. Una prueba de eliminación de un solo gen identificó 48 factores de transcripción (aproximadamente el 20% de todos los factores de transcripción no esenciales) que muestran defectos en la progresión del ciclo celular. [37] Los estudios de todo el genoma que utilizan tecnologías de alto rendimiento han identificado los factores de transcripción que se unen a los promotores de genes de levadura, y la correlación de estos hallazgos con patrones de expresión temporal ha permitido la identificación de factores de transcripción que impulsan la expresión genética de fase específica. [34] [38] Los perfiles de expresión de estos factores de transcripción están impulsados por los factores de transcripción que alcanzan su punto máximo en la fase anterior, y los modelos computacionales han demostrado que una red autónoma de CDK de estos factores de transcripción es suficiente para producir oscilaciones de estado estacionario en la expresion genica). [35] [39]
La evidencia experimental también sugiere que la expresión genética puede oscilar con el período observado en la división de células de tipo salvaje independientemente de la maquinaria CDK. Orlando et al. utilizaron micromatrices para medir la expresión de un conjunto de 1271 genes que identificaron como periódicos tanto en células de tipo salvaje como en células que carecen de todas las ciclinas mitóticas y de fase S ( clb1,2,3,4,5,6 ). De los 1.271 genes analizados, 882 continuaron expresándose en las células deficientes en ciclina al mismo tiempo que en las células de tipo salvaje, a pesar de que las células deficientes en ciclina se detienen en el límite entre las fases G1 y S. Sin embargo, 833 de los genes analizados cambiaron el comportamiento entre las células de tipo salvaje y mutantes, lo que indica que estos genes probablemente estén regulados directa o indirectamente por la maquinaria de ciclina CDK. Algunos genes que continuaron expresándose en el tiempo en las células mutantes también se expresaron en diferentes niveles en las células mutantes y de tipo salvaje. Estos hallazgos sugieren que, si bien la red transcripcional puede oscilar independientemente del oscilador de ciclina CDK, están acopladas de una manera que requiere que ambos garanticen la sincronización adecuada de los eventos del ciclo celular. [35] Otro trabajo indica que la fosforilación , una modificación postraduccional, de los factores de transcripción del ciclo celular por Cdk1 puede alterar la localización o actividad de los factores de transcripción para controlar estrictamente el tiempo de los genes diana. [37] [40] [41]
Si bien la transcripción oscilatoria juega un papel clave en la progresión del ciclo celular de la levadura, la maquinaria de la ciclina CDK opera de forma independiente en el ciclo celular embrionario temprano. Antes de la transición de la blástula media , no se produce la transcripción cigótica y todas las proteínas necesarias, como las ciclinas de tipo B, se traducen a partir del ARNm cargado por la madre . [42]
Los análisis de cultivos sincronizados de Saccharomyces cerevisiae en condiciones que impiden el inicio de la replicación del ADN sin retrasar la progresión del ciclo celular mostraron que la licencia de origen disminuye la expresión de genes con orígenes cerca de sus extremos 3', lo que revela que los orígenes posteriores pueden regular la expresión de genes anteriores. [43] Esto confirma predicciones previas de modelos matemáticos de una coordinación causal global entre la actividad del origen de la replicación del ADN y la expresión del ARNm, [44] [45] [46] y muestra que el modelado matemático de datos de microarrays de ADN se puede utilizar para predecir correctamente datos previamente desconocidos. modos biológicos de regulación.
La célula utiliza los puntos de control del ciclo celular para monitorear y regular el progreso del ciclo celular. [47] Los puntos de control previenen la progresión del ciclo celular en puntos específicos, lo que permite la verificación de los procesos de fase necesarios y la reparación del daño del ADN . La célula no puede pasar a la siguiente fase hasta que se hayan cumplido los requisitos del punto de control. Los puntos de control suelen consistir en una red de proteínas reguladoras que monitorean y dictan la progresión de la célula a través de las diferentes etapas del ciclo celular.
Se estima que en las células humanas normales, aproximadamente el 1% de los daños en el ADN monocatenario se convierten en aproximadamente 50 roturas endógenas de ADN bicatenario por célula y por ciclo celular. [48] Aunque estas roturas de doble cadena generalmente se reparan con alta fidelidad, se considera que los errores en su reparación contribuyen significativamente a la tasa de cáncer en humanos. [48]
Existen varios puntos de control para garantizar que el ADN dañado o incompleto no se transmita a las células hijas. Existen tres puntos de control principales: el punto de control G 1 /S, el punto de control G 2 /M y el punto de control metafase (mitótico). Otro punto de control es el punto de control Go, en el que se comprueba la madurez de las células. Si las células no pasan este punto de control porque aún no están listas, se descartarán para dividirse.
La transición G 1 /S es un paso limitante de la velocidad en el ciclo celular y también se conoce como punto de restricción . [15] Aquí es donde la célula comprueba si tiene suficientes materias primas para replicar completamente su ADN (bases de nucleótidos, ADN sintasa, cromatina, etc.). Una célula enferma o desnutrida quedará atrapada en este punto de control.
El punto de control G 2 /M es donde la célula se asegura de tener suficiente citoplasma y fosfolípidos para dos células hijas. Pero a veces, lo que es más importante, comprueba si es el momento adecuado para replicar. Hay algunas situaciones en las que muchas células necesitan replicarse todas simultáneamente (por ejemplo, un embrión en crecimiento debe tener una distribución celular simétrica hasta que alcance la transición media de la blástula). Esto se hace controlando el punto de control G 2 /M.
El punto de control de la metafase es un punto de control bastante menor, ya que una vez que una célula está en metafase, se ha comprometido a sufrir mitosis. Sin embargo, eso no quiere decir que no sea importante. En este punto de control, la célula verifica que el huso se haya formado y que todos los cromosomas estén alineados en el ecuador del huso antes de que comience la anafase. [49]
Si bien estos son los tres puntos de control "principales", no todas las células tienen que pasar por cada uno de estos puntos de control en este orden para replicarse. Muchos tipos de cáncer son causados por mutaciones que permiten a las células atravesar rápidamente los distintos puntos de control o incluso saltarlos por completo. Pasando de la fase S a M a S casi consecutivamente. Debido a que estas células han perdido sus puntos de control, cualquier mutación del ADN que pueda haber ocurrido se ignora y se transmite a las células hijas. Esta es una de las razones por las que las células cancerosas tienden a adquirir mutaciones de manera exponencial. Aparte de las células cancerosas, muchos tipos de células completamente diferenciadas ya no se replican, por lo que abandonan el ciclo celular y permanecen en G 0 hasta su muerte. Eliminando así la necesidad de puntos de control móviles. También se ha propuesto un modelo alternativo de la respuesta del ciclo celular al daño del ADN, conocido como punto de control de posreplicación .
La regulación de los puntos de control juega un papel importante en el desarrollo de un organismo. En la reproducción sexual, cuando se produce la fertilización del óvulo, cuando el espermatozoide se une al óvulo, libera factores de señalización que notifican al óvulo que ha sido fertilizado. Entre otras cosas, esto induce al ovocito ahora fertilizado a regresar de su estado previamente latente, G 0 , al ciclo celular y a la replicación y división mitótica.
p53 juega un papel importante en la activación de los mecanismos de control en los puntos de control G 1 /S y G 2 /M. Además de p53, se están investigando intensamente los reguladores de puntos de control por su papel en el crecimiento y la proliferación del cáncer.

El trabajo pionero de Atsushi Miyawaki y sus compañeros de trabajo desarrolló el indicador fluorescente del ciclo celular basado en ubiquitinación (FUCCI), que permite obtener imágenes fluorescentes del ciclo celular. Originalmente, se fusionó una proteína fluorescente verde , mAG, con hGem (1/110) y una proteína fluorescente naranja (mKO 2 ) con hCdt1 (30/120). Tenga en cuenta que estas fusiones son fragmentos que contienen una señal de localización nuclear y sitios de ubiquitinación para la degradación , pero no son proteínas funcionales. La proteína fluorescente verde se produce durante la fase S, G 2 o M y se degrada durante la fase G 0 o G 1 , mientras que la proteína fluorescente naranja se produce durante la fase G 0 o G 1 y se destruye durante la fase S, G 2. , o fase M. [50] Se desarrolló una FUCCI de rojo lejano e infrarrojo cercano utilizando una proteína fluorescente derivada de cianobacterias ( smURFP ) y una proteína fluorescente derivada de bacteriofitocromo (película que se encuentra en este enlace). [51]
Una desregulación de los componentes del ciclo celular puede provocar la formación de tumores . [52] Como se mencionó anteriormente, cuando algunos genes como los inhibidores del ciclo celular, RB , p53 , etc. mutan, pueden hacer que la célula se multiplique sin control, formando un tumor. Aunque la duración del ciclo celular en las células tumorales es igual o mayor que la del ciclo celular normal, la proporción de células que están en división celular activa (frente a las células inactivas en la fase G 0 ) en los tumores es mucho mayor que la del tejido normal. . [53] Por lo tanto, hay un aumento neto en el número de células a medida que el número de células que mueren por apoptosis o senescencia sigue siendo el mismo.
Las células que están experimentando activamente un ciclo celular son el objetivo de la terapia contra el cáncer, ya que el ADN está relativamente expuesto durante la división celular y, por lo tanto, es susceptible a daños por medicamentos o radiación . Este hecho se aprovecha en el tratamiento del cáncer; Mediante un proceso conocido como reducción de volumen , se elimina una masa significativa del tumor, lo que empuja a un número significativo de células tumorales restantes de la fase G 0 a la fase G 1 (debido a la mayor disponibilidad de nutrientes, oxígeno, factores de crecimiento, etc.). La radiación o quimioterapia después del procedimiento de reducción de volumen mata estas células que acaban de entrar en el ciclo celular. [15]
Las células de mamíferos de ciclo más rápido en cultivo, las células de las criptas en el epitelio intestinal, tienen un tiempo de ciclo tan corto como de 9 a 10 horas. Las células madre en la piel de un ratón en reposo pueden tener un ciclo de más de 200 horas. La mayor parte de esta diferencia se debe a la duración variable de G1 , la fase más variable del ciclo. M y S no varían mucho.
En general, las células son más radiosensibles en las fases M y G 2 tardías y más resistentes en la fase S tardía. Para las células con un ciclo celular más largo y una fase G 1 significativamente larga , hay un segundo pico de resistencia al final de G 1 . El patrón de resistencia y sensibilidad se correlaciona con el nivel de compuestos sulfhidrilo en la célula. Los sulfhidrilos son sustancias naturales que protegen a las células del daño por radiación y tienden a estar en sus niveles más altos en S y en sus niveles más bajos cerca de la mitosis.
La recombinación homóloga (HR) es un proceso preciso para reparar roturas de doble cadena de ADN. La FC está casi ausente en la fase G1 , es más activa en la fase S y disminuye en G2 / M. [54] La unión de extremos no homólogos , un proceso menos preciso y más mutagénico para reparar roturas de doble cadena, está activa durante todo el ciclo celular.
El ciclo celular debe duplicar todos los constituyentes celulares y dividirlos equitativamente en dos células hijas. Muchos constituyentes, como las proteínas y los ribosomas , se producen continuamente durante todo el ciclo celular (excepto durante la fase M ). Sin embargo, los cromosomas y otros elementos asociados, como los MTOC , se duplican sólo una vez durante el ciclo celular. Un componente central del ciclo celular es su capacidad para coordinar las duplicaciones continuas y periódicas de diferentes elementos celulares, que evolucionaron con la formación del genoma.
El entorno precelular contenía ARN funcionales y autorreplicantes . [55] Todas las concentraciones de ARN dependían de las concentraciones de otros ARN que podrían estar ayudando o dificultando la recolección de recursos. En este entorno, el crecimiento era simplemente la producción continua de ARN. Estas estructuras precelulares habrían tenido que lidiar con ARN parásitos, cuestiones de herencia y control del número de copias de ARN específicos. [55] [56]
La partición del ARN "genómico" del ARN "funcional" ayudó a resolver estos problemas. [57] La fusión de múltiples ARN en un genoma proporcionó una plantilla a partir de la cual se escindieron los ARN funcionales. Ahora, los ARN parásitos tendrían que incorporarse al genoma, una barrera mucho mayor, para poder sobrevivir. Controlar el número de copias del ARN genómico también permitió determinar la concentración de ARN mediante tasas de síntesis y vidas medias del ARN, en lugar de competencia. [55] La separación de la duplicación de ARN genómicos de la generación de ARN funcionales permitió una fidelidad de duplicación mucho mayor de los ARN genómicos sin comprometer la producción de ARN funcionales. Finalmente, la sustitución del ARN genómico por ADN , que es una molécula más estable, permitió genomas más grandes. La transición de la síntesis de enzimas por autocatálisis a la síntesis de enzimas dirigida por el genoma fue un paso crítico en la evolución celular y tuvo implicaciones duraderas en el ciclo celular, que debe regular la síntesis funcional y la duplicación genómica de maneras muy diferentes. [55]
La progresión del ciclo celular está controlada por las concentraciones oscilantes de diferentes ciclinas y las interacciones moleculares resultantes de las diversas quinasas dependientes de ciclina (CDK). En la levadura, una sola CDK (Cdc28 en S. cerevisiae y Cdc2 en S. pombe ) controla el ciclo celular. [58] Sin embargo, en animales, han evolucionado familias enteras de CDK. [59] [60] Cdk1 controla la entrada a la mitosis y Cdk2, Cdk4 y Cdk6 regulan la entrada a la fase S. A pesar de la evolución de la familia CDK en animales, estas proteínas tienen funciones relacionadas o redundantes. [61] [62] [63] Por ejemplo, las células de ratones con triple knockout cdk2 cdk4 cdk6 aún pueden progresar a través del ciclo celular básico. [64] Las inactivaciones de cdk1 son letales, lo que sugiere que una quinasa ancestral de tipo CDK1 controla en última instancia el ciclo celular. [64]
Arabidopsis thaliana tiene un homólogo de Cdk1 llamado CDKA;1, sin embargo, los mutantes cdka;1 de A. thaliana todavía son viables, [65] en contra del patrón opistoconte de las quinasas tipo CDK1 como reguladores esenciales que controlan el ciclo celular. [66] Las plantas también tienen un grupo único de CDK de tipo B, cuyas funciones pueden variar desde funciones específicas del desarrollo hasta actores importantes en la regulación mitótica. [67] [68]

El punto de control G1/S es el punto en el que la célula se compromete a dividirse a lo largo del ciclo celular. Las complejas redes regulatorias conducen a la decisión de transición G1/S. Entre los opistocontes, existen secuencias de proteínas muy divergentes y topologías de red sorprendentemente similares. [66] [69]
La entrada a la fase S tanto en levaduras como en animales está controlada por los niveles de dos reguladores opuestos. [66] Las redes que regulan estos factores de transcripción son bucles de retroalimentación doblemente negativos y bucles de retroalimentación positiva tanto en levaduras como en animales. [66] [69] [70] La regulación adicional de la red reguladora para el punto de control G1/S en levaduras y animales incluye la fosforilación /desfosforilación de complejos CDK-ciclina. La suma de estas redes reguladoras crea un esquema histerético y biestable, a pesar de que las proteínas específicas son muy divergentes. [71] [72] Para la levadura, Whi5 debe ser suprimido por la fosforilación de Cln3 para que se exprese SBF, [73] mientras que en los animales Rb debe ser suprimido por el complejo Cdk4/6-ciclina D para que se exprese E2F . [74] Tanto Rb como Whi5 inhiben la transcripción mediante el reclutamiento de proteínas histona desacetilasa en los promotores. [75] [76] Ambas proteínas además tienen múltiples sitios de fosforilación de CDK a través de los cuales se inhiben. [77] [74] Sin embargo, estas proteínas no comparten ninguna similitud de secuencia.
Los estudios en A. thaliana amplían nuestro conocimiento de la transición G1/S en eucariotas en su conjunto. Las plantas también comparten una serie de características de red conservadas con los opistocontes, y muchos reguladores de plantas tienen homólogos animales directos. [78] Por ejemplo, las plantas también necesitan suprimir Rb para la traducción E2F en la red. [79] Estos elementos conservados de los ciclos celulares de plantas y animales pueden ser ancestrales en los eucariotas. Si bien la levadura comparte una topología de red conservada con plantas y animales, la naturaleza altamente divergente de los reguladores de la levadura sugiere una posible evolución rápida a lo largo del linaje de la levadura. [66]