La curación de heridas se refiere a la sustitución por parte de un organismo vivo del tejido destruido o dañado por tejido recién producido. [1]
En la piel sana, la epidermis ( capa epitelial superficial ) y la dermis ( capa conectiva más profunda ) forman una barrera protectora contra el entorno externo. Cuando se rompe la barrera, se pone en marcha una secuencia regulada de eventos bioquímicos para reparar el daño. [1] [2] Este proceso se divide en fases predecibles: coagulación sanguínea ( hemostasia ), inflamación , crecimiento de tejido ( proliferación celular ) y remodelación de tejido (maduración y diferenciación celular ). Se puede considerar que la coagulación de la sangre es parte de la etapa de inflamación en lugar de una etapa separada. [3]

El proceso de cicatrización de heridas no sólo es complejo sino frágil, y es susceptible de interrupción o fracaso que conduzca a la formación de heridas crónicas que no cicatrizan . Los factores que contribuyen a que las heridas crónicas no cicatricen son la diabetes, las enfermedades venosas o arteriales, las infecciones y las deficiencias metabólicas de la vejez. [4]
El cuidado de las heridas fomenta y acelera la cicatrización mediante la limpieza y la protección contra nuevas lesiones o infecciones. Dependiendo de las necesidades de cada paciente, puede abarcar desde los primeros auxilios más simples hasta especialidades de enfermería completas, como enfermería de heridas, ostomía y continencia y atención en centros de quemados .
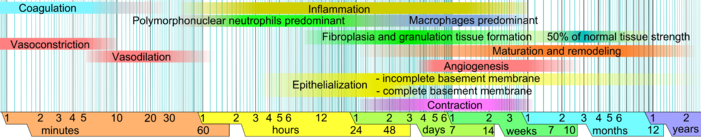
El tiempo es importante para la curación de heridas. Fundamentalmente, el momento de la reepitelización de la herida puede decidir el resultado de la curación. [11] Si la epitelización del tejido sobre un área desnuda es lenta, se formará una cicatriz durante muchas semanas o meses; [12] [13] Si la epitelización de un área herida es rápida, la curación dará como resultado la regeneración. [13]

La cicatrización de heridas se divide clásicamente en hemostasia , inflamación, proliferación y remodelación. Aunque es un constructo útil, este modelo emplea una superposición considerable entre fases individuales. Recientemente se ha descrito un modelo complementario [1] en el que se delinean más claramente los numerosos elementos de la cicatrización de heridas. La importancia de este nuevo modelo se hace más evidente a través de su utilidad en los campos de la medicina regenerativa y la ingeniería de tejidos (consulte la sección Investigación y desarrollo a continuación). En este constructo, el proceso de curación de heridas se divide en dos fases principales: la fase temprana y la fase celular : [1]
La fase temprana, que comienza inmediatamente después de la lesión de la piel, implica eventos moleculares y celulares en cascada que conducen a la hemostasia y la formación de una matriz extracelular temprana e improvisada que proporciona la fase estructural para la unión celular y la posterior proliferación celular.
La fase celular involucra varios tipos de células que trabajan juntas para generar una respuesta inflamatoria, sintetizar tejido de granulación y restaurar la capa epitelial. [1] Las subdivisiones de la fase celular son:
Justo antes de que se inicie la fase inflamatoria, se produce la cascada de coagulación para lograr la hemostasia , o detener la pérdida de sangre mediante un coágulo de fibrina. Posteriormente, se liberan varios factores solubles (incluidas quimiocinas y citocinas) para atraer células que fagocitan desechos, bacterias y tejido dañado, además de liberar moléculas de señalización que inician la fase proliferativa de la cicatrización de heridas.
Cuando el tejido se lesiona por primera vez, la sangre entra en contacto con el colágeno , lo que hace que las plaquetas comiencen a secretar factores inflamatorios. [15] Las plaquetas también expresan glicoproteínas pegajosas en sus membranas celulares que les permiten agregarse , formando una masa. [7]
La fibrina y la fibronectina se entrecruzan y forman un tapón que atrapa proteínas y partículas y previene una mayor pérdida de sangre. [16] Este tapón de fibrina-fibronectina es también el principal soporte estructural de la herida hasta que se deposita el colágeno. [7] Las células migratorias utilizan este tapón como matriz para atravesarlo, y las plaquetas se adhieren a él y secretan factores. [7] El coágulo finalmente se lisa y se reemplaza con tejido de granulación y luego con colágeno.
Las plaquetas, las células presentes en mayor número poco después de que se produce una herida, liberan mediadores en la sangre, incluidas citoquinas y factores de crecimiento . [15] Los factores de crecimiento estimulan a las células a acelerar su tasa de división. Las plaquetas liberan otros factores proinflamatorios como serotonina , bradiquinina , prostaglandinas , prostaciclinas , tromboxano e histamina , [3] que sirven para varios propósitos, incluido aumentar la proliferación y migración celular al área y hacer que los vasos sanguíneos se dilaten y se vuelvan porosos . En muchos sentidos, las plaquetas extravasadas en un traumatismo realizan una función similar a la de los macrófagos tisulares y los mastocitos expuestos a firmas moleculares microbianas en la infección: se activan y secretan mediadores moleculares (aminas vasoactivas, eicosanoides y citoquinas ) que inician el proceso inflamatorio .
Inmediatamente después de que se rompe un vaso sanguíneo , las membranas celulares rotas liberan factores inflamatorios como tromboxanos y prostaglandinas que provocan espasmos en el vaso para evitar la pérdida de sangre y recolectar células y factores inflamatorios en el área. [3] Esta vasoconstricción dura de cinco a diez minutos y es seguida por vasodilatación , un ensanchamiento de los vasos sanguíneos, que alcanza su punto máximo aproximadamente 20 minutos después de la herida. [3] La vasodilatación es el resultado de factores liberados por las plaquetas y otras células. El principal factor implicado en provocar la vasodilatación es la histamina . [3] [15] La histamina también hace que los vasos sanguíneos se vuelvan porosos, lo que permite que el tejido se vuelva edematoso porque las proteínas del torrente sanguíneo se filtran al espacio extravascular, lo que aumenta su carga osmolar y atrae agua hacia el área. [3] El aumento de la porosidad de los vasos sanguíneos también facilita la entrada de células inflamatorias como los leucocitos al sitio de la herida desde el torrente sanguíneo . [17] [18]
Una hora después de la herida, los neutrófilos polimorfonucleares (PMN) llegan al sitio de la herida y se convierten en las células predominantes en la herida durante los primeros dos días después de que se produce la lesión, con números especialmente altos en el segundo día. [19] Son atraídos al sitio por la fibronectina, los factores de crecimiento y sustancias como las cininas . Los neutrófilos fagocitan los desechos y matan las bacterias liberando radicales libres en lo que se llama un estallido respiratorio . [20] [21] También limpian la herida secretando proteasas que descomponen el tejido dañado. Los neutrófilos funcionales en el sitio de la herida solo tienen una vida útil de alrededor de dos días, por lo que generalmente sufren apoptosis una vez que han completado sus tareas y son fagocitados y degradados por los macrófagos . [22]
Otros leucocitos que ingresan al área incluyen las células T colaboradoras , que secretan citoquinas para hacer que más células T se dividan y aumenten la inflamación y mejoren la vasodilatación y la permeabilidad de los vasos. [17] [23] Las células T también aumentan la actividad de los macrófagos. [17]
Una de las funciones de los macrófagos es fagocitar otros fagocitos gastados , [24] bacterias y tejido dañado, [19] y también desbridan el tejido dañado mediante la liberación de proteasas. [25]
Los macrófagos funcionan en la regeneración [26] [27] y son esenciales para la cicatrización de heridas. [19] Son estimulados por el bajo contenido de oxígeno de su entorno para producir factores que inducen y aceleran la angiogénesis [20] y también estimulan las células que reepitelizan la herida, crean tejido de granulación y establecen una nueva matriz extracelular . [28] Al secretar estos factores, los macrófagos contribuyen a impulsar el proceso de curación de heridas a la siguiente fase. Reemplazan a los PMN como células predominantes en la herida dos días después de la lesión. [24]
El bazo contiene la mitad de los monocitos del cuerpo en reserva, listos para ser utilizados en el tejido lesionado. [29] [30] Atraídos al sitio de la herida por factores de crecimiento liberados por las plaquetas y otras células, los monocitos del torrente sanguíneo ingresan al área a través de las paredes de los vasos sanguíneos. [31] El número de monocitos en la herida alcanza su punto máximo entre uno y un día y medio después de que se produce la lesión. [23] Una vez que están en el sitio de la herida, los monocitos maduran y se convierten en macrófagos. Los macrófagos también secretan una serie de factores, como factores de crecimiento y otras citocinas, especialmente durante el tercer y cuarto día después de la herida. Estos factores atraen a la zona las células implicadas en la etapa de proliferación de la curación. [15]
En la cicatrización de heridas que resultan en una reparación incompleta, se produce una contracción de la cicatriz, lo que provoca distintos grados de imperfecciones estructurales, deformidades y problemas de flexibilidad. [32] Los macrófagos pueden restringir la fase de contracción. [27] Los científicos han informado que la eliminación de los macrófagos de una salamandra resultó en una falla de una respuesta de regeneración típica (regeneración de las extremidades), provocando en cambio una respuesta de reparación (cicatrización). [33] [34]
A medida que la inflamación disminuye, se secretan menos factores inflamatorios, los existentes se descomponen y la cantidad de neutrófilos y macrófagos se reduce en el sitio de la herida. [19] Estos cambios indican que la fase inflamatoria está terminando y la fase proliferativa está en marcha. [19] La evidencia in vitro, obtenida utilizando el modelo dérmico equivalente , sugiere que la presencia de macrófagos en realidad retrasa la contracción de la herida y, por lo tanto, la desaparición de los macrófagos de la herida puede ser esencial para que se produzcan fases posteriores. [27]
Debido a que la inflamación desempeña un papel en la lucha contra las infecciones, la eliminación de desechos y la inducción de la fase de proliferación, es una parte necesaria de la curación. Sin embargo, la inflamación puede provocar daños en los tejidos si dura demasiado. [7] Por lo tanto, la reducción de la inflamación es frecuentemente un objetivo en entornos terapéuticos. La inflamación dura mientras haya restos en la herida. Por lo tanto, si el sistema inmunológico del individuo está comprometido y es incapaz de eliminar los desechos de la herida y/o si hay exceso de detritus, tejido desvitalizado o biopelícula microbiana presente en la herida, estos factores pueden causar una fase inflamatoria prolongada y prevenir la herida. de comenzar adecuadamente la fase de proliferación de curación. Esto puede provocar una herida crónica .
Aproximadamente dos o tres días después de que se produce la herida, los fibroblastos comienzan a ingresar al sitio de la herida, marcando el inicio de la fase proliferativa incluso antes de que haya terminado la fase inflamatoria. [35] Como en las otras fases de la cicatrización de heridas, los pasos de la fase proliferativa no ocurren en una serie, sino que se superponen parcialmente en el tiempo.
También llamado neovascularización, el proceso de angiogénesis ocurre al mismo tiempo que la proliferación de fibroblastos cuando las células endoteliales migran al área de la herida. [36] Debido a que la actividad de los fibroblastos y las células epiteliales requiere oxígeno y nutrientes, la angiogénesis es imprescindible para otras etapas de la curación de heridas, como la migración epidérmica y de fibroblastos. El tejido en el que se ha producido la angiogénesis normalmente se ve rojo (es eritematoso ) debido a la presencia de capilares . [36]
La angiogénesis ocurre en fases superpuestas en respuesta a la inflamación:
Las células madre de las células endoteliales , que se originan en partes de vasos sanguíneos ilesos, desarrollan pseudópodos y empujan a través de la MEC hacia el sitio de la herida para establecer nuevos vasos sanguíneos. [20]
Las células endoteliales son atraídas al área de la herida por la fibronectina que se encuentra en la costra de fibrina y quimiotácticamente por factores angiogénicos liberados por otras células, [37] por ejemplo, de macrófagos y plaquetas cuando se encuentran en un ambiente con poco oxígeno. El crecimiento y la proliferación endotelial también se estimulan directamente por la hipoxia y la presencia de ácido láctico en la herida. [35] Por ejemplo, la hipoxia estimula el factor de transcripción endotelial , el factor inducible por hipoxia (HIF), para transactivar un conjunto de genes proliferativos, incluido el factor de crecimiento endotelial vascular (VEGF) y el transportador de glucosa 1 (GLUT1).
Para migrar, las células endoteliales necesitan colagenasas y activador del plasminógeno para degradar el coágulo y parte de la MEC. [3] [19] Las metaloproteinasas dependientes de zinc digieren la membrana basal y la ECM para permitir la migración, proliferación y angiogénesis celular. [38]
Cuando los macrófagos y otras células productoras de factores de crecimiento ya no se encuentran en un ambiente hipóxico lleno de ácido láctico, dejan de producir factores angiogénicos. [20] Por lo tanto, cuando el tejido está adecuadamente perfundido , se reduce la migración y proliferación de células endoteliales. Con el tiempo, los vasos sanguíneos que ya no son necesarios mueren por apoptosis . [37]
Simultáneamente con la angiogénesis, los fibroblastos comienzan a acumularse en el sitio de la herida. Los fibroblastos comienzan a ingresar al sitio de la herida de dos a cinco días después de la herida, cuando termina la fase inflamatoria, y su número alcanza su punto máximo entre una y dos semanas después de la herida. [19] Al final de la primera semana, los fibroblastos son las células principales de la herida. [3] La fibroplasia termina de dos a cuatro semanas después de la herida.
Como modelo, el mecanismo de la fibroplasia puede conceptualizarse como un proceso análogo a la angiogénesis (ver arriba): solo que el tipo de célula involucrada son fibroblastos en lugar de células endoteliales. Inicialmente hay una fase latente donde la herida sufre exudación plasmática, descontaminación inflamatoria y desbridamiento. El edema aumenta la accesibilidad histológica de la herida para una posterior migración fibroplástica. En segundo lugar, a medida que la inflamación se acerca a su finalización, los macrófagos y los mastocitos liberan crecimiento de fibroblastos y factores quimiotácticos para activar los fibroblastos del tejido adyacente. En esta etapa, los fibroblastos se desprenden de las células circundantes y de la ECM. Los fagocitos liberan además proteasas que descomponen la ECM del tejido vecino, liberando a los fibroblastos activados para que proliferen y migren hacia la herida. La diferencia entre el brote vascular y la proliferación de fibroblastos es que el primero se ve potenciado por la hipoxia, mientras que el segundo se inhibe por la hipoxia. El tejido conectivo fibroblástico depositado madura secretando ECM hacia el espacio extracelular, formando tejido de granulación (ver más abajo). Por último, el colágeno se deposita en la ECM.
En los primeros dos o tres días después de la lesión, los fibroblastos migran y proliferan principalmente, mientras que más tarde son las células principales que depositan la matriz de colágeno en el sitio de la herida. [3] Se cree que los orígenes de estos fibroblastos provienen del tejido cutáneo adyacente ileso (aunque nueva evidencia sugiere que algunos se derivan de células madre/precursores adultos circulantes y transmitidos por la sangre). [39] Inicialmente, los fibroblastos utilizan las fibras entrecruzadas de fibrina (bien formadas al final de la fase inflamatoria) para migrar a través de la herida y posteriormente adherirse a la fibronectina. [37] Luego, los fibroblastos depositan sustancia fundamental en el lecho de la herida y luego colágeno, al que pueden adherirse para migrar. [15]
El tejido de granulación funciona como tejido rudimentario y comienza a aparecer en la herida ya durante la fase inflamatoria, de dos a cinco días después de la herida, y continúa creciendo hasta cubrir el lecho de la herida. El tejido de granulación está formado por nuevos vasos sanguíneos, fibroblastos, células inflamatorias, células endoteliales, miofibroblastos y los componentes de una nueva matriz extracelular provisional (MEC). La ECM provisional tiene una composición diferente a la ECM del tejido normal y sus componentes se originan a partir de fibroblastos. [28] Dichos componentes incluyen fibronectina, colágeno, glucosaminoglucanos , elastina , glicoproteínas y proteoglicanos . [37] Sus componentes principales son la fibronectina y el hialuronano , que crean una matriz muy hidratada y facilitan la migración celular. [31] Posteriormente, esta matriz provisional se reemplaza con una MEC que se parece más a la que se encuentra en el tejido no lesionado.
Los factores de crecimiento ( PDGF , TGF-β ) y la fibronectina estimulan la proliferación, la migración al lecho de la herida y la producción de moléculas de ECM por parte de los fibroblastos. Los fibroblastos también secretan factores de crecimiento que atraen células epiteliales al sitio de la herida. La hipoxia también contribuye a la proliferación de fibroblastos y la excreción de factores de crecimiento, aunque muy poco oxígeno inhibirá su crecimiento y la deposición de componentes de la ECM, y puede provocar cicatrices fibróticas excesivas .
Una de las funciones más importantes de los fibroblastos es la producción de colágeno . [36]
La deposición de colágeno es importante porque aumenta la fuerza de la herida; antes de colocarla, lo único que mantiene cerrada la herida es el coágulo de fibrina-fibronectina, que no ofrece mucha resistencia a la lesión traumática . [20] Además, las células involucradas en la inflamación, la angiogénesis y la construcción del tejido conectivo se adhieren, crecen y se diferencian en la matriz de colágeno establecida por los fibroblastos. [40]
El colágeno tipo III y la fibronectina generalmente comienzan a producirse en cantidades apreciables entre aproximadamente 10 horas [41] y 3 días, [37] , dependiendo principalmente del tamaño de la herida. Su deposición alcanza su punto máximo entre una y tres semanas. [28] Son las sustancias de tracción predominantes hasta la última fase de maduración, en la que son reemplazadas por el colágeno tipo I más fuerte .
Incluso cuando los fibroblastos producen nuevo colágeno, las colagenasas y otros factores lo degradan. Poco después de la herida, la síntesis supera la degradación, por lo que los niveles de colágeno en la herida aumentan, pero posteriormente la producción y la degradación se igualan, por lo que no hay ganancia neta de colágeno. [20] Esta homeostasis señala el inicio de la fase de maduración posterior. La granulación cesa gradualmente y los fibroblastos disminuyen en número en la herida una vez finalizado su trabajo. [42] Al final de la fase de granulación, los fibroblastos comienzan a cometer apoptosis, convirtiendo el tejido de granulación de un entorno rico en células a uno que consiste principalmente en colágeno. [3]
La formación de tejido de granulación en una herida abierta permite que tenga lugar la fase de reepitelización, a medida que las células epiteliales migran a través del tejido nuevo para formar una barrera entre la herida y el medio ambiente. [37] Los queratinocitos basales de los bordes de la herida y los apéndices dérmicos, como los folículos pilosos , las glándulas sudoríparas y las glándulas sebáceas (aceite), son las principales células responsables de la fase de epitelización de la cicatrización de las heridas. [42] Avanzan en una sábana a través del sitio de la herida y proliferan en sus bordes, cesando el movimiento cuando se encuentran en el medio. En la curación que produce una cicatriz, no se forman glándulas sudoríparas, folículos pilosos [43] [44] ni nervios. Con la falta de folículos pilosos, nervios y glándulas sudoríparas, la herida y la cicatriz de curación resultante representan un desafío para el cuerpo con respecto al control de la temperatura. [44]
Los queratinocitos migran sin proliferar primero. [45] La migración puede comenzar tan pronto como unas pocas horas después de la herida. Sin embargo, las células epiteliales requieren tejido viable para migrar, por lo que si la herida es profunda, primero debe llenarse con tejido de granulación. [46] Por lo tanto, el momento de inicio de la migración es variable y puede ocurrir aproximadamente un día después de la herida. [47] Las células en los márgenes de la herida proliferan el segundo y tercer día después de la herida para proporcionar más células para la migración. [28]
Si no se rompe la membrana basal , las células epiteliales se reemplazan en tres días mediante división y migración ascendente de células en el estrato basal de la misma manera que ocurre en la piel ilesa. [37] Sin embargo, si la membrana basal se arruina en el sitio de la herida, la reepitelización debe ocurrir desde los márgenes de la herida y desde los apéndices de la piel, como los folículos pilosos y las glándulas sudoríparas y sebáceas que ingresan a la dermis y que están revestidas con queratinocitos viables. [28] Si la herida es muy profunda, los apéndices de la piel también pueden arruinarse y la migración solo puede ocurrir desde los bordes de la herida. [46]
La migración de los queratinocitos sobre el sitio de la herida es estimulada por la falta de inhibición del contacto y por sustancias químicas como el óxido nítrico . [48] Antes de comenzar a migrar, las células deben disolver sus desmosomas y hemidesmosomas , que normalmente anclan las células mediante filamentos intermedios en su citoesqueleto a otras células y a la MEC. [23] Las proteínas receptoras transmembrana llamadas integrinas , que están hechas de glicoproteínas y normalmente anclan la célula a la membrana basal mediante su citoesqueleto , se liberan de los filamentos intermedios de la célula y se reubican en los filamentos de actina para servir como uniones a la MEC para los pseudópodos durante la migración. . [23] Por lo tanto, los queratinocitos se desprenden de la membrana basal y pueden ingresar al lecho de la herida. [35]
Antes de comenzar a migrar, los queratinocitos cambian de forma, se vuelven más largos y planos y extienden procesos celulares como lamellipodios y procesos anchos que parecen volantes. [31] Se forman filamentos de actina y pseudópodos . [35] Durante la migración, las integrinas del pseudópodo se adhieren a la MEC y los filamentos de actina en la proyección tiran de la célula. [23] La interacción con moléculas de la MEC a través de integrinas promueve aún más la formación de filamentos de actina, lamellipodios y filopodios . [23]
Las células epiteliales trepan unas sobre otras para migrar. [42] Esta capa creciente de células epiteliales a menudo se llama lengua epitelial. [45] Las primeras células que se adhieren a la membrana basal forman el estrato basal . Estas células basales continúan migrando a través del lecho de la herida y las células epiteliales que se encuentran encima de ellas también se deslizan. [45] Cuanto más rápido se produzca esta migración, menos cicatriz quedará. [49]
La fibrina , el colágeno y la fibronectina en la MEC pueden indicar aún más a las células que se dividan y migren. Al igual que los fibroblastos, los queratinocitos migratorios utilizan la fibronectina reticulada con fibrina que se depositó en la inflamación como un lugar de unión para arrastrarse. [25] [31] [42]

A medida que los queratinocitos migran, se mueven sobre el tejido de granulación pero permanecen debajo de la costra, separando así la costra del tejido subyacente. [42] [47] Las células epiteliales tienen la capacidad de fagocitar desechos como tejido muerto y materia bacteriana que de otro modo obstruirían su camino. Debido a que deben disolver cualquier costra que se forme, la migración de los queratinocitos se ve favorecida mejor por un ambiente húmedo, ya que uno seco conduce a la formación de una costra más grande y más dura. [25] [37] [42] [50] Para avanzar a lo largo del tejido, los queratinocitos deben disolver el coágulo, los desechos y partes de la ECM para poder pasar. [47] [51] Secretan activador del plasminógeno , que activa el plasminógeno y lo convierte en plasmina para disolver la costra. Las células solo pueden migrar sobre tejido vivo, [42] por lo que deben excretar colagenasas y proteasas como las metaloproteinasas de matriz (MMP) para disolver las partes dañadas de la MEC en su camino, particularmente en la parte frontal de la hoja migratoria. [47] Los queratinocitos también disuelven la membrana basal, utilizando en su lugar la nueva MEC depositada por los fibroblastos para atravesarla. [23]
A medida que los queratinocitos continúan migrando, se deben formar nuevas células epiteliales en los bordes de la herida para reemplazarlas y proporcionar más células para la hoja que avanza. [25] La proliferación detrás de los queratinocitos migratorios normalmente comienza unos días después de la herida [46] y ocurre a un ritmo que es 17 veces mayor en esta etapa de epitelización que en los tejidos normales. [25] Hasta que toda el área de la herida resurja, las únicas células epiteliales que proliferan están en los bordes de la herida. [45]
Los factores de crecimiento, estimulados por integrinas y MMP, hacen que las células proliferen en los bordes de la herida. Los propios queratinocitos también producen y secretan factores, incluidos factores de crecimiento y proteínas de la membrana basal, que ayudan tanto en la epitelización como en otras fases de la curación. [52] Los factores de crecimiento también son importantes para la defensa inmune innata de las heridas de la piel mediante la estimulación de la producción de péptidos antimicrobianos y citocinas quimiotácticas de neutrófilos en los queratinocitos.
Los queratinocitos continúan migrando a través del lecho de la herida hasta que las células de ambos lados se encuentran en el medio, momento en el que la inhibición del contacto hace que dejen de migrar. [31] Cuando han terminado de migrar, los queratinocitos secretan las proteínas que forman la nueva membrana basal. [31] Las células revierten los cambios morfológicos que sufrieron para comenzar a migrar; restablecen desmosomas y hemidesmosomas y vuelven a anclarse a la membrana basal. [23] Las células basales comienzan a dividirse y diferenciarse de la misma manera que lo hacen en la piel normal para restablecer los estratos que se encuentran en la piel reepitelizada. [31]
La contracción es una fase clave de la cicatrización de heridas con reparación. Si la contracción continúa durante demasiado tiempo, puede provocar desfiguración y pérdida de función. [32] Por lo tanto, existe un gran interés en comprender la biología de la contracción de la herida, que puede modelarse in vitro utilizando el ensayo de contracción en gel de colágeno o el modelo dérmico equivalente . [27] [53]
La contracción comienza aproximadamente una semana después de la herida, cuando los fibroblastos se han diferenciado en miofibroblastos . [54] En heridas de espesor total, la contracción alcanza su punto máximo entre 5 y 15 días después de la herida. [37] La contracción puede durar varias semanas [46] y continúa incluso después de que la herida esté completamente reepitelizada. [3] Una herida grande puede volverse entre un 40 y un 80 % más pequeña después de la contracción. [31] [42] Las heridas pueden contraerse a una velocidad de hasta 0,75 mm por día, dependiendo de qué tan suelto esté el tejido en el área de la herida. [37] La contracción generalmente no ocurre simétricamente; más bien, la mayoría de las heridas tienen un "eje de contracción" que permite una mayor organización y alineación de las células con el colágeno. [54]
Al principio, la contracción ocurre sin participación de los miofibroblastos. [55] Más tarde, los fibroblastos, estimulados por factores de crecimiento, se diferencian en miofibroblastos. Los miofibroblastos, que son similares a las células del músculo liso, son responsables de la contracción. [55] Los miofibroblastos contienen el mismo tipo de actina que la que se encuentra en las células del músculo liso . [32]
Los miofibroblastos son atraídos por la fibronectina y los factores de crecimiento y se mueven a lo largo de la fibronectina unida a la fibrina en la ECM provisional para alcanzar los bordes de la herida. [25] Forman conexiones con la ECM en los bordes de la herida y se unen entre sí y a los bordes de la herida mediante desmosomas . Además, en una adhesión llamada fibronexus, la actina del miofibroblasto se une a través de la membrana celular a moléculas de la matriz extracelular como la fibronectina y el colágeno. [55] Los miofibroblastos tienen muchas de estas adherencias, que les permiten tirar de la MEC cuando se contraen, reduciendo el tamaño de la herida. [32] En esta parte de la contracción, el cierre se produce más rápidamente que en la primera parte, independiente de los miofibroblastos. [55]
A medida que la actina de los miofibroblastos se contrae, los bordes de la herida se juntan. Los fibroblastos depositan colágeno para reforzar la herida a medida que los miofibroblastos se contraen. [3] La etapa de contracción en la proliferación termina cuando los miofibroblastos dejan de contraerse y cometen apoptosis. [32] La ruptura de la matriz provisional conduce a una disminución del ácido hialurónico y un aumento del sulfato de condroitina, lo que gradualmente hace que los fibroblastos dejen de migrar y proliferar. [19] Estos eventos señalan el inicio de la etapa de maduración de la curación de heridas.
Cuando los niveles de producción y degradación de colágeno se igualan, se dice que ha comenzado la fase de maduración de la reparación del tejido. [20] Durante la maduración, el colágeno tipo III , que prevalece durante la proliferación, es reemplazado por colágeno tipo I. [17] Las fibras de colágeno originalmente desorganizadas se reorganizan, se entrecruzan y se alinean a lo largo de líneas de tensión . [31] El inicio de la fase de maduración puede variar ampliamente, dependiendo del tamaño de la herida y de si inicialmente se cerró o se dejó abierta, [28] y oscila entre aproximadamente tres días [41] y tres semanas. [56] La fase de maduración puede durar un año o más, dependiendo del tipo de herida. [28]
A medida que avanza la fase, aumenta la resistencia a la tracción de la herida. [28] El colágeno alcanzará aproximadamente el 20% de su resistencia a la tracción después de tres semanas, aumentando al 80% después de 12 meses. La fuerza máxima de la cicatriz es el 80% de la de la piel sana. [57] Dado que la actividad en el sitio de la herida se reduce, la cicatriz pierde su apariencia roja a medida que los vasos sanguíneos que ya no son necesarios se eliminan por apoptosis . [20]
Las fases de cicatrización de heridas normalmente progresan de manera predecible y oportuna; si no lo hacen, la curación puede progresar de manera inapropiada hacia una herida crónica [7] , como una úlcera venosa , o hacia una cicatriz patológica, como una cicatriz queloide . [58] [59]
Muchos factores que controlan la eficacia, la velocidad y la forma de cicatrización de las heridas se clasifican en dos tipos: factores locales y sistémicos. [2]
En la década de 2000 surgieron los primeros modelos matemáticos del proceso de curación, basados en supuestos simplificados y en un sistema de ecuaciones diferenciales resuelto mediante MATLAB . Los modelos muestran que la "velocidad del proceso de curación" parece estar "muy influenciada por la actividad y el tamaño de la lesión en sí, así como por la actividad del agente curativo". [69]
Hasta aproximadamente el año 2000, el paradigma clásico de la curación de heridas, que involucraba células madre restringidas a linajes específicos de órganos, nunca había sido seriamente cuestionado. Desde entonces, la noción de que las células madre adultas tienen plasticidad celular o la capacidad de diferenciarse en células que no pertenecen al linaje ha surgido como una explicación alternativa. [1] Para ser más específicos, las células progenitoras hematopoyéticas (que dan lugar a células maduras en la sangre) pueden tener la capacidad de desdiferenciarse nuevamente en células madre hematopoyéticas y/o transdiferenciarse en células que no pertenecen al linaje, como los fibroblastos. [39]
Las células madre adultas multipotentes tienen la capacidad de autorrenovarse y dar lugar a diferentes tipos celulares. Las células madre dan lugar a células progenitoras, que son células que no se renuevan solas, pero que pueden generar varios tipos de células. El alcance de la participación de las células madre en la cicatrización de heridas cutáneas es complejo y no se comprende completamente. [ cita necesaria ] La inyección de células madre conduce a la curación de heridas principalmente mediante la estimulación de la angiogénesis. [70]
Se cree que la epidermis y la dermis son reconstituidas por células madre mitóticamente activas que residen en el vértice de las crestas de la red (células madre basales o BSC), el bulto de los folículos pilosos (células madre foliculares del cabello o HFSC) y la dermis papilar ( células madre dérmicas). [1] Además, la médula ósea también puede contener células madre que desempeñan un papel importante en la cicatrización de heridas cutáneas. [39]
En circunstancias raras, como en el caso de una lesión cutánea extensa, se induce a subpoblaciones de autorrenovación en la médula ósea a participar en el proceso de curación, mediante lo cual dan lugar a células secretoras de colágeno que parecen desempeñar un papel durante la reparación de la herida. [1] Estas dos subpoblaciones de autorrenovación son (1) células madre mesenquimales (MSC) derivadas de la médula ósea y (2) células madre hematopoyéticas (HSC). La médula ósea también alberga una subpoblación progenitora ( células progenitoras endoteliales o EPC) que, en el mismo tipo de entorno, se movilizan para ayudar en la reconstrucción de los vasos sanguíneos. [39] Además, se cree que las lesiones extensas en la piel también promueven el tráfico temprano de una subclase única de leucocitos ( fibrocitos circulantes ) a la región lesionada, donde realizan diversas funciones relacionadas con la cicatrización de heridas. [1]
Una lesión es una interrupción de la morfología y/o funcionalidad de un tejido determinado. Después de una lesión, el tejido estructural sana con una regeneración completa o incompleta. [71] [72] El tejido sin interrupción de la morfología casi siempre se regenera por completo. Un ejemplo de regeneración completa sin interrupción de la morfología es el tejido no lesionado, como la piel. [73] La piel no lesionada tiene un reemplazo y regeneración continuos de células que siempre resulta en una regeneración completa. [73]
Existe una distinción sutil entre "reparación" y "regeneración". [1] [71] [72] Reparación significa regeneración incompleta . [71] Reparación o regeneración incompleta, se refiere a la adaptación fisiológica de un órgano después de una lesión en un esfuerzo por restablecer la continuidad sin tener en cuenta el reemplazo exacto del tejido perdido/dañado. [71] La verdadera regeneración del tejido o regeneración completa , [72] se refiere a la sustitución del tejido perdido/dañado con una copia "exacta", de modo que tanto la morfología como la funcionalidad se restauren por completo. [72] Aunque después de una lesión los mamíferos pueden regenerarse completamente de forma espontánea, por lo general no se regeneran por completo. Un ejemplo de tejido que se regenera completamente tras una interrupción de su morfología es el endometrio ; El endometrio después del proceso de degradación a través del ciclo menstrual sana con una regeneración completa. [73]
En algunos casos, después de una degradación del tejido, como en la piel, se puede inducir una regeneración más cercana a la regeneración completa mediante el uso de estructuras biodegradables ( colágeno - glucoaminoglicano ). Estos andamios son estructuralmente análogos a la matriz extracelular (MEC) que se encuentra en la dermis normal o no lesionada. [74] Las condiciones fundamentales requeridas para la regeneración de tejidos a menudo se oponen a las condiciones que favorecen la reparación eficiente de la herida, incluida la inhibición de (1) la activación plaquetaria, (2) la respuesta inflamatoria y (3) la contracción de la herida. [1] Además de brindar soporte para la unión de fibroblastos y células endoteliales, los andamios biodegradables inhiben la contracción de la herida, lo que permite que el proceso de curación avance hacia una vía más regenerativa y con menos cicatrices. Se han investigado agentes farmacéuticos que pueden desactivar la diferenciación de miofibroblastos . [75]
Una nueva forma de pensar deriva de la noción de que los heparán sulfatos son un actor clave en la homeostasis del tejido: el proceso que hace que el tejido reemplace las células muertas por células idénticas. En las áreas de las heridas, la homeostasis del tejido se pierde a medida que los sulfatos de heparán se degradan, lo que impide la sustitución de las células muertas por células idénticas. Los análogos de sulfato de heparán no pueden ser degradados por todas las heparanasas y glucanasas conocidas y se unen a los puntos de unión de sulfato de heparina libres en la ECM, preservando así la homeostasis normal del tejido y previniendo la cicatrización. [76] [77] [78]
Reparación o regeneración respecto al factor 1-alfa inducible por hipoxia (HIF-1a). En circunstancias normales, después de una lesión, HIF-1a es degradado por las prolil hidroxilasas (PHD). Los científicos descubrieron que la simple regulación positiva de HIF-1a a través de inhibidores de PHD regenera tejido perdido o dañado en mamíferos que tienen una respuesta de reparación; y la continua regulación a la baja de Hif-1a da como resultado una curación con una respuesta cicatrizante en mamíferos con una respuesta regenerativa previa a la pérdida de tejido. El acto de regular HIF-1a puede desactivar o activar el proceso clave de regeneración de los mamíferos. [79] [80]
La curación de heridas sin cicatrices es un concepto basado en la curación o reparación de la piel (u otros tejidos/órganos) después de una lesión con el objetivo de curar subjetivamente y con menos tejido cicatricial de lo que normalmente se espera. La curación sin cicatrices a veces se mezcla con el concepto de curación sin cicatrices , que es la curación de heridas que no deja absolutamente ninguna cicatriz ( libre de cicatrices). Sin embargo son conceptos diferentes.
Lo contrario a la cicatrización de heridas sin cicatrices es la escarificación (la cicatrización de heridas deja más cicatrices). Históricamente, ciertas culturas consideran atractiva la escarificación; [81] sin embargo, este no es generalmente el caso en la sociedad occidental moderna, en la que muchos pacientes recurren a clínicas de cirugía plástica con expectativas poco realistas. Dependiendo del tipo de cicatriz , el tratamiento puede ser invasivo (inyecciones intralesionales de esteroides, cirugía) y/o conservador ( terapia de compresión , gel de silicona tópico , braquiterapia , terapia fotodinámica ). [82] El criterio clínico es necesario para equilibrar con éxito los beneficios potenciales de los diversos tratamientos disponibles con la probabilidad de una respuesta deficiente y las posibles complicaciones resultantes de estos tratamientos. Es posible que muchos de estos tratamientos solo tengan un efecto placebo y la base de evidencia para el uso de muchos tratamientos actuales es deficiente. [83]
Desde la década de 1960, la comprensión de los procesos biológicos básicos implicados en la reparación de heridas y la regeneración de tejidos se ha ampliado debido a los avances en la biología celular y molecular . [84] Actualmente, los objetivos principales en el tratamiento de heridas son lograr un cierre rápido de la herida con un tejido funcional que tenga una cicatriz estética mínima. [85] Sin embargo, el objetivo final de la biología de la curación de heridas es inducir una reconstrucción más perfecta del área de la herida. La curación de heridas sin cicatrices sólo se produce en tejidos fetales de mamíferos [86] y la regeneración completa se limita a los vertebrados inferiores, como las salamandras y los invertebrados . [87] En los seres humanos adultos, el tejido lesionado se repara mediante la deposición de colágeno , la remodelación del colágeno y la eventual formación de cicatrices, donde se cree que la curación de heridas fetales es más un proceso regenerativo con una formación mínima o nula de cicatrices. [86] Por lo tanto, la curación de heridas fetales se puede utilizar para proporcionar un modelo mamífero accesible de una respuesta de curación óptima en tejidos humanos adultos. Las pistas sobre cómo se podría lograr esto provienen de estudios sobre la curación de heridas en embriones, donde la reparación es rápida y eficiente y da como resultado una regeneración esencialmente perfecta de cualquier tejido perdido.
La etimología del término cicatrización de heridas sin cicatrices tiene una larga historia. [88] [89] [90] En forma impresa, el concepto anticuado de curación sin cicatrices surgió a principios del siglo XX y apareció en un artículo publicado en el London Lancet. Este proceso implicó cortar con una inclinación quirúrgica con respecto a la superficie de la piel, en lugar de hacerlo en ángulo recto; El proceso fue descrito en varios periódicos. [88] [89] [90]
Después de la inflamación, la restauración de la integridad y función normal del tejido se preserva mediante interacciones de retroalimentación entre diversos tipos de células mediadas por moléculas de adhesión y citoquinas secretadas. La alteración de los mecanismos de retroalimentación normales en el cáncer amenaza la integridad del tejido y permite que un tumor maligno escape del sistema inmunológico. [91] [92] Un ejemplo de la importancia de la respuesta de curación de heridas dentro de los tumores se ilustra en el trabajo de Howard Chang y sus colegas de la Universidad de Stanford que estudian el cáncer de mama. [8]
Los resultados preliminares son prometedores para el uso a corto y largo plazo de suplementos de colágeno oral para la cicatrización de heridas y el envejecimiento de la piel. Los suplementos de colágeno oral también aumentan la elasticidad, la hidratación y la densidad del colágeno dérmico de la piel. La suplementación con colágeno es generalmente segura y no se han reportado eventos adversos. Se necesitan más estudios para dilucidar el uso médico en enfermedades de la barrera cutánea como la dermatitis atópica y determinar los regímenes de dosificación óptimos. [93]
Los apósitos modernos para ayudar en la reparación de heridas han sido objeto de considerable investigación y desarrollo en los últimos años. Los científicos pretenden desarrollar apósitos para heridas que tengan las siguientes características: [94]
Los apósitos de gasa de algodón han sido el estándar de atención, a pesar de sus propiedades secas que pueden adherirse a las superficies de las heridas y causar molestias al retirarlos. Investigaciones recientes se han propuesto mejorar los apósitos de gasa de algodón para acercarlos a lograr propiedades modernas de apósito para heridas, recubriendo el apósito de gasa de algodón con un nanocompuesto de quitosano / Ag / ZnO . Estos apósitos actualizados aumentan la absorción de agua y mejoran la eficacia antibacteriana . [94]
Se puede limpiar la suciedad o el polvo de la superficie de la herida, las bacterias, el tejido muerto y el líquido de la herida. La evidencia que respalda la técnica más efectiva no es clara y no hay evidencia suficiente para concluir si la limpieza de las heridas es beneficiosa para promover la curación o si las soluciones de limpieza de heridas (polihexametilenbiguanida, peróxido de oxígeno acuoso, etc.) son mejores que el agua esterilizada o las soluciones salinas para ayudar a curar las úlceras venosas de las piernas. [95] No está claro si la elección de la solución de limpieza o el método de aplicación marca alguna diferencia en la curación de las úlceras venosas de la pierna. [95]
Se han dedicado esfuerzos considerables a comprender las relaciones físicas que rigen la cicatrización de heridas y las cicatrices posteriores, y se han desarrollado modelos matemáticos y simulaciones para dilucidar estas relaciones. [96] El crecimiento de tejido alrededor del sitio de la herida es el resultado de la migración de células y la deposición de colágeno por parte de estas células. La alineación del colágeno describe el grado de cicatrización; La orientación del colágeno en forma de cesta es característica de la piel normal, mientras que las fibras de colágeno alineadas provocan cicatrices importantes. [97] Se ha demostrado que el crecimiento de tejido y el grado de formación de cicatrices se pueden controlar modulando la tensión en el sitio de la herida. [98]
El crecimiento de tejido se puede simular utilizando las relaciones antes mencionadas desde un punto de vista bioquímico y biomecánico. Las sustancias químicas biológicamente activas que desempeñan un papel importante en la cicatrización de heridas se modelan con difusión Fickiana para generar perfiles de concentración. La ecuación de equilibrio para sistemas abiertos al modelar la curación de heridas incorpora el crecimiento masivo debido a la migración y proliferación celular. Aquí se utiliza la siguiente ecuación:
D t ρ 0 = Div (R) + R 0 ,
donde ρ representa la densidad de masa, R representa un flujo de masa (de la migración celular) y R 0 representa una fuente de masa (de la proliferación, división o agrandamiento celular). [99] Relaciones como estas se pueden incorporar en modelos basados en agentes , donde se puede probar la sensibilidad a parámetros individuales como la alineación inicial del colágeno, las propiedades de las citoquinas y las tasas de proliferación celular. [100]
La cicatrización exitosa de heridas depende de varios tipos de células, mediadores moleculares y elementos estructurales. [101]
La intención principal es la curación de una herida limpia sin pérdida de tejido. [101] En este proceso, los bordes de la herida se juntan, de modo que queden adyacentes entre sí (reaproximados). El cierre de la herida se realiza con suturas (puntos), grapas o cinta adhesiva o pegamento.
La intención primaria sólo puede implementarse cuando la herida es precisa y existe una alteración mínima del tejido local y de la membrana basal epitelial, por ejemplo, incisiones quirúrgicas. [102]
Este proceso es más rápido que la curación por segunda intención. [101] También hay menos cicatrices asociadas con la intención primaria, ya que no hay grandes pérdidas de tejido para llenar con tejido de granulación, aunque se formará algo de tejido de granulación. [101]
(Cierre primario retrasado):
Si los bordes de la herida no se reaproximan inmediatamente, se produce un retraso en la cicatrización primaria de la herida. Este tipo de curación puede ser deseable en el caso de heridas contaminadas. Al cuarto día, la fagocitosis de los tejidos contaminados está en marcha y tienen lugar los procesos de epitelización, deposición de colágeno y maduración. Los materiales extraños están protegidos por macrófagos que pueden metamorfosearse en células epitelioides, que están rodeadas por leucocitos mononucleares, formando granulomas. Por lo general, la herida se cierra quirúrgicamente en este punto, o se come la costra, y si la "limpieza" de la herida es incompleta, puede sobrevenir una inflamación crónica que produce cicatrices prominentes.
Los siguientes son los principales factores de crecimiento implicados en la cicatrización de heridas:
Las principales complicaciones son muchas:
Otras complicaciones pueden incluir infección y úlcera de Marjolin .
Los avances en la comprensión clínica de las heridas y su fisiopatología han generado importantes innovaciones biomédicas en el tratamiento de heridas agudas, crónicas y de otro tipo. Se han desarrollado muchos productos biológicos, sustitutos de la piel, biomembranas y andamios para facilitar la curación de heridas a través de diversos mecanismos. [108] Esto incluye una serie de productos con nombres comerciales como Epicel , Laserskin , Transcyte, Dermagraft, AlloDerm/Strattice, Biobrane, Integra, Apligraf, OrCel, GraftJacket y PermaDerm. [109]
Formación de una escara espesa, curación lenta (>1 mes), cicatrización evidente,
Curación en 2 semanas: cicatriz mínima o nula;
Curación en 3 semanas: cicatriz mínima o nula, excepto en formadores de cicatrices de alto riesgo; Curación en 4 semanas o más: hipertrófica en más del 50 % de los pacientes.
Los macrófagos están presentes esencialmente en todos los tejidos, comenzando con el desarrollo embrionario y, además de su papel en la defensa del huésped y en la eliminación de células apoptóticas, se reconocen cada vez más por su función trófica y su papel en la regeneración.
Los investigadores han identificado una célula que ayuda a que las salamandras vuelvan a crecer las extremidades.
Los macrófagos son un tipo de células reparadoras que devoran células muertas y patógenos, y hacen que otras células inmunes respondan a los patógenos.
Cuando se destruye la dermis, en las cicatrices no vuelve a crecer pelo, nervios ni glándulas sudoríparas, lo que plantea desafíos adicionales para el control de la temperatura corporal.
El tejido nuevo no es el mismo que el tejido que se perdió.
Una vez completado el proceso de reparación, se produce una pérdida en la estructura o función del tejido lesionado.
En este tipo de reparación, es común que el tejido de granulación (tejido conectivo estromal) prolifere para llenar el defecto creado por las células necróticas.
Luego, las células necróticas son reemplazadas por tejido cicatricial.
(1) Regeneración completa: el tejido nuevo es el mismo que el tejido que se perdió.
Una vez completado el proceso de reparación, la estructura y función del tejido lesionado son completamente normales.
Una vez finalizado el proceso de reparación, la estructura y función del tejido lesionado son completamente normales.
Este tipo de regeneración es común en situaciones fisiológicas.
Ejemplos de regeneración fisiológica son el reemplazo continuo de las células de la piel y la reparación del endometrio después de la menstruación.
La regeneración completa puede ocurrir en situaciones patológicas en tejidos que tienen buena capacidad regenerativa.