El cobalto es un elemento químico ; tiene símbolo Co y número atómico 27. Al igual que el níquel , el cobalto se encuentra en la corteza terrestre sólo en forma químicamente combinada, salvo pequeños depósitos que se encuentran en aleaciones de hierro meteórico natural . El elemento libre , producido por fundición reductiva, es un metal gris, duro, brillante y algo quebradizo .
Los pigmentos azules a base de cobalto ( azul cobalto ) se han utilizado desde la antigüedad para joyería y pinturas, y para impartir un tinte azul distintivo al vidrio. Durante mucho tiempo se pensó que el color se debía al bismuto metálico . Los mineros habían utilizado durante mucho tiempo el nombre de mineral kobold ( en alemán , mineral de duende ) para algunos de los minerales productores de pigmento azul . Se llamaban así porque eran pobres en metales conocidos y al fundirlos desprendían vapores venenosos que contenían arsénico . [7] En 1735, se descubrió que dichos minerales eran reducibles a un nuevo metal (el primero descubierto desde la antigüedad), que finalmente recibió el nombre del kobold .
Hoy en día, algo de cobalto se produce específicamente a partir de uno de varios minerales con brillo metálico, como la cobaltita (CoAsS). El elemento suele producirse como subproducto de la minería del cobre y el níquel. El cinturón de cobre en la República Democrática del Congo (RDC) y Zambia produce la mayor parte de la producción mundial de cobalto. La producción mundial en 2016 fue de 116.000 toneladas (114.000 toneladas largas; 128.000 toneladas cortas) (según Natural Resources Canada ), y la República Democrática del Congo por sí sola representó más del 50%. [8]
El cobalto se utiliza principalmente en baterías de iones de litio y en la fabricación de aleaciones magnéticas , resistentes al desgaste y de alta resistencia . Los compuestos silicato de cobalto y aluminato de cobalto (II) (CoAl 2 O 4 , azul cobalto) dan un color azul intenso distintivo al vidrio , la cerámica , las tintas , las pinturas y los barnices . El cobalto se produce naturalmente como un solo isótopo estable , el cobalto-59. El cobalto-60 es un radioisótopo de importancia comercial, utilizado como trazador radiactivo y para la producción de rayos gamma de alta energía . El cobalto también se utiliza en la industria petrolera como catalizador al refinar el petróleo crudo. Esto es para purgarlo del azufre, que al quemarse es muy contaminante y provoca la lluvia ácida. [9]
El cobalto es el centro activo de un grupo de coenzimas llamadas cobalaminas . La vitamina B 12 , el ejemplo más conocido de este tipo, es una vitamina esencial para todos los animales. El cobalto en forma inorgánica es también un micronutriente para bacterias , algas y hongos .

El cobalto es un metal ferromagnético con una gravedad específica de 8,9. La temperatura de Curie es de 1115 °C (2039 °F) [10] y el momento magnético es de 1,6 a 1,7 magnetones de Bohr por átomo . [11] El cobalto tiene una permeabilidad relativa de dos tercios de la del hierro . [12] El cobalto metálico se presenta como dos estructuras cristalográficas : hcp y fcc . La temperatura de transición ideal entre las estructuras hcp y fcc es 450 °C (842 °F), pero en la práctica la diferencia de energía entre ellas es tan pequeña que el intercrecimiento aleatorio de las dos es común. [13] [14] [15]
El cobalto es un metal débilmente reductor que está protegido de la oxidación por una película de óxido pasivante . Es atacado por halógenos y azufre . Calentar oxígeno produce Co 3 O 4 que pierde oxígeno a 900 °C (1650 °F) para dar el monóxido CoO. [16] El metal reacciona con flúor (F 2 ) a 520 K para dar CoF 3 ; con cloro (Cl 2 ), bromo (Br 2 ) y yodo (I 2 ), produciendo haluros binarios equivalentes . No reacciona con gas hidrógeno ( H 2 ) o nitrógeno ( N 2 ) incluso cuando se calienta, pero sí reacciona con boro , carbono , fósforo , arsénico y azufre. [17] A temperaturas normales, reacciona lentamente con ácidos minerales y muy lentamente con aire húmedo, pero no seco. [ cita necesaria ]
Los estados de oxidación comunes del cobalto incluyen +2 y +3, aunque también se conocen compuestos con estados de oxidación que van de -3 a +5 . Un estado de oxidación común para compuestos simples es +2 (cobalto (II)). Estas sales forman el complejo acuoso metálico de color rosa [Co(H
2Oh)
6]2+
en agua. La adición de cloruro da el color intensamente azul [CoCl
4]2-
. [5] En una prueba de llama con perlas de bórax , el cobalto muestra un azul profundo tanto en llamas oxidantes como reductoras. [18]
Se conocen varios óxidos de cobalto. El óxido de cobalto (II) verde (CoO) tiene una estructura de sal gema . Se oxida fácilmente con agua y oxígeno para dorar el hidróxido de cobalto (III) (Co (OH) 3 ). A temperaturas de 600 a 700 °C, el CoO se oxida formando óxido azul de cobalto(II,III) (Co 3 O 4 ), que tiene una estructura de espinela . [5] También se conoce el óxido negro de cobalto (III) (Co 2 O 3 ). [19] Los óxidos de cobalto son antiferromagnéticos a baja temperatura : CoO ( temperatura de Néel 291 K) y Co 3 O 4 (temperatura de Néel: 40 K), que es análogo a la magnetita (Fe 3 O 4 ), con una mezcla de +2 y +3 estados de oxidación. [20]
Los principales calcogenuros de cobalto son los sulfuros de cobalto negro (II) , CoS 2 ( estructura de pirita ), Co 2 S 3 ( estructura de espinela ) y CoS ( estructura de arseniuro de níquel ). [5] : 1118
-chloride-hexahydrate-sample.jpg/440px-Cobalt(II)-chloride-hexahydrate-sample.jpg)
Se conocen cuatro dihaluros de cobalto(II): fluoruro de cobalto(II) (CoF 2 , rosa), cloruro de cobalto(II) (CoCl 2 , azul), bromuro de cobalto(II) (CoBr 2 , verde), cobalto(II) yoduro (CoI 2 , azul-negro). Estos haluros existen en formas anhidras e hidratadas. Mientras que el dicloruro anhidro es azul, el hidrato es rojo. [21]
El potencial de reducción de la reacción Co3+
+ mi − → Co2+
es +1,92 V, más allá del cloro a cloruro, +1,36 V. En consecuencia, el cloruro de cobalto (III) se reduciría espontáneamente a cloruro de cobalto (II) y cloro. Debido a que el potencial de reducción del flúor a fluoruro es tan alto, +2,87 V, el fluoruro de cobalto (III) es uno de los pocos compuestos de cobalto (III) simples y estables. El fluoruro de cobalto (III), que se utiliza en algunas reacciones de fluoración, reacciona vigorosamente con el agua. [dieciséis]
El inventario de complejos es muy grande. A partir de estados de oxidación superiores, los complejos de Co(IV) y Co(V) son raros. Se encuentran ejemplos en el hexafluorocobaltato(IV) de cesio (Cs 2 CoF 6 ) y el percobaltato de potasio (K 3 CoO 4 ). [dieciséis]
El cobalto (III) forma una amplia variedad de complejos de coordinación con amoníaco y aminas, que se denominan complejos de amina . Los ejemplos incluyen [Co(NH 3 ) 6 ] 3+ , [Co(NH 3 ) 5 Cl] 2+ ( cloropentaminocobalto (III) ) y cis - y trans - [Co(NH 3 ) 4 Cl 2 ] + . También son bien conocidos los correspondientes complejos de etilendiamina . Se conocen análogos en los que los haluros se reemplazan por nitrito , hidróxido , carbonato , etc. Alfred Werner trabajó extensamente en estos complejos en su trabajo ganador del Premio Nobel. [22] La robustez de estos complejos se demuestra por la resolución óptica de tris(etilendiamina)cobalto(III) ( [Co(en)
3]3+
). [23]
El cobalto (II) forma una amplia variedad de complejos, pero principalmente con ligandos débilmente básicos. El catión de color rosado hexaaquocobalto(II) [Co(H 2 O) 6 ] 2+ se encuentra en varias sales de cobalto habituales, como el nitrato y el sulfato. Tras la adición de un exceso de cloruro, las soluciones del complejo hexaaquo se convierten en CoCl de color azul intenso.2-4, que es tetraédrico.
Ligandos más blandos como la trifenilfosfina forman complejos con Co(II) y Co(I), por ejemplo cloruro de bis y tris(trifenilfosfina)cobalto(I), CoCl 2 (PPh 3 ) 2 y CoCl(PPh 3 ) 3 . Estos complejos de Co(I) y Co(II) representan un enlace a los complejos organometálicos que se describen a continuación.
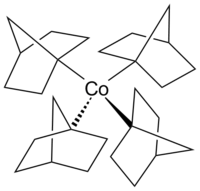
El cobaltoceno es un análogo estructural del ferroceno , con cobalto en lugar de hierro. El cobaltoceno es mucho más sensible a la oxidación que el ferroceno. [24] Cobalto carbonilo ( Co 2 (CO) 8 ) es un catalizador en reacciones de carbonilación e hidrosililación . [25] La vitamina B 12 (ver más abajo ) es un compuesto organometálico que se encuentra en la naturaleza y es la única vitamina que contiene un átomo de metal. [26] Un ejemplo de un complejo de alquilcobalto en el poco común estado de oxidación +4 del cobalto es el complejo homoléptico tetrakis(1-norbornil)cobalto(IV) (Co(1-norb) 4 ), un complejo de metal-alquilo de transición que Destaca por su resistencia a la eliminación del β-hidrógeno , [27] de acuerdo con la regla de Bredt . Los complejos de cobalto (III) y cobalto (V) [Li (THF)
4]+
[Co(1-norb)
4]−
y [Co(1-norb)
4]+
[novio
4]−
también son conocidos. [28]
59 Co es el único isótopo de cobalto estable y el único isótopo que existe naturalmente en la Tierra. Se han caracterizado veintidós radioisótopos : el más estable, el 60 Co , tiene una vida media de 5,2714 años; 57 Co tiene una vida media de 271,8 días; 56 Co tiene una vida media de 77,27 días; y el 58 Co tiene una vida media de 70,86 días. Todos los demás isótopos radiactivos del cobalto tienen vidas medias inferiores a 18 horas y, en la mayoría de los casos, inferiores a 1 segundo. Este elemento también tiene 4 metaestados , todos los cuales tienen vidas medias inferiores a 15 minutos. [29]
Los isótopos del cobalto varían en peso atómico de 50 u ( 50 Co) a 73 u ( 73 Co). El modo de desintegración principal de los isótopos con valores de unidad de masa atómica inferiores a los del único isótopo estable, el 59 Co, es la captura de electrones y el modo principal de desintegración en isótopos con masa atómica superior a 59 unidades de masa atómica es la desintegración beta . Los principales productos de desintegración por debajo del 59 Co son los isótopos del elemento 26 ( hierro ); arriba, los productos de desintegración son isótopos del elemento 28 (níquel). [29]

Los compuestos de cobalto se han utilizado durante siglos para impartir un intenso color azul al vidrio , los vidriados y la cerámica . Se ha detectado cobalto en la escultura egipcia, en joyas persas del tercer milenio a.C., en las ruinas de Pompeya , destruidas en el 79 d.C., y en China, que datan de la dinastía Tang (618-907 d.C.) y la dinastía Ming (1368-1644 ). ANUNCIO). [30]
El cobalto se ha utilizado para colorear el vidrio desde la Edad del Bronce . La excavación del naufragio de Uluburun arrojó un lingote de vidrio azul, fundido durante el siglo XIV a.C. [31] [32] El vidrio azul de Egipto estaba coloreado con cobre, hierro o cobalto. El vidrio de color cobalto más antiguo pertenece a la dinastía XVIII de Egipto (1550-1292 a. C.). Se desconoce la fuente del cobalto que utilizaban los egipcios. [33]
La palabra cobalto se deriva del alemán kobalt , de kobold que significa "duende", un término supersticioso utilizado por los mineros para referirse al mineral de cobalto. Los primeros intentos de fundir esos minerales para obtener cobre o plata fracasaron y en su lugar se obtuvo simplemente polvo (óxido de cobalto (II)). Debido a que los minerales primarios de cobalto siempre contienen arsénico, la fundición del mineral oxidó el arsénico en óxido de arsénico altamente tóxico y volátil , lo que aumentó la notoriedad del mineral. [34] Paracelso , Georgius Agricola y Basil Valentine se refirieron a estos silicatos como "cobalto". [35]
Al químico sueco Georg Brandt (1694-1768) se le atribuye el descubrimiento del cobalto c. 1735 , lo que demuestra que se trata de un elemento hasta ahora desconocido, distinto del bismuto y otros metales tradicionales. Brandt lo llamó un nuevo "semimetal". [36] [37] Demostró que los compuestos de cobalto metálico eran la fuente del color azul en el vidrio, que anteriormente se había atribuido al bismuto encontrado con el cobalto. El cobalto se convirtió en el primer metal descubierto desde la época prehistórica. Todos los metales conocidos anteriormente (hierro, cobre, plata, oro, zinc, mercurio, estaño, plomo y bismuto) no tuvieron descubridores registrados. [38]
Durante el siglo XIX, una parte importante de la producción mundial de azul cobalto (un pigmento elaborado con compuestos de cobalto y alúmina) y esmalte ( vidrio de cobalto en polvo para su uso como pigmento en cerámica y pintura) se llevó a cabo en la noruega Blaafarveværket . [39] [40] Las primeras minas para la producción de esmalte en el siglo XVI estaban ubicadas en Noruega, Suecia, Sajonia y Hungría. Con el descubrimiento de mineral de cobalto en Nueva Caledonia en 1864, la extracción de cobalto en Europa decayó. Con el descubrimiento de depósitos de mineral en Ontario , Canadá, en 1904 y el descubrimiento de depósitos aún mayores en la provincia de Katanga en el Congo en 1914, las operaciones mineras cambiaron nuevamente. [34] Cuando comenzó el conflicto de Shaba en 1978, las minas de cobre de la provincia de Katanga casi dejaron de producir. [41] [42] El impacto de este conflicto en la economía mundial del cobalto fue menor de lo esperado: el cobalto es un metal raro, el pigmento es altamente tóxico y la industria ya había establecido formas efectivas de reciclar materiales de cobalto. En algunos casos, la industria pudo cambiar a alternativas sin cobalto. [41] [42]
En 1938, John Livingood y Glenn T. Seaborg descubrieron el radioisótopo cobalto-60 . [43] Este isótopo se utilizó en la Universidad de Columbia en la década de 1950 para establecer la violación de la paridad en la desintegración beta radiactiva . [44] [45]
Después de la Segunda Guerra Mundial, Estados Unidos quería garantizar el suministro de mineral de cobalto para usos militares (como lo habían estado haciendo los alemanes) y realizó prospecciones de cobalto dentro de Estados Unidos. El cobalto de alta pureza era muy buscado para su uso en motores a reacción y turbinas de gas. [46] Se encontró un suministro adecuado del mineral en Idaho, cerca del cañón Blackbird . Calera Mining Company inició la producción en el sitio. [47]
La demanda de cobalto se ha acelerado aún más en el siglo XXI como componente esencial de los materiales utilizados en baterías recargables, superaleaciones y catalizadores. [46] Se ha argumentado que el cobalto será uno de los principales objetos de competencia geopolítica en un mundo que funciona con energía renovable y depende de baterías, pero esta perspectiva también ha sido criticada por subestimar el poder de los incentivos económicos para ampliar la producción. [48]
La forma estable del cobalto se produce en las supernovas mediante el proceso r . [49] Comprende el 0,0029% de la corteza terrestre . Excepto en el caso reciente del hierro meteórico, el cobalto libre (el metal nativo ) no se encuentra en la superficie de la Tierra debido a su tendencia a reaccionar con el oxígeno de la atmósfera. Se encuentran pequeñas cantidades de compuestos de cobalto en la mayoría de las rocas, suelos, plantas y animales. [50] En el océano, el cobalto normalmente reacciona con el cloro.
En la naturaleza, el cobalto se asocia frecuentemente con el níquel . Ambos son componentes característicos del hierro meteórico , aunque el cobalto es mucho menos abundante en los meteoritos de hierro que el níquel. Al igual que el níquel, el cobalto en las aleaciones meteóricas de hierro puede haber estado suficientemente protegido del oxígeno y la humedad para permanecer como metal libre (pero aleado). [51]
El cobalto en forma compuesta se encuentra en minerales de cobre y níquel. Es el principal componente metálico que se combina con azufre y arsénico en los minerales sulfídicos de cobaltita (CoAsS), safflorita (CoAs 2 ), glaucodoto ( (Co,Fe)AsS ) y skutterudita (CoAs 3 ). [16] El mineral cattierita es similar a la pirita y se encuentra junto con la vaesita en los depósitos de cobre de la provincia de Katanga . [52] Cuando llega a la atmósfera, se produce la erosión ; los minerales sulfurados se oxidan y forman eritrita rosa ("vista de cobalto": Co 3 (AsO 4 ) 2 ·8H 2 O ) y esferocobaltita (CoCO 3 ). [53] [54]
El cobalto también es un componente del humo del tabaco . [55] La planta de tabaco absorbe y acumula fácilmente metales pesados como el cobalto del suelo circundante en sus hojas. Estos se inhalan posteriormente al fumar tabaco . [56]

Los principales minerales de cobalto son cobaltita , eritrita , glaucodot y skutterudita (ver arriba), pero la mayor parte del cobalto se obtiene reduciendo los subproductos de cobalto de la minería y fundición de níquel y cobre . [58] [59]
Dado que el cobalto generalmente se produce como subproducto, el suministro de cobalto depende en gran medida de la viabilidad económica de la extracción de cobre y níquel en un mercado determinado. Se proyectó que la demanda de cobalto crecería un 6% en 2017. [60]
Los depósitos primarios de cobalto son raros, como los que se encuentran en los depósitos hidrotermales , asociados a rocas ultramáficas , tipificados por el distrito de Bou-Azzer en Marruecos . En esos lugares, los minerales de cobalto se extraen exclusivamente, aunque en una concentración más baja, y por lo tanto requieren más procesamiento posterior para la extracción de cobalto. [61] [62]
Existen varios métodos para separar el cobalto del cobre y el níquel, según la concentración de cobalto y la composición exacta del mineral utilizado. Un método es la flotación por espuma , en la que los tensioactivos se unen a los componentes del mineral, lo que lleva a un enriquecimiento de los minerales de cobalto. La tostación posterior convierte los minerales en sulfato de cobalto , y el cobre y el hierro se oxidan hasta obtener el óxido. La lixiviación con agua extrae el sulfato junto con los arseniatos . Los residuos se lixivian adicionalmente con ácido sulfúrico , produciendo una solución de sulfato de cobre. El cobalto también se puede lixiviar de la escoria de la fundición del cobre. [63]
Los productos de los procesos antes mencionados se transforman en óxido de cobalto (Co 3 O 4 ). Este óxido se reduce a metal mediante la reacción aluminotérmica o reducción con carbono en un alto horno . [dieciséis]


El Servicio Geológico de los Estados Unidos estima las reservas mundiales de cobalto en 7.100.000 toneladas métricas. [64] La República Democrática del Congo (RDC) produce actualmente el 63% del cobalto del mundo. Esta participación de mercado puede alcanzar el 73% para 2025 si las expansiones planificadas por productores mineros como Glencore Plc se llevan a cabo como se espera. Bloomberg New Energy Finance ha estimado que para 2030, la demanda mundial de cobalto podría ser 47 veces mayor que en 2017. [65]
Los cambios que el Congo introdujo en las leyes mineras en 2002 atrajeron nuevas inversiones en proyectos congoleños de cobre y cobalto. La mina Mutanda de Glencore envió 24.500 toneladas de cobalto en 2016, el 40% de la producción de la República Democrática del Congo y casi una cuarta parte de la producción mundial. Después de un exceso de oferta, Glencore cerró Mutanda durante dos años a fines de 2019. [66] [67] El proyecto Katanga Mining de Glencore también se está reanudando y debería producir 300.000 toneladas de cobre y 20.000 toneladas de cobalto para 2019, según Glencore. [60]

En 2005, el principal productor de cobalto fueron los depósitos de cobre en la provincia de Katanga en la República Democrática del Congo . La antigua provincia de Shaba, el área tenía casi el 40% de las reservas globales, informó el Servicio Geológico Británico en 2009. [68]
La minería artesanal suministró entre el 17% y el 40% de la producción de la República Democrática del Congo. [69] Unos 100.000 mineros de cobalto en la República Democrática del Congo utilizan herramientas manuales para excavar cientos de pies, con poca planificación y menos medidas de seguridad, dicen trabajadores y funcionarios gubernamentales y de ONG, así como las observaciones de los periodistas del Washington Post sobre visitas a minas aisladas. La falta de precauciones de seguridad frecuentemente causa lesiones o la muerte. [70] La minería contamina los alrededores y expone la vida silvestre local y las comunidades indígenas a metales tóxicos que se cree que causan defectos de nacimiento y dificultades respiratorias, según funcionarios de salud. [71]
El trabajo infantil se utiliza en la extracción de cobalto de minas artesanales africanas . [69] [72] Los activistas de derechos humanos han destacado esto y los informes periodísticos de investigación lo han confirmado. [73] [74] Esta revelación llevó al fabricante de teléfonos celulares Apple Inc. , el 3 de marzo de 2017, a dejar de comprar mineral de proveedores como Zhejiang Huayou Cobalt , que se abastecen de minas artesanales en la República Democrática del Congo, y comenzar a utilizar solo proveedores que estén verificados. para cumplir con sus estándares laborales. [75] [76]
La UE y los principales fabricantes de automóviles (OEM) están presionando a nivel mundial para que la producción global de cobalto se obtenga y se produzca de manera sostenible, responsable y con trazabilidad de la cadena de suministro. Las empresas mineras están adoptando y practicando iniciativas ESG en línea con la Guía de la OCDE y están implementando evidencia de actividades con huella de carbono cero o baja en la cadena de suministro de producción de baterías de iones de litio . Estas iniciativas ya se están llevando a cabo con las principales empresas mineras, artesanales y de pequeña escala (MAPE). Fabricantes de automóviles y cadenas de suministro de fabricantes de baterías: Tesla, VW, BMW, BASF y Glencore participan en varias iniciativas, como el estudio Responsible Cobalt Initiative y Cobalt for Development. En 2018, BMW Group, en asociación con BASF, Samsung SDI y Samsung Electronics, lanzó un proyecto piloto en la República Democrática del Congo en una mina piloto, para mejorar las condiciones y abordar los desafíos de los mineros artesanales y las comunidades circundantes.
La dinámica política y étnica de la región ha provocado en el pasado estallidos de violencia y años de conflicto armado y poblaciones desplazadas. Esta inestabilidad afectó el precio del cobalto y también creó incentivos perversos para que los combatientes de la Primera y Segunda Guerra del Congo prolongaran los combates, ya que el acceso a las minas de diamantes y otros recursos valiosos ayudaba a financiar sus objetivos militares (que con frecuencia equivalían a genocidio) y También enriqueció a los propios combatientes. Si bien la República Democrática del Congo ha sido invadida recientemente por fuerzas militares vecinas en la década de 2010, algunos de los depósitos minerales más ricos lindan con áreas donde los tutsis y hutus todavía se enfrentan con frecuencia, los disturbios continúan, aunque en menor escala, y los refugiados aún huyen de los brotes de violencia. [77]
El cobalto extraído de pequeñas empresas mineras artesanales congoleñas en 2007 abastecía a una única empresa china, Congo DongFang International Mining. Congo DongFang, filial de Zhejiang Huayou Cobalt, uno de los mayores productores de cobalto del mundo, suministraba cobalto a algunos de los mayores fabricantes de baterías del mundo, que producían baterías para productos omnipresentes como los iPhone de Apple . Debido a las acusaciones de violaciones laborales y preocupaciones ambientales, LG Chem posteriormente auditó Congo DongFang de acuerdo con las directrices de la OCDE. LG Chem, que también produce materiales para baterías para empresas automotrices, impuso un código de conducta a todos los proveedores que inspecciona. [78]
El proyecto de la Montaña Mukondo , operado por la Compañía de Exploración y Minería de África Central (CAMEC) en la provincia de Katanga, puede ser la reserva de cobalto más rica del mundo. Se estima que produjo un tercio de la producción total mundial de cobalto en 2008. [79] En julio de 2009, CAMEC anunció un acuerdo a largo plazo para entregar toda su producción anual de concentrado de cobalto desde la montaña Mukondo a Zhejiang Galico Cobalt & Nickel Materials de Porcelana. [80]
En 2016, la propiedad china de la producción de cobalto en el Congo se estimó en más del 10% del suministro mundial de cobalto, lo que constituye un insumo clave para la industria china de refinación de cobalto y otorga a China una influencia sustancial sobre la cadena de suministro mundial de cobalto. [81] El control chino del cobalto congoleño ha generado preocupación en las naciones occidentales que han tratado de reducir la dependencia de la cadena de suministro de China y han expresado preocupación por las violaciones de derechos laborales y humanos en las minas de cobalto en la República Democrática del Congo. [82] [83]
En febrero de 2018, la firma global de gestión de activos AllianceBernstein definió a la República Democrática del Congo como económicamente "la Arabia Saudita de la era de los vehículos eléctricos", debido a sus recursos de cobalto, esencial para las baterías de iones de litio que impulsan los vehículos eléctricos . [84]
El 9 de marzo de 2018, el presidente Joseph Kabila actualizó el código de minería de 2002, aumentando las regalías y declarando al cobalto y al coltán "metales estratégicos". [85] [86] El código de minería de 2002 se actualizó efectivamente el 4 de diciembre de 2018. [87]
En diciembre de 2019, International Rights Advocates, una ONG de derechos humanos, presentó una demanda histórica contra Apple, Tesla , Dell , Microsoft y la empresa Google Alphabet por "beneficiarse a sabiendas, ayudar e instigar el uso cruel y brutal de niños pequeños" en la extracción de cobalto. . [88] Las empresas en cuestión negaron su participación en el trabajo infantil . [89]
En 2017, algunas empresas de exploración planeaban inspeccionar antiguas minas de plata y cobalto en el área de Cobalt, Ontario , donde se cree que se encuentran depósitos importantes. [90]
La canadiense Sherritt International procesa minerales de cobalto en depósitos de níquel de las minas de Moa en Cuba , y la isla tiene varias otras minas en Mayarí , Camagüey y Pinar del Río . Las continuas inversiones de Sherritt International en la producción cubana de níquel y cobalto mientras adquiría derechos mineros durante 17 a 20 años hicieron que el país comunista ocupara el tercer lugar en reservas de cobalto en 2019, por delante del propio Canadá. [91]
A partir de cantidades menores en 2021, Indonesia comenzó a producir cobalto como subproducto de la producción de níquel . Para 2022, el país se había convertido en el segundo mayor productor de cobalto del mundo, y Benchmark Mineral Intelligence pronosticaba que la producción indonesia representaría el 20 por ciento de la producción mundial para 2030. [92]
En 2016 se utilizaron 116.000 toneladas (128.000 toneladas cortas) de cobalto. [8] El cobalto se ha utilizado en la producción de aleaciones de alto rendimiento. [58] [59] También se utiliza en algunas baterías recargables.
Históricamente, las superaleaciones a base de cobalto han consumido la mayor parte del cobalto producido. [58] [59] La estabilidad de temperatura de estas aleaciones las hace adecuadas para álabes de turbinas de gas y motores a reacción de aviones , aunque las aleaciones monocristalinas a base de níquel las superan en rendimiento. [93] Las aleaciones a base de cobalto también son resistentes a la corrosión y al desgaste, lo que las hace, como el titanio , útiles para fabricar implantes ortopédicos que no se desgastan con el tiempo. El desarrollo de aleaciones de cobalto resistentes al desgaste comenzó en la primera década del siglo XX con las aleaciones de estelita , que contienen cromo con cantidades variables de tungsteno y carbono. Las aleaciones con carburos de cromo y tungsteno son muy duras y resistentes al desgaste. [94] Las aleaciones especiales de cobalto, cromo y molibdeno, como Vitallium, se utilizan para piezas protésicas (reemplazos de cadera y rodilla). [95] Las aleaciones de cobalto también se utilizan para prótesis dentales como un sustituto útil del níquel, que puede ser alergénico. [96] Algunos aceros rápidos también contienen cobalto para aumentar la resistencia al calor y al desgaste. En los imanes permanentes se utilizan aleaciones especiales de aluminio, níquel, cobalto y hierro, conocidas como Alnico , y de samario y cobalto ( imán de samario-cobalto ) . [97] También se alea con 95% de platino para joyería, lo que produce una aleación adecuada para fundición fina, que también es ligeramente magnética. [98]
El óxido de litio y cobalto (LiCoO 2 ) se utiliza ampliamente en los cátodos de baterías de iones de litio . El material está compuesto por capas de óxido de cobalto con litio intercalado . Durante la descarga ( es decir, cuando no se está cargando activamente), el litio se libera en forma de iones de litio. [99] Las baterías de níquel-cadmio [100] (NiCd) y de hidruro metálico de níquel [101] (NiMH) también incluyen cobalto para mejorar la oxidación del níquel en la batería. [100] Transparency Market Research estimó el mercado mundial de baterías de iones de litio en 30 mil millones de dólares en 2015 y predijo un aumento a más de 75 mil millones de dólares para 2024. [102]
Aunque en 2018 la mayor parte del cobalto de las baterías se utilizó en un dispositivo móvil, [103] una aplicación más reciente del cobalto son las baterías recargables para coches eléctricos. Esta industria ha quintuplicado su demanda de cobalto, lo que hace urgente encontrar nuevas materias primas en zonas más estables del mundo. [104] Se espera que la demanda continúe o aumente a medida que aumente la prevalencia de vehículos eléctricos. [105] La exploración en 2016-2017 incluyó el área alrededor de Cobalt, Ontario, un área donde muchas minas de plata dejaron de operar hace décadas. [104] El cobalto para vehículos eléctricos aumentó un 81% desde el primer semestre de 2018 a 7.200 toneladas en el primer semestre de 2019, para una capacidad de batería de 46,3 GWh. [106] [107]
Dado que se ha informado repetidamente sobre trabajo infantil y esclavo en la minería de cobalto, principalmente en las minas artesanales de la República Democrática del Congo, las empresas de tecnología que buscan una cadena de suministro ética se han enfrentado a escasez de esta materia prima y [108] el precio del metal cobalto alcanzó su nivel más alto en nueve años. en octubre de 2017, más de 30 dólares la libra, frente a 10 dólares a finales de 2015. [109] Después del exceso de oferta, el precio cayó a 15 dólares más normales en 2019. [110] [111] Como reacción a los problemas con los productos artesanales Minería de cobalto en la República Democrática del Congo Varios proveedores de cobalto y sus clientes han formado la Fair Cobalt Alliance (FCA), cuyo objetivo es poner fin al uso de trabajo infantil y mejorar las condiciones laborales en la minería y el procesamiento de cobalto en la República Democrática del Congo. Los miembros de FCA incluyen Zhejiang Huayou Cobalt , Sono Motors , Responsible Cobalt Initiative, Fairphone , Glencore y Tesla, Inc. [112] [113]
La Unión Europea está investigando la posibilidad de eliminar los requisitos de cobalto en la producción de baterías de iones de litio. [114] [115] A partir de agosto de 2020, los fabricantes de baterías han reducido gradualmente el contenido de cobalto del cátodo de 1/3 ( NMC 111) a 1/5 (NMC 442) hasta actualmente 1/10 (NMC 811) y también han introducido el cobalto. cátodo libre de fosfato de hierro y litio en paquetes de baterías de coches eléctricos como el Tesla Model 3 . [116] [117] En septiembre de 2020, Tesla describió sus planes para fabricar sus propias celdas de batería sin cobalto. [118]
Las baterías de fosfato de hierro y litio superaron oficialmente a las baterías ternarias de cobalto en 2021 con un 52% de la capacidad instalada. Los analistas estiman que su cuota de mercado superará el 60% en 2024. [119]
Varios compuestos de cobalto son catalizadores de oxidación . El acetato de cobalto se utiliza para convertir el xileno en ácido tereftálico , el precursor del polímero a granel tereftalato de polietileno . Los catalizadores típicos son los carboxilatos de cobalto (conocidos como jabones de cobalto). También se utilizan en pinturas, barnices y tintas como "agentes secantes" mediante la oxidación de los aceites secantes . [120] [99] Sin embargo, su uso se está eliminando debido a preocupaciones de toxicidad. [121] Los mismos carboxilatos se utilizan para mejorar la adherencia entre el acero y el caucho en neumáticos radiales con cinturones de acero. Además se utilizan como aceleradores en sistemas de resina de poliéster . [122] [123] [124]
Los catalizadores a base de cobalto se utilizan en reacciones que involucran monóxido de carbono . El cobalto también es un catalizador en el proceso Fischer-Tropsch para la hidrogenación de monóxido de carbono en combustibles líquidos. [125] La hidroformilación de alquenos a menudo utiliza cobalto octacarbonilo como catalizador. [126]
La hidrodesulfuración del petróleo utiliza un catalizador derivado del cobalto y el molibdeno. Este proceso ayuda a limpiar el petróleo de impurezas de azufre que interfieren con el refinado de los combustibles líquidos. [99]


Antes del siglo XIX, el cobalto se utilizaba predominantemente como pigmento. Se utiliza desde la Edad Media para fabricar esmalte , un vidrio de color azul. El esmalte se produce fundiendo una mezcla de esmaltita mineral tostada , cuarzo y carbonato de potasio , lo que produce un vidrio de silicato de color azul oscuro, que se muele finamente después de la producción. [127] El esmalte se usaba ampliamente para colorear vidrio y como pigmento para pinturas. [128] En 1780, Sven Rinman descubrió el verde cobalto , y en 1802 Louis Jacques Thénard descubrió el azul cobalto . [129] Pigmentos de cobalto como el azul cobalto (aluminato de cobalto), el azul cerúleo (estanato de cobalto (II), varios tonos de verde cobalto (una mezcla de óxido de cobalto (II) y óxido de zinc ) y violeta de cobalto ( fosfato de cobalto ). Se utilizan como pigmentos artísticos debido a su estabilidad cromática superior. [130] [131]
El cobalto-60 (Co-60 o 60 Co) es útil como fuente de rayos gamma porque puede producirse en cantidades predecibles con alta actividad bombardeando cobalto con neutrones . Produce rayos gamma con energías de 1,17 y 1,33 MeV . [29] [132]
El cobalto se utiliza en radioterapia de haz externo , esterilización de suministros y desechos médicos, tratamiento con radiación de alimentos para esterilización ( pasteurización en frío ), [133] radiografía industrial (por ejemplo, radiografías de integridad de soldadura), mediciones de densidad (por ejemplo, mediciones de densidad del hormigón) y tanques. interruptores de altura de llenado. El metal tiene la desafortunada propiedad de producir un polvo fino, lo que provoca problemas con la protección radiológica . El cobalto de las máquinas de radioterapia ha representado un grave peligro cuando no se desecha adecuadamente, y uno de los peores accidentes de contaminación por radiación en América del Norte ocurrió en 1984, cuando una unidad de radioterapia desechada que contenía cobalto-60 fue desarmada por error en un depósito de chatarra en Juárez, México. [134] [135]
El cobalto-60 tiene una vida media radiactiva de 5,27 años. La pérdida de potencia requiere el reemplazo periódico de la fuente en radioterapia y es una de las razones por las cuales las máquinas de cobalto han sido reemplazadas en gran medida por aceleradores lineales en la radioterapia moderna. [136] El cobalto-57 (Co-57 o 57 Co) es un radioisótopo de cobalto que se utiliza con mayor frecuencia en pruebas médicas, como radiomarcador para la absorción de vitamina B 12 y para la prueba de Schilling . El cobalto-57 se utiliza como fuente en la espectroscopia de Mössbauer y es una de varias fuentes posibles en dispositivos de fluorescencia de rayos X. [137] [138]
Los diseños de armas nucleares podrían incorporar intencionalmente 59 Co, parte del cual se activaría en una explosión nuclear para producir 60 Co. El 60 Co, disperso como lluvia nuclear , a veces se llama bomba de cobalto . [139]
[140]
Debido a las propiedades ferromagnéticas del cobalto, se utiliza en la producción de diversos materiales magnéticos. [141] Se utiliza en la creación de imanes permanentes como los imanes de Alnico , conocidos por sus fuertes propiedades magnéticas utilizadas en motores eléctricos , sensores y máquinas de resonancia magnética . [142] [143] También se utiliza en la producción de aleaciones magnéticas como el acero de cobalto , ampliamente utilizado en medios de grabación magnéticos como discos duros y cintas . [144]
La capacidad del cobalto para mantener las propiedades magnéticas a altas temperaturas lo hace valioso en aplicaciones de grabación magnética, lo que garantiza dispositivos de almacenamiento de datos confiables . [145] El cobalto también contribuye a los imanes especializados, como los imanes de samario-cobalto y neodimio-hierro-boro , que son vitales en la electrónica para componentes como sensores y actuadores . [146]
El cobalto es esencial para el metabolismo de todos los animales. Es un componente clave de la cobalamina , también conocida como vitamina B 12 , el principal reservorio biológico de cobalto como elemento ultratraza . [149] [150] Las bacterias en el estómago de los animales rumiantes convierten las sales de cobalto en vitamina B 12 , un compuesto que sólo puede ser producido por bacterias o arqueas . Por tanto, una presencia mínima de cobalto en el suelo mejora notablemente la salud de los animales que pastan , y se recomienda una ingesta de 0,20 mg/kg al día, porque no tienen otra fuente de vitamina B 12 . [151]
Las proteínas basadas en cobalamina utilizan corrina para retener el cobalto. La coenzima B 12 presenta un enlace C-Co reactivo que participa en las reacciones. [152] En humanos, B 12 tiene dos tipos de ligando alquilo : metilo y adenosilo. MeB 12 promueve las transferencias de grupos metilo (-CH 3 ). La versión adenosil de B 12 cataliza reordenamientos en los que un átomo de hidrógeno se transfiere directamente entre dos átomos adyacentes con intercambio concomitante del segundo sustituyente, X, que puede ser un átomo de carbono con sustituyentes, un átomo de oxígeno de un alcohol o una amina. La metilmalonil coenzima A mutasa (MUT) convierte MMl-CoA en Su-CoA , un paso importante en la extracción de energía de proteínas y grasas. [153]
Aunque mucho menos comunes que otras metaloproteínas (por ejemplo, las de zinc y hierro), se conocen otras cobaltoproteínas además de la B 12 . Estas proteínas incluyen la metionina aminopeptidasa 2 , una enzima que se produce en humanos y otros mamíferos y que no utiliza el anillo de corrina de B 12 , sino que se une al cobalto directamente. Otra enzima de cobalto distinta de la corrina es la nitrilo hidratasa , una enzima de las bacterias que metaboliza los nitrilos . [154]
En los seres humanos, el consumo de vitamina B 12 que contiene cobalto satisface todas las necesidades de cobalto. Para el ganado vacuno y ovino, que satisfacen las necesidades de vitamina B 12 mediante la síntesis de bacterias residentes en el rumen, el cobalto inorgánico tiene una función. A principios del siglo XX, durante el desarrollo de la agricultura en la meseta volcánica de la Isla Norte de Nueva Zelanda, el ganado padecía lo que se denominó "enfermedad de los arbustos". Se descubrió que los suelos volcánicos carecían de las sales de cobalto esenciales para la cadena alimentaria del ganado. [155] [156] Se descubrió que la "enfermedad de la costa" de las ovejas en el desierto de las noventa millas del sureste de Australia del Sur en la década de 1930 se originaba en deficiencias nutricionales de oligoelementos cobalto y cobre. La deficiencia de cobalto se superó mediante el desarrollo de "balas de cobalto", densas bolitas de óxido de cobalto mezcladas con arcilla que se administran por vía oral para alojarse en el rumen del animal . [ se necesita aclaración ] [157] [156] [158]
Se ha estimado que el valor LD 50 para las sales de cobalto solubles está entre 150 y 500 mg/kg. [160] En los EE.UU., la Administración de Salud y Seguridad Ocupacional (OSHA) ha designado un límite de exposición permisible (PEL) en el lugar de trabajo como un promedio ponderado en el tiempo (TWA) de 0,1 mg/m 3 . El Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH) ha establecido un límite de exposición recomendado (REL) de 0,05 mg/m 3 , promedio ponderado en el tiempo. El valor IDLH (inmediatamente peligroso para la vida y la salud) es de 20 mg/m 3 . [161]
Sin embargo, la ingestión crónica de cobalto ha causado graves problemas de salud en dosis muy inferiores a la letal. En 1966, la adición de compuestos de cobalto para estabilizar la espuma de la cerveza en Canadá provocó una forma peculiar de miocardiopatía inducida por toxinas , que llegó a conocerse como miocardiopatía del bebedor de cerveza . [162] [163]
Además, se sospecha que el metal cobalto causa cáncer (es decir, posiblemente cancerígeno , grupo 2B de la IARC ) según las monografías de la Agencia Internacional para la Investigación del Cáncer (IARC). [164]
Provoca problemas respiratorios cuando se inhala. [165] También causa problemas en la piel cuando se toca; Después del níquel y el cromo, el cobalto es una de las principales causas de dermatitis de contacto . [166]
La mina sería puesta en cuidado y mantenimiento por un período no menor a dos años.