La genómica es un campo interdisciplinario de la biología molecular que se centra en la estructura, función, evolución, mapeo y edición de genomas . Un genoma es el conjunto completo de ADN de un organismo , incluidos todos sus genes, así como su configuración estructural jerárquica y tridimensional. [1] [2] [3] [4] A diferencia de la genética , que se refiere al estudio de genes individuales y sus roles en la herencia, la genómica apunta a la caracterización y cuantificación colectiva de todos los genes de un organismo, sus interrelaciones e influencia. sobre el organismo. [5] Los genes pueden dirigir la producción de proteínas con la ayuda de enzimas y moléculas mensajeras. A su vez, las proteínas forman estructuras corporales como órganos y tejidos, además de controlar reacciones químicas y transportar señales entre las células. La genómica también implica la secuenciación y el análisis de genomas mediante el uso de secuenciación de ADN de alto rendimiento y bioinformática para ensamblar y analizar la función y estructura de genomas completos. [6] [7] Los avances en genómica han desencadenado una revolución en la investigación basada en descubrimientos y en la biología de sistemas para facilitar la comprensión incluso de los sistemas biológicos más complejos, como el cerebro. [8]
El campo también incluye estudios de fenómenos intragenómicos (dentro del genoma) como epistasis (efecto de un gen sobre otro), pleiotropía (un gen que afecta a más de un rasgo), heterosis (vigor híbrido) y otras interacciones entre loci y alelos dentro del genoma. el genoma. [9]
Del griego ΓΕΝ [10] gen , "gen" (gamma, épsilon, nu, épsilon) que significa "llegar a ser, crear, creación, nacimiento", y variantes posteriores: genealogía, génesis, genética, genic, genómero, genotipo, género, etc. Mientras que la palabra genoma (del alemán Genom , atribuida a Hans Winkler ) se utilizaba en inglés ya en 1926, [11] el término genómica fue acuñado por Tom Roderick, genetista del Laboratorio Jackson ( Bar Harbor, Maine ) . , tomando cervezas con Jim Womack, Tom Shows y Stephen O'Brien en una reunión celebrada en Maryland sobre el mapeo del genoma humano en 1986. [12] Primero como nombre de una nueva revista y luego como una disciplina científica completamente nueva. [13]
Tras la confirmación de Rosalind Franklin de la estructura helicoidal del ADN, la publicación de James D. Watson y Francis Crick de la estructura del ADN en 1953 y la publicación de Fred Sanger de la secuencia de aminoácidos de la insulina en 1955, la secuenciación de ácidos nucleicos se volvió un objetivo importante de los primeros biólogos moleculares . [14] En 1964, Robert W. Holley y sus colegas publicaron la primera secuencia de ácido nucleico jamás determinada, la secuencia de ribonucleótidos del ARN de transferencia de alanina . [15] [16] Ampliando este trabajo, Marshall Nirenberg y Philip Leder revelaron la naturaleza triplete del código genético y pudieron determinar las secuencias de 54 de 64 codones en sus experimentos. [17] En 1972, Walter Fiers y su equipo en el Laboratorio de Biología Molecular de la Universidad de Gante ( Gante , Bélgica ) fueron los primeros en determinar la secuencia de un gen: el gen de la proteína de cubierta del bacteriófago MS2 . [18] El grupo de Fiers amplió su trabajo sobre la proteína de cubierta MS2, determinando la secuencia completa de nucleótidos del bacteriófago MS2-RNA (cuyo genoma codifica sólo cuatro genes en 3569 pares de bases [pb]) y el virus 40 del simio en 1976 y 1978, respectivamente. . [19] [20]
Además de su trabajo fundamental sobre la secuencia de aminoácidos de la insulina, Frederick Sanger y sus colegas desempeñaron un papel clave en el desarrollo de técnicas de secuenciación de ADN que permitieron el establecimiento de proyectos integrales de secuenciación del genoma. [9] En 1975, él y Alan Coulson publicaron un procedimiento de secuenciación utilizando ADN polimerasa con nucleótidos radiomarcados al que llamó técnica Más y Menos . [21] [22] Esto implicó dos métodos estrechamente relacionados que generaron oligonucleótidos cortos con extremos 3' definidos. Estos podrían fraccionarse mediante electroforesis en un gel de poliacrilamida (llamada electroforesis en gel de poliacrilamida) y visualizarse mediante autorradiografía. El procedimiento podía secuenciar hasta 80 nucleótidos de una sola vez y supuso una gran mejora, pero seguía siendo muy laborioso. Sin embargo, en 1977 su grupo pudo secuenciar la mayoría de los 5.386 nucleótidos del bacteriófago monocatenario φX174 , completando el primer genoma basado en ADN completamente secuenciado. [23] El refinamiento del método Más y Menos dio como resultado la terminación de cadena, o método Sanger (ver más abajo), que formó la base de las técnicas de secuenciación de ADN, mapeo del genoma, almacenamiento de datos y análisis bioinformático más ampliamente utilizados en el siguiente cuarto de siglo de investigación. [24] [25] En el mismo año, Walter Gilbert y Allan Maxam de la Universidad de Harvard desarrollaron de forma independiente el método Maxam-Gilbert (también conocido como método químico ) de secuenciación de ADN, que implica la escisión preferencial del ADN en bases conocidas, una forma menos eficiente. método. [26] [27] Por su trabajo innovador en la secuenciación de ácidos nucleicos, Gilbert y Sanger compartieron la mitad del Premio Nobel de Química de 1980 con Paul Berg ( ADN recombinante ).
La llegada de estas tecnologías dio lugar a una rápida intensificación del alcance y la velocidad de finalización de los proyectos de secuenciación del genoma . La primera secuencia genómica completa de un orgánulo eucariótico , la mitocondria humana (16.568 pb, aproximadamente 16,6 kb [kilobase]), se informó en 1981, [28] y los primeros genomas de cloroplasto siguieron en 1986. [29] [30] En 1992 Se secuenció el primer cromosoma eucariota , el cromosoma III de la levadura de cerveza Saccharomyces cerevisiae (315 kb). [31] El primer organismo de vida libre que se secuenció fue el de Haemophilus influenzae (1,8 Mb [megabase]) en 1995. [32] Al año siguiente, un consorcio de investigadores de laboratorios de América del Norte , Europa y Japón anunció la finalización de la primera secuencia completa del genoma de un eucariota, S. cerevisiae (12,1 Mb), y desde entonces se han seguido secuenciando genomas a un ritmo exponencialmente creciente. [33] En octubre de 2011 [update], las secuencias completas están disponibles para: 2.719 virus , 1.115 arqueas y bacterias , y 36 eucariotas , de los cuales aproximadamente la mitad son hongos . [34] [35]

La mayoría de los microorganismos cuyos genomas han sido completamente secuenciados son patógenos problemáticos , como Haemophilus influenzae , lo que ha dado lugar a un sesgo pronunciado en su distribución filogenética en comparación con la amplitud de la diversidad microbiana. [36] [37] De las otras especies secuenciadas, la mayoría fueron elegidas porque eran organismos modelo bien estudiados o prometían convertirse en buenos modelos. La levadura ( Saccharomyces cerevisiae ) ha sido durante mucho tiempo un organismo modelo importante para la célula eucariota , mientras que la mosca de la fruta Drosophila melanogaster ha sido una herramienta muy importante (especialmente en las primeras etapas de la genética premolecular ). El gusano Caenorhabditis elegans es un modelo simple de uso frecuente para organismos multicelulares . El pez cebra Brachydanio rerio se utiliza para muchos estudios de desarrollo a nivel molecular, y la planta Arabidopsis thaliana es un organismo modelo para plantas con flores. El pez globo japonés ( Takifugu rubripes ) y el pez globo verde manchado ( Tetraodon nigroviridis ) son interesantes por sus genomas pequeños y compactos, que contienen muy poco ADN no codificante en comparación con la mayoría de las especies. [38] [39] Los mamíferos perro ( Canis familiaris ), [40] la rata parda ( Rattus norvegicus ), el ratón ( Mus musculus ) y el chimpancé ( Pan troglodytes ) son animales modelo importantes en la investigación médica. [27]
El Proyecto Genoma Humano completó un borrador del genoma humano a principios de 2001, generando mucha fanfarria. [41] Este proyecto, completado en 2003, secuenció el genoma completo de una persona específica, y en 2007 esta secuencia fue declarada "terminada" (menos de un error en 20.000 bases y todos los cromosomas ensamblados). [41] En los años transcurridos desde entonces, se han secuenciado los genomas de muchos otros individuos, en parte bajo los auspicios del Proyecto 1000 Genomas , que anunció la secuenciación de 1.092 genomas en octubre de 2012. [42] La finalización de este proyecto fue posible por el desarrollo de tecnologías de secuenciación dramáticamente más eficientes y requirió el compromiso de importantes recursos bioinformáticos de una gran colaboración internacional. [43] El análisis continuo de datos genómicos humanos tiene profundas repercusiones políticas y sociales para las sociedades humanas. [44]
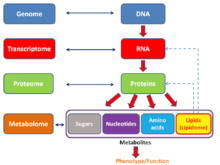
El neologismo en inglés ómica se refiere informalmente a un campo de estudio de la biología que termina en -ómica , como la genómica, la proteómica o la metabolómica . El sufijo relacionado -ome se utiliza para referirse a los objetos de estudio de dichos campos, como el genoma , el proteoma o el metaboloma ( lipidoma ), respectivamente. El sufijo -ome, tal como se utiliza en biología molecular, se refiere a una totalidad de algún tipo; De manera similar, la ómica ha llegado a referirse generalmente al estudio de conjuntos de datos biológicos grandes y completos. Si bien el crecimiento en el uso del término ha llevado a algunos científicos ( Jonathan Eisen , entre otros [45] ) a afirmar que se ha sobrevendido, [46] refleja el cambio de orientación hacia el análisis cuantitativo de resultados completos o casi completos. conjunto de todos los constituyentes de un sistema. [47] En el estudio de las simbiosis , por ejemplo, los investigadores que antes se limitaban al estudio de un solo producto genético ahora pueden comparar simultáneamente el complemento total de varios tipos de moléculas biológicas. [48] [49]
Una vez seleccionado un organismo, los proyectos genómicos implican tres componentes: la secuenciación del ADN, el ensamblaje de esa secuencia para crear una representación del cromosoma original y la anotación y análisis de esa representación. [9]
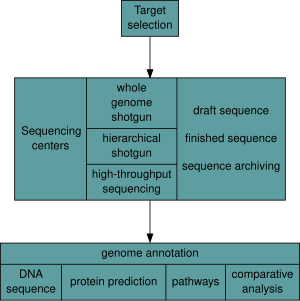
Históricamente, la secuenciación se realizaba en centros de secuenciación , instalaciones centralizadas (que van desde grandes instituciones independientes como el Joint Genome Institute, que secuencia docenas de terabases al año, hasta instalaciones locales centrales de biología molecular) que contienen laboratorios de investigación con la costosa instrumentación y el soporte técnico necesarios. Sin embargo, a medida que la tecnología de secuenciación continúa mejorando, una nueva generación de secuenciadores de sobremesa eficaces y de respuesta rápida se ha puesto al alcance del laboratorio académico promedio. [50] [51] En general, los enfoques de secuenciación del genoma se dividen en dos categorías amplias: secuenciación de escopeta y secuenciación de alto rendimiento (o de próxima generación ). [9]

La secuenciación de escopeta es un método de secuenciación diseñado para el análisis de secuencias de ADN de más de 1000 pares de bases, hasta cromosomas completos inclusive. [52] Se denomina así por analogía con el patrón de disparo casi aleatorio de una escopeta que se expande rápidamente . Dado que la secuenciación por electroforesis en gel solo se puede utilizar para secuencias bastante cortas (de 100 a 1000 pares de bases), las secuencias de ADN más largas deben dividirse en pequeños segmentos aleatorios que luego se secuencian para obtener lecturas . Se obtienen múltiples lecturas superpuestas para el ADN objetivo realizando varias rondas de esta fragmentación y secuenciación. Luego, los programas de computadora utilizan los extremos superpuestos de diferentes lecturas para ensamblarlas en una secuencia continua. [52] [53] La secuenciación directa es un proceso de muestreo aleatorio que requiere un sobremuestreo para garantizar que un nucleótido determinado esté representado en la secuencia reconstruida; el número promedio de lecturas mediante las cuales se sobremuestrea un genoma se denomina cobertura . [54]
Durante gran parte de su historia, la tecnología subyacente a la secuenciación shotgun fue el método clásico de terminación de cadena o ' método Sanger ', que se basa en la incorporación selectiva de didesoxinucleótidos terminales de cadena por la ADN polimerasa durante la replicación in vitro del ADN . [23] [55] Recientemente, la secuenciación directa ha sido reemplazada por métodos de secuenciación de alto rendimiento , especialmente para análisis genómicos automatizados a gran escala . Sin embargo, el método Sanger sigue utilizándose ampliamente, principalmente para proyectos de menor escala y para obtener lecturas de secuencias de ADN contiguas especialmente largas (>500 nucleótidos). [56] Los métodos de terminación de cadena requieren una plantilla de ADN monocatenario, un cebador de ADN , una ADN polimerasa , desoxinucleosidetrifosfatos normales (dNTP) y nucleótidos modificados (didesoxiNTP) que terminan el alargamiento de la cadena de ADN. Estos nucleótidos terminales de cadena carecen de un grupo 3'- OH necesario para la formación de un enlace fosfodiéster entre dos nucleótidos, lo que hace que la ADN polimerasa deje de extender el ADN cuando se incorpora un ddNTP. Los ddNTP pueden marcarse radiactiva o fluorescentemente para su detección en secuenciadores de ADN . [9] Normalmente, estas máquinas pueden secuenciar hasta 96 muestras de ADN en un solo lote (ejecución) en hasta 48 ejecuciones por día. [57]
La gran demanda de secuenciación de bajo costo ha impulsado el desarrollo de tecnologías de secuenciación de alto rendimiento que paralelizan el proceso de secuenciación y producen miles o millones de secuencias a la vez. [58] [59] La secuenciación de alto rendimiento tiene como objetivo reducir el costo de la secuenciación de ADN más allá de lo que es posible con los métodos estándar de terminación de colorante. En la secuenciación de rendimiento ultraalto, se pueden ejecutar en paralelo hasta 500.000 operaciones de secuenciación por síntesis. [60] [61]

El método de secuenciación de tintes de Illumina se basa en terminadores de tintes reversibles y fue desarrollado en 1996 en el Instituto de Investigación Biomédica de Ginebra por Pascal Mayer y Laurent Farinelli. [62] En este método, las moléculas de ADN y los cebadores se unen primero a un portaobjetos y se amplifican con polimerasa para que se formen colonias clonales locales, inicialmente denominadas "colonias de ADN". Para determinar la secuencia, se añaden cuatro tipos de bases terminadoras reversibles (bases RT) y los nucleótidos no incorporados se eliminan por lavado. A diferencia de la pirosecuenciación, las cadenas de ADN se extienden un nucleótido a la vez y la adquisición de imágenes se puede realizar en un momento retrasado, lo que permite capturar conjuntos muy grandes de colonias de ADN mediante imágenes secuenciales tomadas con una sola cámara. Desacoplar la reacción enzimática y la captura de imágenes permite un rendimiento óptimo y una capacidad de secuenciación teóricamente ilimitada; Con una configuración óptima, el rendimiento final del instrumento depende únicamente de la tasa de conversión A/D de la cámara. La cámara toma imágenes de los nucleótidos marcados con fluorescencia y luego el tinte junto con el bloqueador terminal 3' se elimina químicamente del ADN, lo que permite el siguiente ciclo. [63]
Un enfoque alternativo, la secuenciación de semiconductores de iones, se basa en la química de replicación del ADN estándar. Esta tecnología mide la liberación de un ion hidrógeno cada vez que se incorpora una base. Un micropocillo que contiene ADN molde se inunda con un solo nucleótido ; si el nucleótido es complementario a la cadena molde, se incorporará y se liberará un ion hidrógeno. Esta liberación activa un sensor de iones ISFET . Si hay un homopolímero presente en la secuencia plantilla, se incorporarán múltiples nucleótidos en un único ciclo de inundación y la señal eléctrica detectada será proporcionalmente mayor. [64]
El ensamblaje de secuencia se refiere a alinear y fusionar fragmentos de una secuencia de ADN mucho más larga para reconstruir la secuencia original. [9] Esto es necesario ya que la tecnología actual de secuenciación de ADN no puede leer genomas completos como una secuencia continua, sino que lee pequeños fragmentos de entre 20 y 1000 bases, dependiendo de la tecnología utilizada. Las tecnologías de secuenciación de tercera generación, como PacBio u Oxford Nanopore, generan habitualmente lecturas de secuenciación de >10 kb de longitud; sin embargo, tienen una alta tasa de error de aproximadamente el 15 por ciento. [65] [66] Por lo general, los fragmentos cortos, llamados lecturas, resultan de la secuenciación rápida de ADN genómico o transcripciones de genes ( EST ). [9]
El ensamblaje se puede clasificar en términos generales en dos enfoques: ensamblaje de novo , para genomas que no son similares a ninguno secuenciado en el pasado, y ensamblaje comparativo, que utiliza la secuencia existente de un organismo estrechamente relacionado como referencia durante el ensamblaje. [54] En relación con el ensamblaje comparativo, el ensamblaje de novo es computacionalmente difícil ( NP-hard ), lo que lo hace menos favorable para las tecnologías NGS de lectura corta. Dentro del paradigma de ensamblaje de novo existen dos estrategias principales para el ensamblaje, las estrategias de ruta euleriana y las estrategias de consenso de diseño de superposición (OLC). En última instancia, las estrategias OLC intentan crear una ruta hamiltoniana a través de un gráfico de superposición, lo cual es un problema NP difícil. Las estrategias de caminos eulerianos son computacionalmente más manejables porque intentan encontrar un camino euleriano a través de un gráfico de DeBruijn. [54]
Los genomas terminados se definen como aquellos que tienen una única secuencia contigua sin ambigüedades que representen cada replicón . [67]
El ensamblaje de la secuencia de ADN por sí solo tiene poco valor sin análisis adicionales. [9] La anotación del genoma es el proceso de adjuntar información biológica a secuencias y consta de tres pasos principales: [68]
Las herramientas de anotación automática intentan realizar estos pasos in silico , a diferencia de la anotación manual (también conocida como curación), que implica experiencia humana y una posible verificación experimental. [69] Idealmente, estos enfoques coexisten y se complementan entre sí en el mismo proceso de anotación (ver también más abajo).
Tradicionalmente, el nivel básico de anotación consiste en utilizar BLAST para encontrar similitudes y luego anotar genomas basándose en homólogos. [9] Más recientemente, se agrega información adicional a la plataforma de anotaciones. La información adicional permite a los anotadores manuales desconvolucionar las discrepancias entre genes a los que se les asigna la misma anotación. Algunas bases de datos utilizan información del contexto del genoma, puntuaciones de similitud, datos experimentales e integraciones de otros recursos para proporcionar anotaciones del genoma a través de su enfoque de subsistemas. Otras bases de datos (por ejemplo, Ensembl ) se basan tanto en fuentes de datos seleccionadas como en una variedad de herramientas de software en su proceso de anotación automatizada del genoma. [70] La anotación estructural consiste en la identificación de elementos genómicos, principalmente ORF y su localización, o estructura genética. La anotación funcional consiste en adjuntar información biológica a elementos genómicos.
La necesidad de reproducibilidad y gestión eficiente de la gran cantidad de datos asociados con los proyectos del genoma significa que los procesos computacionales tienen aplicaciones importantes en genómica. [71]
La genómica funcional es un campo de la biología molecular que intenta hacer uso de la gran riqueza de datos producidos por proyectos genómicos (como los proyectos de secuenciación del genoma ) para describir funciones e interacciones de genes (y proteínas ). La genómica funcional se centra en los aspectos dinámicos como la transcripción , traducción y las interacciones proteína-proteína de genes , a diferencia de los aspectos estáticos de la información genómica como la secuencia o las estructuras del ADN. La genómica funcional intenta responder preguntas sobre la función del ADN a nivel de genes, transcripciones de ARN y productos proteicos. Una característica clave de los estudios de genómica funcional es su enfoque de todo el genoma para estas cuestiones, que generalmente implica métodos de alto rendimiento en lugar de un enfoque más tradicional "gen por gen".
Una rama importante de la genómica todavía se ocupa de la secuenciación de los genomas de diversos organismos, pero el conocimiento de los genomas completos ha creado la posibilidad para el campo de la genómica funcional , que se ocupa principalmente de los patrones de expresión genética durante diversas condiciones. Las herramientas más importantes aquí son los microarrays y la bioinformática .

La genómica estructural busca describir la estructura tridimensional de cada proteína codificada por un genoma determinado . [72] [73] Este enfoque basado en el genoma permite un método de alto rendimiento para la determinación de la estructura mediante una combinación de enfoques experimentales y de modelado . La principal diferencia entre la genómica estructural y la predicción estructural tradicional es que la genómica estructural intenta determinar la estructura de cada proteína codificada por el genoma, en lugar de centrarse en una proteína en particular. Con secuencias de genoma completo disponibles, la predicción de la estructura se puede hacer más rápidamente mediante una combinación de enfoques experimentales y de modelado, especialmente porque la disponibilidad de una gran cantidad de genomas secuenciados y estructuras de proteínas previamente resueltas permite a los científicos modelar la estructura de las proteínas a partir de estructuras de proteínas previamente resueltas. homólogos. La genómica estructural implica adoptar una gran cantidad de enfoques para la determinación de la estructura, incluidos métodos experimentales que utilizan secuencias genómicas o enfoques basados en modelos basados en la homología secuencial o estructural con una proteína de estructura conocida o basados en principios químicos y físicos para una proteína sin homología con cualquier estructura conocida. A diferencia de la biología estructural tradicional , la determinación de la estructura de una proteína a través de un esfuerzo de genómica estructural a menudo (pero no siempre) ocurre antes de que se sepa algo sobre la función de la proteína. Esto plantea nuevos desafíos en bioinformática estructural , es decir, determinar la función de las proteínas a partir de su estructura tridimensional . [74]
La epigenómica es el estudio del conjunto completo de modificaciones epigenéticas sobre el material genético de una célula, conocido como epigenoma . [75] Las modificaciones epigenéticas son modificaciones reversibles en el ADN o las histonas de una célula que afectan la expresión genética sin alterar la secuencia del ADN (Russell 2010 p. 475). Dos de las modificaciones epigenéticas más caracterizadas son la metilación del ADN y la modificación de histonas . [76] Las modificaciones epigenéticas desempeñan un papel importante en la expresión y regulación genética, y están implicadas en numerosos procesos celulares, como la diferenciación/desarrollo [77] y la tumorigénesis . [75] El estudio de la epigenética a nivel global ha sido posible sólo recientemente gracias a la adaptación de ensayos genómicos de alto rendimiento. [78]
La metagenómica es el estudio de los metagenomas , material genético recuperado directamente de muestras ambientales . El campo amplio también puede denominarse genómica ambiental, ecogenómica o genómica comunitaria. Mientras que la microbiología tradicional y la secuenciación del genoma microbiano se basan en cultivos clonales cultivados , la secuenciación temprana de genes ambientales clonaba genes específicos (a menudo el gen 16S rRNA ) para producir un perfil de diversidad en una muestra natural. Dicho trabajo reveló que los métodos basados en el cultivo habían pasado por alto la gran mayoría de la biodiversidad microbiana . [79] Estudios recientes utilizan secuenciación de Sanger "escopeta" o pirosecuenciación masiva paralela para obtener muestras en gran medida imparciales de todos los genes de todos los miembros de las comunidades muestreadas. [80] Debido a su poder para revelar la diversidad previamente oculta de la vida microscópica, la metagenómica ofrece una lente poderosa para ver el mundo microbiano que tiene el potencial de revolucionar la comprensión de todo el mundo vivo. [81] [82]
Los bacteriófagos han desempeñado y siguen desempeñando un papel clave en la genética bacteriana y la biología molecular . Históricamente, se utilizaron para definir la estructura genética y la regulación genética. Además, el primer genoma en ser secuenciado fue el de un bacteriófago . Sin embargo, la investigación sobre bacteriófagos no lideró la revolución genómica, que está claramente dominada por la genómica bacteriana. Sólo muy recientemente el estudio de los genomas de los bacteriófagos se ha vuelto prominente, lo que permite a los investigadores comprender los mecanismos subyacentes a la evolución de los fagos . Las secuencias del genoma de los bacteriófagos se pueden obtener mediante secuenciación directa de bacteriófagos aislados, pero también se pueden derivar como parte de genomas microbianos. El análisis de genomas bacterianos ha demostrado que una cantidad sustancial de ADN microbiano consta de secuencias de profagos y elementos similares a profagos. [83] Una extracción detallada de la base de datos de estas secuencias ofrece información sobre el papel de los profagos en la configuración del genoma bacteriano: en general, este método verificó muchos grupos de bacteriófagos conocidos, lo que lo convierte en una herramienta útil para predecir las relaciones de los profagos a partir de genomas bacterianos. [84] [85]
En la actualidad hay 24 cianobacterias de las que se dispone de una secuencia genómica total. 15 de estas cianobacterias proceden del medio marino. Se trata de seis cepas de Proclorococo , siete cepas marinas de Synechococcus , Trichodesmium erythraeum IMS101 y Crocosphaera watsonii WH8501. Varios estudios han demostrado cómo estas secuencias podrían usarse con mucho éxito para inferir importantes características ecológicas y fisiológicas de las cianobacterias marinas. Sin embargo, actualmente hay muchos más proyectos genómicos en marcha, entre ellos se encuentran otros aislados de Proclorococos y Synechococcus marinos , Acaryochloris y Procloron , las cianobacterias filamentosas fijadoras de N 2 Nodularia spumigena , Lyngbya aestuarii y Lyngbya majuscula , así como bacteriófagos que infectan cianobacerias marinas. . Por lo tanto, el creciente cuerpo de información genómica también puede aprovecharse de una manera más general para abordar problemas globales aplicando un enfoque comparativo. Algunos ejemplos nuevos y apasionantes de avances en este campo son la identificación de genes para los ARN reguladores, el conocimiento del origen evolutivo de la fotosíntesis o la estimación de la contribución de la transferencia horizontal de genes a los genomas que se han analizado. [86]

La genómica ha proporcionado aplicaciones en muchos campos, incluida la medicina , la biotecnología , la antropología y otras ciencias sociales . [44]
Las tecnologías genómicas de próxima generación permiten a los médicos e investigadores biomédicos aumentar drásticamente la cantidad de datos genómicos recopilados en grandes poblaciones de estudio. [87] Cuando se combina con nuevos enfoques informáticos que integran muchos tipos de datos con datos genómicos en la investigación de enfermedades, esto permite a los investigadores comprender mejor las bases genéticas de la respuesta a los medicamentos y las enfermedades. [88] [89] Los primeros esfuerzos para aplicar el genoma a la medicina incluyeron los de un equipo de Stanford dirigido por Euan Ashley, quien desarrolló las primeras herramientas para la interpretación médica de un genoma humano. [90] [91] [92] El programa de investigación Genomes2People en Brigham and Women's Hospital , Broad Institute y Harvard Medical School se estableció en 2012 para realizar investigaciones empíricas sobre la traducción de la genómica en salud. El Brigham and Women's Hospital abrió una Clínica de Genómica Preventiva en agosto de 2019, y el Hospital General de Massachusetts le siguió un mes después. [93] [94] El programa de investigación All of Us tiene como objetivo recopilar datos de secuencia del genoma de 1 millón de participantes para convertirse en un componente crítico de la plataforma de investigación de medicina de precisión. [95]
El crecimiento del conocimiento genómico ha permitido aplicaciones cada vez más sofisticadas de la biología sintética . [96] En 2010, investigadores del Instituto J. Craig Venter anunciaron la creación de una especie de bacteria parcialmente sintética , Mycoplasma laboratorium , derivada del genoma de Mycoplasma genitalium . [97]
La genómica de poblaciones se ha convertido en un campo de investigación popular, donde se utilizan métodos de secuenciación genómica para realizar comparaciones a gran escala de secuencias de ADN entre poblaciones, más allá de los límites de los marcadores genéticos como los productos de PCR de corto alcance o los microsatélites utilizados tradicionalmente en genética de poblaciones . La genómica de poblaciones estudia los efectos en todo el genoma para mejorar nuestra comprensión de la microevolución, de modo que podamos conocer la historia filogenética y la demografía de una población. [98] Los métodos genómicos de poblaciones se utilizan en muchos campos diferentes, incluidos la biología evolutiva , la ecología , la biogeografía , la biología de la conservación y la ordenación pesquera . De manera similar, la genómica del paisaje se ha desarrollado a partir de la genética del paisaje para utilizar métodos genómicos para identificar relaciones entre patrones de variación ambiental y genética.
Los conservacionistas pueden utilizar la información recopilada mediante la secuenciación genómica para evaluar mejor los factores genéticos clave para la conservación de las especies, como la diversidad genética de una población o si un individuo es heterocigoto para un trastorno genético hereditario recesivo. [99] Al utilizar datos genómicos para evaluar los efectos de los procesos evolutivos y detectar patrones de variación en una población determinada, los conservacionistas pueden formular planes para ayudar a una especie determinada sin que queden tantas variables desconocidas como las que no abordan los enfoques genéticos estándar . [100]
{{cite book}}: CS1 maint: DOI inactive as of January 2024 (link)libro electrónico ISBN 978-94-007-5561-1 ISSN 1559-0836 electrónico- ISSN 1868-0402