
Existen varios métodos para almacenar hidrógeno . Estos incluyen enfoques mecánicos como el uso de altas presiones y bajas temperaturas, o el empleo de compuestos químicos que liberan H 2 según sea necesario. Si bien diversas industrias producen grandes cantidades de hidrógeno, su mayor parte se consume en el lugar de producción, en particular para la síntesis de amoníaco . Durante muchos años, el hidrógeno se ha almacenado como gas comprimido o líquido criogénico y se ha transportado como tal en cilindros, tubos y tanques criogénicos para su uso en la industria o como propulsor en programas espaciales. El desafío general es el bajísimo punto de ebullición del H2 : hierve alrededor de 20,268 K (-252,882 °C o -423,188 °F). Lograr temperaturas tan bajas requiere gastar una cantidad significativa de energía.
Aunque el hidrógeno molecular tiene una densidad de energía muy alta en términos de masa, en parte debido a su bajo peso molecular , como gas en condiciones ambientales tiene una densidad de energía muy baja en volumen. Si se va a utilizar como combustible almacenado a bordo de un vehículo, el gas hidrógeno puro debe almacenarse en una forma densa en energía para proporcionar una autonomía de conducción suficiente. Como el hidrógeno es la molécula más pequeña, se escapa fácilmente de los contenedores. Teniendo en cuenta las fugas, los costes de transporte y producción, el hidrógeno podría tener un potencial de calentamiento global (GWP100) de 11,6. El metano, en comparación, tiene un PCA de 34. [1]

El hidrógeno comprimido es una forma de almacenamiento mediante la cual el gas hidrógeno se mantiene bajo presión para aumentar la densidad de almacenamiento. El hidrógeno comprimido en tanques de hidrógeno a 350 bar (5000 psi) y 700 bar (10 000 psi) se utiliza para sistemas de tanques de hidrógeno en vehículos, basados en tecnología de compuestos de carbono tipo IV. [2] Los fabricantes de automóviles, incluidos Honda [3] y Nissan [4], han estado desarrollando esta solución.
Depósitos de hidrógeno líquido para automóviles, del que se produce, por ejemplo, el BMW Hydrogen 7 . Japón tiene un sitio de almacenamiento de hidrógeno líquido (LH2) en el puerto de Kobe. [5] El hidrógeno se licua reduciendo su temperatura a -253 °C, similar al gas natural licuado (GNL), que se almacena a -162 °C. Se puede lograr una pérdida potencial de eficiencia de sólo el 12,79 %, o 4,26 kW⋅h/kg de 33,3 kW⋅h/kg. [6]
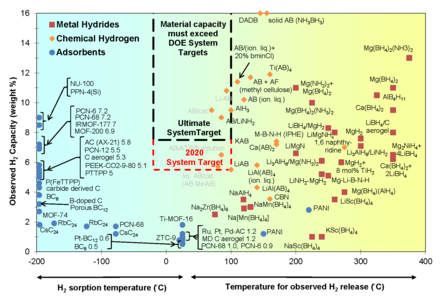
El almacenamiento de productos químicos podría ofrecer un alto rendimiento de almacenamiento debido a las altas densidades de almacenamiento. Por ejemplo, el hidrógeno supercrítico a 30 °C y 500 bar solo tiene una densidad de 15,0 mol/L, mientras que el metanol tiene una densidad de hidrógeno de 49,5 mol H 2 /L. El metanol y el dimetiléter saturado a 30 °C y 7 bar tienen una densidad de 42,1 moles de H2 / l de dimetiléter. [ cita necesaria ]
La regeneración del material de almacenamiento es problemática. Se han investigado una gran cantidad de sistemas de almacenamiento de productos químicos. La liberación de H2 puede ser inducida por reacciones de hidrólisis o reacciones de deshidrogenación catalizadas . Compuestos de almacenamiento ilustrativos son hidrocarburos, hidruros de boro , amoníaco y alano , etc. [8] Un enfoque químico muy prometedor es el almacenamiento electroquímico de hidrógeno, ya que la liberación de hidrógeno puede controlarse mediante la electricidad aplicada. [9] La mayoría de los materiales enumerados a continuación se pueden utilizar directamente para el almacenamiento electroquímico de hidrógeno.
Como se mostró antes, los nanomateriales ofrecen ventajas para los sistemas de almacenamiento de hidrógeno. Los nanomateriales ofrecen una alternativa que supera las dos barreras principales de los materiales a granel: la tasa de sorción y la temperatura de liberación. [ cita necesaria ]
La mejora de la cinética de sorción y la capacidad de almacenamiento se puede mejorar mediante el dopaje de catalizadores basados en nanomateriales , como se muestra en el trabajo del Centro de Investigación de Energía Limpia de la Universidad del Sur de Florida . [10] Este grupo de investigación estudió LiBH 4 dopado con nanopartículas de níquel y analizó la pérdida de peso y la temperatura de liberación de las diferentes especies. Observaron que una cantidad cada vez mayor de nanocatalizador reduce la temperatura de liberación en aproximadamente 20 °C y aumenta la pérdida de peso del material en un 2-3 %. La cantidad óptima de partículas de Ni fue del 3% molar, para lo cual la temperatura estuvo dentro de los límites establecidos (alrededor de 100 °C) y la pérdida de peso fue notablemente mayor que las especies no dopadas.
La tasa de sorción de hidrógeno mejora a nanoescala debido a la corta distancia de difusión en comparación con los materiales a granel. También tienen una relación superficie-volumen favorable .
La temperatura de liberación de un material se define como la temperatura a la que comienza el proceso de desorción . La energía o temperatura para inducir la liberación afecta el costo de cualquier estrategia de almacenamiento de sustancias químicas. Si el hidrógeno se une demasiado débilmente, la presión necesaria para la regeneración es alta, anulando así cualquier ahorro de energía. El objetivo para los sistemas de combustible de hidrógeno a bordo es aproximadamente <100 °C para la liberación y <700 bar para la recarga (20–60 kJ/mol H 2 ). [11] Una ecuación de van 't Hoff modificada , relaciona la temperatura y la presión parcial del hidrógeno durante el proceso de desorción. Las modificaciones a la ecuación estándar están relacionadas con efectos de tamaño a nanoescala.
Donde p H 2 es la presión parcial del hidrógeno, Δ H es la entalpía del proceso de sorción (exotérmico), Δ S es el cambio de entropía , R es la constante del gas ideal , T es la temperatura en Kelvin, V m es la volumen molar del metal, r es el radio de la nanopartícula y γ es la energía libre superficial de la partícula.
De la relación anterior vemos que el cambio de entalpía y entropía de los procesos de desorción depende del radio de la nanopartícula. Además, se incluye un nuevo término que tiene en cuenta el área de superficie específica de la partícula y se puede demostrar matemáticamente que una disminución en el radio de la partícula conduce a una disminución en la temperatura de liberación para una presión parcial determinada. [12]
El enfoque actual para reducir el CO 2 incluye capturarlo y almacenarlo en instalaciones de todo el mundo. Sin embargo, el almacenamiento plantea barreras técnicas y económicas que impiden su aplicación a escala global. Para utilizar CO 2 en la fuente puntual, la hidrogenación de CO 2 es un enfoque realista y práctico. La hidrogenación convencional reduce los compuestos orgánicos insaturados mediante la adición de H2 . Un método de hidrogenación de CO 2 es a través de la vía del metanol. El metanol se puede utilizar para producir hidrocarburos de cadena larga. Algunas barreras de la hidrogenación de CO 2 incluyen la purificación del CO 2 capturado , la fuente de H 2 procedente de la división del agua y los aportes de energía para la hidrogenación. Para superar estas barreras, podemos seguir desarrollando la tecnología verde del H2 y fomentar la investigación de catalizadores a nivel industrial y académico. Para aplicaciones industriales, el CO 2 a menudo se convierte en metanol. Hasta ahora se han hecho muchos progresos en el caso de las moléculas de CO 2 a C1. Sin embargo, la conversión de CO 2 en moléculas de alto valor aún enfrenta muchos obstáculos y el futuro de la hidrogenación de CO 2 depende del avance de las tecnologías catalíticas. [13]
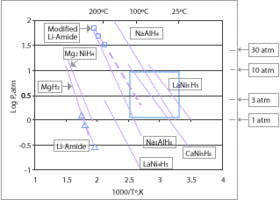
Los hidruros metálicos , como MgH 2 , NaAlH 4 , LiAlH 4 , LiH , LaNi5H6, TiFeH2, borano de amoníaco e hidruro de paladio representan fuentes de hidrógeno almacenado. Nuevamente los problemas persistentes son el % en peso de H2 que transportan y la reversibilidad del proceso de almacenamiento. [14] Algunos son líquidos fáciles de alimentar a temperatura y presión ambiente, mientras que otros son sólidos que podrían convertirse en gránulos. Estos materiales tienen buena densidad energética , aunque su energía específica suele ser peor que la de los principales combustibles de hidrocarburos .
LiNH2 , LiBH4 y NaBH4 . [15]
Un método alternativo para reducir las temperaturas de disociación es el dopado con activadores. Esta estrategia se ha utilizado para el hidruro de aluminio , pero la síntesis compleja hace que el enfoque sea poco atractivo. [dieciséis]
Los hidruros propuestos para su uso en una economía de hidrógeno incluyen hidruros simples de magnesio [17] o metales de transición e hidruros metálicos complejos , que normalmente contienen sodio , litio o calcio y aluminio o boro . Los hidruros elegidos para aplicaciones de almacenamiento proporcionan baja reactividad (alta seguridad) y altas densidades de almacenamiento de hidrógeno. Los principales candidatos son el hidruro de litio , el borohidruro de sodio , el hidruro de litio y aluminio y el borano amoniacal . La empresa francesa McPhy Energy está desarrollando el primer producto industrial, a base de hidruro de magnesio, que ya se vende a algunos clientes importantes como Iwatani y ENEL.
El almacenamiento reversible de hidrógeno lo exhibe el par de Lewis frustrado , que produce un borohidruro. [18] [19] [20]
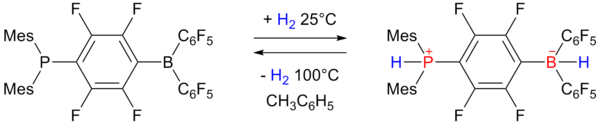
El fosfinoborano de la izquierda acepta un equivalente de hidrógeno en una atmósfera y 25 °C y lo expulsa nuevamente calentándolo a 100 °C. La capacidad de almacenamiento es del 0,25% en peso.
Se puede producir hidrógeno utilizando aluminio haciéndolo reaccionar con agua. [21] Anteriormente se creía que, para reaccionar con el agua, el aluminio debía ser despojado de su capa de óxido natural utilizando sustancias cáusticas, aleaciones, [22] o mezclándolo con galio (que produce nanopartículas de aluminio que permiten que el 90% del aluminio reaccione). ). [23] Desde entonces se ha demostrado que es posible una reacción eficiente aumentando la temperatura y la presión de la reacción. [24] El subproducto de la reacción para crear hidrógeno es óxido de aluminio , que puede reciclarse nuevamente para obtener aluminio con el proceso Hall-Héroult , lo que hace que la reacción sea teóricamente renovable. Aunque esto requiere electrólisis, que consume una gran cantidad de energía, la energía luego se almacena en el aluminio (y se libera cuando el aluminio reacciona con agua).
Los materiales de almacenamiento de hidrógeno a base de Mg generalmente pueden clasificarse en tres categorías, es decir, Mg puro, aleaciones a base de Mg y compuestos a base de Mg. En particular, más de 300 tipos de aleaciones de almacenamiento de hidrógeno basadas en Mg han recibido amplia atención [25] debido a su rendimiento general relativamente mejor. Sin embargo, la cinética inferior de absorción/desorción de hidrógeno que se debe a la excesiva estabilidad termodinámica del hidruro metálico hace que las aleaciones de almacenamiento de hidrógeno basadas en Mg no sean actualmente apropiadas para las aplicaciones reales y, por lo tanto, se han dedicado esfuerzos masivos para superar esta escasez. Algunos métodos de preparación de muestras, como la fundición, la sinterización de polvo, la difusión, la aleación mecánica, el método de síntesis de combustión con hidruros, el tratamiento de superficies y el tratamiento térmico, etc., se han empleado ampliamente para alterar el rendimiento dinámico y el ciclo de vida del almacenamiento de hidrógeno a base de Mg. aleaciones. Además, algunas estrategias de modificación intrínseca, incluida la aleación, [26] [27] [28] [29] nanoestructuración, [30] [31] [32] dopaje con aditivos catalíticos, [33] [34] y adquisición de nanocompuestos con otros hidruros , [35] [36] etc., se han explorado principalmente para mejorar intrínsecamente el rendimiento de las aleaciones de almacenamiento de hidrógeno basadas en Mg. [37] Al igual que el aluminio, el magnesio también reacciona con el agua para producir hidrógeno. [38]
De las aleaciones primarias de almacenamiento de hidrógeno desarrolladas anteriormente, se cree que el Mg y los materiales de almacenamiento de hidrógeno a base de Mg proporcionan la notable posibilidad de aplicación práctica, debido a las siguientes ventajas: 1) el recurso de Mg es abundante y económico. El elemento Mg existe en abundancia y representa ≈2,35% de la corteza terrestre con el rango del octavo; 2) baja densidad de apenas 1,74 g cm-3; 3) capacidad superior de almacenamiento de hidrógeno. La cantidad teórica de almacenamiento de hidrógeno del Mg puro es 7,6 % en peso (porcentaje en peso), [39] [40] [41] y el Mg2Ni es 3,6 % en peso, respectivamente. [37]
El alanato de litio (LiAlH 4 ) se sintetizó por primera vez en 1947 mediante la disolución de hidruro de litio en una solución etérea de cloruro de aluminio. [42] LiAlH 4 tiene una capacidad gravimétrica teórica de 10,5 % en peso de H 2 y se deshidrogena en los siguientes tres pasos: [43] [44] [45] 3LiAlH 4 ↔ Li 3 AlH 6 + 3H 2 + 2Al (423–448 K 5,3% en peso de H2 ; ∆H = −10 kJ·mol−1 H2 ) ; Li 3 AlH 6 ↔ 3LiH + Al + 1,5H 2 (453–493 K; 2,6 % en peso de H 2 ; ∆H = 25 kJ·mol-1 H 2 ); 3LiH + 3Al ↔ 3LiAl + 3/2H2 ( >673 K; 2,6 % en peso de H2 ; ∆H = 140 kJ·mol-1 H2 ) . [46] Los dos primeros pasos conducen a una cantidad total de hidrógeno liberado igual al 7,9% en peso, lo que podría ser atractivo para aplicaciones prácticas, pero las temperaturas de trabajo y la cinética de desorción aún están lejos de los objetivos prácticos. En los últimos años se han aplicado varias estrategias para superar estos límites, como la molienda de bolas y la adición de catalizadores. [47] [48] [49] [50] [51] [46]
El alanato de potasio (KAlH 4 ) fue preparado por primera vez por Ashby et al. [52] mediante síntesis en un solo paso en tolueno, tetrahidrofurano y diglima. En cuanto a las propiedades de absorción y desorción de hidrógeno, este alanato apenas ha sido estudiado. Morioka et al., [53] mediante análisis de desorción programada por temperatura (TPD), propusieron el siguiente mecanismo de deshidrogenación: 3KAlH 4 →K 3 AlH 6 + 2Al + 3H 2 (573 K, ∆H = 55 kJ·mol−1 H 2 2,9 % en peso H 2 ), K 3 AlH 6 → 3KH + Al + 3/2H 2 (613 K, ∆H = 70 kJ · mol −1 H 2 ; 1,4 % en peso H 2 ), 3KH → 3K + 3/ 2H2 (703 K, 1,4 % en peso de H2 ) . Se demostró que estas reacciones son reversibles sin la adición de catalizadores a presiones y temperaturas de hidrógeno relativamente bajas. Se encontró que la adición de TiCl3 disminuía la temperatura de trabajo del primer paso de deshidrogenación de 50 K, [54] pero no se registraron variaciones para los dos últimos pasos de reacción. [46]
Los compuestos orgánicos insaturados pueden almacenar enormes cantidades de hidrógeno. Estos portadores de hidrógeno orgánico líquido (LOHC) se hidrogenan para su almacenamiento y se deshidrogenan nuevamente cuando se necesita energía/hidrógeno. Utilizando LOHC, se pueden alcanzar densidades de almacenamiento gravimétrico relativamente altas (alrededor del 6% en peso) y la eficiencia energética general es mayor que con otras opciones de almacenamiento de productos químicos, como la producción de metano a partir de hidrógeno. [55] Tanto la hidrogenación como la deshidrogenación de LOHC requieren catalizadores. [56] Se demostró que la sustitución de hidrocarburos por heteroátomos, como N, O, etc., mejora las propiedades de deshidrogenación reversible.
La investigación sobre LOHC se concentró en los cicloalcanos en una etapa temprana, con su capacidad de hidrógeno relativamente alta (6-8 % en peso) y producción de hidrógeno libre de COx . [56] Los compuestos aromáticos heterocíclicos (o N-heterociclos) también son apropiados para esta tarea. Un compuesto que aparece en la investigación de LOHC es el N-etilcarbazol [de] (NEC) [57], pero existen muchos otros. [58] El dibenciltolueno, que ya se utiliza como fluido de transferencia de calor en la industria, fue identificado como LOHC potencial. Con un amplio rango de líquidos entre -39 °C (punto de fusión) y 390 °C (punto de ebullición) y una densidad de almacenamiento de hidrógeno del 6,2 % en peso, el dibenciltolueno es ideal como material LOHC. [59] Se ha sugerido que el ácido fórmico es un material prometedor para el almacenamiento de hidrógeno con una capacidad de hidrógeno del 4,4% en peso. [60]
Los cicloalcanos reportados como LOHC incluyen ciclohexano, metilciclohexano y decalina. La deshidrogenación de cicloalcanos es altamente endotérmica (63-69 kJ/mol H 2 ), lo que significa que este proceso requiere alta temperatura. [56] La deshidrogenación de decalina es la más favorecida termodinámicamente entre los tres cicloalcanos, y el metilciclohexano ocupa el segundo lugar debido a la presencia del grupo metilo. [61] Durante décadas se han llevado a cabo investigaciones sobre el desarrollo de catalizadores para la deshidrogenación de cicloalcanos. Los catalizadores a base de níquel (Ni), molibdeno (Mo) y platino (Pt) son muy investigados para la deshidrogenación. Sin embargo, la coquización sigue siendo un gran desafío para la estabilidad a largo plazo del catalizador. [62] [63]
La temperatura requerida para la hidrogenación y deshidrogenación cae significativamente en los heterociclos frente a los carbociclos simples. [64] Entre todos los N-heterociclos, el par saturado-insaturado de dodecahidro-N-etilcarbazol (12H-NEC) y NEC se ha considerado como un candidato prometedor para el almacenamiento de hidrógeno con un contenido de hidrógeno bastante grande (5,8% en peso). [65] La figura de la parte superior derecha muestra la deshidrogenación y la hidrogenación del par 12H-NEC y NEC. El catalizador estándar para NEC a 12H-NEC se basa en Ru y Rh. La selectividad de la hidrogenación puede alcanzar el 97% a 7 MPa y 130 °C-150 °C. [56] Aunque los N-heterociclos pueden optimizar las propiedades termodinámicas desfavorables de los cicloalcanos, quedan muchos problemas sin resolver, como el alto costo, la alta toxicidad y las barreras cinéticas, etc. [56]
Los líquidos iónicos de imidazolio, como las sales de N-bis(trifluorometanosulfonil)imidato de alquil(aril)-3-metilimidazolio, pueden agregar de forma reversible de 6 a 12 átomos de hidrógeno en presencia de catalizadores de nanopartículas clásicas de Pd/C o Ir0 y pueden usarse como materiales alternativos para -Dispositivos de almacenamiento de hidrógeno a bordo. Estas sales pueden contener hasta 30 g L −1 de hidrógeno a presión atmosférica. [66]
El ácido fórmico es un material de almacenamiento de hidrógeno muy eficaz, aunque su densidad de H2 es baja. Se ha generado hidrógeno libre de monóxido de carbono en un rango de presión muy amplio (1-600 bar). Un sistema catalítico homogéneo basado en catalizadores de rutenio solubles en agua descompone selectivamente el HCOOH en H 2 y CO 2 en solución acuosa. [67] Este sistema catalítico supera las limitaciones de otros catalizadores (por ejemplo, mala estabilidad, vida útil catalítica limitada, formación de CO) para la descomposición del ácido fórmico, convirtiéndolo en un material viable para el almacenamiento de hidrógeno. [68] Y el coproducto de esta descomposición, el dióxido de carbono, se puede utilizar como vector de hidrógeno hidrogenándolo nuevamente a ácido fórmico en un segundo paso. La hidrogenación catalítica del CO 2 se ha estudiado durante mucho tiempo y se han desarrollado procedimientos eficaces. [69] [70] El ácido fórmico contiene 53 g L −1 de hidrógeno a temperatura ambiente y presión atmosférica. En peso, el ácido fórmico puro almacena 4,3% en peso de hidrógeno. El ácido fórmico puro es un líquido con un punto de inflamación de 69 °C (cf. gasolina -40 °C, etanol 13 °C). El ácido fórmico al 85% no es inflamable.
El amoníaco (NH 3 ) libera H 2 en un reformador catalítico apropiado. El amoníaco proporciona altas densidades de almacenamiento de hidrógeno como líquido con una presurización suave y restricciones criogénicas: también se puede almacenar como líquido a temperatura y presión ambiente cuando se mezcla con agua. El amoníaco es la segunda sustancia química que se produce más comúnmente en el mundo y existe una gran infraestructura para producir, transportar y distribuir amoníaco. El amoníaco se puede reformar para producir hidrógeno sin residuos nocivos, o puede mezclarse con los combustibles existentes y, en las condiciones adecuadas, quemarse de manera eficiente. Como no hay carbono en el amoníaco, no se producen subproductos de carbono; convirtiendo así esta posibilidad en una opción "neutra en carbono" para el futuro. El amoníaco puro se quema mal a las presiones atmosféricas que se encuentran en los calentadores de agua y estufas de gas natural. Bajo compresión en un motor de automóvil, es un combustible adecuado para motores de gasolina ligeramente modificados. El amoníaco es un combustible alternativo adecuado porque tiene una densidad energética de 18,6 MJ/kg a NTP y subproductos de combustión libres de carbono. [71]
El amoníaco enfrenta varios desafíos para una adaptación generalizada como material de almacenamiento de hidrógeno. El amoníaco es un gas tóxico con un olor potente a temperatura y presión estándar. [72] Además, se necesitan avances en la eficiencia y escalabilidad de la descomposición del amoníaco para la viabilidad comercial, ya que las membranas de las pilas de combustible son muy sensibles al amoníaco residual y las técnicas de descomposición actuales tienen bajas tasas de rendimiento. [73] Se puede utilizar una variedad de metales de transición para catalizar la reacción de descomposición del amoníaco, siendo el más eficaz el rutenio . Esta catálisis funciona mediante quimisorción , donde la energía de adsorción de N 2 es menor que la energía de reacción de disociación. [74] La purificación del hidrógeno se puede lograr de varias maneras. El hidrógeno se puede separar del amoníaco que no ha reaccionado utilizando una membrana permeable selectiva para el hidrógeno. [75] También se puede purificar mediante la adsorción de amoníaco, que puede quedar atrapado selectivamente debido a su polaridad. [76]
En septiembre de 2005, químicos de la Universidad Técnica de Dinamarca anunciaron un método para almacenar hidrógeno en forma de amoníaco saturado en una pastilla de sal. Afirman que será un método de almacenamiento económico y seguro. [77] [ necesita actualización ]
La hidracina se descompone en la célula para formar nitrógeno e hidrógeno / [78] Los hidruros de silicio y los hidruros de germanio también son candidatos como materiales de almacenamiento de hidrógeno, ya que pueden estar sujetos a una reacción energéticamente favorecida para formar dímeros unidos covalentemente con pérdida de una molécula de hidrógeno. [79] [80]
Antes de 1980, se investigaron varios compuestos para el almacenamiento de hidrógeno, incluidos borohidruros complejos o aluminohidruros y sales de amonio. Estos hidruros tienen un rendimiento de hidrógeno teórico superior limitado a aproximadamente 8,5% en peso. Entre los compuestos que contienen solo B, N y H (iones positivos y negativos), los ejemplos representativos incluyen: amina boranos, amoníatos de hidruro de boro, complejos de hidrazina-borano y octahidrotriboratos o tetrahidroboratos de amonio. De estos, los aminaboranos (y especialmente el borano amoniacal ) se han investigado ampliamente como portadores de hidrógeno. Durante las décadas de 1970 y 1980, el Ejército y la Marina de los EE. UU. financiaron esfuerzos destinados a desarrollar compuestos generadores de gas de hidrógeno/deuterio para su uso en láseres químicos HF/DF y HCl , y láseres dinámicos de gas. Las anteriores formulaciones generadoras de gas hidrógeno utilizaban aminaboranos y sus derivados. La ignición de los amina borano forma nitruro de boro (BN) y gas hidrógeno. Además del borano de amoníaco (H 3 BNH 3 ), otros generadores de gas incluyen diammoniato de diborano, H 2 B (NH 3 ) 2 BH 4 . [ cita necesaria ]
En este caso el hidrógeno permanece en forma física, es decir, como gas, fluido supercrítico, adsorbato o inclusiones moleculares. Se consideran las limitaciones teóricas y los resultados experimentales [81] con respecto a la capacidad volumétrica y gravimétrica de los microvasos de vidrio, medios microporosos y nanoporosos, así como las demandas de seguridad y tiempo de llenado. Como el hidrógeno es la molécula más pequeña, se escapa fácilmente de los contenedores y durante la transferencia de un contenedor a otro, y el hidrógeno filtrado tiene un efecto de calentamiento global 11,6 veces más fuerte que el CO₂. [82]
Las zeolitas son materiales de aluminosilicato microporosos y altamente cristalinos . Como exhiben estructuras de jaula y túnel, ofrecen el potencial para la encapsulación de gases no polares como el H 2 . En este sistema, el hidrógeno se fisisorbe en la superficie de los poros de la zeolita mediante un mecanismo de adsorción que implica que el hidrógeno sea forzado a entrar en los poros bajo presión y baja temperatura. [83] Por lo tanto, al igual que otros materiales porosos, su capacidad de almacenamiento de hidrógeno depende del área de la superficie BET , el volumen de los poros, la interacción del hidrógeno molecular con las superficies internas de los microporos y las condiciones de trabajo como la presión y la temperatura. [84]
Las investigaciones muestran que el diámetro del canal es también uno de los parámetros que determinan esta capacidad, especialmente a alta presión. En este caso, un material eficaz debería presentar un gran volumen de poros y un diámetro de canal cercano al diámetro cinético de la molécula de hidrógeno (d H = 2,89 Å). [83]
La siguiente tabla muestra la absorción de hidrógeno de varias zeolitas a la temperatura del nitrógeno líquido (77 K):
Los carbones activados son materiales de carbono amorfos muy porosos con una gran superficie aparente. La fisisorción de hidrógeno se puede aumentar en estos materiales aumentando el área de superficie aparente y optimizando el diámetro de los poros a alrededor de 7 Å. [86] Estos materiales son de particular interés debido al hecho de que pueden fabricarse a partir de materiales de desecho, como colillas de cigarrillos, que han demostrado un gran potencial como materiales precursores de materiales de almacenamiento de hidrógeno de alta capacidad. [87] [88]
El grafeno puede almacenar hidrógeno de manera eficiente. El H 2 se suma a los dobles enlaces dando grafeno . El hidrógeno se libera al calentarlo a 450 °C. [89] [90]
Se han propuesto portadores de hidrógeno basados en carbono nanoestructurado (como buckybolas y nanotubos de carbono). Sin embargo, el contenido de hidrógeno asciende a ≈3,0-7,0 % en peso a 77 K, lo que está lejos del valor establecido por el Departamento de Energía de EE. UU. (6 % en peso en condiciones casi ambientales). [ cita necesaria ]
Para convertir los materiales de carbono en tecnologías eficaces de almacenamiento de hidrógeno, se han dopado nanotubos de carbono (CNT) con MgH 2 . [10] Se ha demostrado que el hidruro metálico tiene una capacidad de almacenamiento teórica (7,6 % en peso) que cumple con el requisito del Departamento de Energía de los Estados Unidos de 6 % en peso, pero tiene aplicaciones prácticas limitadas debido a su alta temperatura de liberación. El mecanismo propuesto implica la creación de canales de difusión rápida por parte de los CNT dentro de la red de MgH 2 . Los fullerenos son otros nanomateriales carbonosos que se han probado para el almacenamiento de hidrógeno en este centro. Las moléculas de fullereno están compuestas por una estructura cerrada de C 60 , que permite la hidrogenación de los carbonos con doble enlace, lo que conduce a un isómero teórico C 60 H 60 con un contenido de hidrógeno del 7,7% en peso. Sin embargo, la temperatura de liberación en estos sistemas es alta (600 °C).
Las estructuras organometálicas representan otra clase de materiales porosos sintéticos que almacenan hidrógeno y energía a nivel molecular. Los MOF son estructuras híbridas inorgánicas-orgánicas altamente cristalinas que contienen grupos o iones metálicos (unidades de construcción secundarias) como nodos y ligandos orgánicos como conectores. Cuando las moléculas invitadas (disolvente) que ocupan los poros se eliminan durante el intercambio de disolvente y el calentamiento al vacío, se puede lograr una estructura porosa de los MOF sin desestabilizar la estructura y las moléculas de hidrógeno se adsorberán en la superficie de los poros mediante fisisorción. En comparación con las zeolitas tradicionales y los materiales de carbono porosos, los MOF tienen un número muy elevado de poros y área de superficie que permiten una mayor absorción de hidrógeno en un volumen determinado. Por lo tanto, el interés en la investigación sobre el almacenamiento de hidrógeno en MOF ha ido creciendo desde 2003, cuando se introdujo el primer almacenamiento de hidrógeno basado en MOF. Dado que existen infinitas variaciones geométricas y químicas de los MOF basadas en diferentes combinaciones de SBU y enlazadores, muchas investigaciones exploran qué combinación proporcionará la máxima absorción de hidrógeno mediante diferentes materiales de iones metálicos y enlazadores. [ cita necesaria ]
La temperatura, la presión y la composición de los MOF pueden influir en su capacidad de almacenamiento de hidrógeno. La capacidad de adsorción de los MOF es menor a temperaturas más altas y mayor a temperaturas más bajas. Con el aumento de temperatura, la fisisorción disminuye y la quimisorción aumenta. [91] Para MOF-519 y MOF-520, el calor isostérico de adsorción disminuyó con el aumento de presión. [92] Para MOF-5, la absorción de hidrógeno tanto gravimétrica como volumétrica aumentó con el aumento de la presión. [91] La capacidad total puede no ser coherente con la capacidad utilizable en condiciones de oscilación de presión. Por ejemplo, MOF-5 e IRMOF-20, que tienen la capacidad volumétrica total más alta, muestran la capacidad volumétrica menos utilizable. [93] La capacidad de absorción puede aumentarse modificando la estructura. Por ejemplo, la absorción de hidrógeno del PCN-68 es mayor que la del PCN-61. [94] Las estructuras aromáticas porosas (PAF-1), que se conocen como materiales de alta superficie, pueden lograr una mayor superficie mediante dopaje. [95]
Hay muchas formas diferentes de modificar los MOF, como catalizadores de MOF, híbridos de MOF, MOF con centros metálicos y dopaje. Los catalizadores MOF tienen alta superficie, porosidad y capacidad de almacenamiento de hidrógeno. Sin embargo, los centros metálicos activos son bajos. Los híbridos MOF tienen mayor superficie, porosidad, capacidad de carga y capacidad de almacenamiento de hidrógeno. Sin embargo, no son estables y carecen de centros activos. El dopaje en los MOF puede aumentar la capacidad de almacenamiento de hidrógeno, pero puede haber un efecto estérico y los metales inertes tienen una estabilidad inadecuada. Podría haber formación de poros interconectados y baja resistencia a la corrosión en los MOF con centros metálicos, mientras que podrían tener buena energía de unión y mayor estabilidad. Estas ventajas y desventajas para diferentes tipos de MOF modificados muestran que los híbridos MOF son más prometedores debido a la buena controlabilidad en la selección de materiales para una alta superficie, porosidad y estabilidad. [91]
En 2006, los químicos lograron concentraciones de almacenamiento de hidrógeno de hasta el 7,5% en peso en MOF-74 a una temperatura baja de 77 K. [96] [97] En 2009, los investigadores alcanzaron el 10% en peso a 77 bar (1117 psi) y 77 K con MOF NOTT-112. [98] La mayoría de los artículos sobre el almacenamiento de hidrógeno en MOF informan sobre la capacidad de absorción de hidrógeno a una temperatura de 77 K y una presión de 1 bar porque estas condiciones están comúnmente disponibles y la energía de enlace entre el hidrógeno y el MOF a esta temperatura es grande en comparación con la vibración térmica. energía. Variar varios factores, como el área de superficie, el tamaño de los poros, la catenación, la estructura del ligando y la pureza de la muestra, puede dar como resultado diferentes cantidades de absorción de hidrógeno en los MOF.
En 2020, los investigadores informaron que NU-1501-Al, una estructura organometálica (MOF) ultraporosa basada en grupos trinucleares metálicos, produjo "impresionantes rendimientos de almacenamiento gravimétrico y volumétrico para hidrógeno y metano", con una capacidad de suministro de hidrógeno del 14,0% w. /p, 46,2 g/litro. [99] [100]
El almacenamiento criocomprimido de hidrógeno es la única tecnología que cumple con los objetivos del DOE para 2015 en cuanto a eficiencia volumétrica y gravimétrica (ver "CcH2" en la diapositiva 6 en [101] ).
Además, otro estudio ha demostrado que la criocompresión presenta interesantes ventajas de costos: el costo de propiedad (precio por milla) y el costo del sistema de almacenamiento (precio por vehículo) son en realidad los más bajos en comparación con cualquier otra tecnología (consulte la tercera fila en la diapositiva 13 de [ 102] ).
Al igual que el almacenamiento de líquidos, el criocomprimido utiliza hidrógeno frío (20,3 K y ligeramente más) para alcanzar una alta densidad de energía. Sin embargo, la principal diferencia es que, cuando el hidrógeno se calienta debido a la transferencia de calor con el medio ambiente ("ebullición"), se permite que el tanque alcance presiones mucho más altas (hasta 350 bares frente a un par de bares para almacenamiento de líquidos). Como consecuencia, se necesita más tiempo antes de que el hidrógeno tenga que ventilarse y, en la mayoría de situaciones de conducción, el automóvil utiliza suficiente hidrógeno para mantener la presión muy por debajo del límite de ventilación. [ cita necesaria ]
En consecuencia, se ha demostrado que se podía lograr una gran autonomía con un tanque criocomprimido: se recorrieron más de 650 millas (1.050 km) con el tanque lleno montado en un motor de Toyota Prius alimentado con hidrógeno . [103] Aún se están realizando investigaciones para estudiar y demostrar todo el potencial de la tecnología. [104]
A partir de 2010, BMW Group inició una validación exhaustiva a nivel de componentes y sistemas del almacenamiento criocomprimido de vehículos en su camino hacia un producto comercial. [105]
El H2 enjaulado en un hidrato de clatrato se informó por primera vez en 2002, pero requiere presiones muy altas para ser estable. En 2004, los investigadores demostraron que se podían formar hidratos sólidos que contenían H2 a temperatura ambiente y decenas de bares añadiendo pequeñas cantidades de sustancias promotoras como el THF . [106] [107] Estos clatratos tienen una densidad máxima teórica de hidrógeno de alrededor del 5% en peso y 40 kg/m 3 .
Un equipo de científicos rusos, israelíes y alemanes ha desarrollado en colaboración una tecnología innovadora basada en matrices de capilares de vidrio para la infusión, el almacenamiento y la liberación controlada de hidrógeno de forma segura en aplicaciones móviles. [108] [109] La tecnología C.En ha alcanzado los objetivos de 2010 del Departamento de Energía de los Estados Unidos (DOE) para sistemas de almacenamiento de hidrógeno a bordo. [110] Los objetivos del DOE 2015 se pueden lograr utilizando capilares de vidrio flexibles y un método criocomprimido de almacenamiento de hidrógeno. [111]
Las microesferas de vidrio huecas (HGM) se pueden utilizar para el almacenamiento y liberación controlados de hidrógeno. Para el almacenamiento de hidrógeno se consideran HGM con un diámetro de 1 a 100 μm, una densidad de 1,0 a 2,0 gm/cc y una pared porosa con aberturas de 10 a 1000 angstroms . Las ventajas de los HGM para el almacenamiento de hidrógeno son que no son tóxicos, son livianos, baratos, reciclables, reversibles, fáciles de manipular en condiciones atmosféricas, capaces de almacenarse en un tanque y el hidrógeno que contienen no es explosivo. [112] Cada uno de estos HGM es capaz de contener hidrógeno hasta 150 MPa sin el peso y el volumen de un gran tanque presurizado. Todas estas cualidades son favorables en aplicaciones vehiculares. Más allá de estas ventajas, los HGM se consideran una posible solución de hidrógeno debido a que la difusividad del hidrógeno tiene una gran dependencia de la temperatura. A temperatura ambiente, la difusividad es muy baja y el hidrógeno queda atrapado en el HGM. La desventaja de los HGM es que para llenar y desgasificar hidrógeno de manera efectiva, la temperatura debe ser de al menos 300 °C, lo que aumenta significativamente el costo operativo de los HGM en el almacenamiento de hidrógeno. [113] La alta temperatura se puede atribuir en parte a que el vidrio es un aislante y tiene una baja conductividad térmica ; esto dificulta la difusividad del hidrógeno y, posteriormente, se requiere una temperatura más alta para lograr la capacidad de almacenamiento deseada.
Para que esta tecnología sea más viable económicamente para uso comercial, se están realizando investigaciones para aumentar la eficiencia de la difusión de hidrógeno a través de los HGM. Un estudio realizado por Dalai et al. Se buscó aumentar la conductividad térmica del HGM dopando el vidrio con cobalto . Al hacerlo, aumentaron la conductividad térmica de 0,0072 a 0,198 W/mK con un 10 % en peso de Co. Sin embargo, solo se observaron aumentos en la adsorción de hidrógeno hasta un 2 % en peso de Co (0,103 W/mK) cuando el óxido metálico comenzó a cubrir los poros en la concha de cristal. Este estudio concluyó con una capacidad de almacenamiento de hidrógeno de 3,31% en peso con 2% en peso de Co a 200 °C y 10 bar. [112]
Un estudio realizado por Rapp y Shelby buscó aumentar la tasa de liberación de hidrógeno mediante desgasificación fotoinducida en HGM dopados en comparación con los métodos de calentamiento convencionales. El vidrio fue dopado con metales ópticamente activos para interactuar con la luz infrarroja de alta intensidad . El estudio encontró que el vidrio de borosilicato 7070 dopado con Fe 3 O 4 al 0,5% en peso tenía un aumento en la liberación de hidrógeno proporcional a la intensidad de la lámpara infrarroja. Además de las mejoras en la difusividad por infrarrojos solo, las reacciones entre el hidrógeno y el vidrio dopado con hierro aumentaron la relación Fe 2+ /Fe 3+ , lo que aumentó la absorción de infrarrojos y, por lo tanto, aumentó aún más el rendimiento de hidrógeno. [114]
A partir de 2020, los avances realizados en el estudio de los HGM han aumentado su eficiencia, pero aún no alcanzan los objetivos del Departamento de Energía para esta tecnología. Las temperaturas de operación tanto para la adsorción como para la liberación de hidrógeno son la mayor barrera para la comercialización . [115]
A diferencia de las aplicaciones móviles, la densidad del hidrógeno no es un gran problema para las aplicaciones estacionarias. En cuanto a las aplicaciones móviles, las aplicaciones estacionarias pueden utilizar tecnología establecida:

El almacenamiento subterráneo de hidrógeno [118] es la práctica de almacenamiento de hidrógeno en cavernas , domos de sal y campos de petróleo y gas agotados. ICI almacena desde hace muchos años grandes cantidades de hidrógeno gaseoso sin dificultades en cavernas. [119] El almacenamiento subterráneo de grandes cantidades de hidrógeno líquido puede funcionar como almacenamiento de energía de la red . La eficiencia de ida y vuelta es de aproximadamente el 40 % (frente al 75-80 % de la hidroeléctrica de bombeo (PHES) ) y el costo es ligeramente mayor que la hidroeléctrica de bombeo, si solo se requiere un número limitado de horas de almacenamiento. [120] Otro estudio al que hace referencia un documento de trabajo del personal europeo encontró que para el almacenamiento a gran escala, la opción más barata es el hidrógeno a 140 €/MWh por 2.000 horas de almacenamiento utilizando un electrolizador, almacenamiento en cavernas de sal y una planta de energía de ciclo combinado. [117] : 15 El proyecto europeo Hyunder [121] indicó en 2013 que para el almacenamiento de energía eólica y solar se necesitan 85 cavernas adicionales, ya que no pueden ser cubiertas por los sistemas PHES y CAES . [122] Un estudio de caso alemán sobre el almacenamiento de hidrógeno en cavernas de sal encontró que si el excedente de energía alemán (7% de la generación renovable variable total para 2025 y 20% para 2050) se convirtiera en hidrógeno y se almacenara bajo tierra, estas cantidades requerirían unas 15 cavernas de 500.000 metros cúbicos cada una hasta 2025 y unas 60 cavernas hasta 2050, lo que corresponde aproximadamente a un tercio del número de cavernas de gas actualmente en funcionamiento en Alemania. [123] En Estados Unidos, Sandia Labs está llevando a cabo investigaciones sobre el almacenamiento de hidrógeno en yacimientos de petróleo y gas agotados, que podrían absorber fácilmente grandes cantidades de hidrógeno producido de forma renovable, ya que existen unos 2,7 millones de pozos agotados. [124]
El almacenamiento subterráneo de hidrógeno es la práctica de almacenamiento de hidrógeno en cavernas , [125] [126] domos de sal y campos agotados de petróleo y gas . [127] [128] Durante muchos años se han almacenado grandes cantidades de hidrógeno gaseoso en cavernas. [129] [ verificación fallida – ver discusión ] [ ¿fuente no confiable? ] El almacenamiento de grandes cantidades de hidrógeno bajo tierra en domos de sal extraídas en solución , [130] acuíferos , [131] cavernas de roca excavadas o minas puede funcionar como almacenamiento de energía de la red , [132] esencial para la economía del hidrógeno . [133] Utilizando un turboexpansor, las necesidades de electricidad para el almacenamiento comprimido a 200 bar ascienden al 2,1% del contenido energético. [134]
La terminal Chevron Phillips Clemens en Texas ha almacenado hidrógeno desde la década de 1980 en una caverna de sal extraída en solución. El techo de la caverna está a unos 850 m (2800 pies) bajo tierra. La caverna es un cilindro con un diámetro de 49 m (160 pies), una altura de 300 m (1000 pies) y una capacidad de hidrógeno utilizable de 30,2 × 10 6 m 3 (1.066 millones de pies cúbicos ), o 2.520 toneladas métricas ( 2.480 toneladas largas; 2.780 toneladas cortas). [135]
Las cavernas de sal se crean artificialmente inyectando agua desde la superficie en un pozo en la sal gema, donde la sal gema es un material policristalino hecho de NaCl, halita. Generalmente se eligen lugares como domos de sal o lechos de sal para la creación de cavernas de sal. Las cavernas de sal pueden alcanzar una profundidad máxima de 2.000 m y una capacidad de volumen máxima de 1.000.000 m3. La frecuencia de los ciclos de inyección y retirada oscila entre 10 y 12 ciclos por año. Y la tasa de fuga ronda el 1%. [136] [137]
Debido a las propiedades fisicoquímicas de la sal gema, las cavernas de sal presentan múltiples ventajas. Las características clave son el bajo contenido de agua, la baja porosidad y permeabilidad y su inercia química hacia el hidrógeno. [138] La permeabilidad es un parámetro clave en el almacenamiento subterráneo de hidrógeno, lo que afecta su capacidad de sellado. Aunque los estudios han encontrado que la dilatancia y la fractura por extensión pueden causar un aumento significativo de la permeabilidad, la recristalización de los cristales de sal de roca, que es un proceso de curación de los límites de los granos, puede contribuir a su rigidez mecánica y recuperación de la permeabilidad. [139] Sus propiedades plásticas previenen la formación y propagación de fracturas y lo protegen de perder su estanqueidad, lo cual es particularmente importante para el almacenamiento de hidrógeno. [138] Algunas de las desventajas de las cavernas de sal incluyen una menor capacidad de almacenamiento, una gran cantidad de agua necesaria y el efecto de la corrosión. Se necesita gas colchón para evitar la fluencia debida a la caída de presión al retirar gas del yacimiento. Aunque la necesidad de gas colchón es relativamente pequeña, alrededor del 20%, el costo operativo aún puede aumentar cuando se trabaja con una mayor capacidad de almacenamiento. El costo es otra gran preocupación, ya que los costos de construcción y operación siguen siendo altos. [137] [140]
Aunque la gente tiene experiencia en el almacenamiento de gas natural, almacenar hidrógeno es mucho más complejo. Factores como la difusividad del hidrógeno en los sólidos provocan restricciones en el almacenamiento en cavernas de sal. La actividad microbiana es objeto de extensas investigaciones en todo el mundo debido a su impacto en la pérdida de hidrógeno. Como resultado del metabolismo bacteriano de las bacterias metanogénicas, se consumen dióxido de carbono e hidrógeno y se produce metano, lo que conduce a la pérdida del hidrógeno almacenado en las cavernas de sal. [141] [140]
Una caverna de 800 m de altura y 50 m de diámetro puede contener hidrógeno equivalente a 150 GWh. [147] [148]
Power to gas es una tecnología que convierte la energía eléctrica en gas combustible . Existen dos métodos: el primero consiste en utilizar la electricidad para descomponer el agua e inyectar el hidrógeno resultante en la red de gas natural; el segundo método, menos eficiente, se utiliza para convertir dióxido de carbono e hidrógeno en metano (ver gas natural ) mediante electrólisis y la reacción de Sabatier . Una tercera opción es combinar el hidrógeno mediante electrólisis con una fuente de carbono (ya sea dióxido de carbono o monóxido de carbono procedente de biogás , de procesos industriales o mediante dióxido de carbono capturado directamente en el aire ) mediante biometanación , [149] [150] donde los biometanógenos (arqueas ) consumen dióxido de carbono e hidrógeno y producen metano en un ambiente anaeróbico. Este proceso es muy eficiente, ya que las arqueas se autorreplican y solo requieren calor bajo (60 °C) para realizar la reacción.
SoCalGas también ha logrado otro proceso para convertir el dióxido de carbono del biogás crudo en metano en un solo paso electroquímico, lo que representa un método más simple para convertir el exceso de electricidad renovable en gas natural almacenable. [151]
El Reino Unido ha completado los estudios y se está preparando para comenzar a inyectar hidrógeno en la red de gas, ya que anteriormente la red transportaba "gas ciudad", que es un 50% de hidrógeno y metano formado a partir de carbón. Los auditores KPMG descubrieron que convertir el Reino Unido al gas hidrógeno podría ser entre £150 mil millones y £200 mil millones más barato que volver a cablear los hogares británicos para que utilicen calefacción eléctrica alimentada por fuentes con bajas emisiones de carbono. [152]
El exceso de energía o la energía de temporada baja generada por generadores eólicos o paneles solares se puede utilizar para equilibrar la carga en la red energética. Utilizando el sistema de gas natural existente para hidrógeno, el fabricante de pilas de combustible Hydrogenics y el distribuidor de gas natural Enbridge se han asociado para desarrollar un sistema de energía a gas en Canadá. [153]
Almacenamiento de hidrógeno por tuberías donde se utiliza una red de gas natural para el almacenamiento de hidrógeno. Antes de pasar al gas natural , las redes de gas alemanas funcionaban con gas urbano , que en su mayor parte (60-65%) estaba compuesto por hidrógeno. La capacidad de almacenamiento de la red alemana de gas natural es de más de 200.000 GW·h, suficiente para cubrir las necesidades energéticas de varios meses. En comparación, la capacidad de todas las centrales eléctricas alemanas de almacenamiento por bombeo asciende a sólo unos 40 GW·h. El transporte de energía a través de una red de gas se realiza con muchas menos pérdidas (<0,1%) que en una red eléctrica (8%). NaturalHy estudió el uso de los gasoductos de gas natural existentes para hidrógeno [154]
La portabilidad es uno de los mayores desafíos en la industria automotriz , donde los sistemas de almacenamiento de alta densidad son problemáticos debido a preocupaciones de seguridad. Los tanques de alta presión pesan mucho más que el hidrógeno que pueden contener. Por ejemplo, en el Toyota Mirai 2014 , un tanque lleno contiene solo un 5,7% de hidrógeno, siendo el resto del peso el tanque. [155]
Las densidades del sistema suelen ser alrededor de la mitad de las del material de trabajo, por lo tanto, mientras que un material puede almacenar 6 % en peso de H2 , un sistema de trabajo que utiliza ese material solo puede alcanzar el 3% en peso cuando se reduce el peso de los tanques, los equipos de control de temperatura y presión, etc. , se considera. [ cita necesaria ]
Debido a sus características de combustión limpia, el hidrógeno es una alternativa de combustible limpio para la industria automotriz. El combustible basado en hidrógeno podría reducir significativamente las emisiones de gases de efecto invernadero como CO 2 , SO 2 y NO x . Tres problemas para el uso de pilas de combustible de hidrógeno (HFC) son la eficiencia, el tamaño y el almacenamiento seguro del gas a bordo. Otras desventajas importantes de esta tecnología emergente implican problemas de costo, operatividad y durabilidad, que aún deben mejorarse con respecto a los sistemas existentes. Para abordar estos desafíos, se ha propuesto el uso de nanomateriales como una opción alternativa a los sistemas tradicionales de almacenamiento de hidrógeno. El uso de nanomateriales podría proporcionar un sistema de mayor densidad y aumentar la autonomía hacia el objetivo fijado por el DOE en 300 millas. Los materiales carbonosos como los nanotubos de carbono y los hidruros metálicos son el principal foco de investigación. Actualmente se están considerando para sistemas de almacenamiento a bordo por su versatilidad, multifuncionalidad, propiedades mecánicas y bajo coste respecto a otras alternativas. [156]
La introducción de nanomateriales en los sistemas de almacenamiento de hidrógeno a bordo puede suponer un importante punto de inflexión en la industria del automóvil. Sin embargo, el almacenamiento no es el único aspecto de la pila de combustible al que pueden contribuir los nanomateriales. Diferentes estudios han demostrado que las propiedades catalíticas y de transporte de las membranas de Nafion utilizadas en HFC se pueden mejorar con nanopartículas de TiO 2 / SnO 2 . [156] El mayor rendimiento se debe a una mejora en la cinética de división del hidrógeno debido a la actividad catalítica de las nanopartículas. Además, este sistema muestra un transporte más rápido de protones a través de la célula, lo que convierte a los HFC con membranas compuestas de nanopartículas en una alternativa prometedora.
Un grupo de investigación de la Universidad Metropolitana de Manchester (Reino Unido ) ha introducido otra aplicación de los nanomateriales en la división del agua utilizando electrodos serigrafiados que consisten en un material similar al grafeno . [157] Se han desarrollado sistemas similares utilizando técnicas fotoelectroquímicas .
El aumento de la presión del gas mejora la densidad de energía por volumen, lo que genera tanques contenedores más pequeños. El material estándar para contener hidrógeno presurizado en remolques tubulares es el acero (no hay problema de fragilización por hidrógeno con el gas hidrógeno). Los tanques fabricados con plástico reforzado con fibras de carbono y vidrio, como los que se instalan en los camiones Toyota Marai y Kenworth, deben cumplir con las normas de seguridad. Pocos materiales son adecuados para tanques, ya que el hidrógeno, al ser una molécula pequeña, tiende a difundirse a través de muchos materiales poliméricos. El almacenamiento de hidrógeno a bordo más común en los vehículos de 2020 fue hidrógeno a una presión de 700 bar = 70 MPa. El coste energético de comprimir el hidrógeno a esta presión es significativo. [ cita necesaria ]
Los gasoductos presurizados siempre están hechos de acero y funcionan a presiones mucho más bajas que los remolques tubulares.
Alternativamente, se puede usar hidrógeno líquido o hidrógeno granizado con mayor densidad de energía volumétrica. Sin embargo, el hidrógeno líquido es criogénico y hierve a 20,268 K (-252,882 °C o -423,188 °F). El almacenamiento criogénico reduce el peso pero requiere grandes energías de licuación . El proceso de licuefacción, que implica pasos de presurización y enfriamiento, consume mucha energía. [158] El hidrógeno licuado tiene una densidad de energía por volumen menor que la gasolina en aproximadamente un factor de cuatro, debido a la baja densidad del hidrógeno líquido; en realidad, hay más átomos de hidrógeno oxidables en un litro de gasolina (116 gramos) que en un litro de hidrógeno líquido puro (71 gramos). Como cualquier otro líquido a temperaturas criogénicas , los tanques de almacenamiento de hidrógeno líquido también deben estar bien aislados para minimizar la ebullición.
Japón tiene una instalación de almacenamiento de hidrógeno líquido (LH2) en una terminal en Kobe, y se esperaba que recibiera el primer envío de hidrógeno líquido a través del transportador LH2 en 2020. [159] El hidrógeno se licua reduciendo su temperatura a -253 °C, de manera similar. al gas natural licuado (GNL) que se almacena a -162 °C. Se puede lograr una pérdida potencial de eficiencia del 12,79 %, o 4,26 kWh/kg de 33,3 kWh/kg. [160]
El almacenamiento subterráneo de hidrógeno es la práctica de almacenamiento de hidrógeno en cavernas , domos de sal y campos de petróleo y gas agotados. ICI almacena desde hace muchos años grandes cantidades de hidrógeno gaseoso sin dificultades en cavernas. [161] El almacenamiento subterráneo de grandes cantidades de hidrógeno líquido puede funcionar como almacenamiento de energía de la red . La eficiencia de ida y vuelta es de aproximadamente el 40 % (frente al 75-80 % de la hidroeléctrica de bombeo (PHES) ) y el costo es ligeramente mayor que el de la hidroeléctrica de bombeo. [162]
Otro estudio al que hace referencia un documento de trabajo del personal europeo encontró que para el almacenamiento a gran escala, la opción más barata es el hidrógeno a 140 €/MWh por 2.000 horas de almacenamiento utilizando un electrolizador, almacenamiento en cavernas de sal y una central eléctrica de ciclo combinado. [163] El proyecto europeo Hyunder [164] indicó en 2013 que para el almacenamiento de energía eólica y solar se necesitan 85 cavernas adicionales, ya que no pueden ser cubiertas por los sistemas PHES y CAES . [165]
Un estudio de caso alemán sobre el almacenamiento de hidrógeno en cavernas de sal encontró que si el excedente de energía alemán (7% de la generación renovable variable total para 2025 y 20% para 2050) se convirtiera en hidrógeno y se almacenara bajo tierra, estas cantidades requerirían unas 15 cavernas. de 500.000 metros cúbicos cada una hasta 2025 y unas 60 cavernas hasta 2050, lo que corresponde aproximadamente a un tercio del número de cavernas de gas actualmente en funcionamiento en Alemania. [166] En Estados Unidos, Sandia Labs está llevando a cabo investigaciones sobre el almacenamiento de hidrógeno en yacimientos de petróleo y gas agotados, que podrían absorber fácilmente grandes cantidades de hidrógeno producido de forma renovable, ya que existen unos 2,7 millones de pozos agotados. [167]
El campo de investigación de materiales de almacenamiento de hidrógeno es vasto y cuenta con decenas de miles de artículos publicados. [168] Según artículos del período 2000 a 2015 recopilados de Web of Science y procesados en el software bibliométrico VantagePoint ® , se constituyó una revisión cienciométrica de la investigación en materiales de almacenamiento de hidrógeno. Según la literatura, la energía del hidrógeno pasó por un tipo de desarrollo de ciclo exagerado en la década de 2000. La investigación en materiales de almacenamiento de hidrógeno creció a un ritmo creciente entre 2000 y 2010. Posteriormente, el crecimiento continuó, pero a un ritmo decreciente, y se alcanzó una meseta en 2015. Si se analiza la producción de cada país, hay una división entre países que después de 2010 se inclinó hasta llegar a un nivel constante. o una producción ligeramente en descenso, como los países de la Unión Europea, EE.UU. y Japón, y aquellos cuya producción siguió creciendo hasta 2015, como China y Corea del Sur. Los países con más publicaciones fueron China, la UE y Estados Unidos, seguidos de Japón. China mantuvo la posición de liderazgo durante todo el período y tuvo una mayor proporción de publicaciones sobre materiales de almacenamiento de hidrógeno en su producción total de investigación. [169]
Entre las clases de materiales, las estructuras metalorgánicas fueron los materiales más investigados, seguidas de los hidruros simples. Se identificaron tres comportamientos típicos:
Sin embargo, las tecnologías actuales de fisisorción aún están lejos de comercializarse. Los estudios experimentales se ejecutan para muestras pequeñas de menos de 100 g. [170] Las tecnologías descritas requieren por regla general alta presión y/o bajas temperaturas. Por lo tanto, en el estado actual de la técnica, estas técnicas no se consideran una tecnología novedosa separada, sino un tipo de complemento valioso a los métodos actuales de compresión y licuefacción .
Los procesos de fisisorción son reversibles ya que no interviene energía de activación y la energía de interacción es muy baja. En materiales como estructuras organometálicas , carbonos porosos, zeolitas, clatratos y polímeros orgánicos, el hidrógeno se fisisorbe en la superficie de los poros. En estas clases de materiales, la capacidad de almacenamiento de hidrógeno depende principalmente de la superficie y el volumen de los poros. La principal limitación del uso de estos sorbentes como materiales de almacenamiento de H2 es la débil energía de interacción de Van der Waals entre el hidrógeno y la superficie de los sorbentes. Por lo tanto, muchos de los materiales basados en fisisorción tienen altas capacidades de almacenamiento a temperatura y presión de nitrógeno líquido, pero sus capacidades se vuelven muy bajas a temperatura y presión ambiente. [ cita necesaria ]
LOHC , sistemas de almacenamiento de hidrógeno orgánico líquido, es una técnica prometedora para el futuro almacenamiento de hidrógeno. Los LOHC son compuestos orgánicos que pueden absorber y liberar hidrógeno mediante reacciones químicas . Estos compuestos se caracterizan por el hecho de que pueden cargarse y descargarse con cantidades considerables de hidrógeno en un proceso cíclico. En principio, todo compuesto insaturado (moléculas orgánicas con enlaces dobles o triples CC ) puede absorber hidrógeno durante la hidrogenación . Esta técnica garantiza que se evite por completo la liberación de compuestos a la atmósfera durante el almacenamiento de hidrógeno. Por lo tanto, los LOHC son una forma atractiva de proporcionar energía eólica y solar para aplicaciones de movilidad en forma de energía líquida que transporta moléculas con densidades de almacenamiento de energía y manejabilidad similares a las de los combustibles fósiles actuales. [171] [ fuente obsoleta ]
Sin embargo, la situación es mucho peor, porque antes de que el hidrógeno pueda transportarse a cualquier lugar, es necesario comprimirlo o licuarlo. Para licuarlo hay que refrigerarlo a una temperatura de -253 °C (20 grados sobre el cero absoluto). A estas temperaturas, las leyes fundamentales de la termodinámica hacen que los refrigeradores sean extremadamente ineficientes. Como resultado, alrededor del 40 por ciento de la energía del hidrógeno debe gastarse para licuarlo. Esto reduce el contenido energético neto real de nuestro combustible producto a 792 kcal. Además, debido a que es un líquido criogénico, se podría esperar que se pierda aún más energía a medida que el hidrógeno se evapora al calentarse por el calor que se filtra desde el ambiente exterior durante el transporte y el almacenamiento.