Nafion es una marca de un fluoropolímero - copolímero a base de tetrafluoroetileno sulfonado descubierto a finales de los años 1960 por el Dr. Walther Grot de DuPont . [1] Nafion es una marca de la empresa Chemours . Es el primero de una clase de polímeros sintéticos con propiedades iónicas que se denominan ionómeros . Las propiedades iónicas únicas de Nafion son el resultado de la incorporación de grupos de éter perfluorovinílico terminados con grupos sulfonato en una estructura principal de tetrafluoroetileno ( PTFE ). [2] [3] [4] Nafion ha recibido una atención considerable como conductor de protones para celdas de combustible de membrana de intercambio de protones (PEM) debido a su excelente estabilidad química y mecánica en las duras condiciones de esta aplicación.
La base química de las propiedades conductoras de iones de Nafion sigue siendo objeto de extensas investigaciones. [2] La conductividad iónica de Nafion aumenta con el nivel de hidratación. La exposición de Nafion a un ambiente humidificado o agua líquida aumenta la cantidad de moléculas de agua asociadas con cada grupo de ácido sulfónico. La naturaleza hidrófila de los grupos iónicos atrae a las moléculas de agua, que comienzan a solvatar los grupos iónicos y a disociar los protones del grupo -SO 3 H ( ácido sulfónico ). Los protones disociados "saltan" de un sitio ácido a otro mediante mecanismos facilitados por las moléculas de agua y los enlaces de hidrógeno . [2] Tras la hidratación, la fase de Nafion se separa a escalas de longitud nanométrica, lo que da como resultado la formación de una red interconectada de dominios hidrófilos que permiten el movimiento de agua y cationes , pero las membranas no conducen electrones y conducen mínimamente aniones debido a la permselectividad (basada en carga). exclusión). Nafion se puede fabricar o intercambiar con formas catiónicas alternativas para diferentes aplicaciones (por ejemplo, litiado para baterías de iones de litio) y en diferentes pesos equivalentes (EW), considerados alternativamente como capacidades de intercambio iónico (IEC), para lograr una variedad de conductividades catiónicas. con compensaciones a otras propiedades fisicoquímicas como la absorción de agua y la hinchazón.
Nafion se puede producir como resina en polvo y como copolímero . Tiene varias configuraciones químicas y, por tanto, varios nombres químicos en el sistema IUPAC . Nafion-H, por ejemplo, incluye los siguientes nombres sistemáticos:
El peso molecular de Nafion es variable debido a las diferencias en el procesamiento y la morfología de la solución. [3] [4] La estructura de una unidad Nafion ilustra la variabilidad del material; por ejemplo, el monómero más básico contiene variación de cadena entre los grupos éter (el subíndice z). Los métodos convencionales para determinar el peso molecular, como la cromatografía de dispersión de luz y de permeación en gel , no son aplicables porque Nafion es insoluble, aunque el peso molecular se ha estimado en 10 5 –10 6 Da. [3] [4] En cambio, el peso equivalente (EW) y el espesor del material se utilizan para describir la mayoría de las membranas disponibles comercialmente. El EW es el número de gramos de Nafion seco por mol de grupos de ácido sulfónico cuando el material está en forma ácida. [4] Las membranas de Nafion se clasifican comúnmente en términos de su EW y espesor. [2] [5] Por ejemplo, Nafion 117 indica una membrana moldeada por extrusión con 1100 g/mol EW y 0,007 pulgadas (7 mil) de espesor. [5] A diferencia del peso equivalente, las resinas de intercambio iónico convencionales generalmente se describen en términos de su capacidad de intercambio iónico (IEC), que es el inverso multiplicativo o recíproco del peso equivalente, es decir, IEC = 1000/EW.
Los derivados de nafion se sintetizan primero mediante la copolimerización de tetrafluoroetileno (TFE) (el monómero del teflón) y un derivado de un perfluoro (alquil vinil éter) con fluoruro de ácido sulfonílico. Este último reactivo se puede preparar mediante pirólisis de su respectivo óxido o ácido carboxílico para dar la estructura olefinada. [6]
El producto resultante es un termoplástico que contiene -SO 2 F que se extruye en películas. El NaOH acuoso caliente convierte estos grupos de fluoruro de sulfonilo (-SO 2 F) en grupos sulfonato (-SO 3 − Na + ). Esta forma de Nafion, denominada forma neutra o sal, finalmente se convierte en la forma ácida que contiene los grupos ácido sulfónico (-SO 3 H). Nafion se puede dispersar en solución calentándolo en alcohol acuoso a 250 °C en un autoclave para su posterior moldeado en películas delgadas o uso como aglutinante polimérico en electrodos. Mediante este proceso, Nafion se puede utilizar para generar películas compuestas, recubrir electrodos o reparar membranas dañadas. [3]
La combinación de la estructura estable de PTFE con los grupos sulfónicos ácidos le da a Nafion sus características: [2] [7]
La morfología de las membranas de Nafion es una cuestión de estudio continuo para permitir un mayor control de sus propiedades. Otras propiedades como la gestión del agua, la estabilidad de la hidratación a altas temperaturas, la resistencia electroosmótica , así como la estabilidad mecánica, térmica y oxidativa, se ven afectadas por la estructura de Nafion. Se han propuesto varios modelos para la morfología de Nafion para explicar sus propiedades de transporte únicas. [2]

El primer modelo para Nafion, llamado modelo de canal de racimo o de red de racimo , consistía en una distribución equitativa de racimos de iones sulfonato (también descritos como " micelas invertidas " [4] ) con un diámetro de 40 Å (4 nm ) mantenidos dentro de un Red continua de fluorocarbono. Canales estrechos de aproximadamente 10 Å (1 nm) de diámetro interconectan los grupos, lo que explica las propiedades de transporte. [3] [4] [12]
La dificultad para determinar la estructura exacta de Nafion se debe a la inconsistencia de la solubilidad y la estructura cristalina entre sus diversos derivados. Los modelos morfológicos avanzados han incluido un modelo de núcleo-capa donde el núcleo rico en iones está rodeado por una capa pobre en iones, un modelo de varilla donde los grupos sulfónicos se organizan en varillas similares a cristales y un modelo sándwich donde el polímero forma dos capas cuyas capas sulfónicas Los grupos se atraen a través de una capa acuosa donde ocurre el transporte. [4] La coherencia entre los modelos incluye una red de grupos iónicos; Los modelos difieren en la geometría y distribución del grupo. Aunque todavía no se ha determinado que ningún modelo sea completamente correcto, algunos científicos han demostrado que a medida que la membrana se hidrata, la morfología de Nafion se transforma del modelo de canal de racimo a un modelo en forma de varilla. [4]
También se propuso un modelo de canal de agua cilíndrico [13] basado en simulaciones de datos de dispersión de rayos X de ángulo pequeño y estudios de resonancia magnética nuclear de estado sólido. En este modelo, los grupos funcionales del ácido sulfónico se autoorganizan en conjuntos de canales de agua hidrófilos, cada uno de ~ 2,5 nm de diámetro, a través de los cuales se pueden transportar fácilmente pequeños iones. Intercalados entre los canales hidrofílicos hay cadenas principales de polímeros hidrofóbicos que proporcionan la estabilidad mecánica observada. Sin embargo, muchos estudios recientes favorecieron una nanoestructura separada en fases que consiste en dominios hidrófilos localmente planos o en forma de cinta basados en evidencia de estudios de imágenes directas [14] y análisis más completos de la estructura y las propiedades de transporte. [2] [15]
Las propiedades de Nafion lo hacen adecuado para una amplia gama de aplicaciones. Nafion ha encontrado uso en pilas de combustible , dispositivos electroquímicos, producción de cloro-álcali, recuperación de iones metálicos, electrólisis de agua , enchapado , tratamiento de superficies de metales, baterías, sensores , celdas de diálisis de Donnan, liberación de fármacos, secado o humidificación de gases y catálisis de superácidos . para la producción de productos químicos finos. [3] [4] [7] [16] Nafion también se cita a menudo por su potencial teórico (es decir, hasta ahora no probado) en varios campos. Teniendo en cuenta la amplia funcionalidad de Nafion, a continuación sólo se analizarán las más importantes.
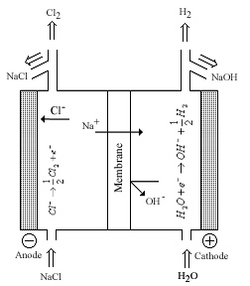
El cloro y el hidróxido de sodio/potasio se encuentran entre los productos químicos básicos más producidos en el mundo. Los métodos de producción modernos producen Cl 2 y NaOH/KOH a partir de la electrólisis de salmuera utilizando una membrana de Nafion entre medias celdas. Antes del uso de Nafion, las industrias utilizaban amalgama de sodio que contenía mercurio para separar el sodio metálico de las celdas o diafragmas de asbesto para permitir la transferencia de iones de sodio entre medias celdas; Ambas tecnologías se desarrollaron en la segunda mitad del siglo XIX. Las desventajas de estos sistemas son la seguridad de los trabajadores y las preocupaciones ambientales asociadas con el mercurio y el asbesto, los factores económicos también influyen y, en el proceso del diafragma, la contaminación por cloruro del producto de hidróxido. Nafion fue el resultado directo de que la industria cloro-álcalina abordara estas preocupaciones; Nafion podría tolerar las altas temperaturas, las altas corrientes eléctricas y el ambiente corrosivo de las celdas electrolíticas. [3] [4] [7]
La figura de la derecha muestra una célula cloro-álcalina donde Nafion funciona como una membrana entre medias células. La membrana permite que los iones de sodio se transfieran de una celda a otra con una resistencia eléctrica mínima. La membrana también se reforzó con membranas adicionales para evitar la mezcla de productos gaseosos y minimizar la transferencia inversa de iones Cl - y - OH. [3]
Aunque las pilas de combustible se han utilizado desde la década de 1960 como fuente de energía para satélites, recientemente han recibido una atención renovada por su potencial para producir eficientemente energía limpia a partir de hidrógeno. Nafion resultó eficaz como membrana para pilas de combustible de membrana de intercambio de protones (PEM) al permitir el transporte de iones de hidrógeno y al mismo tiempo prevenir la conducción de electrones. Los electrolitos de polímero sólido, que se fabrican conectando o depositando electrodos (generalmente de metales nobles) en ambos lados de la membrana, conducen los electrones a través de un proceso que requiere energía y vuelven a unir los iones de hidrógeno para reaccionar con el oxígeno y producir agua. [3] Se espera que las pilas de combustible encuentren un uso importante en la industria del transporte.
Nafion, como superácido , tiene potencial como catalizador de síntesis orgánica . Los estudios han demostrado propiedades catalíticas en alquilación , isomerización , oligomerización , acilación , cetalización , esterificación , hidrólisis de azúcares y éteres y oxidación . Constantemente se descubren nuevas aplicaciones. [16] Estos procesos, sin embargo, aún no han encontrado un uso comercial importante. A continuación se muestran varios ejemplos:
Nafion-H proporciona una conversión eficiente, mientras que el método alternativo, que emplea la síntesis de Friedel-Crafts , puede promover la polialquilación: [17]
La cantidad de Nafion-H necesaria para catalizar la acilación del benceno con cloruro de aroilo es entre un 10 y un 30% menor que la del catalizador de Friedel-Crafts: [17]
Nafion-H aumenta las velocidades de reacción de protección mediante dihidropirano u o-trialquilsilación de alcoholes, fenol y ácidos carboxílicos. [dieciséis]
Nafion puede catalizar un cambio de 1,2-hidruro . [dieciséis]
Es posible inmovilizar enzimas dentro del Nafion agrandando los poros con sales lipófilas . Nafion mantiene una estructura y un pH para proporcionar un entorno estable para las enzimas. Las aplicaciones incluyen la oxidación catalítica de adenina dinucleótidos. [dieciséis]
Nafion ha encontrado uso en la producción de sensores , con aplicación en biosensores ópticos, metalizados, selectivos de iones y biosensores . Lo que hace que Nafion sea especialmente interesante es su demostración de biocompatibilidad . Se ha demostrado que Nafion es estable en cultivos celulares y en el cuerpo humano, y se están realizando considerables investigaciones para la producción de sensores de glucosa de mayor sensibilidad . [3]
Las superficies de Nafion presentan una zona de exclusión frente a la colonización bacteriana. [18] Además, los recubrimientos capa por capa que comprenden Nafion muestran excelentes propiedades antimicrobianas. [19]
La nave espacial SpaceX Dragon 2 con clasificación humana utiliza membranas Nafion para deshumidificar el aire de la cabina. Un lado de la membrana está expuesto a la atmósfera de la cabina y el otro al vacío del espacio. Esto da como resultado la deshumidificación ya que Nafion es permeable a las moléculas de agua pero no al aire. Esto ahorra energía y complejidad ya que no se requiere enfriamiento (como se necesita con un deshumidificador de condensación) y el agua extraída se rechaza al espacio sin necesidad de ningún mecanismo adicional. [20]
El Nafion normal se deshidratará (por lo tanto perderá conductividad de protones) cuando la temperatura sea superior a ~80 °C. Esta limitación preocupa el diseño de las pilas de combustible porque son deseables temperaturas más altas para una mejor eficiencia y tolerancia al CO del catalizador de platino. El fosfato de sílice y circonio se puede incorporar a los canales de agua de Nafion mediante reacciones químicas in situ para aumentar la temperatura de trabajo por encima de 100 °C.
{{cite journal}}: Citar diario requiere |journal=( ayuda ){{cite journal}}: Mantenimiento de CS1: bot: estado de la URL original desconocido ( enlace ) Mantenimiento de CS1: varios nombres: lista de autores ( enlace )