La enfermedad de Wilson es un trastorno genético en el que se acumula un exceso de cobre en el cuerpo. Los síntomas suelen estar relacionados con el cerebro y el hígado . Los síntomas relacionados con el hígado incluyen vómitos , debilidad, acumulación de líquido en el abdomen , hinchazón de las piernas , piel amarillenta y picazón . Los síntomas relacionados con el cerebro incluyen temblores , rigidez muscular, dificultad para hablar, cambios de personalidad, ansiedad y psicosis . [1]
La enfermedad de Wilson es causada por una mutación en el gen de la proteína de la enfermedad de Wilson ( ATP7B ) . Esta proteína transporta el exceso de cobre a la bilis , donde se excreta en los productos de desecho. La condición es autosómica recesiva ; Para que las personas se vean afectadas, deben heredar una copia mutada del gen de ambos padres. El diagnóstico puede ser difícil y, a menudo, implica una combinación de análisis de sangre, análisis de orina y una biopsia de hígado . Se pueden utilizar pruebas genéticas para evaluar a los familiares de los afectados. [1]
La enfermedad de Wilson generalmente se trata con cambios en la dieta y medicamentos. Los cambios en la dieta implican llevar una dieta baja en cobre y no utilizar utensilios de cocina de cobre. Los medicamentos utilizados incluyen agentes quelantes , como trientina y D -penicilamina , y suplementos de zinc . Las complicaciones de la enfermedad de Wilson pueden incluir insuficiencia hepática y problemas renales . Un trasplante de hígado puede ser útil para quienes otros tratamientos no son eficaces o si se produce insuficiencia hepática. [1]
La enfermedad de Wilson ocurre en aproximadamente una de cada 30.000 personas. [1] Los síntomas generalmente comienzan entre las edades de 5 y 35 años. [1] Fue descrito por primera vez en 1854 por el patólogo alemán Friedrich Theodor von Frerichs y lleva el nombre del neurólogo británico Samuel Wilson . [4]
Los principales sitios de acumulación de cobre son el hígado y el cerebro , y en consecuencia la enfermedad hepática y los síntomas neuropsiquiátricos son las principales características que conducen al diagnóstico. [5] Las personas con problemas hepáticos tienden a buscar atención médica antes, generalmente cuando son niños o adolescentes, que aquellas con síntomas neurológicos y psiquiátricos, que tienden a tener 20 años o más. Algunos se identifican sólo porque a sus familiares se les ha diagnosticado la enfermedad de Wilson; muchos de ellos, cuando se les hace la prueba, resultan haber experimentado síntomas de la afección, pero no han recibido un diagnóstico. [6]
La enfermedad hepática puede presentarse como cansancio , ictericia , [7] aumento de la tendencia al sangrado o confusión (debido a encefalopatía hepática ) e hipertensión portal . La última, una afección en la que la presión en la vena porta aumenta notablemente, provoca várices esofágicas , vasos sanguíneos en el esófago que pueden sangrar de forma potencialmente mortal, así como agrandamiento del bazo ( esplenomegalia ) y acumulación de líquido en la cavidad abdominal ( ascitis ). En el examen, se pueden observar signos de enfermedad hepática crónica, como angiomas en araña (pequeños vasos sanguíneos distendidos, generalmente en el pecho). La hepatitis crónica activa ha causado cirrosis hepática en la mayoría de los casos cuando desarrollan síntomas. Si bien la mayoría de las personas con cirrosis tienen un mayor riesgo de carcinoma hepatocelular (cáncer de hígado), este riesgo es relativamente muy bajo en la enfermedad de Wilson. [5]
Alrededor del 5% de todas las personas son diagnosticadas sólo cuando desarrollan insuficiencia hepática aguda fulminante , a menudo en el contexto de una anemia hemolítica (anemia debida a la destrucción de los glóbulos rojos). Esto conduce a anomalías en la producción de proteínas (identificadas por una coagulación alterada ) y en el metabolismo en el hígado. El metabolismo alterado de las proteínas conduce a la acumulación de productos de desecho como el amoníaco en el torrente sanguíneo. Cuando estos irritan el cerebro, la persona desarrolla encefalopatía hepática (confusión, coma, convulsiones y, finalmente, inflamación del cerebro que pone en peligro la vida ). [5]

Aproximadamente la mitad de las personas con enfermedad de Wilson tienen síntomas neurológicos o psiquiátricos. La mayoría presenta inicialmente un leve deterioro cognitivo y torpeza, así como cambios de comportamiento. A continuación suelen aparecer síntomas neurológicos específicos, a menudo en forma de parkinsonismo (rigidez en rueda dentada, bradicinesia o movimientos lentos y falta de equilibrio son las características parkinsonianas más comunes [8] ), con o sin un temblor típico en las manos , expresiones faciales enmascaradas, dificultad para hablar. habla, ataxia (falta de coordinación) o distonía (torsiones y movimientos repetitivos de una parte del cuerpo). Las convulsiones y la migraña parecen ser más comunes en la enfermedad de Wilson. [5] Muchas personas con enfermedad de Wilson presentan un temblor característico descrito como "temblor de aleteo"; esto no existe en reposo, pero puede provocarse abduciendo los brazos y flexionando los codos hacia la línea media. [9]
La cognición también puede verse afectada en la enfermedad de Wilson, en dos categorías, no mutuamente excluyentes: trastorno del lóbulo frontal (puede presentarse como impulsividad , deterioro del juicio, promiscuidad , apatía y disfunción ejecutiva con mala planificación y toma de decisiones) y demencia subcortical (puede presentarse como pensamiento lento, pérdida de memoria y disfunción ejecutiva , sin signos de afasia , apraxia o agnosia ). Se cree que estas implicaciones cognitivas están relacionadas y estrechamente vinculadas con las manifestaciones psiquiátricas de la enfermedad. [8]
Los problemas psiquiátricos debidos a la enfermedad de Wilson pueden incluir cambios de comportamiento, depresión , trastornos de ansiedad y psicosis . [5] Los síntomas psiquiátricos se observan comúnmente junto con síntomas neurológicos y rara vez se manifiestan por sí solos. Estos síntomas suelen estar mal definidos y, en ocasiones, pueden atribuirse a otras causas. Debido a esto, el diagnóstico de la enfermedad de Wilson rara vez se realiza cuando sólo hay síntomas psiquiátricos presentes. [8]
Las condiciones médicas se han relacionado con la acumulación de cobre en la enfermedad de Wilson:

El gen de la enfermedad de Wilson ( ATP7B ) está en el cromosoma 13 (13q14.3) y se expresa principalmente en el hígado, el riñón y la placenta . El gen codifica una ATPasa de tipo P (enzima transportadora de cationes) que transporta cobre a la bilis y lo incorpora a la ceruloplasmina . [5] Las mutaciones se pueden detectar en el 90% de los casos. La mayoría (60%) son homocigotos para mutaciones ATP7B (dos copias anormales) y el 30% tiene solo una copia anormal. Alrededor del 10% no tiene ninguna mutación detectable. [6]
Aunque se han descrito 300 mutaciones de ATP7B , en la mayoría de las poblaciones los casos de enfermedad de Wilson se deben a un pequeño número de mutaciones específicas de esa población. Por ejemplo, en las poblaciones occidentales, la mutación H1069Q (sustitución de una histidina por una glutamina en la posición 1069 de la proteína) está presente en el 37-63% de los casos, mientras que en China esta mutación es muy poco común y R778L ( arginina a leucina en 778) se encuentra con más frecuencia. Se sabe relativamente poco sobre el impacto relativo de varias mutaciones, aunque la mutación H1069Q parece predecir problemas de aparición más tardía y predominantemente neurológicos, según algunos estudios. [5] [15] WilsonGen, un recurso integral con anotaciones clínicas, proporciona una clasificación clínica para las variantes según las pautas recientes de ACMG y AMP [16]
Una variación normal en el gen PRNP puede modificar el curso de la enfermedad retrasando la edad de aparición y afectando el tipo de síntomas que se desarrollan. Este gen produce proteína priónica , que está activa en el cerebro y otros tejidos y también parece estar implicada en el transporte de cobre. [17] Inicialmente se sospechó un papel del gen ApoE , pero no se pudo confirmar. [15]
La enfermedad se hereda con un patrón autosómico recesivo. Para heredarlo, ambos padres de un individuo deben portar un gen afectado. La mayoría no tiene antecedentes familiares de la afección. [15] Las personas con un solo gen anormal se denominan portadores (heterocigotos) y pueden tener anomalías leves, pero médicamente insignificantes, del metabolismo del cobre. [14]
La enfermedad de Wilson es la más común de un grupo de enfermedades hereditarias que causan una sobrecarga de cobre en el hígado. Todos pueden causar cirrosis a una edad temprana. Los otros miembros del grupo son la cirrosis infantil india (ICC), la cirrosis infantil endémica del Tirol y la toxicosis idiopática por cobre. Éstas no están relacionadas con mutaciones de ATP7B ; por ejemplo, ICC se ha relacionado con mutaciones en los genes KRT8 y KRT18 . [15]

El cuerpo necesita el cobre para una serie de funciones , predominantemente como cofactor de varias enzimas como la ceruloplasmina, la citocromo c oxidasa , la dopamina β-hidroxilasa , la superóxido dismutasa y la tirosinasa . [15]
El cobre ingresa al cuerpo a través del tracto digestivo . Una proteína transportadora en las células del intestino delgado , el transportador de membrana de cobre 1 (Ctr1; SLC31A1), transporta cobre dentro de las células, donde una parte se une a la metalotioneína y una parte es transportada por ATOX1 a un orgánulo conocido como red trans-Golgi . Aquí, en respuesta al aumento de las concentraciones de cobre, una enzima llamada ATP7A (proteína de Menkes) libera cobre en la vena porta del hígado. Las células del hígado también transportan la proteína CMT1, y la metalotioneína y ATOX1 la unen dentro de la célula, pero aquí, ATP7B une el cobre a la ceruloplasmina y lo libera en el torrente sanguíneo, además de eliminar el exceso de cobre secretándolo en la bilis. Ambas funciones de ATP7B están alteradas en la enfermedad de Wilson. El cobre se acumula en el tejido hepático; La ceruloplasmina todavía se secreta, pero en una forma que carece de cobre (denominada apoceruloplasmina) y se degrada rápidamente en el torrente sanguíneo. [15]
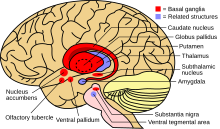
Cuando la cantidad de cobre en el hígado supera a las proteínas que normalmente lo unen, se produce daño oxidativo mediante un proceso conocido como química de Fenton ; este daño eventualmente conduce a hepatitis crónica activa , fibrosis (depósito de tejido conectivo) y cirrosis . El hígado también libera cobre en el torrente sanguíneo que no está unido a la ceruloplasmina. Este cobre libre precipita en todo el cuerpo, pero particularmente en los riñones, los ojos y el cerebro. En el cerebro, la mayor parte del cobre se deposita en los ganglios basales , particularmente en el putamen y el globo pálido (llamados en conjunto núcleo lenticular ); Estas áreas normalmente participan en la coordinación del movimiento y desempeñan un papel importante en procesos neurocognitivos como el procesamiento de estímulos y la regulación del estado de ánimo. El daño a estas áreas, nuevamente por la química de Fenton, produce los síntomas neuropsiquiátricos que se observan en la enfermedad de Wilson. [15]
No está claro por qué la enfermedad de Wilson causa hemólisis, pero varias líneas de evidencia sugieren que un alto nivel de cobre libre (no unido a ceruloplasmina) tiene un efecto directo sobre la oxidación de la hemoglobina , la inhibición de las enzimas que suministran energía en los glóbulos rojos o la daño a las membranas celulares . [18]
Se puede sospechar la enfermedad de Wilson sobre la base de cualquiera de los síntomas mencionados anteriormente, o cuando se ha descubierto que un pariente cercano tiene la enfermedad de Wilson. La mayoría tiene pruebas de función hepática levemente anormales , como niveles elevados de aspartato transaminasa , alanina transaminasa y bilirrubina . Si el daño hepático es significativo, la albúmina puede disminuir debido a la incapacidad de las células hepáticas dañadas para producir esta proteína; Asimismo, el tiempo de protrombina (una prueba de coagulación ) puede prolongarse ya que el hígado es incapaz de producir proteínas conocidas como factores de coagulación. [5] Los niveles de fosfatasa alcalina son relativamente bajos en aquellos con insuficiencia hepática aguda relacionada con la enfermedad de Wilson. [19] Si se observan síntomas neurológicos, generalmente se realiza una resonancia magnética del cerebro; esto muestra hiperintensidades en la parte del cerebro llamada ganglios basales en la configuración T2 . [14] La resonancia magnética también puede demostrar el patrón característico de "cara del panda gigante" . [20]
No se conoce ninguna prueba totalmente fiable para la enfermedad de Wilson, pero los niveles de ceruloplasmina y cobre en la sangre, así como la cantidad de cobre excretada en la orina durante un período de 24 horas, se utilizan en conjunto para formarse una impresión de la cantidad de cobre en la sangre. el cuerpo. El estándar de oro , o la prueba más ideal, es una biopsia de hígado . [5]

Las concentraciones de ceruloplasmina son anormalmente bajas (<0,2 g/L) en 80 a 95% de los casos. [5] Sin embargo, puede estar presente en niveles normales en personas con inflamación continua , ya que es una proteína de fase aguda . Los niveles bajos de ceruloplasmina también se encuentran en la enfermedad de Menkes y la aceruloplasminemia , que están relacionadas con la enfermedad de Wilson, pero son mucho más raras. [5] [14] La combinación de síntomas neurológicos, signos oculares y un nivel bajo de ceruloplasmina se considera suficiente para el diagnóstico de la enfermedad de Wilson. Sin embargo, en muchos casos se necesitan más pruebas. [14]
El cobre sérico es bajo, lo que puede parecer paradójico dado que la enfermedad de Wilson es una enfermedad por exceso de cobre. Sin embargo, el 95% del cobre plasmático es transportado por la ceruloplasmina, que suele ser baja en la enfermedad de Wilson. El cobre en la orina está elevado en la enfermedad de Wilson y se recolecta durante 24 horas en un frasco con un revestimiento sin cobre. Los niveles superiores a 100 μg/24 h (1,6 μmol/24 h) confirman la enfermedad de Wilson, y los niveles superiores a 40 μg/24 h (0,6 μmol/24 h) son fuertemente indicativos. [5] Los niveles altos de cobre en la orina no son exclusivos de la enfermedad de Wilson; a veces se observan en la hepatitis autoinmune y en la colestasis (cualquier enfermedad que obstruya el flujo de bilis desde el hígado al intestino delgado). [14]
En niños, se puede utilizar la prueba de penicilamina . Se administra una dosis oral de 500 mg de penicilamina y se recolecta orina durante 24 horas. Si contiene más de 1600 μg (25 μmol), es un indicador fiable de la enfermedad de Wilson. [ se necesita aclaración ] Esta prueba no ha sido validada en adultos. [14]
Los ojos del paciente se examinan utilizando una lámpara de hendidura para buscar anillos de Kayser-Fleischer , que están fuertemente asociados con la enfermedad de Wilson y son causados por la deposición de cobre en la córnea interna en la membrana de Descemet . [10]
Una vez que otras investigaciones han indicado la enfermedad de Wilson, la prueba ideal es la extirpación de una pequeña cantidad de tejido hepático mediante una biopsia hepática. Esto se evalúa microscópicamente para determinar el grado de esteatosis y cirrosis, y la histoquímica y la cuantificación del cobre se utilizan para medir la gravedad de la acumulación de cobre. Un nivel de 250 μg de cobre por gramo de tejido hepático seco confirma la enfermedad de Wilson. Ocasionalmente se encuentran niveles más bajos de cobre; en ese caso, la combinación de los hallazgos de la biopsia con todas las demás pruebas aún podría conducir a un diagnóstico formal de enfermedad de Wilson. [5]
En las primeras etapas de la enfermedad, la biopsia generalmente muestra esteatosis (deposición de material graso), aumento de glucógeno en el núcleo y áreas de necrosis (muerte celular). En la enfermedad más avanzada, los cambios observados son bastante similares a los observados en la hepatitis autoinmune, como infiltración por células inflamatorias , necrosis gradual y fibrosis (tejido cicatricial). Finalmente, en la enfermedad avanzada, la cirrosis es el hallazgo principal. En la insuficiencia hepática aguda, se observa degeneración de las células hepáticas y colapso de la arquitectura del tejido hepático, típicamente sobre un fondo de cambios cirróticos. Los métodos histoquímicos para detectar cobre son inconsistentes y poco confiables, y por sí solos se consideran insuficientes para establecer un diagnóstico. [14]
Se pueden realizar análisis de mutaciones del gen ATP7B , así como de otros genes relacionados con la acumulación de cobre en el hígado. Una vez que se confirma una mutación, los miembros de la familia pueden ser examinados para detectar la enfermedad como parte del asesoramiento familiar sobre genética clínica . [5] Es importante seguir las distribuciones regionales de genes asociados con la enfermedad de Wilson, ya que esto puede ayudar a los médicos a diseñar estrategias de detección adecuadas. Dado que las mutaciones del gen ATP7B varían entre poblaciones, las investigaciones y pruebas genéticas realizadas en países como Estados Unidos o el Reino Unido pueden plantear problemas, ya que tienden a tener poblaciones más mixtas. [21]
En general, se recomienda una dieta baja en alimentos que contengan cobre evitando las setas , las nueces , el chocolate , los frutos secos , el hígado, las semillas y el aceite de sésamo, y los mariscos . [5]
Hay tratamientos médicos disponibles para la enfermedad de Wilson. Algunos aumentan la eliminación de cobre del cuerpo, mientras que otros impiden la absorción de cobre de la dieta.
Generalmente, la penicilamina es el primer tratamiento utilizado. Esto une el cobre ( quelación ) y conduce a la excreción de cobre en la orina. Por lo tanto, se puede controlar la cantidad de cobre en la orina para garantizar que se tome una dosis suficientemente alta. La penicilamina no está exenta de problemas; alrededor del 20% experimenta un efecto secundario o una complicación del tratamiento con penicilamina, como lupus inducido por fármacos (que causa dolores en las articulaciones y erupción cutánea) o miastenia (una afección nerviosa que provoca debilidad muscular). En quienes presentaron síntomas neurológicos, casi la mitad experimenta un empeoramiento paradójico de sus síntomas. Si bien este fenómeno se observa en otros tratamientos para el síndrome de Wilson, generalmente se toma como una indicación para suspender la penicilamina y comenzar un tratamiento de segunda línea. [5] [14] Aquellos intolerantes a la penicilamina pueden comenzar con clorhidrato de trientina , que también tiene propiedades quelantes. Algunos recomiendan la trientina como tratamiento de primera línea, pero la experiencia con la penicilamina es más amplia. [14] Otro agente, bajo investigación clínica por Wilson Therapeutics , con actividad conocida en la enfermedad de Wilson es el tetratiomolibdato . Esto se considera experimental, [14] aunque algunos estudios han demostrado un efecto beneficioso. [5]
Una vez que todos los resultados hayan vuelto a la normalidad, se puede usar zinc (generalmente en forma de acetato de zinc recetado llamado Galzin) en lugar de quelantes para mantener niveles estables de cobre en el cuerpo. El zinc estimula la metalotioneína , una proteína de las células intestinales que se une al cobre e impide su absorción y transporte al hígado. El tratamiento con zinc se continúa a menos que los síntomas reaparezcan o si aumenta la excreción urinaria de cobre. [14]
En casos raros en los que ninguno de los tratamientos orales es eficaz, especialmente en enfermedades neurológicas graves, ocasionalmente es necesario dimercaprol (antilewisita británico). Este tratamiento se inyecta por vía intramuscular (en un músculo) cada pocas semanas y tiene efectos secundarios desagradables como dolor. [22]
Las personas asintomáticas (por ejemplo, las diagnosticadas mediante exámenes familiares o sólo como resultado de resultados anormales en las pruebas) generalmente reciben tratamiento, ya que la acumulación de cobre puede causar daños a largo plazo en el futuro. No está claro si estas personas reciben mejor tratamiento con penicilamina o acetato de zinc. [14]
La fisioterapia y la terapia ocupacional son beneficiosas para los pacientes con la forma neurológica de la enfermedad. El tratamiento quelante de cobre puede tardar hasta seis meses en comenzar a funcionar, y estas terapias pueden ayudar a afrontar la ataxia , la distonía y los temblores, así como a prevenir el desarrollo de contracturas que pueden resultar de la distonía. [23]
El trasplante de hígado es una cura eficaz para la enfermedad de Wilson, pero se utiliza sólo en situaciones particulares debido a los riesgos y complicaciones asociados con el procedimiento. Se utiliza principalmente en personas con insuficiencia hepática fulminante que no responden al tratamiento médico o en personas con enfermedad hepática crónica avanzada. El trasplante de hígado se evita en enfermedades neuropsiquiátricas graves, en las que no se ha demostrado su beneficio. [5] [14]
Si no se trata, la enfermedad de Wilson tiende a empeorar progresivamente y, finalmente, es mortal. Las complicaciones graves incluyen cirrosis hepática, insuficiencia renal aguda y psicosis. Pueden ocurrir cáncer de hígado y colangiocarcinoma , pero con una incidencia menor que otras enfermedades hepáticas crónicas, y el riesgo se reduce en gran medida con tratamiento. [13] Con una detección y tratamiento tempranos, la mayoría de los afectados pueden vivir una vida relativamente normal y tener una esperanza de vida cercana a la de la población general. [13] El daño hepático y neurológico que ocurre antes del tratamiento puede mejorar, pero a menudo es permanente. [24] La fertilidad suele ser normal y las complicaciones del embarazo no aumentan en aquellas personas con enfermedad de Wilson tratada. [13]
La enfermedad lleva el nombre del médico británico Samuel Alexander Kinnier Wilson (1878-1937), un neurólogo que describió la afección, incluidos los cambios patológicos en el cerebro y el hígado, en 1912. [25] El trabajo de Wilson había sido precedido por, y se dibujó más adelante, informes del neurólogo alemán Karl Westphal (en 1883), quien la denominó "pseudoesclerosis"; por el neurólogo británico William Gowers (en 1888); [26] por el neuropatólogo finlandés Ernst Alexander Homén (en 1889-1892), quien observó la naturaleza hereditaria de la enfermedad; [27] y por Adolph Strümpell (en 1898), quien notó cirrosis hepática. [26] El neuropatólogo John Nathaniel Cumings estableció el vínculo con la acumulación de cobre tanto en el hígado como en el cerebro en 1948. [28] La aparición de hemólisis se observó en 1967. [29]
En 1951, Cumings y el neurólogo neozelandés Derek Denny-Brown , que trabajaba en Estados Unidos, informaron simultáneamente del primer tratamiento eficaz, utilizando un quelante metálico británico anti-Lewisita . [30] [31] Este tratamiento tenía que ser inyectado, pero fue una de las primeras terapias disponibles en el campo de la neurología, un campo que clásicamente era capaz de observar y diagnosticar, pero tenía pocos tratamientos para ofrecer. [26] [32] El primer agente quelante oral eficaz, la penicilamina , fue descubierto en 1956 por el neurólogo británico John Walshe. [33] En 1982, Walshe también introdujo la trientina, [34] y fue el primero en desarrollar tetratiomolibdato para uso clínico. [35] La terapia con acetato de zinc apareció inicialmente en los Países Bajos, donde los médicos Schouwink y Hoogenraad la utilizaron en 1961 y en la década de 1970, respectivamente, pero fue desarrollada más tarde por Brewer y sus colegas de la Universidad de Michigan . [22] [36]
La base genética de la enfermedad de Wilson y su vínculo con las mutaciones ATP7B fue aclarada por varios grupos de investigación en las décadas de 1980 y 1990. [37] [38]
La acumulación hereditaria de cobre se ha descrito en Bedlington Terriers , [39] donde generalmente sólo afecta al hígado. Se debe a mutaciones en el gen COMMD1 (o MURR1 ). [40] A pesar de estos hallazgos, las mutaciones COMMD1 no pudieron detectarse en humanos con estados de acumulación de cobre no wilsonianos (como la cirrosis infantil india ) para explicar su origen genético. [41]