Mendelevio
El mendelevio es un elemento de la tabla periódica cuyo símbolo es Md (anteriormente Mv) y su número atómico es 101.
Este isótopo es el que se utiliza para estudiar las propiedades químicas y físicas.
[4] No obstante, se han realizado una serie de predicciones y algunos resultados experimentales preliminares sobre sus propiedades.
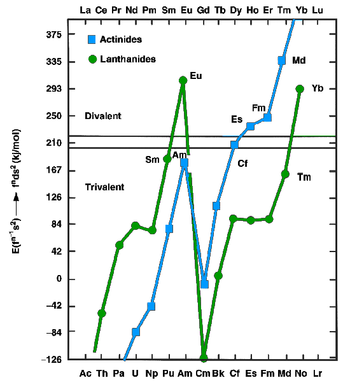
[5][6] La conclusión fue que el aumento de la energía de enlace de la configuración [Rn]5f126d17s2 sobre la configuración [Rn]5f La configuración 137s2 para el mendelevio no fue suficiente para compensar la energía necesaria para promover un electrón 5f a 6d, como también ocurre con los actínidos muy tardíos: por lo que se esperaba que el einsteinio, el fermio, el mendelevio y el nobelio fueran metales bivalentes.
[4] Al igual que los otros actínidos tardíos bivalentes (excepto el lawrencio una vez más trivalente), el mendelevio metálico debería asumir una estructura cristalina cúbica centrada en las caras.
[8] El punto de fusión del mendelevio se ha estimado en 827 °C, el mismo valor previsto para el elemento vecino nobelio.
[8] La química del mendelevio se conoce principalmente solo en solución, en la que puede tomar los estados de oxidación +3 o +2.
Se encontró que era estable en agua neutra–etanol solución y ser homólogo al cesio(I).
[10] No obstante, el equipo ruso realizó más estudios sobre la termodinámica de la cocristalización del mendelevio con cloruros de metales alcalinos y concluyó que el mendelevio(I) se había formado y podía formar mezclas cristales con elementos divalentes, cocristalizando así con ellos.
[12] El procedimiento anterior es el más utilizado para la separación de los elementos del transeinsteinio.
Luego se reoxida al estado +3 usando peróxido de hidrógeno y luego se aísla por elución selectiva con ácido clorhídrico 2 M (para eliminar impurezas, incluido el cromo) y finalmente ácido clorhídrico 6 M (para eliminar el mendelevio ).
[12] También es posible utilizar una columna de cationita y amalgama de zinc, utilizando como eluyente ácido clorhídrico 1 M reduciendo Md(III) a Md(II) donde se comporta como metales alcalinotérreos.