El tereftalato de polietileno (o poli(tereftalato de etileno) , PET , PETE o el obsoleto PETP o PET-P ), es la resina polimérica termoplástica más común de la familia del poliéster y se utiliza en fibras para ropa, recipientes para líquidos y alimentos, y termoformado para fabricación y en combinación con fibra de vidrio para resinas de ingeniería . [5]
En 2016, la producción anual de PET fue de 56 millones de toneladas. [6] La mayor aplicación es en fibras (más del 60%), y la producción de botellas representa alrededor del 30% de la demanda mundial. [7] En el contexto de las aplicaciones textiles, al PET se le conoce por su nombre común, poliéster , mientras que el acrónimo PET se utiliza generalmente en relación con los envases. [ cita necesaria ] El poliéster representa aproximadamente el 18% de la producción mundial de polímeros y es el cuarto polímero más producido después del polietileno (PE), el polipropileno (PP) y el cloruro de polivinilo (PVC). [ cita necesaria ]
El PET consta de unidades repetidas (C 10 H 8 O 4 ). El PET se recicla comúnmente y tiene el dígito 1 (♳) como código de identificación de resina (RIC). La Asociación Nacional de Recursos de Envases de PET (NAPCOR) define el PET como: "Los artículos de tereftalato de polietileno a los que se hace referencia se derivan del ácido tereftálico (o tereftalato de dimetilo ) y monoetilenglicol , en los que la suma del ácido tereftálico (o tereftalato de dimetilo) y el monoetilenglicol reaccionan constituye al menos el 90 por ciento de la masa de monómero que reaccionó para formar el polímero y debe exhibir una temperatura máxima de fusión entre 225 °C y 255 °C, como se identificó durante el segundo escaneo térmico en el procedimiento 10.1 en ASTM D3418, al calentar la muestra. a una velocidad de 10 °C/minuto." [8]
Dependiendo de su procesamiento y su historial térmico, el tereftalato de polietileno puede existir como polímero amorfo (transparente) y semicristalino . El material semicristalino puede parecer transparente (tamaño de partícula inferior a 500 nm ) u opaco y blanco (tamaño de partícula de hasta unos pocos micrómetros ) dependiendo de su estructura cristalina y tamaño de partícula.
Un proceso para fabricar PET utiliza tereftalato de bis (2-hidroxietilo) , [ cita necesaria ] que puede sintetizarse mediante la reacción de esterificación entre el ácido tereftálico y el etilenglicol con agua como subproducto (esto también se conoce como reacción de condensación), o por Reacción de transesterificación entre etilenglicol y tereftalato de dimetilo (DMT) con metanol como subproducto. La polimerización se realiza mediante una reacción de policondensación de los monómeros (realizada inmediatamente después de la esterificación/transesterificación) con agua como subproducto. [5]
Las fibras de poliéster se utilizan ampliamente en la industria textil. La invención de la fibra de poliéster se atribuye a J.R. Whinfield. [9] Fue comercializado por primera vez en la década de 1940 por ICI , bajo la marca 'Terylene'. [10] Posteriormente, EI DuPont lanzó la marca 'Dacron'. A partir de 2022, existen muchas marcas en todo el mundo, en su mayoría asiáticas.
Las fibras de poliéster se utilizan en prendas de moda, a menudo mezcladas con algodón, como capas de aislamiento térmico en ropa térmica, ropa deportiva y de trabajo y tapicería de automóviles.
Las botellas de plástico fabricadas con PET se utilizan ampliamente para refrescos , tanto sin gas como con gas . Para bebidas que se degradan por el oxígeno, como la cerveza, se utiliza una estructura multicapa. El PET intercala una capa adicional de alcohol polivinílico (PVOH) o poliamida (PA) para reducir aún más su permeabilidad al oxígeno.
La lámina de PET no orientada se puede termoformar para fabricar bandejas de embalaje y blisters . [11] El PET cristalizable resiste temperaturas de congelación y horneado. [12] : 1378 Tanto el PET amorfo como el BoPET son transparentes a simple vista. Los tintes que confieren color se pueden formular fácilmente en láminas de PET.
El PET es permeable al oxígeno y al dióxido de carbono y esto impone limitaciones en la vida útil del contenido envasado en PET. [13] : 104
A principios de la década de 2000, el mercado mundial de envases de PET creció a una tasa de crecimiento anual compuesta del 9% hasta alcanzar los 17 mil millones de euros en 2006. [14]
La película de PET biaxialmente orientada (BOPET) (a menudo conocida por uno de sus nombres comerciales, "Mylar") se puede aluminizar evaporando una fina película de metal sobre ella para reducir su permeabilidad y hacerla reflectante y opaca ( MPET ). Estas propiedades son útiles en muchas aplicaciones, incluido el envasado flexible de alimentos y el aislamiento térmico (como las mantas espaciales ).
BOPET se utiliza en la lámina posterior de módulos fotovoltaicos . La mayoría de las láminas posteriores consisten en una capa de BOPET laminada con un fluoropolímero o una capa de BOPET estabilizada contra los rayos UV. [15]
El PET también se utiliza como sustrato en células solares de película delgada.
El PET se puede combinar con fibra de vidrio y aceleradores de cristalización para producir resinas termoplásticas. Estos pueden moldearse por inyección en piezas como carcasas, cubiertas, componentes de aparatos eléctricos y elementos del sistema de encendido. [dieciséis]
El PET es estequiométricamente una mezcla de carbono y H 2 O y, por lo tanto, se ha utilizado en un experimento que implica compresión de choque impulsada por láser que creó nanodiamantes y agua superiónica . Esta podría ser una posible forma de producir nanodiamantes comercialmente. [17] [18]
El PET fue patentado en 1941 por John Rex Whinfield , James Tennant Dickson y su empleador, la Calico Printers' Association de Manchester , Inglaterra. EI DuPont de Nemours en Delaware, Estados Unidos, utilizó por primera vez la marca Mylar en junio de 1951 y recibió su registro en 1952. [27] Sigue siendo el nombre más conocido utilizado para las películas de poliéster. El propietario actual de la marca es DuPont Teijin Films. [28]
En la Unión Soviética, el PET se fabricó por primera vez en los laboratorios del Instituto de Compuestos de Alto Peso Molecular de la Academia de Ciencias de la URSS en 1949, y su nombre "Lavsan" es un acrónimo del mismo ( ла боратории Института в ысокомолекулярных с оединений А кадемии н аук СССР). [29]
La botella de PET fue inventada en 1973 por Nathaniel Wyeth [30] y patentada por DuPont. [31]

El PET en su estado más estable es una resina semicristalina incolora . Sin embargo, su cristalización es intrínsecamente lenta en comparación con otros polímeros semicristalinos . Dependiendo de las condiciones de procesamiento, se puede formar en artículos no cristalinos ( amorfos ) o cristalinos. Su facilidad para estirarse en la fabricación hace que el PET sea útil en aplicaciones de fibras y películas. Como la mayoría de los polímeros aromáticos , tiene mejores propiedades de barrera ( se necesita clarificación ) que los polímeros alifáticos . Es fuerte y resistente a los impactos. El PET es higroscópico y absorbe agua. [32]
Aproximadamente el 60% de cristalización es el límite superior para productos comerciales, con excepción de las fibras de poliéster . [ se necesita aclaración ] Se pueden producir productos transparentes enfriando rápidamente el polímero fundido por debajo de la temperatura de transición vítrea (Tg ) para formar un sólido amorfo no cristalino . [33] Al igual que el vidrio, el PET amorfo se forma cuando a sus moléculas no se les da tiempo suficiente para organizarse de manera ordenada y cristalina a medida que se enfría la masa fundida. Mientras que a temperatura ambiente las moléculas están congeladas en su lugar, si luego se les devuelve suficiente energía térmica calentando el material por encima de Tg , pueden comenzar a moverse nuevamente, permitiendo que los cristales se nucleen y crezcan. Este procedimiento se conoce como cristalización en estado sólido. [ cita requerida ] El PET amorfo también cristaliza y se vuelve opaco cuando se expone a solventes , como cloroformo o tolueno . [34]
Se puede producir un producto más cristalino dejando que el polímero fundido se enfríe lentamente. En lugar de formar un solo cristal grande, este material tiene varias esferulitas (áreas cristalizadas), cada una de las cuales contiene muchos cristalitos (granos) pequeños . La luz tiende a dispersarse cuando cruza los límites entre los cristalitos y las regiones amorfas entre ellos, lo que hace que el sólido resultante sea translúcido. [ cita necesaria ] La orientación también hace que los polímeros sean más transparentes. [ se necesita aclaración ] Esta es la razón por la que la película y las botellas de BOPET son cristalinas, hasta cierto punto, y transparentes. [ cita necesaria ]
El PET tiene afinidad por los sabores hidrofóbicos y, a veces, las bebidas deben formularse con una dosis de sabor más alta, en comparación con las de vidrio, para compensar el sabor absorbido por el recipiente. [35] : 115 Si bien las botellas de PET de gran calibre se devuelven para su reutilización, como en algunos países de la UE, la propensión del PET a absorber sabores hace necesario realizar una "prueba de olfateo" en las botellas devueltas para evitar la contaminación cruzada de sabores. [35] : 115
Diferentes aplicaciones de PET requieren diferentes grados de polimerización, que pueden obtenerse modificando las condiciones del proceso. El peso molecular del PET se mide por la viscosidad de la solución. [ aclaración necesaria ] El método preferido para medir esta viscosidad es la viscosidad intrínseca (IV) del polímero. [36] La viscosidad intrínseca es una medida adimensional que se obtiene extrapolando la viscosidad relativa (medida en (dℓ/g)) a una concentración cero. A continuación se muestran los rangos IV para aplicaciones comunes: [37]
El PET a menudo se copolimeriza con otros dioles o diácidos para optimizar las propiedades para aplicaciones particulares. Por ejemplo, se puede agregar ciclohexanodimetanol (CHDM) a la estructura principal del polímero en lugar de etilenglicol . Dado que este componente básico es mucho más grande (seis átomos de carbono adicionales) que la unidad de etilenglicol que reemplaza, no encaja con las cadenas vecinas como lo haría una unidad de etilenglicol. Esto interfiere con la cristalización y reduce la temperatura de fusión del polímero. En general, dicho PET se conoce como PETG o PET-G (tereftalato de polietileno modificado con glicol). Es un termoplástico amorfo transparente que puede moldearse por inyección, extruirse en láminas o extruirse como filamento para impresión 3D . El PETG se puede colorear durante el procesamiento. Otro modificador común es el ácido isoftálico , que reemplaza algunas de las unidades de tereftalato unidas 1,4-( para- ) . El enlace 1,2-( orto- ) o 1,3-( meta- ) produce un ángulo en la cadena, que también altera la cristalinidad.
Dichos copolímeros son ventajosos para determinadas aplicaciones de moldeo, como el termoformado , que se utiliza, por ejemplo, para fabricar envases en bandeja o tipo blíster a partir de película de co-PET, o lámina de PET amorfa (A-PET/PETA) o lámina de PETG. Por otro lado, la cristalización es importante en otras aplicaciones donde la estabilidad mecánica y dimensional es importante, como los cinturones de seguridad. Para las botellas de PET, puede resultar útil el uso de pequeñas cantidades de ácido isoftálico, CHDM, dietilenglicol (DEG) u otros comonómeros: si sólo se utilizan pequeñas cantidades de comonómeros, la cristalización se ralentiza pero no se evita por completo. Como resultado, se pueden obtener botellas mediante moldeo por estirado-soplado ("SBM"), que son lo suficientemente claras y cristalinas para ser una barrera adecuada para aromas e incluso gases, como el dióxido de carbono en las bebidas carbonatadas.
El tereftalato de polietileno se produce en gran medida a partir de ácido tereftálico purificado (PTA), así como, en menor medida, a partir de (mono)etilenglicol (MEG) y tereftalato de dimetilo (DMT). [38] [5] A partir de 2022, el etilenglicol se fabrica a partir de eteno que se encuentra en el gas natural , mientras que el ácido tereftálico proviene del p-xileno elaborado a partir del petróleo crudo . Normalmente se utiliza un compuesto de antimonio o titanio como catalizador, se añade un fosfito como estabilizador y un agente azulante como la sal de cobalto para enmascarar cualquier coloración amarillenta. [39]
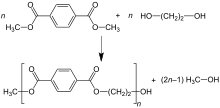
En el proceso de tereftalato de dimetilo (DMT), el DMT y el exceso de etilenglicol (MEG) se transesterifican en la masa fundida a 150-200 °C con un catalizador básico . El metanol (CH 3 OH) se elimina por destilación para impulsar la reacción. El exceso de MEG se destila a mayor temperatura con ayuda del vacío. El segundo paso de transesterificación se realiza a 270-280 °C, con destilación continua también de MEG. [38]
Las reacciones se pueden resumir de la siguiente manera:

En el proceso del ácido tereftálico , el MEG y el PTA se esterifican directamente a presión moderada (2,7 a 5,5 bar) y alta temperatura (220 a 260 °C). El agua se elimina en la reacción y también se elimina continuamente por destilación : [38]
Bio-PET es la contraparte biológica del PET. [40] [41] Esencialmente en Bio-PET, el MEG se fabrica a partir de etileno derivado del etanol de caña de azúcar . Se ha propuesto un mejor proceso basado en la oxidación del etanol [42] y también es técnicamente posible producir PTA a partir de furfural de base biológica fácilmente disponible . [43]

Existen dos métodos básicos de moldeo para botellas de PET, de un paso y de dos pasos. En el moldeo en dos pasos se utilizan dos máquinas independientes. La primera máquina moldea por inyección la preforma, que se asemeja a un tubo de ensayo, con las roscas de las tapas de las botellas ya moldeadas en su lugar. El cuerpo del tubo es significativamente más grueso, ya que se inflará hasta alcanzar su forma final en el segundo paso mediante moldeo por soplado y estiramiento .
En el segundo paso, las preformas se calientan rápidamente y luego se inflan contra un molde de dos partes para darles la forma final de la botella. Las preformas (botellas desinfladas) ahora también se utilizan como contenedores robustos y únicos; Además de los dulces novedosos, algunos capítulos de la Cruz Roja los distribuyen como parte del programa Vial of Life a los propietarios de viviendas para almacenar el historial médico para el personal de emergencia.
En las máquinas de un solo paso, todo el proceso desde la materia prima hasta el recipiente terminado se lleva a cabo dentro de una sola máquina, lo que las hace especialmente adecuadas para moldear formas no estándar (moldeo personalizado), incluidos frascos, óvalos planos, formas de matraces, etc. Su mayor mérito es la reducción de espacio, manipulación del producto y energía, y una calidad visual mucho mayor que la que se puede lograr con el sistema de dos pasos. [ cita necesaria ]
El PET está sujeto a degradación durante el procesamiento. Si el nivel de humedad es demasiado alto, la hidrólisis reducirá el peso molecular por escisión de la cadena , lo que provocará fragilidad. Si el tiempo de residencia y/o la temperatura de fusión (temperatura de fusión) son demasiado altos, entonces se producirá una degradación térmica o una degradación termooxidativa, lo que dará como resultado una decoloración y un peso molecular reducido, así como la formación de acetaldehído y la formación de "gel" o " formaciones de "ojo de pez" mediante reticulación . Las medidas de mitigación incluyen la copolimerización con otros polímeros como CHDM o ácido isoftálico , que reducen el punto de fusión y, por tanto, la temperatura de fusión de la resina, así como la adición de estabilizadores de polímeros como los fosfitos . [44]
El acetaldehído , que puede formarse por degradación del PET después de una mala manipulación del material, es una sustancia volátil incolora con olor afrutado. Aunque se forma naturalmente en algunas frutas, puede provocar un mal sabor en el agua embotellada. Además de las altas temperaturas (el PET se descompone por encima de los 300 °C o 570 °F) y los largos tiempos de residencia en el cilindro, las altas presiones y las altas velocidades del extrusor (que provocan un cizallamiento que eleva la temperatura) también pueden contribuir a la producción de acetaldehído. La fotooxidación también puede provocar la formación gradual de acetaldehído a lo largo de la vida útil del objeto. Esto se produce a través de una reacción de Norrish de tipo II . [45]
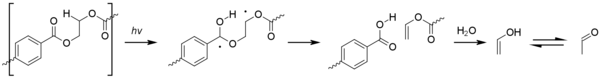
Cuando se produce acetaldehído, una parte del mismo queda disuelta en las paredes de un recipiente y luego se difunde en el producto almacenado en su interior, alterando su sabor y aroma. Esto no supone un problema para los productos no consumibles (como el champú), los zumos de frutas (que ya contienen acetaldehído) o las bebidas de sabor fuerte como los refrescos. Sin embargo, para el agua embotellada, un bajo contenido de acetaldehído es muy importante, porque si nada enmascara el aroma, incluso concentraciones extremadamente bajas (10 a 20 partes por mil millones en el agua) de acetaldehído pueden producir un mal sabor. [46]
Un comentario publicado en Environmental Health Perspectives en abril de 2010 sugirió que el PET podría producir disruptores endocrinos en condiciones de uso común y recomendó investigaciones sobre este tema. [47] Los mecanismos propuestos incluyen la lixiviación de ftalatos y la lixiviación de antimonio . Un artículo publicado en Journal of Environmental Monitoring en abril de 2012 concluye que la concentración de antimonio en el agua desionizada almacenada en botellas de PET se mantiene dentro del límite aceptable de la UE incluso si se almacena brevemente a temperaturas de hasta 60 °C (140 °F), mientras que el contenido embotellado (agua o refrescos) pueden ocasionalmente exceder el límite de la UE después de menos de un año de almacenamiento a temperatura ambiente. [48]
El antimonio (Sb) es un elemento metaloide que se utiliza como catalizador en forma de compuestos como el trióxido de antimonio (Sb 2 O 3 ) o el triacetato de antimonio en la producción de PET. Después de la fabricación, se puede encontrar una cantidad detectable de antimonio en la superficie del producto. Este residuo se puede eliminar con lavado. El antimonio también permanece en el propio material y, por tanto, puede migrar a alimentos y bebidas. Exponer el PET a ebullición o al microondas puede aumentar significativamente los niveles de antimonio, posiblemente por encima de los niveles máximos de contaminación de la EPA de EE. UU. [49] El límite de agua potable evaluado por la OMS es de 20 partes por mil millones (OMS, 2003), y el límite de agua potable en los Estados Unidos es de 6 partes por mil millones. [50] Aunque el trióxido de antimonio es de baja toxicidad cuando se toma por vía oral, [51] su presencia sigue siendo motivo de preocupación. La Oficina Federal Suiza de Salud Pública investigó la cantidad de migración de antimonio comparando aguas embotelladas en PET y vidrio: las concentraciones de antimonio en el agua en las botellas de PET eran mayores, pero aún muy por debajo de la concentración máxima permitida. La Oficina Federal Suiza de Salud Pública concluyó que pequeñas cantidades de antimonio migran del PET al agua embotellada, pero que el riesgo para la salud de las bajas concentraciones resultantes es insignificante (1% de la " ingesta diaria tolerable " determinada por la OMS ). Un estudio posterior (2006), pero más publicitado, encontró cantidades similares de antimonio en el agua contenida en botellas de PET. [52] La OMS ha publicado una evaluación de riesgos del antimonio en el agua potable. [51]
Sin embargo, se encontró que los concentrados de jugo de frutas (para los cuales no se han establecido pautas) que fueron producidos y embotellados en PET en el Reino Unido contenían hasta 44,7 μg/L de antimonio, muy por encima de los límites de la UE para agua del grifo de 5 μg/L. . [53]
La ropa desprende microfibras durante el uso, durante el lavado y el secado a máquina. La basura de plástico forma lentamente pequeñas partículas. Los microplásticos que están presentes en el fondo de los ríos o en el lecho marino pueden ser ingeridos por pequeñas especies marinas, entrando así en la cadena alimentaria. Como el PET tiene una densidad mayor que el agua, una cantidad significativa de micropartículas de PET puede precipitar en las plantas de tratamiento de aguas residuales. Las microfibras de PET generadas por el uso de prendas de vestir, el lavado o el secado a máquina pueden transportarse por el aire y dispersarse en los campos, donde son ingeridas por el ganado o las plantas y terminan en el suministro de alimentos humanos. SAPEA ha declarado que tales partículas "no representan un riesgo generalizado". [54] Se sabe que el PET se degrada cuando se expone a la luz solar y al oxígeno. [55] A partir de 2016, existe escasa información sobre la vida útil de los polímeros sintéticos en el medio ambiente. [56]



Si bien la mayoría de los termoplásticos pueden, en principio, reciclarse, el reciclaje de botellas de PET es más práctico que muchas otras aplicaciones de plástico debido al alto valor de la resina y al uso casi exclusivo de PET para el embotellado de agua y refrescos carbonatados, de uso generalizado. [57] [58] Las botellas de PET se prestan bien para el reciclaje (ver más abajo). En muchos países las botellas de PET se reciclan en gran medida [57] , por ejemplo alrededor del 75% en Suiza. [59] El término rPET se usa comúnmente para describir el material reciclado, aunque también se lo conoce como R-PET o PET posconsumo (POSTC-PET). [60] [61]
Los usos principales del PET reciclado son la fibra de poliéster, los flejes y los contenedores no alimentarios. [ cita necesaria ] Debido a la reciclabilidad del PET y la relativa abundancia de desechos posconsumo en forma de botellas, el PET también está ganando rápidamente participación de mercado como fibra para alfombras. [62] El PET, como muchos plásticos, también es un excelente candidato para la eliminación térmica ( incineración ), ya que está compuesto de carbono, hidrógeno y oxígeno, con sólo trazas de elementos catalizadores (pero sin azufre). [ cita necesaria ] En general, el PET se puede reciclar químicamente en sus materias primas originales (PTA, DMT y EG), destruyendo completamente la estructura del polímero; [ cita necesaria ] reciclado mecánicamente en una forma diferente, sin destruir el polímero; [ cita necesaria ] o reciclado en un proceso que incluye transesterificación y la adición de otros glicoles, polioles o glicerol para formar un nuevo poliol. El poliol del tercer método se puede utilizar en la producción de poliuretano (espuma de PU), [63] [64] [65] [66] o productos a base de epoxi, incluidas pinturas. [67]
En 2023 se anunció un proceso para utilizar PET como base para la producción de supercondensadores . El PET, que estequiométricamente es carbono y H 2 O , se puede convertir en una forma de carbono que contiene láminas y nanoesferas, con una superficie muy alta. El proceso consiste en mantener una mezcla de PET, agua, ácido nítrico y etanol a alta temperatura y presión durante ocho horas, seguido de centrifugación y secado. [68] [69]
En 2021 y 2022 se anunciaron importantes inversiones para el reciclaje químico de PET mediante glucólisis, metanólisis [70] [71] y reciclaje enzimático [72] para recuperar monómeros. Inicialmente también utilizarán botellas como materia prima, pero se espera que en el futuro las fibras también se reciclen de esta manera. [73]
El PET también es un combustible deseable para las plantas de valorización de energía , ya que tiene un alto poder calorífico que ayuda a reducir el uso de recursos primarios para la generación de energía. [74]
Al menos una especie de bacteria del género Nocardia puede degradar el PET con una enzima esterasa. [75] Las esterasas son enzimas capaces de romper el enlace éster entre dos oxígenos que une las subunidades de PET. [75] La degradación inicial del PET también puede lograrse con esterasas expresadas por Bacillus , así como por Nocardia . [76] Los científicos japoneses han aislado otra bacteria, Ideonella sakaiensis , que posee dos enzimas que pueden descomponer el PET en trozos más pequeños digeribles por las bacterias. Una colonia de I. sakaiensis puede desintegrar una película plástica en unas seis semanas. [77] [78] Investigadores franceses informan que han desarrollado una PET hidrolasa mejorada que puede despolimerizar (romper) al menos el 90 por ciento del PET en 10 horas, descomponiéndolo en monómeros individuales . [79] [80] [81] Además, la Universidad de Texas en Austin diseñó una enzima basada en una PET-asa natural con la ayuda de un algoritmo de aprendizaje automático para poder tolerar cambios de pH y temperatura . Se descubrió que la PET-ase podía degradar varios productos y podía descomponerlos en tan solo 24 horas. [82] [83]