El dióxido de silicio , también conocido como sílice , es un óxido de silicio con la fórmula química SiO 2 , que se encuentra comúnmente en la naturaleza como cuarzo . [5] [6] En muchas partes del mundo, la sílice es el principal componente de la arena . El sílice es abundante ya que comprende varios minerales y productos sintéticos. Todas las formas son blancas o incoloras, aunque las muestras impuras pueden colorearse.
El dióxido de silicio es un componente fundamental común del vidrio .

En la mayoría de los dióxidos de silicio, el átomo de silicio muestra coordinación tetraédrica , con cuatro átomos de oxígeno rodeando un átomo de Si central (ver celda unitaria 3-D). Así, el SiO 2 forma una red tridimensional sólida en la que cada átomo de silicio está unido covalentemente de forma tetraédrica a 4 átomos de oxígeno. [8] [9] Por el contrario, el CO 2 es una molécula lineal. Las estructuras marcadamente diferentes de los dióxidos de carbono y silicio son una manifestación de la regla del doble enlace . [10]
Según las diferencias estructurales de los cristales, el dióxido de silicio se puede dividir en dos categorías: cristalino y no cristalino (amorfo). En forma cristalina, esta sustancia se puede encontrar de forma natural como cuarzo, tridimita , cristobalita , stishovita y coesita . Por otro lado, la sílice amorfa se puede encontrar en la naturaleza como ópalo , tierra infusoria y tierra de diatomeas . El vidrio de cuarzo es la forma de estado intermedio entre esta estructura. [11]
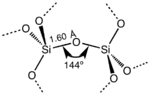
Todas estas formas cristalinas distintas siempre tienen la misma estructura local alrededor del Si y el O. En el cuarzo α, la longitud del enlace Si-O es de 161 pm, mientras que en la tridimita α está en el rango de 154 a 171 pm. El ángulo Si-O-Si también varía entre un valor bajo de 140° en α-tridimita, hasta 180° en β-tridimita. En el cuarzo α, el ángulo Si-O-Si es de 144°. [12]
El cuarzo alfa es la forma más estable de SiO 2 sólido a temperatura ambiente. Los minerales de alta temperatura, cristobalita y tridimita, tienen densidades e índices de refracción más bajos que el cuarzo. La transformación del cuarzo α en cuarzo beta se produce abruptamente a 573 °C. Dado que la transformación va acompañada de un cambio significativo de volumen, puede inducir fácilmente la fractura de cerámicas o rocas que pasan por este límite de temperatura. [13] Sin embargo, los minerales de alta presión, seifertita , stishovita y coesita, tienen densidades e índices de refracción más altos que el cuarzo. [14] La stishovita tiene una estructura similar al rutilo donde el silicio tiene 6 coordenadas. La densidad de la stishovita es de 4,287 g/cm 3 , en comparación con el cuarzo α, la más densa de las formas de baja presión, que tiene una densidad de 2,648 g/cm 3 . [15] La diferencia en densidad se puede atribuir al aumento de la coordinación, ya que las seis longitudes de enlace Si-O más cortas en la stishovita (cuatro longitudes de enlace Si-O de 176 pm y otras dos de 181 pm) son mayores que las de Si-O. longitud del enlace (161 pm) en cuarzo α. [16] El cambio en la coordinación aumenta la ionicidad del enlace Si-O. [17]
La sílice faujasita , otro polimorfo, se obtiene mediante la desaluminación de una zeolita Y ultraestable y baja en sodio con tratamiento combinado ácido y térmico. El producto resultante contiene más del 99% de sílice y tiene una alta cristalinidad y área superficial específica (más de 800 m 2 /g). La faujasita-sílice tiene una estabilidad térmica y ácida muy alta. Por ejemplo, mantiene un alto grado de orden molecular o cristalinidad de largo alcance incluso después de hervir en ácido clorhídrico concentrado . [18]
La sílice fundida exhibe varias características físicas peculiares que son similares a las observadas en el agua líquida : expansión de temperatura negativa, densidad máxima a temperaturas ~5000 °C y una capacidad calorífica mínima. [19] Su densidad disminuye de 2,08 g/cm 3 a 1950 °C a 2,03 g/cm 3 a 2200 °C. [20]
El SiO 2 molecular tiene una estructura lineal como el CO 2 . Se ha producido combinando monóxido de silicio (SiO) con oxígeno en una matriz de argón . El dióxido de silicio dimérico (SiO 2 ) 2 se ha obtenido haciendo reaccionar O 2 con monóxido de silicio dimérico aislado en matriz (Si 2 O 2 ). En el dióxido de silicio dimérico hay dos átomos de oxígeno que forman puentes entre los átomos de silicio con un ángulo Si-O-Si de 94 ° y una longitud de enlace de 164,6 pm y la longitud del enlace Si-O terminal es de 150,2 pm. La longitud del enlace Si-O es de 148,3 pm, que se compara con la longitud de 161 pm en el cuarzo α. La energía del enlace se estima en 621,7 kJ/mol. [21]
El SiO 2 se encuentra más comúnmente en la naturaleza como cuarzo , que constituye más del 10% en masa de la corteza terrestre. [22] El cuarzo es el único polimorfo de sílice estable en la superficie de la Tierra. Se han encontrado apariciones metaestables de las formas de alta presión coesita y stishovita alrededor de estructuras de impacto y asociadas con eclogitas formadas durante el metamorfismo de presión ultra alta . Las formas de alta temperatura de tridimita y cristobalita se conocen a partir de rocas volcánicas ricas en sílice . En muchas partes del mundo, la sílice es el principal constituyente de la arena . [23]
Aunque es poco soluble, la sílice se encuentra en muchas plantas como el arroz . Los materiales vegetales con alto contenido de fitolitos de sílice parecen ser importantes para los animales de pastoreo, desde insectos masticadores hasta ungulados . La sílice acelera el desgaste de los dientes, y es posible que se hayan desarrollado altos niveles de sílice en plantas consumidas frecuentemente por herbívoros como mecanismo de defensa contra la depredación. [24] [25]
La sílice también es el componente principal de la ceniza de cáscara de arroz , que se utiliza, por ejemplo, en filtración y como material cementante suplementario (SCM) en la fabricación de cemento y hormigón . [26]
Durante más de 1.000 millones de años, la silicificación en y por las células ha sido común en el mundo biológico. En el mundo moderno, ocurre en bacterias, protistas, plantas y animales (invertebrados y vertebrados).
Ejemplos destacados incluyen:
Los minerales cristalinos formados en el entorno fisiológico a menudo muestran propiedades físicas excepcionales (por ejemplo, resistencia, dureza, resistencia a la fractura) y tienden a formar estructuras jerárquicas que exhiben un orden microestructural en una variedad de escalas. Los minerales se cristalizan en un entorno infrasaturado de silicio y en condiciones de pH neutro y baja temperatura (0-40 °C).
Aproximadamente el 95% del uso comercial del dióxido de silicio (arena) se produce en la industria de la construcción, por ejemplo, para la producción de hormigón ( hormigón de cemento Portland ). [22]
Ciertos depósitos de arena de sílice, con tamaño y forma de partículas deseables y contenido deseable de arcilla y otros minerales, eran importantes para la fundición en arena de productos metálicos. [27] El alto punto de fusión de la sílice permite su uso en aplicaciones como la fundición de hierro; La fundición en arena moderna a veces utiliza otros minerales por otras razones.
La sílice cristalina se utiliza en la fracturación hidráulica de formaciones que contienen petróleo compacto y gas de esquisto . [28]
La sílice es el ingrediente principal en la producción de la mayor parte del vidrio . Como otros minerales se funden con sílice, el principio de depresión del punto de congelación reduce el punto de fusión de la mezcla y aumenta la fluidez. La temperatura de transición vítrea del SiO 2 puro es de aproximadamente 1475 K. [29] Cuando el dióxido de silicio SiO 2 fundido se enfría rápidamente, no cristaliza, sino que se solidifica como un vidrio. Debido a esto, la mayoría de los esmaltes cerámicos tienen sílice como ingrediente principal.
La geometría estructural del silicio y el oxígeno en el vidrio es similar a la del cuarzo y la mayoría de las otras formas cristalinas de silicio y oxígeno, con el silicio rodeado por tetraedros regulares de centros de oxígeno. La diferencia entre las formas vítrea y cristalina surge de la conectividad de las unidades tetraédricas: aunque no hay una periodicidad de largo alcance en la red vítrea, el orden permanece en escalas de longitud mucho más allá de la longitud del enlace SiO. Un ejemplo de este orden es la preferencia por formar anillos de 6 tetraedros. [30]
La mayoría de las fibras ópticas para telecomunicaciones también están hechas de sílice. Es una materia prima primaria para muchas cerámicas como la loza , el gres y la porcelana .
El dióxido de silicio se utiliza para producir silicio elemental . El proceso implica una reducción carbotérmica en un horno de arco eléctrico : [31]
La sílice pirógena , también conocida como sílice pirogénica, se prepara quemando SiCl 4 en una llama de hidrógeno rica en oxígeno para producir un "humo" de SiO 2 . [15]
También se puede producir vaporizando arena de cuarzo en un arco eléctrico a 3000 °C. Ambos procesos dan como resultado gotitas microscópicas de sílice amorfa fusionadas en partículas secundarias tridimensionales, ramificadas, en forma de cadenas, que luego se aglomeran en partículas terciarias, un polvo blanco con una densidad aparente extremadamente baja (0,03-0,15 g/cm 3 ) y, por lo tanto, una alta área superficial. [32] Las partículas actúan como un agente espesante tixotrópico o como un agente antiaglomerante, y pueden tratarse para hacerlas hidrófilas o hidrófobas para aplicaciones de agua o líquidos orgánicos.

El humo de sílice es un polvo ultrafino que se recoge como subproducto de la producción de aleaciones de silicio y ferrosilicio . Consiste en partículas esféricas amorfas (no cristalinas) con un diámetro medio de partícula de 150 nm, sin ramificación del producto pirogénico. El uso principal es como material puzolánico para hormigones de alto rendimiento. Las nanopartículas de sílice pirógena se pueden utilizar con éxito como agente antienvejecimiento en aglutinantes asfálticos. [33]
La sílice, ya sea coloidal, precipitada o pirógena, es un aditivo común en la producción de alimentos. Se utiliza principalmente como agente fluido o antiapelmazante en alimentos en polvo, como especias y cremas de café no lácteas, o polvos para formar tabletas farmacéuticas. [32] Puede adsorber agua en aplicaciones higroscópicas . La sílice coloidal se utiliza como agente clarificante para vino, cerveza y jugos, con el número E de referencia E551 . [22]
En cosmética, la sílice es útil por sus propiedades difusoras de la luz [34] y su absorbencia natural. [35]
La tierra de diatomeas , un producto extraído, se utiliza en alimentación y cosmética desde hace siglos. Está formado por las conchas de sílice de diatomeas microscópicas ; en una forma menos procesada se vendía como "polvo de dientes". [ cita requerida ] La sílice hidratada fabricada o extraída se utiliza como abrasivo duro en la pasta de dientes .
El dióxido de silicio se utiliza ampliamente en la tecnología de semiconductores.
Debido a que el dióxido de silicio es un óxido nativo de silicio, se usa más ampliamente en comparación con otros semiconductores como el arseniuro de galio o el fosfuro de indio .
El dióxido de silicio podría cultivarse sobre una superficie semiconductora de silicio. [36] Las capas de óxido de silicio podrían proteger las superficies de silicio durante los procesos de difusión y podrían usarse para enmascarar la difusión. [37] [38]
La pasivación de superficies es el proceso mediante el cual una superficie semiconductora se vuelve inerte y no cambia las propiedades del semiconductor como resultado de la interacción con el aire u otros materiales en contacto con la superficie o el borde del cristal. [39] [40] La formación de una capa de dióxido de silicio crecida térmicamente reduce en gran medida la concentración de estados electrónicos en la superficie del silicio . [40] Las películas de SiO 2 preservan las características eléctricas de las uniones p-n y evitan que estas características eléctricas se deterioren por el ambiente gaseoso. [38] Las capas de óxido de silicio podrían usarse para estabilizar eléctricamente las superficies de silicio. [37] El proceso de pasivación de superficies es un método importante de fabricación de dispositivos semiconductores que implica recubrir una oblea de silicio con una capa aislante de óxido de silicio para que la electricidad pueda penetrar de manera confiable hasta el silicio conductor que se encuentra debajo. Hacer crecer una capa de dióxido de silicio sobre una oblea de silicio le permite superar los estados superficiales que de otro modo impedirían que la electricidad llegue a la capa semiconductora. [39] [41]
El proceso de pasivación de la superficie del silicio mediante oxidación térmica (dióxido de silicio) es fundamental para la industria de los semiconductores . Se utiliza comúnmente para fabricar transistores de efecto de campo semiconductores de óxido metálico (MOSFET) y chips de circuitos integrados de silicio (con el proceso plano ). [39] [41]
La sílice hidrofóbica se utiliza como componente antiespumante .
En su calidad de refractario , es útil en forma de fibra como tejido de protección térmica a altas temperaturas . [ cita necesaria ]
La sílice se utiliza en la extracción de ADN y ARN debido a su capacidad para unirse a los ácidos nucleicos en presencia de caotropos . [42]
El aerogel de sílice se utilizó en la nave espacial Stardust para recolectar partículas extraterrestres. [43]
La sílice pura (dióxido de silicio), cuando se enfría como cuarzo fundido en un vidrio sin punto de fusión real, se puede utilizar como fibra de vidrio para fibra de vidrio.
Se ha investigado el dióxido de silicio para aplicaciones agrícolas como insecticida potencial . [44] [45]
El dióxido de silicio se obtiene principalmente mediante minería, incluida la extracción de arena y la purificación de cuarzo . El cuarzo es adecuado para muchos propósitos, mientras que se requiere procesamiento químico para obtener un producto más puro o más adecuado (por ejemplo, más reactivo o de grano fino). [ cita necesaria ]
La sílice precipitada o sílice amorfa se produce mediante la acidificación de soluciones de silicato de sodio . El precipitado gelatinoso o gel de sílice , primero se lava y luego se deshidrata para producir sílice microporosa incolora. [15] La ecuación idealizada que involucra un trisilicato y ácido sulfúrico es:
De esta manera se produjeron aproximadamente mil millones de kilogramos/año (1999) de sílice, principalmente para su uso en compuestos poliméricos: neumáticos y suelas de zapatos. [22]
Películas delgadas de sílice crecen espontáneamente en obleas de silicio mediante oxidación térmica , produciendo una capa muy poco profunda de aproximadamente 1 nm o 10 Å del llamado óxido nativo. [46] Se utilizan temperaturas más altas y entornos alternativos para hacer crecer capas bien controladas de dióxido de silicio sobre silicio, por ejemplo a temperaturas entre 600 y 1200 °C, utilizando la llamada oxidación seca con O 2
u oxidación húmeda con H 2 O. [47] [48]
La capa de óxido nativo es beneficiosa en microelectrónica , donde actúa como aislante eléctrico con alta estabilidad química. Puede proteger el silicio, almacenar carga, bloquear la corriente e incluso actuar como una vía controlada para limitar el flujo de corriente. [49]
Muchas rutas para obtener dióxido de silicio comienzan con un compuesto organosilícico, por ejemplo, HMDSO, [50] TEOS. La síntesis de sílice se ilustra a continuación utilizando ortosilicato de tetraetilo (TEOS). [51] Simplemente calentar TEOS a 680–730 °C da como resultado el óxido:
Del mismo modo, TEOS arde a unos 400 °C:
TEOS se hidróliza mediante el llamado proceso sol-gel . El curso de la reacción y la naturaleza del producto se ven afectados por los catalizadores, pero la ecuación idealizada es: [52]
Al ser muy estable, el dióxido de silicio surge de muchos métodos. Conceptualmente simple, pero de poco valor práctico, la combustión de silano produce dióxido de silicio. Esta reacción es análoga a la combustión de metano:
Sin embargo, la deposición química de vapor de dióxido de silicio sobre la superficie del cristal a partir de silano se utilizó utilizando nitrógeno como gas portador a 200-500 °C. [53]
El dióxido de silicio es un material relativamente inerte (de ahí su amplia aparición como mineral). La sílice se utiliza a menudo como recipientes inertes para reacciones químicas. A altas temperaturas, se convierte en silicio por reducción con carbono.
El flúor reacciona con el dióxido de silicio para formar SiF 4 y O 2 , mientras que los otros gases halógenos (Cl 2 , Br 2 , I 2 ) no reaccionan. [15]
La mayoría de las formas de dióxido de silicio son atacadas ("grabadas") por ácido fluorhídrico (HF) para producir ácido hexafluorosilícico : [12]
La stishovita no reacciona al HF en ningún grado significativo. [54] El HF se utiliza para eliminar o modelar el dióxido de silicio en la industria de los semiconductores.
El dióxido de silicio actúa como un ácido Lux-Flood , pudiendo reaccionar con bases en determinadas condiciones. Como no contiene hidrógeno, la sílice no hidratada no puede actuar directamente como ácido de Brønsted-Lowry . Mientras que el dióxido de silicio es poco soluble en agua a pH bajo o neutro (típicamente, 2 × 10 −4 M para cuarzo hasta 10 −3 M para calcedonia criptocristalina ), las bases fuertes reaccionan con el vidrio y lo disuelven fácilmente. Por lo tanto, las bases fuertes deben almacenarse en botellas de plástico para evitar que se atasque la tapa de la botella, preservar la integridad del recipiente y evitar una contaminación indeseable por aniones de silicato. [55]
El dióxido de silicio se disuelve en álcali concentrado caliente o hidróxido fundido, como se describe en esta ecuación idealizada: [15]
El dióxido de silicio neutralizará los óxidos metálicos básicos (por ejemplo , óxido de sodio , óxido de potasio , óxido de plomo (II) , óxido de zinc o mezclas de óxidos, formando silicatos y vidrios a medida que los enlaces Si-O-Si en la sílice se rompen sucesivamente). [12] Como ejemplo, la reacción del óxido de sodio y SiO 2 puede producir ortosilicato de sodio , silicato de sodio y vidrios, dependiendo de las proporciones de los reactivos: [15]
Ejemplos de este tipo de vidrios tienen importancia comercial, por ejemplo, vidrio sodocálcico , vidrio de borosilicato , vidrio de plomo . En estos vidrios, la sílice se denomina formador de red o formador de red. [12] La reacción también se utiliza en altos hornos para eliminar las impurezas de la arena en el mineral mediante neutralización con óxido de calcio , formando escoria de silicato de calcio .

El dióxido de silicio reacciona a reflujo calentado bajo dinitrógeno con etilenglicol y una base de metal alcalino para producir silicatos pentacoordinados altamente reactivos que brindan acceso a una amplia variedad de nuevos compuestos de silicio. [56] Los silicatos son esencialmente insolubles en todos los disolventes polares excepto el metanol .
El dióxido de silicio reacciona con el silicio elemental a altas temperaturas para producir SiO: [12]
La solubilidad del dióxido de silicio en agua depende en gran medida de su forma cristalina y es de tres a cuatro veces mayor para la sílice [ se necesita clarificación ] que para el cuarzo; en función de la temperatura, alcanza un máximo de alrededor de 340 °C (644 °F). [57] Esta propiedad se utiliza para hacer crecer monocristales de cuarzo en un proceso hidrotermal donde el cuarzo natural se disuelve en agua sobrecalentada en un recipiente a presión que está más frío en la parte superior. Se pueden cultivar cristales de 0,5 a 1 kg durante 1 a 2 meses. [12] Estos cristales son una fuente de cuarzo muy puro para su uso en aplicaciones electrónicas. [15] Por encima de la temperatura crítica del agua 647,096 K (373,946 °C; 705,103 °F) y una presión de 22,064 megapascales (3200,1 psi) o más, el agua es un fluido supercrítico y la solubilidad es una vez más mayor que a temperaturas más bajas. [58]

La sílice ingerida por vía oral es esencialmente no tóxica, con una LD50 de 5000 mg/kg (5 g/kg). [22] Un estudio de 2008 que siguió a sujetos durante 15 años encontró que niveles más altos de sílice en el agua parecían disminuir el riesgo de demencia . Un aumento de 10 mg/día de sílice en el agua potable se asoció con una disminución del riesgo de demencia del 11%. [59]
La inhalación de polvo de sílice cristalina finamente dividido puede provocar silicosis , bronquitis o cáncer de pulmón , ya que el polvo se aloja en los pulmones e irrita continuamente el tejido, reduciendo la capacidad pulmonar. [60] Cuando las partículas finas de sílice se inhalan en cantidades suficientemente grandes (como a través de exposición ocupacional), aumenta el riesgo de enfermedades autoinmunes sistémicas como el lupus [61] y la artritis reumatoide en comparación con las tasas esperadas en la población general. [45]
La sílice es un riesgo laboral para las personas que realizan trabajos de limpieza con chorro de arena o trabajan con productos que contienen sílice cristalina en polvo. La sílice amorfa, como la sílice pirógena, puede causar daño pulmonar irreversible en algunos casos, pero no está asociada con el desarrollo de silicosis. Los niños, los asmáticos de cualquier edad, los alérgicos y los ancianos (todos ellos con capacidad pulmonar reducida ) pueden verse afectados en menos tiempo. [62]
La sílice cristalina es un riesgo laboral para quienes trabajan con encimeras de piedra , porque el proceso de corte e instalación de las encimeras genera grandes cantidades de sílice en el aire. [63] La sílice cristalina utilizada en la fracturación hidráulica presenta un riesgo para la salud de los trabajadores. [28]
En el cuerpo, las partículas de sílice cristalina no se disuelven durante períodos clínicamente relevantes. Los cristales de sílice dentro de los pulmones pueden activar el inflamasoma NLRP3 dentro de los macrófagos y las células dendríticas y, por lo tanto, dar como resultado la producción de interleucina , una citocina altamente proinflamatoria en el sistema inmunológico. [64] [65] [66]
Las regulaciones que restringen la exposición a la sílice "con respecto al riesgo de silicosis" especifican que se refieren únicamente a la sílice, que es a la vez cristalina y forma polvo. [67] [68] [69] [70] [71] [72]
En 2013, la Administración de Salud y Seguridad Ocupacional de EE. UU . redujo el límite de exposición a 50 µg /m 3 de aire. Antes de 2013, se permitían 100 µg/m 3 y en los trabajadores de la construcción incluso 250 µg/m 3 . [28] En 2013, OSHA también exigió la "terminación verde" de los pozos fracturados para reducir la exposición a la sílice cristalina, además de restringir el límite de exposición. [28]
El SiO 2 , más que casi cualquier material, existe en muchas formas cristalinas. Estas formas se llaman polimorfos .
La inhalación de sílice cristalina finamente dividida puede provocar inflamación grave del tejido pulmonar , silicosis , bronquitis , cáncer de pulmón y enfermedades autoinmunes sistémicas , como lupus y artritis reumatoide . La inhalación de dióxido de silicio amorfo , en dosis altas, provoca una inflamación no permanente a corto plazo, en la que todos los efectos desaparecen. [88]
Esta lista ampliada enumera sinónimos de dióxido de silicio; todos estos valores provienen de una sola fuente; los valores en la fuente se presentaron en mayúsculas. [89]
Estos pigmentos de enfoque suave, compuestos principalmente por polímeros, micas y talcos recubiertos de partículas rugosas o esféricas de pequeño diámetro, como sílice o dióxido de titanio, se utilizan para reducir ópticamente la apariencia de las arrugas. Estos efectos se obtienen optimizando los contornos de las arrugas y reduciendo la diferencia de brillo debida al reflejo difuso.
La sílice es un ingrediente multiporoso que absorbe la grasa y el sebo.