
Los filtros UV son compuestos, mezclas o materiales que bloquean o absorben la luz ultravioleta (UV). Una de las principales aplicaciones de los filtros UV es su uso como protectores solares para proteger la piel de las quemaduras solares y otros daños relacionados con el sol y los rayos UV. Después de que la invención de las cámaras digitales cambiara el campo de la fotografía , los filtros UV se han utilizado para recubrir los discos de vidrio instalados en las lentes de las cámaras para proteger el hardware sensible a la luz UV.
Los tipos anteriores de películas fotográficas eran bastante sensibles a la luz ultravioleta, que solía provocar turbidez o niebla y un tono azulado en las películas de color. Se utilizaron filtros UV para filtrar longitudes de onda ultravioleta más cortas y al mismo tiempo permanecer transparentes a la luz visible. Sin embargo, las películas fotográficas y las cámaras digitales modernas son menos sensibles a las longitudes de onda ultravioleta.
Los filtros UV a veces se denominan filtros L37 o L39, según las longitudes de onda de luz que filtran. Por ejemplo, un filtro L37 elimina la luz ultravioleta con longitudes de onda inferiores a 370 nanómetros (nm), mientras que un filtro L39 elimina la luz con longitudes de onda inferiores a 390 nm.
Los filtros UV abarcan [ se necesita aclaración ] todo el espectro de colores y se utilizan para una amplia variedad de aplicaciones. Las luces denominadas Ortho Red y Deep Ortho Red se utilizan habitualmente en transferencia por difusión, en la composición tipográfica de películas o papel y en otras aplicaciones relacionadas con materiales ortocromáticos . Los filtros o luces de seguridad Yellow Gold, Yellow, Lithostar Yellow y Fuji Yellow brindan espacios de trabajo seguros para aplicaciones de prueba de contacto como serigrafía y fabricación de planchas. Los filtros o luces de seguridad verde panorámico, verde infrarrojo y verde oscuro se utilizan comúnmente en aplicaciones de escaneo, funcionan con películas , papeles y rayos X pancromáticos .
Muchos fotógrafos y directores de fotografía todavía utilizan filtros UV para proteger el cristal y el revestimiento de sus lentes . Sin embargo, los filtros UV, como ocurre con cualquier filtro óptico, pueden introducir reflejos en la lente y perjudicar el contraste y la nitidez. Los parasoles pueden contrarrestar esto, ya que ofrecen cierta protección contra impactos y sombrean los elementos ópticos, evitando así el destello de la lente. Además, los filtros UV de calidad ofrecen cierta protección contra la contaminación de las lentes y al mismo tiempo minimizan la distorsión adicional inherente.
En fotografía, el término "filtro UV" también puede usarse incorrectamente como un filtro que deja pasar la luz UV mientras bloquea otras longitudes de onda en el espectro de luz, de la misma manera, el término " filtro IR " se usa para filtrar todo el espectro. El nombre correcto para estos filtros es "filtro de paso UV" y "filtro de paso IR", respectivamente, y sólo se utilizan en fotografía muy especializada.
Dado que la radiación ultravioleta excesiva puede provocar quemaduras solares , fotoenvejecimiento y cáncer de piel , los productos de cuidado como los protectores solares suelen incluir una clasificación según las longitudes de onda específicas que filtran. [1] Las clasificaciones de UV incluyen UVA (320-400 nm), UVB (290-320 nm) y UVC (200-280 nm). Los compuestos que absorben los rayos UV se utilizan no sólo en protectores solares, sino también en otros productos de cuidado personal, como lápices labiales, champús, lacas para el cabello, geles de baño, jabones de tocador y repelentes de insectos. [2] Los filtros químicos protegen contra la radiación UV absorbiéndola, reflejándola o dispersándola . [2] [3] La reflexión y la dispersión se logran mediante filtros UV físicos inorgánicos, como el dióxido de titanio (TiO 2 ) y el óxido de zinc (ZnO). La absorción, principalmente de UVB, se realiza mediante filtros UV orgánicos, que se conocen como filtros UV químicos. [4] Los niveles de filtros UV en los protectores solares suelen variar entre el 0,5% y el 10%, aunque a veces alcanzan el 25%. [5]
Muchos compuestos orgánicos diferentes pueden servir como filtros UV. Se dividen en varias clases estructurales: [6]
El uso de filtros UV ha aumentado recientemente debido a la creciente preocupación por la radiación UV y el cáncer de piel, especialmente como resultado del agotamiento de la capa de ozono , lo que a su vez ha causado preocupación por su impacto ambiental. [3]
El material filtrante puede entrar al medio ambiente directamente, a través de la descarga de aguas residuales industriales, o indirectamente, a través de la descarga de agua doméstica durante la ducha, el baño, la excreción de orina o mediante el tratamiento de aguas residuales. Las plantas de tratamiento de aguas residuales (PTAR) no son muy efectivas para eliminar estos contaminantes. [5] Se han detectado varios filtros UV a niveles de ppb o ppt [ vagos ] en aguas superficiales y aguas residuales, con concentraciones máximas en el verano. [7] [8]
Debido a que la mayoría de los filtros UV son lipófilos , tienden a bioacumularse en ambientes acuáticos y en las cadenas alimentarias que se originan en ellos. Confirmando la bioacumulación , varios estudios han demostrado la presencia de filtros UV en organismos acuáticos. Se detectó alcanfor 4-metilbencilideno en el tejido muscular de truchas en aguas suizas y alemanas, mientras que se encontraron trazas de metoxicinamato de etilhexilo y octocrileno en mariscos en las costas mediterránea y atlántica de Francia . [9] [10] Además, se encontraron dieciocho protectores solares orgánicos en sedimentos de ríos y lagos japoneses, en concentraciones que oscilaban entre 2 y aproximadamente 3000 ng/g. [11] La acumulación de filtros UV orgánicos en organismos vivos es motivo de gran preocupación porque algunos de ellos (y sus metabolitos ) pueden actuar como disruptores endocrinos tanto in vitro como in vivo. [12] Además, Goksøyr et al. (2009) informaron concentraciones de filtros UV orgánicos en aguas abiertas del Océano Pacífico, lo que proporciona evidencia de la persistencia y amplia dispersión de estos componentes en el medio marino. [13]
Debido a que los filtros UV no siempre son estables en condiciones ambientales, es común que se transformen en otros compuestos. El agua de los embalses naturales, por ejemplo, está sometida a la irradiación solar, mientras que el agua de las piscinas suele desinfectarse mediante cloración , bromación , ozonización o irradiación ultravioleta . [14] Estos subproductos a menudo pueden ser más tóxicos que el filtro UV original. Por ejemplo, la avobenzona se transforma en presencia de productos de desinfección clorados y radiación ultravioleta, produciendo acetofenonas y fenoles clorados sustituidos , conocidos por su toxicidad. [5]
Algunos filtros UV orgánicos bajo radiación UV pueden generar especies reactivas de oxígeno (ROS) (OH, H 2 O 2 ) (por ejemplo, BP-3, octocrileno (OCR), metoxicinamato de octilo (OMC), ácido fenilbencimidazolsulfónico (PBS, PABA, etc.). .). Algunos estudios han registrado niveles elevados de peróxido de hidrógeno o H 2 O 2 en las playas directamente atribuibles a la transformación del filtro UV [15] El H 2 O 2 es responsable de dañar los lípidos , las proteínas y el ADN , y generar altos niveles de estrés en el medio marino. [16] Los filtros UV inorgánicos (es decir, TiO 2 ) también pueden generar ROS, otro compuesto tóxico para el fitoplancton marino .
_with_signs_of_bleaching_or_crown-of-thorns_starfish_damage.jpg/440px-Favia_pallida_(hard_coral)_with_signs_of_bleaching_or_crown-of-thorns_starfish_damage.jpg)
Los filtros UV han mostrado graves efectos en los arrecifes de coral debido al blanqueamiento de los corales en concentraciones muy bajas. Como resultado, pequeñas cantidades de protectores solares provocan la producción de grandes cantidades de mucosa coralina en un plazo de 18 a 48 horas y el blanqueamiento de los corales duros en un plazo de 96 horas. Entre los filtros UV que según los estudios provocan el blanqueamiento de los corales se encuentran el metoxicinamato de etilhexilo, la 3- benzofenona y el alcanfor 4-metilbencilideno , incluso en concentraciones muy bajas. El blanqueo se vio favorecido por temperaturas más altas que actúan como factores sinérgicos. Los experimentos demostraron que el blanqueamiento de los corales no depende de la dosis, por lo que puede ocurrir tras la exposición a cantidades muy pequeñas. [17]
Según una estimación aproximada de 78 millones de turistas al año en las zonas de arrecifes de coral, la cantidad estimada de protector solar utilizado anualmente en los países tropicales oscila entre 16.000 y 25.000 toneladas. El 25% de esta cantidad se elimina durante las actividades de baño, lo que genera una liberación de 4.000 a 6.000 toneladas/año en las zonas de arrecifes. Esto resulta en una amenaza para el 10% de los arrecifes del mundo sólo por el blanqueamiento de los corales inducido por el protector solar. [17] Los protectores solares pueden mejorar significativamente la producción viral en el agua de mar. [17]

La fotólisis es la principal ruta abiótica para la transformación de los filtros UV. La fotólisis disocia los filtros orgánicos en radicales libres. [6]
La fotólisis puede ser directa o indirecta. La forma directa se produce cuando el cromóforo del filtro orgánico absorbe la luz solar en determinadas longitudes de onda. La vía indirecta se produce en presencia de un fotosensibilizador. La materia orgánica disuelta (DOM) en las aguas superficiales actúa como fotosensibilizador y produce fotooxidación reactiva como radicales hidroxilo , radicales peroxilo y oxígeno singlete .
La fotólisis de los productos de protección solar es más complicada que el comportamiento de los filtros UV individuales, como muestra este ejemplo. En presencia de otros filtros UV, benzotriazol y ácidos húmicos, se observó degradación de la benzofenona -3 mediante la pérdida de grupos funcionales hidroxilo y benzoílo, lo que resultó en la formación de 2,4 dimetil anisol. [18]
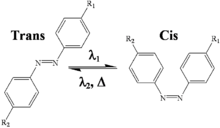
La fotoisomerización puede dar como resultado productos que absorben menos luz ultravioleta que su compuesto original. [19] Esto se evidencia por los cinamatos , salicilatos , alcanfor de bencilidina y derivados de dibenzoilmetano . El metoxicinamato de octilo (OMC) puede sufrir fotoisomerización , fotodegradación y fotodimerización para obtener varios isómeros dímeros y ciclodímeros . La mayoría de los productos comerciales son isómeros trans, pero existen en el medio ambiente como una mezcla de isómeros trans y cis tras la exposición a la radiación UV debido a la presencia del doble enlace C=C adyacente a los anillos aromáticos . Los isómeros pueden tener propiedades fisicoquímicas idénticas, pero pueden diferir en su comportamiento y efectos biológicos. [6]
El agua de las piscinas suele desinfectarse mediante cloración , bromación , ozonización o radiación UV. Ante la presencia de algunos filtros UV como la Avobenzona en piscinas, estos pueden descomponerse y crear subproductos de desinfección , incluidos productos tóxicos, como resultado de la interacción entre la Avobenzona y el cloro activo y la radiación UV. [5]

Las benzofenonas (BP) se utilizan ampliamente en filtros UV, potenciadores de fragancias y aditivos plásticos. Se informa que las principales fuentes de BP-3 son las actividades recreativas humanas y los efluentes de las plantas de tratamiento de aguas residuales (PTAR) . Las formas aniónicas tanto de BP-3 como de 4-OH-BP3 pueden sufrir fotodegradación directa. Las tasas fotolíticas de ambos compuestos en aguas naturales son más rápidas que las del agua pura. Los experimentos de eliminación de radicales revelaron que la materia orgánica disuelta excitada por triplete (3DOM*) era responsable de la fotodegradación indirecta de BP-3 y 4-OH-BP3 en agua de mar, mientras que, en agua dulce, la fotodegradación indirecta de estos dos compuestos se atribuía a la materia orgánica disuelta. Materia Orgánica y radical OH. [20]

El ácido p -aminobenzoico fue uno de los primeros filtros UV utilizados en protectores solares (1943). Se utilizó en concentraciones de hasta el 5%. En 1982 se descubrió que el PABA aumenta la formación de un defecto particular del ADN en las células humanas. [ cita necesaria ] El destino fotoquímico del PABA puede verse afectado por los componentes del agua, por ejemplo, NO 3 - , materia orgánica disuelta (DOM) y HCO 3 - . [21] PABA sufre fotólisis tanto directa como indirecta en la solución con presencia de NO 3 . La fotólisis directa representa el 25% de la degradación del PABA y se considera una vía secundaria. Por otro lado, la fotólisis indirecta fue la vía dominante.
Zhou y Mopper demostraron que el nitrato mejoraba la fotodegradación de PABA en un factor de 2. Sin embargo, en presencia de eliminadores de radicales libres, como formas de carbonato y materia orgánica natural (NOM), la fotodegradación de PABA disminuía. Se propuso que la fotólisis indirecta del PABA se debía principalmente al producto de la fotólisis NO 3 •OH. [ cita necesaria ]
El anión bicarbonato es abundante en el agua. El bicarbonato provocó un 10% de eliminación de •OH. La reacción entre el bicarbonato y el •OH produce un radical carbonato (•CO3), que es menos reactivo que el •OH. En aguas naturales, el •CO3 puede alcanzar una concentración en estado estacionario mayor que el •OH debido a su menor reactividad. La mejora de la fotólisis de PABA por el bicarbonato se debe a los radicales carbonato. [21]
La NOM soluble en agua está compuesta de ácidos orgánicos. Estos ácidos orgánicos son principalmente sustancias húmicas , que se pueden clasificar en una fracción de ácido fúlvico y húmico. NOM favorece la fotólisis indirecta del PABA absorbiendo la luz solar y debilitando su intensidad.
Pueden tener lugar dos reacciones durante la degradación de PABA en presencia de nitrato en agua, como se muestra en la figura. Tres de los cuatro productos contienen grupos fenólicos y, por tanto, pueden ser estrogénicos. Por lo tanto, los subproductos peligrosos generados durante la fotorreacción de PABA deberían preocuparse por su estrogenicidad.

El 4- terc -butil-4'-metoxidibenzoilmetano, conocido como avobenzona , pertenece a los dibenzoilmetanos . Es uno de los filtros UVA (400-320 nm) más comunes utilizados en formulaciones de protectores solares. Se vende con los nombres comerciales Parsol 1789 o Eusolex 9020. La avobenzona existe en dos formas tautoméricas : enol y ceto . En las formulaciones de protección solar, la avobenzona existe predominantemente en forma de enol, que tiene una absorción máxima en longitudes de onda que oscilan entre 350 y 365 nm, según el disolvente utilizado. Se demostró que el doble enlace de la forma enólica es más reactivo en condiciones de cloración acuática que el anillo aromático. En un ambiente acuático clorado, la avobenzona se transforma en dos aldehídos y ácidos correspondientes , como se muestra en la figura. Ambos aldehídos se forman como resultado del enlace CO- CH2 . Son menos estables en condiciones oxidativas y se transforman fácilmente en los ácidos correspondientes.
Los derivados clorados de acetofenona también se forman debido a la escisión del mismo enlace CO-CH 2 . Los derivados clorados de la acetofenona son gases lacrimógenos , desencadenan dermatitis y algunos otros problemas de salud. Se informó que la cloración de la avobenzona original en la posición del anillo aromático es menos posible. La ruptura del enlace CO-Ar da como resultado la formación de 4-cloroanisol. [5]

El metoxicinamato de etilhexilo ( EHMC ) es uno de los filtros UVB más utilizados en todo el mundo. Se conoce como Eusolex 2292 y Uvinul MC80. Está incluido en la lista de productos químicos de alto volumen de producción (HPVC), que incluye productos químicos producidos o importados en la UE a un ritmo de más de 1000 toneladas por año. Se predijo que la vida útil del EHMC sería de horas a unos pocos días. EHMC es bien tolerado por la piel. Sin embargo, tiene algunos efectos secundarios, incluida su capacidad para producir especies reactivas de oxígeno (ROS) y penetrar la piel humana después de la exposición a la luz ultravioleta. También se ha encontrado EHMC en mariscos, pescados y cormoranes en niveles de ng/g, lo que sugiere que puede acumularse en la cadena alimentaria. [22] Se demostró que EHMC es responsable del blanqueamiento de los corales al promover infecciones virales. [17] Desde el punto de vista toxicológico, EHMC tiene propiedades estrogénicas tanto in vitro como in vivo. Por ejemplo, la exposición a este compuesto provocó un aumento del peso del útero en las ratas. La exposición prenatal a EHMC puede afectar tanto el desarrollo reproductivo como neurológico en las crías de ratas, lo que puede ser motivo de preocupación porque los humanos están expuestos habitualmente a este compuesto mediante el uso de protectores solares y otros cosméticos.
La principal vía de transformación de EHMC es la fotólisis. La fotólisis directa representa la vía de transformación dominante. Por otro lado, la fotólisis indirecta por OH es despreciable y, por materia orgánica disuelta, será una vía secundaria. Se detectaron cuatro productos de transformación para EHMC tras la exposición a la radiación UV. El 4-metoxi benzaldehído (MOBA) y el ácido 4-metoxicinámico son dos productos de transformación de EHMC mediante desalquilación . El MOBA intermedio es más tóxico que el EHMC para las bacterias.