Los glóbulos rojos ( RBC ), conocidos como eritrocitos (del griego antiguo erythros 'rojo' y kytos 'vaso hueco', con - cyte traducido como 'célula' en el uso moderno) en el mundo académico y en las publicaciones médicas, también conocidos como glóbulos rojos , [1] las células eritroides , y raramente las hemátidas , son el tipo más común de célula sanguínea y el principal medio de los vertebrados para suministrar oxígeno ( O 2 ) a los tejidos corporales , a través del flujo sanguíneo a través del sistema circulatorio . [2] Los eritrocitos absorben oxígeno en los pulmones , o en los peces en las branquias , y lo liberan en los tejidos mientras se aprietan a través de los capilares del cuerpo .
El citoplasma de un glóbulo rojo es rico en hemoglobina (Hb), una biomolécula que contiene hierro , que puede unirse al oxígeno y es responsable del color rojo de las células y la sangre. Cada glóbulo rojo humano contiene aproximadamente 270 millones de moléculas de hemoglobina. [3] La membrana celular está compuesta de proteínas y lípidos , y esta estructura proporciona propiedades esenciales para la función celular fisiológica , como la deformabilidad y la estabilidad de la célula sanguínea mientras atraviesa el sistema circulatorio y, específicamente, la red capilar .
En los seres humanos, los glóbulos rojos maduros son discos bicóncavos flexibles . Carecen de núcleo celular (que se expulsa durante el desarrollo ) y de orgánulos , para acomodar el máximo espacio para la hemoglobina; pueden considerarse como sacos de hemoglobina, con una membrana plasmática como saco. Aproximadamente 2,4 millones de nuevos eritrocitos se producen por segundo en adultos humanos. [4] Las células se desarrollan en la médula ósea y circulan durante unos 100 a 120 días en el cuerpo antes de que sus componentes sean reciclados por los macrófagos . Cada circulación dura unos 60 segundos (un minuto). [5] Aproximadamente el 84% de las células del cuerpo humano son los 20 a 30 billones de glóbulos rojos. [6] [7] [8] [9] Casi la mitad del volumen de la sangre ( 40% a 45% ) son glóbulos rojos.
Los glóbulos rojos concentrados son glóbulos rojos que han sido donados, procesados y almacenados en un banco de sangre para transfusiones sanguíneas .


La gran mayoría de los vertebrados, incluidos los mamíferos y los humanos, tienen glóbulos rojos. Los glóbulos rojos son células presentes en la sangre para transportar oxígeno. Los únicos vertebrados conocidos sin glóbulos rojos son los peces de hielo cocodrilo (familia Channichthyidae ); viven en aguas frías muy ricas en oxígeno y transportan el oxígeno libremente disuelto en su sangre. [11] Si bien ya no utilizan hemoglobina, se pueden encontrar restos de genes de hemoglobina en su genoma . [12]
Los glóbulos rojos de los vertebrados están compuestos principalmente de hemoglobina , una metaloproteína compleja que contiene grupos hemo cuyos átomos de hierro se unen temporalmente a las moléculas de oxígeno (O 2 ) en los pulmones o las branquias y las liberan por todo el cuerpo. El oxígeno puede difundirse fácilmente a través de la membrana celular del glóbulo rojo . La hemoglobina en los glóbulos rojos también transporta parte del producto de desecho dióxido de carbono de regreso de los tejidos; sin embargo, la mayor parte del dióxido de carbono de desecho se transporta de regreso a los capilares pulmonares de los pulmones como bicarbonato (HCO 3 − ) disuelto en el plasma sanguíneo . La mioglobina , un compuesto relacionado con la hemoglobina, actúa para almacenar oxígeno en las células musculares . [13]
El color de los glóbulos rojos se debe al grupo hemo de la hemoglobina. El plasma sanguíneo por sí solo es de color pajizo, pero los glóbulos rojos cambian de color según el estado de la hemoglobina: cuando se combina con oxígeno, la oxihemoglobina resultante es escarlata, y cuando se ha liberado el oxígeno, la desoxihemoglobina resultante es de un color rojo burdeos oscuro. Sin embargo, la sangre puede parecer azulada cuando se ve a través de la pared de los vasos y la piel. [14] La oximetría de pulso aprovecha el cambio de color de la hemoglobina para medir directamente la saturación de oxígeno en la sangre arterial mediante técnicas colorimétricas . La hemoglobina también tiene una afinidad muy alta por el monóxido de carbono , formando carboxihemoglobina que es de un color rojo muy brillante. A veces se descubre que los pacientes enrojecidos y confundidos con una lectura de saturación del 100% en la oximetría de pulso sufren intoxicación por monóxido de carbono. [ cita requerida ]
El hecho de que las proteínas transportadoras de oxígeno se encuentren dentro de células especializadas (en lugar de que los transportadores de oxígeno estén disueltos en el líquido corporal) fue un paso importante en la evolución de los vertebrados, ya que permite que la sangre sea menos viscosa , que haya mayores concentraciones de oxígeno y que el oxígeno se difunda mejor desde la sangre a los tejidos. El tamaño de los glóbulos rojos varía ampliamente entre las especies de vertebrados; el ancho de los glóbulos rojos es, en promedio, un 25 % mayor que el diámetro de los capilares , y se ha planteado la hipótesis de que esto mejora la transferencia de oxígeno de los glóbulos rojos a los tejidos. [15]
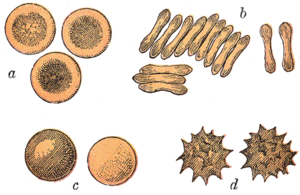
Los glóbulos rojos de los mamíferos tienen forma típica de discos bicóncavos: aplanados y deprimidos en el centro, con una sección transversal en forma de mancuerna y un borde en forma de toro en el borde del disco. Esta forma permite una alta relación área-superficie-volumen (SA/V) para facilitar la difusión de gases. [16] Sin embargo, hay algunas excepciones con respecto a la forma en el orden de los artiodáctilos ( ungulados de dedos pares, incluidos el ganado, los ciervos y sus parientes), que muestra una amplia variedad de morfologías extrañas de glóbulos rojos: células pequeñas y muy ovaladas en llamas y camellos (familia Camelidae ), células esféricas diminutas en ciervos ratón (familia Tragulidae ) y células que asumen formas fusiformes, lanceoladas, en medialuna e irregularmente poligonales y otras formas angulares en ciervos rojos y wapiti (familia Cervidae ). Los miembros de este orden han desarrollado claramente un modo de desarrollo de glóbulos rojos sustancialmente diferente de la norma de los mamíferos. [10] [17] En general, los glóbulos rojos de los mamíferos son notablemente flexibles y deformables para pasar a través de pequeños capilares , así como para maximizar su superficie de contacto al asumir una forma de cigarro, donde liberan eficientemente su carga de oxígeno. [18]
Los glóbulos rojos de los mamíferos son únicos entre los vertebrados, ya que no tienen núcleo cuando maduran. Tienen núcleo durante las primeras fases de la eritropoyesis , pero lo extruyen durante el desarrollo a medida que maduran; esto proporciona más espacio para la hemoglobina. Los glóbulos rojos sin núcleo, llamados reticulocitos , pierden posteriormente todos los demás orgánulos celulares , como sus mitocondrias , el aparato de Golgi y el retículo endoplasmático .
El bazo actúa como reservorio de glóbulos rojos, pero este efecto es algo limitado en los seres humanos. En otros mamíferos, como los perros y los caballos, el bazo secuestra grandes cantidades de glóbulos rojos, que se vierten en la sangre durante los períodos de estrés, lo que produce una mayor capacidad de transporte de oxígeno.



Un glóbulo rojo humano típico tiene un diámetro de disco de aproximadamente 6,2–8,2 μm [19] y un espesor máximo de 2–2,5 μm y un espesor mínimo en el centro de 0,8–1 μm, siendo mucho más pequeño que la mayoría de las otras células humanas . Estas células tienen un volumen promedio de aproximadamente 90 fL [20] con un área de superficie de aproximadamente 136 μm 2 , y pueden hincharse hasta una forma esférica que contiene 150 fL, sin distensión de la membrana.
Los adultos tienen en un momento dado entre 20 y 30 billones de glóbulos rojos, lo que supone aproximadamente el 70% de todas las células. [21] Las mujeres tienen entre 4 y 5 millones de glóbulos rojos por microlitro (milímetro cúbico) de sangre y los hombres entre 5 y 6 millones; las personas que viven a grandes altitudes con baja tensión de oxígeno tendrán más. Por tanto, los glóbulos rojos son mucho más comunes que las demás partículas sanguíneas: hay entre 4.000 y 11.000 glóbulos blancos y entre 150.000 y 400.000 plaquetas por microlitro.
Los glóbulos rojos humanos tardan en promedio 60 segundos en completar un ciclo de circulación. [5] [9] [22]
El color rojo de la sangre se debe a las propiedades espectrales de los iones de hierro hemínico en la hemoglobina . Cada molécula de hemoglobina lleva cuatro grupos hemo; la hemoglobina constituye aproximadamente un tercio del volumen celular total. La hemoglobina es responsable del transporte de más del 98% del oxígeno en el cuerpo (el oxígeno restante se transporta disuelto en el plasma sanguíneo ). Los glóbulos rojos de un hombre adulto promedio almacenan colectivamente alrededor de 2,5 gramos de hierro, lo que representa aproximadamente el 65% del hierro total contenido en el cuerpo. [23] [24]
Los glóbulos rojos de los mamíferos son anucleados cuando maduran, lo que significa que carecen de núcleo celular . En comparación, los glóbulos rojos de otros vertebrados tienen núcleo; las únicas excepciones conocidas son las salamandras de la familia Plethodontidae , donde cinco clados diferentes han desarrollado varios grados de glóbulos rojos enucleados (la mayoría evolucionaron en algunas especies del género Batrachoseps ), y los peces del género Maurolicus . [25] [26] [27]
La eliminación del núcleo en los glóbulos rojos de vertebrados se ha propuesto como explicación de la posterior acumulación de ADN no codificante en el genoma . [17] El argumento es el siguiente: el transporte eficiente de gas requiere que los glóbulos rojos pasen por capilares muy estrechos, y esto limita su tamaño. En ausencia de eliminación nuclear, la acumulación de secuencias repetidas está limitada por el volumen ocupado por el núcleo, que aumenta con el tamaño del genoma.
Los glóbulos rojos nucleados en los mamíferos constan de dos formas: los normoblastos, que son precursores eritropoyéticos normales de los glóbulos rojos maduros, y los megaloblastos, que son precursores anormalmente grandes que aparecen en las anemias megaloblásticas .
Los glóbulos rojos son deformables, flexibles, capaces de adherirse a otras células y de interactuar con las células inmunitarias. Su membrana desempeña muchas funciones en este sentido. Estas funciones dependen en gran medida de la composición de la membrana. La membrana de los glóbulos rojos está compuesta por tres capas: el glicocáliz en el exterior, que es rico en carbohidratos ; la bicapa lipídica que contiene muchas proteínas transmembrana , además de sus principales constituyentes lipídicos; y el esqueleto de la membrana, una red estructural de proteínas ubicada en la superficie interna de la bicapa lipídica. La mitad de la masa de la membrana de los glóbulos rojos humanos y de la mayoría de los mamíferos son proteínas. La otra mitad son lípidos, a saber, fosfolípidos y colesterol . [28]

La membrana de los glóbulos rojos está formada por una bicapa lipídica típica , similar a la que se encuentra en prácticamente todas las células humanas. En pocas palabras, esta bicapa lipídica está compuesta de colesterol y fosfolípidos en proporciones iguales en peso. La composición lipídica es importante, ya que define muchas propiedades físicas, como la permeabilidad y la fluidez de la membrana. Además, la actividad de muchas proteínas de membrana está regulada por interacciones con los lípidos de la bicapa.
A diferencia del colesterol, que se distribuye uniformemente entre las láminas internas y externas, los 5 fosfolípidos principales están dispuestos asimétricamente, como se muestra a continuación:
Monocapa exterior
Monocapa interna
Esta distribución asimétrica de los fosfolípidos en la bicapa es el resultado de la función de varias proteínas transportadoras de fosfolípidos dependientes e independientes de la energía. Las proteínas llamadas " flippasas " mueven los fosfolípidos desde la monocapa externa a la interna, mientras que otras llamadas " floppasas " realizan la operación opuesta, en contra de un gradiente de concentración de una manera dependiente de la energía. Además, también existen proteínas " scramblasas " que mueven los fosfolípidos en ambas direcciones al mismo tiempo, a favor de sus gradientes de concentración de una manera independiente de la energía. Todavía existe un considerable debate en curso sobre la identidad de estas proteínas de mantenimiento de la membrana en la membrana de los glóbulos rojos.
El mantenimiento de una distribución asimétrica de fosfolípidos en la bicapa (como una localización exclusiva de PS y PI en la monocapa interna) es fundamental para la integridad y la función celular debido a varias razones:
Estudios recientes han descrito la presencia de estructuras especializadas llamadas " balsas lipídicas " en la membrana de los glóbulos rojos. Se trata de estructuras enriquecidas con colesterol y esfingolípidos asociados a proteínas de membrana específicas, a saber, flotilinas , STOMatins (banda 7), proteínas G y receptores β-adrenérgicos . Se ha demostrado que las balsas lipídicas que se han implicado en eventos de señalización celular en células no eritroides median en las células eritroides la señalización del receptor β2-adregénico y aumentan los niveles de AMPc , regulando así la entrada de parásitos de la malaria en los glóbulos rojos normales. [29] [30]

Las proteínas del esqueleto de la membrana son responsables de la deformabilidad, flexibilidad y durabilidad del glóbulo rojo, permitiéndole pasar a través de capilares de menos de la mitad del diámetro del glóbulo rojo (7-8 μm) y recuperar la forma discoide tan pronto como estas células dejan de recibir fuerzas de compresión, de forma similar a un objeto de caucho.
Actualmente se conocen más de 50 proteínas de membrana, que pueden existir en unos pocos cientos hasta un millón de copias por glóbulo rojo. Aproximadamente 25 de estas proteínas de membrana transportan los diversos antígenos de los grupos sanguíneos, como los antígenos A, B y Rh, entre muchos otros. Estas proteínas de membrana pueden realizar una amplia diversidad de funciones, como el transporte de iones y moléculas a través de la membrana del glóbulo rojo, la adhesión e interacción con otras células como las células endoteliales, como receptores de señalización, así como otras funciones actualmente desconocidas. Los tipos de sangre de los humanos se deben a variaciones en las glucoproteínas de superficie de los glóbulos rojos. Los trastornos de las proteínas de estas membranas se asocian a muchos trastornos, como la esferocitosis hereditaria , la eliptocitosis hereditaria , la estomatocitosis hereditaria y la hemoglobinuria paroxística nocturna . [28] [29]
Las proteínas de la membrana de los glóbulos rojos organizadas según su función:
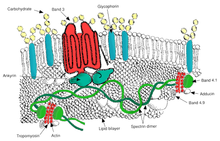
Transporte
Adhesión celular
Función estructural : Las siguientes proteínas de membrana establecen enlaces con proteínas esqueléticas y pueden desempeñar un papel importante en la regulación de la cohesión entre la bicapa lipídica y el esqueleto de la membrana, probablemente permitiendo que el glóbulo rojo mantenga su área de superficie de membrana favorable al evitar que la membrana colapse (forme vesículas).
[28] [29]
El potencial zeta es una propiedad electroquímica de las superficies celulares que está determinada por la carga eléctrica neta de las moléculas expuestas en la superficie de las membranas celulares de la célula. El potencial zeta normal del glóbulo rojo es de -15,7 milivoltios ( mV). [35] Gran parte de este potencial parece deberse a los residuos de ácido siálico expuestos en la membrana: su eliminación da como resultado un potencial zeta de -6,06 mV.
Recordemos que la respiración , como se ilustra esquemáticamente aquí con una unidad de carbohidrato, produce aproximadamente tantas moléculas de dióxido de carbono, CO 2 , como de oxígeno, O 2 , consume . [36]
Por lo tanto, la función del sistema circulatorio tiene que ver tanto con el transporte de dióxido de carbono como con el transporte de oxígeno. Como se afirma en otra parte de este artículo, la mayor parte del dióxido de carbono en la sangre está en forma de ion bicarbonato. El bicarbonato proporciona un tampón de pH crítico . [37] Por lo tanto, a diferencia de la hemoglobina para el transporte de O 2 , existe una ventaja fisiológica en no tener una molécula transportadora de CO 2 específica .
Los glóbulos rojos, sin embargo, desempeñan un papel clave en el proceso de transporte de CO2 , por dos razones. En primer lugar, porque, además de la hemoglobina, contienen un gran número de copias de la enzima anhidrasa carbónica en el interior de su membrana celular. [38] La anhidrasa carbónica, como su nombre indica, actúa como catalizador del intercambio entre el ácido carbónico y el dióxido de carbono (que es el anhídrido del ácido carbónico). Al ser un catalizador, puede afectar a muchas moléculas de CO2 , por lo que realiza su papel esencial sin necesitar tantas copias como las necesarias para el transporte de O2 por la hemoglobina. En presencia de este catalizador, el dióxido de carbono y el ácido carbónico alcanzan un equilibrio muy rápidamente, mientras que los glóbulos rojos todavía se están moviendo a través del capilar. Por lo tanto, son los glóbulos rojos los que se aseguran de que la mayor parte del CO2 se transporte como bicarbonato. [39] [40] A pH fisiológico, el equilibrio favorece fuertemente al ácido carbónico, que se disocia principalmente en iones bicarbonato. [41]
Los iones H+ liberados por esta reacción rápida dentro de los glóbulos rojos, mientras aún están en el capilar, actúan para reducir la afinidad de unión del oxígeno de la hemoglobina, el efecto Bohr .
La segunda contribución importante de los glóbulos rojos al transporte de dióxido de carbono es que el dióxido de carbono reacciona directamente con los componentes proteicos de la globina de la hemoglobina para formar compuestos de carbaminohemoglobina . A medida que se libera oxígeno en los tejidos, más CO 2 se une a la hemoglobina y, a medida que el oxígeno se une en el pulmón, desplaza el CO 2 unido a la hemoglobina , esto se llama efecto Haldane . A pesar del hecho de que solo una pequeña cantidad del CO 2 en la sangre está unido a la hemoglobina en la sangre venosa, una mayor proporción del cambio en el contenido de CO 2 entre la sangre venosa y arterial proviene del cambio en este CO 2 unido . [42] Es decir, siempre hay una abundancia de bicarbonato en la sangre, tanto venosa como arterial, debido a su papel mencionado anteriormente como amortiguador del pH.
En resumen, el dióxido de carbono producido por la respiración celular se difunde muy rápidamente a áreas de menor concentración, específicamente a los capilares cercanos. [43] [44] Cuando se difunde en un GR, el CO2 es rápidamente convertido por la anhidrasa carbónica que se encuentra en el interior de la membrana del GR en ion bicarbonato. Los iones bicarbonato a su vez abandonan el GR a cambio de iones cloruro del plasma, facilitado por la proteína de transporte de aniones de banda 3 ubicada en la membrana del GR. El ion bicarbonato no se difunde de regreso fuera del capilar, sino que es transportado al pulmón. En el pulmón, la menor presión parcial de dióxido de carbono en los alvéolos hace que el dióxido de carbono se difunda rápidamente desde el capilar hacia los alvéolos. La anhidrasa carbónica en los glóbulos rojos mantiene el ion bicarbonato en equilibrio con el dióxido de carbono. Entonces, cuando el dióxido de carbono sale del capilar y el CO2 es desplazado por el O2 en la hemoglobina, el ion bicarbonato suficiente se convierte rápidamente en dióxido de carbono para mantener el equilibrio. [38] [45] [46] [47]
Cuando los glóbulos rojos sufren esfuerzo cortante en vasos constreñidos, liberan ATP , lo que hace que las paredes de los vasos se relajen y dilaten para promover el flujo sanguíneo normal. [48]
Cuando sus moléculas de hemoglobina se desoxigenan, los glóbulos rojos liberan S-nitrosotioles , que también actúan dilatando los vasos sanguíneos, [49] dirigiendo así más sangre a las zonas del cuerpo carentes de oxígeno.
Los glóbulos rojos también pueden sintetizar óxido nítrico enzimáticamente, utilizando L-arginina como sustrato, al igual que las células endoteliales . [50] La exposición de los glóbulos rojos a niveles fisiológicos de estrés cortante activa la óxido nítrico sintasa y la exportación de óxido nítrico, [51] lo que puede contribuir a la regulación del tono vascular.
Los glóbulos rojos también pueden producir sulfuro de hidrógeno , un gas señalizador que actúa para relajar las paredes de los vasos sanguíneos. Se cree que los efectos cardioprotectores del ajo se deben a que los glóbulos rojos convierten sus compuestos de azufre en sulfuro de hidrógeno. [52]
Los glóbulos rojos también juegan un papel en la respuesta inmune del cuerpo : cuando son destruidos por patógenos como las bacterias, su hemoglobina libera radicales libres , que rompen la pared celular y la membrana del patógeno, matándolo. [53] [54]
Como resultado de no contener mitocondrias , los glóbulos rojos no utilizan nada del oxígeno que transportan; en su lugar, producen el transportador de energía ATP mediante la glucólisis de la glucosa y la fermentación del ácido láctico en el piruvato resultante . [55] [56] Además, la vía de la pentosa fosfato juega un papel importante en los glóbulos rojos; consulte deficiencia de glucosa-6-fosfato deshidrogenasa para obtener más información.
Como los glóbulos rojos no contienen núcleo, actualmente se supone que la biosíntesis de proteínas está ausente en estas células.
Debido a la falta de núcleos y orgánulos, los glóbulos rojos maduros no contienen ADN y no pueden sintetizar ningún ARN (aunque sí contienen ARN), [57] [58] y, en consecuencia, no pueden dividirse y tienen capacidades de reparación limitadas. [59] La incapacidad de llevar a cabo la síntesis de proteínas significa que ningún virus puede evolucionar para dirigirse a los glóbulos rojos de los mamíferos. [60] Sin embargo, la infección con parvovirus (como el parvovirus humano B19 ) puede afectar a los precursores eritroides mientras aún tienen ADN, como se reconoce por la presencia de pronormoblastos gigantes con partículas virales y cuerpos de inclusión , agotando temporalmente la sangre de reticulocitos y causando anemia . [61]
Los glóbulos rojos humanos se producen a través de un proceso llamado eritropoyesis , y se desarrollan a partir de células madre comprometidas hasta glóbulos rojos maduros en aproximadamente 7 días. Cuando maduran, en un individuo sano estas células viven en la circulación sanguínea durante aproximadamente 100 a 120 días (y 80 a 90 días en un bebé a término ). [62] Al final de su vida útil, se eliminan de la circulación. En muchas enfermedades crónicas, la vida útil de los glóbulos rojos se reduce.
La eritropoyesis es el proceso por el cual se producen nuevos glóbulos rojos; dura aproximadamente 7 días. A través de este proceso, los glóbulos rojos se producen continuamente en la médula ósea roja de los huesos grandes. (En el embrión , el hígado es el sitio principal de producción de glóbulos rojos). La producción puede ser estimulada por la hormona eritropoyetina (EPO), sintetizada por el riñón. Justo antes y después de salir de la médula ósea, las células en desarrollo se conocen como reticulocitos ; estos constituyen aproximadamente el 1% de los glóbulos rojos circulantes.
La vida útil funcional de un glóbulo rojo es de aproximadamente 100 a 120 días, tiempo durante el cual los glóbulos rojos se mueven continuamente por el empuje del flujo sanguíneo (en las arterias ), el tirón (en las venas ) y una combinación de los dos a medida que pasan a través de microvasos como los capilares. También se reciclan en la médula ósea. [63]
El glóbulo rojo envejecido sufre cambios en su membrana plasmática , haciéndolo susceptible al reconocimiento selectivo por los macrófagos y la posterior fagocitosis en el sistema fagocítico mononuclear ( bazo , hígado y ganglios linfáticos ), eliminando así las células viejas y defectuosas y purgando continuamente la sangre. Este proceso se denomina eriptosis , muerte programada de los glóbulos rojos. [64] Este proceso normalmente ocurre a la misma tasa de producción por eritropoyesis, equilibrando el recuento total de glóbulos rojos circulantes. La eriptosis aumenta en una amplia variedad de enfermedades, incluidas la sepsis , el síndrome hemolítico urémico , la malaria , la anemia de células falciformes , la beta- talasemia , la deficiencia de glucosa-6-fosfato deshidrogenasa , el agotamiento de fosfato, la deficiencia de hierro y la enfermedad de Wilson . La eriptosis puede ser provocada por choque osmótico, estrés oxidativo y agotamiento energético, así como por una amplia variedad de mediadores endógenos y xenobióticos . Se observa una eriptosis excesiva en los glóbulos rojos que carecen de la proteína quinasa tipo I dependiente de cGMP o de la proteína quinasa activada por AMP AMPK. Los inhibidores de la eriptosis incluyen eritropoyetina , óxido nítrico , catecolaminas y altas concentraciones de urea .
Gran parte de los productos de degradación resultantes se recirculan en el cuerpo. El componente hemo de la hemoglobina se descompone en hierro (Fe 3+ ) y biliverdina . La biliverdina se reduce a bilirrubina , que se libera en el plasma y recircula al hígado unida a la albúmina . El hierro se libera en el plasma para ser recirculado por una proteína transportadora llamada transferrina . Casi todos los glóbulos rojos se eliminan de esta manera de la circulación antes de que tengan la edad suficiente para hemolizarse . La hemoglobina hemolizada está unida a una proteína en el plasma llamada haptoglobina , que no es excretada por el riñón. [65]
Las enfermedades de la sangre que afectan a los glóbulos rojos incluyen:

Los glóbulos rojos pueden administrarse como parte de una transfusión de sangre . La sangre puede ser donada por otra persona o almacenada por el receptor en una fecha anterior. La sangre donada generalmente requiere una evaluación para garantizar que los donantes no tengan factores de riesgo para la presencia de enfermedades transmitidas por la sangre o que no las sufrirán ellos mismos al donar sangre. La sangre generalmente se recolecta y se analiza para detectar enfermedades comunes o graves transmitidas por la sangre, como la hepatitis B , la hepatitis C y el VIH. El tipo de sangre (A, B, AB u O) o el producto sanguíneo se identifica y se combina con la sangre del receptor para minimizar la probabilidad de una reacción transfusional hemolítica aguda , un tipo de reacción transfusional . Esto se relaciona con la presencia de antígenos en la superficie de la célula. Después de este proceso, la sangre se almacena y, en un corto período de tiempo, se utiliza. La sangre puede donarse como un producto completo o los glóbulos rojos separados como glóbulos rojos concentrados .
La sangre se transfunde a menudo cuando se sabe que hay anemia, sangrado activo o cuando se espera una pérdida de sangre importante, como antes de una operación. Antes de donar sangre, se analiza una pequeña muestra de sangre del receptor junto con la transfusión en un proceso conocido como prueba cruzada .
En 2008 se informó de que se había logrado que células madre embrionarias humanas se convirtieran en glóbulos rojos en el laboratorio. El paso más complicado fue inducir a las células a expulsar su núcleo; esto se logró cultivando las células en células del estroma de la médula ósea. Se espera que estos glóbulos rojos artificiales puedan utilizarse en transfusiones de sangre. [67]
En 2022 se realizará un ensayo en humanos, utilizando sangre cultivada a partir de células madre obtenidas de sangre de donantes. [68]

Existen varios análisis de sangre que involucran glóbulos rojos. Entre ellos se encuentran el recuento de glóbulos rojos (la cantidad de glóbulos rojos por volumen de sangre), el cálculo del hematocrito (porcentaje del volumen de sangre ocupado por glóbulos rojos) y la velocidad de sedimentación globular . Es necesario determinar el tipo de sangre para prepararse para una transfusión de sangre o un trasplante de órgano .
Muchas enfermedades que afectan a los glóbulos rojos se diagnostican con un frotis de sangre periférica, en el que se extiende una fina capa de sangre sobre un portaobjetos de microscopio. Esto puede revelar poiquilocitosis , que son variaciones en la forma de los glóbulos rojos. Cuando los glóbulos rojos se presentan a veces en forma de pila, con un lado plano junto al lado plano. Esto se conoce como formación de rouleaux y ocurre con más frecuencia si los niveles de ciertas proteínas séricas están elevados, como por ejemplo durante la inflamación .
Los glóbulos rojos se pueden obtener de la sangre entera mediante centrifugación , que separa las células del plasma sanguíneo en un proceso conocido como fraccionamiento de la sangre . Los glóbulos rojos concentrados , que se obtienen de esta manera a partir de sangre entera sin el plasma, se utilizan en la medicina transfusional . [69] Durante la donación de plasma , los glóbulos rojos se bombean de nuevo al cuerpo de inmediato y solo se recolecta el plasma.
Algunos atletas han intentado mejorar su rendimiento mediante el dopaje sanguíneo : primero se les extrae aproximadamente un litro de sangre, luego se aíslan los glóbulos rojos, se congelan y se almacenan, para ser reinyectados poco antes de la competencia. (Los glóbulos rojos se pueden conservar durante 5 semanas a -79 °C o -110 °F, o durante 10 años utilizando crioprotectores [70] ). Esta práctica es difícil de detectar, pero puede poner en peligro el sistema cardiovascular humano, que no está equipado para lidiar con la sangre de la viscosidad más alta resultante . Otro método de dopaje sanguíneo implica la inyección de eritropoyetina para estimular la producción de glóbulos rojos. Ambas prácticas están prohibidas por la Agencia Mundial Antidopaje .
La primera persona en describir los glóbulos rojos fue el joven biólogo holandés Jan Swammerdam , quien había utilizado un microscopio temprano en 1658 para estudiar la sangre de una rana. [71] Sin saber de este trabajo, Anton van Leeuwenhoek proporcionó otra descripción microscópica en 1674, esta vez proporcionando una descripción más precisa de los glóbulos rojos, incluso aproximando su tamaño, "25.000 veces más pequeños que un grano fino de arena".
En la década de 1740, Vincenzo Menghini en Bolonia logró demostrar la presencia de hierro al pasar imanes sobre el polvo o las cenizas que quedaban de los glóbulos rojos calentados.
En 1901, Karl Landsteiner publicó su descubrimiento de los tres grupos sanguíneos principales : A, B y C (que más tarde rebautizó como O). Landsteiner describió los patrones regulares en que se producían las reacciones cuando se mezclaba suero con glóbulos rojos, identificando así combinaciones compatibles y conflictivas entre estos grupos sanguíneos. Un año después, Alfred von Decastello y Adriano Sturli, dos colegas de Landsteiner, identificaron un cuarto grupo sanguíneo: AB.
En 1959, mediante el uso de cristalografía de rayos X , Max Perutz pudo desentrañar la estructura de la hemoglobina , la proteína de los glóbulos rojos que transporta el oxígeno. [72]
Los glóbulos rojos intactos más antiguos que se han descubierto se encontraron en Ötzi , el hombre de hielo, una momia natural de un hombre que murió alrededor del año 3255 a. C. Estas células se descubrieron en mayo de 2012. [73]
es de 1:1 cuando se consumen carbohidratos y es tan baja como 0,7 cuando se consumen grasas.
Estado ácido-base: El transporte de CO2 tiene un profundo efecto en el estado ácido-base de la sangre y del organismo en su conjunto. Los pulmones excretan más de 10.000 mEq de ácido carbónico al día, en comparación con menos de 100 mEq de ácidos fijados por los riñones.
con el agua en los glóbulos rojos: efecto de la anhidrasa carbónica
cataliza la reacción entre el dióxido de carbono y el agua.
[La anhidrasa carbónica] hace que la reacción vaya hacia la derecha aproximadamente 13000 veces más rápido.
En el plasma, aproximadamente el 5% del CO2 se encuentra en solución física: el 94% como bicarbonato y el 1% como compuestos carbamino; en los eritrocitos, las cifras correspondientes son el 7%, el 82% y el 11%.
de la figura 41-5, la Hgb.CO2 representa aproximadamente el 23% y el bicarbonato representa aproximadamente el 70% del dióxido de carbono total transportado a los pulmones.
A pesar de ser una molécula más pesada, por ser más soluble, la velocidad relativa de difusión del CO2 es aproximadamente 20 veces la del O2.
porque la membrana celular es mucho menos permeable al bicarbonato que al gas disuelto).
El almacenamiento en búfer se produjo en el glóbulo rojo.
Transporte
de
CO2
de CO2 como bicarbonato
Un equipo de investigadores dirigido por la unidad de Sangre y Trasplante del Servicio Nacional de Salud (NHS) lanzó recientemente el primer ensayo clínico para transfundir glóbulos rojos cultivados en laboratorio a un ser humano vivo.