Los receptores tipo peaje ( TLR ) son una clase de proteínas que desempeñan un papel clave en el sistema inmunológico innato . Son receptores de una sola extensión generalmente expresados en células centinela como macrófagos y células dendríticas , que reconocen moléculas estructuralmente conservadas derivadas de microbios . Una vez que estos microbios han alcanzado barreras físicas como la piel o la mucosa del tracto intestinal , son reconocidos por los TLR, que activan las respuestas de las células inmunitarias . Los TLR incluyen TLR1 , TLR2 , TLR3 , TLR4 , TLR5 , TLR6 , TLR7 , TLR8 , TLR9 , TLR10 , TLR11 , TLR12 y TLR13. Los humanos carecen de genes para TLR11, TLR12 y TLR13 [1] y los ratones carecen de un gen funcional para TLR10. [2] Los receptores TLR1, TLR2, TLR4, TLR5, TLR6 y TLR10 están ubicados en la membrana celular , mientras que TLR3, TLR7, TLR8 y TLR9 están ubicados en vesículas intracelulares (porque son sensores de ácidos nucleicos ). [3]
Los TLR recibieron su nombre por su similitud con la proteína codificada por el gen toll . [4]
La capacidad del sistema inmunitario para reconocer moléculas que comparten ampliamente los patógenos se debe, en parte, a la presencia de receptores inmunitarios llamados receptores tipo peaje (TLR) que se expresan en las membranas de los leucocitos, incluidas las células dendríticas , los macrófagos y las células naturales. células asesinas , células de la inmunidad adaptativa , células T y células B , y células no inmunes ( células epiteliales y endoteliales , y fibroblastos ). [5]
La unión de ligandos -ya sea en forma de adyuvante utilizado en vacunas o en forma de fracciones invasivas durante épocas de infección natural- al TLR marca los eventos moleculares clave que en última instancia conducen a respuestas inmunes innatas y al desarrollo de respuestas inmunes adquiridas específicas de antígeno. inmunidad. [6] [7]
Tras la activación, los TLR reclutan proteínas adaptadoras (proteínas que median otras interacciones proteína-proteína) dentro del citosol de la célula inmune para propagar la vía de transducción de señales inducida por antígenos . Estas proteínas reclutadas son luego responsables de la activación posterior de otras proteínas posteriores , incluidas las proteínas quinasas (IKKi, IRAK1 , IRAK4 y TBK1 ) que amplifican aún más la señal y, en última instancia, conducen a la regulación positiva o supresión de genes que orquestan respuestas inflamatorias y otras respuestas transcripcionales. eventos. Algunos de estos eventos conducen a la producción, proliferación y supervivencia de citoquinas , mientras que otros conducen a una mayor inmunidad adaptativa. [7] Si el ligando es un factor bacteriano, el patógeno podría ser fagocitado y digerido, y sus antígenos podrían presentarse a las células T CD4+ . En el caso de un factor viral, la célula infectada puede interrumpir su síntesis de proteínas y sufrir una muerte celular programada ( apoptosis ). Las células inmunes que han detectado un virus también pueden liberar factores antivirales como los interferones .
También se ha demostrado que los receptores tipo peaje son un vínculo importante entre la inmunidad innata y adaptativa a través de su presencia en las células dendríticas . [8] La flagelina , un ligando de TLR5, induce la secreción de citocinas al interactuar con TLR5 en las células T humanas. [8]

Los TLR son un tipo de receptor de reconocimiento de patrones (PRR) y reconocen moléculas que los patógenos comparten ampliamente pero que se distinguen de las moléculas del huésped, denominadas colectivamente patrones moleculares asociados a patógenos (PAMP). Además del reconocimiento de PAMP exógenos, los TLR también pueden unirse a patrones moleculares asociados a daños endógenos (DAMP), como las proteínas de choque térmico (HSP) o los constituyentes de la membrana plasmática. [9] Los TLR junto con los receptores de interleucina-1 forman una superfamilia de receptores , conocida como "superfamilia de receptores de interleucina-1/receptores tipo peaje"; Todos los miembros de esta familia tienen en común el llamado dominio TIR (receptor de IL-1 de peaje).
Existen tres subgrupos de dominios TIR. Las proteínas con dominios TIR del subgrupo 1 son receptores de interleucinas producidas por macrófagos , monocitos y células dendríticas y todas tienen dominios de inmunoglobulina (Ig) extracelulares. Las proteínas con dominios TIR del subgrupo 2 son TLR clásicos y se unen directa o indirectamente a moléculas de origen microbiano. Un tercer subgrupo de proteínas que contienen dominios TIR consta de proteínas adaptadoras que son exclusivamente citosólicas y median la señalización de proteínas de los subgrupos 1 y 2.
Los TLR están presentes tanto en vertebrados como en invertebrados . Los componentes moleculares de los TLR están representados en bacterias y plantas, y se sabe que los receptores de reconocimiento de patrones vegetales son necesarios para la defensa del huésped contra las infecciones. Por tanto, los TLR parecen ser uno de los componentes más antiguos y conservados del sistema inmunológico .
En los últimos años también se han identificado TLR en el sistema nervioso de los mamíferos. Se detectaron miembros de la familia TLR en la glía, las neuronas y las células progenitoras neurales en las que regulan la decisión del destino celular. [10]
Se ha estimado que la mayoría de las especies de mamíferos tienen entre diez y quince tipos de receptores tipo peaje. Se han identificado trece TLR (llamados simplemente TLR1 a TLR13) en humanos y ratones juntos, y se han encontrado formas equivalentes de muchos de ellos en otras especies de mamíferos. [11] [12] [13] Sin embargo, los equivalentes de ciertos TLR que se encuentran en humanos no están presentes en todos los mamíferos. Por ejemplo, un gen que codifica una proteína análoga a TLR10 en humanos está presente en ratones , pero parece haber sido dañado en algún momento del pasado por un retrovirus . Por otro lado, los ratones expresan los TLR 11, 12 y 13, ninguno de los cuales está representado en humanos. Otros mamíferos pueden expresar TLR que no se encuentran en los humanos. Otras especies no mamíferas pueden tener TLR distintos de los de los mamíferos, como lo demuestra el TLR14 anti-pared celular, que se encuentra en el pez globo Takifugu . [14] Esto puede complicar el proceso de utilizar animales de experimentación como modelos de inmunidad innata humana.
Los TLR de vertebrados se dividen por similitud en las familias de TLR 1/2/6/10/14/15, TLR 3, TLR 4, TLR 5, TLR 7/8/9 y TLR 11/12/13/16/21. /22/23. [14]

La implicación de la señalización de peaje en la inmunidad se demostró por primera vez en la mosca de la fruta, Drosophila melanogaster . [19] Las moscas de la fruta solo tienen respuestas inmunes innatas, lo que permite que los estudios eviten la interferencia de los mecanismos inmunes adaptativos en la transducción de señales. La respuesta de las moscas a una infección fúngica o bacteriana se produce a través de dos cascadas de señalización distintas, una de las cuales es la vía del peaje y la otra es la vía de la inmunodeficiencia . La vía de peaje es similar a la señalización de TLR de mamíferos, pero a diferencia de los TLR de mamíferos, el peaje no se activa directamente mediante patrones moleculares asociados a patógenos ( PAMP ). Su ectodominio receptor reconoce la forma escindida de la citocina spätzle, que se secreta en la hemolinfa como precursor dimérico inactivo. El receptor de peaje comparte el dominio TIR citoplasmático con los TLR de mamíferos, pero el ectodominio y la cola intracitoplasmática son diferentes. Esta diferencia podría reflejar una función de estos receptores como receptores de citoquinas en lugar de PRR .
La vía del peaje se activa ante diferentes estímulos, como bacterias grampositivas , hongos y factores de virulencia . [17] [20] Primero, la enzima procesadora de Spätzle (SPE) se activa en respuesta a la infección y escinde el spätzle ( spz ). El spätzle escindido luego se une al receptor de peaje y entrecruza sus ectodominios. Esto desencadena cambios conformacionales en el receptor que dan como resultado la señalización a través del peaje. A partir de ahora, la cascada de señalización es muy similar a la señalización de los mamíferos a través de los TLR. El complejo de señalización inducida por peaje (TICS) está compuesto por MyD88 , Tube y Pelle (el ortólogo del mamífero IRAK). La señal de TICS luego se transduce a Cactus (homólogo del IκB de mamífero ), el Cactus fosforilado se poliubiquitila y degrada, lo que permite la translocación nuclear de DIF (factor de inmunidad relacionado con la parte dorsal; un homólogo del NF-κB de mamífero ) y la inducción de la transcripción de genes antimicrobianos. péptidos (AMP) como la drosomicina . [21]
Drosophila tiene un total de 9 genes de la familia toll y 6 de la familia spz que interactúan entre sí en diferentes grados. [22]
TLR2 también ha sido designado como CD282 (grupo de diferenciación 282).
TLR3 no utiliza la vía dependiente de MyD88. Su ligando es el ARN bicatenario retroviral ( dsRNA ), que activa la vía de señalización dependiente de TRIF . Para explorar el papel de esta vía en la reprogramación retroviral, se prepararon técnicas de eliminación de TLR3 o TRIF, y los resultados mostraron que solo se requiere la vía TLR3 para la inducción completa de la expresión del gen objetivo por parte del vector de expresión del retrovirus. Esta expresión retroviral de cuatro factores transcripcionales ( Oct4 , Sox2 , Klf4 y c-Myc ; OSKM) induce pluripotencia en las células somáticas. Esto está respaldado por un estudio que muestra que la eficiencia y la cantidad de generación de iPSC humanas, utilizando vectores retrovirales, se reducen mediante la eliminación de la vía con inhibidores peptídicos o la eliminación del shRNA de TLR3 o su proteína adaptadora TRIF. En conjunto, la estimulación de TLR3 provoca grandes cambios en la remodelación de la cromatina y la reprogramación nuclear, y para estos cambios se requiere la activación de vías inflamatorias, la inducción de genes de pluripotencia y la generación de colonias de células madre pluripotentes inducidas por humanos (iPSC). [23]
Como se señaló anteriormente, las células humanas no expresan TLR11 , pero las células de ratón sí. "El TLR11 específico de ratón reconoce E. coli uropatógena y el parásito apicomplejo Toxoplasma gondii" . En Toxoplasma su ligando es la proteína profilina y el ligando en E. coli es la flagelina . La flagelina del enteropatógeno Salmonella también es reconocida por TLR11. [24]
Como el TLR11 de ratón es capaz de reconocer Salmonella eficazmente, los ratones normales no se infectan con Salmonella Typhi oral , que causa gastroenteritis transmitida por alimentos y agua y fiebre tifoidea en humanos. Los ratones knockout con deficiencia de TLR11 , por otro lado, se infectan eficazmente. Como resultado, este ratón knockout puede actuar como modelo de enfermedad de la fiebre tifoidea humana. [25]
Los receptores tipo peaje se unen y son activados por diferentes ligandos, que, a su vez, se encuentran en diferentes tipos de organismos o estructuras. También tienen diferentes adaptadores para responder a la activación y están ubicados a veces en la superficie celular y otras veces en los compartimentos celulares internos . [26] Además, se expresan mediante diferentes tipos de leucocitos u otros tipos de células :

Debido a la especificidad de los receptores tipo peaje (y otros receptores inmunes innatos), no pueden cambiarse fácilmente en el curso de la evolución, estos receptores reconocen moléculas que están constantemente asociadas con amenazas (es decir, patógenos o estrés celular) y son altamente específicos para estas amenazas (es decir, no pueden confundirse con moléculas propias que normalmente se expresan en condiciones fisiológicas). Se cree que las moléculas asociadas a patógenos que cumplen este requisito son fundamentales para la función del patógeno y difíciles de cambiar mediante mutación; se dice que están conservados evolutivamente. Las características algo conservadas en los patógenos incluyen lipopolisacáridos (LPS), lipoproteínas , lipopéptidos y lipoarabinomanano de la superficie celular bacteriana ; proteínas como la flagelina de flagelos bacterianos ; ARN bicatenario de virus; o las islas CpG no metiladas del ADN bacteriano y viral ; y también de las islas CpG que se encuentran en los promotores del ADN eucariota; así como algunas otras moléculas de ARN y ADN. Como los ligandos de TLR están presentes en la mayoría de los patógenos, también pueden estar presentes en vacunas derivadas de patógenos (por ejemplo, vacunas triple vírica, contra la influenza y contra la polio). Se ha evaluado la capacidad inherente de los ligandos de TLR para activar distintos subconjuntos de células inmunitarias en la mayoría de las vacunas disponibles comercialmente. [46] [47] Para la mayoría de los TLR, la especificidad de reconocimiento del ligando ahora se ha establecido mediante la selección genética (también conocida como "inactivación de genes"): una técnica mediante la cual genes individuales pueden eliminarse selectivamente en ratones. [48] [49] Consulte la tabla anterior para obtener un resumen de los ligandos de TLR conocidos.
La respuesta inflamatoria estereotipada provocada por la activación de los receptores tipo peaje ha provocado la especulación de que los activadores endógenos de los receptores tipo peaje podrían participar en enfermedades autoinmunes. Se sospecha que los TLR se unen a moléculas del huésped, incluido el fibrinógeno (implicado en la coagulación de la sangre ), proteínas de choque térmico (HSP), HMGB1 , componentes de la matriz extracelular y ADN propio (normalmente se degrada mediante nucleasas, pero en condiciones inflamatorias y autoinmunes puede formarse). un complejo con proteínas endógenas, se vuelven resistentes a estas nucleasas y obtienen acceso a TLR endosómicos como TLR7 o TLR9). Estos ligandos endógenos suelen producirse como resultado de una muerte celular no fisiológica. [50]
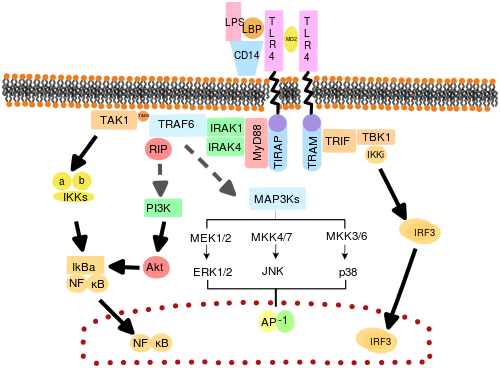
Se cree que los TLR funcionan como dímeros . Aunque la mayoría de los TLR parecen funcionar como homodímeros , el TLR2 forma heterodímeros con TLR1 o TLR6, y cada dímero tiene una especificidad de ligando diferente. Los TLR también pueden depender de otros correceptores para una sensibilidad total al ligando, como en el caso del reconocimiento de LPS por parte de TLR4 , que requiere MD-2. Se sabe que CD14 y la proteína de unión a LPS ( LBP ) facilitan la presentación de LPS a MD-2.
Un conjunto de TLR endosómicos que comprende TLR3, TLR7, TLR8 y TLR9 reconocen ácidos nucleicos derivados de virus, así como ácidos nucleicos endógenos en el contexto de eventos patógenos. La activación de estos receptores conduce a la producción de citocinas inflamatorias , así como de interferones tipo I ( interferón tipo I ) para ayudar a combatir las infecciones virales.
También se han atacado las proteínas adaptadoras y las quinasas que median la señalización de TLR. Además, se ha utilizado mutagénesis aleatoria de la línea germinal con ENU para descifrar las vías de señalización de los TLR. Cuando se activan, los TLR reclutan moléculas adaptadoras dentro del citoplasma de las células para propagar una señal. Se sabe que cuatro moléculas adaptadoras participan en la señalización. Estas proteínas se conocen como MyD88 , TIRAP (también llamada Mal), TRIF y TRAM (molécula adaptadora relacionada con TRIF). [51] [52] [53]
La señalización de TLR se divide en dos vías de señalización distintas, la vía dependiente de MyD88 y la vía dependiente de TRIF.
La respuesta dependiente de MyD88 se produce en la dimerización de los TLR y es utilizada por todos los TLR excepto por el TLR3. Su efecto principal es la activación de NFκB y de la proteína quinasa activada por mitógenos . La unión del ligando y el cambio conformacional que se produce en el receptor reclutan la proteína adaptadora MyD88, un miembro de la familia TIR . MyD88 luego recluta IRAK4 , IRAK1 e IRAK2 . Las quinasas IRAK luego fosforilan y activan la proteína TRAF6 , que a su vez poliubiquina la proteína TAK1, así como a sí misma para facilitar la unión a IKK-β . Al unirse, TAK1 fosforila IKK-β, que luego fosforila IκB provocando su degradación y permitiendo que NFκB se difunda hacia el núcleo celular y active la transcripción y la consiguiente inducción de citoquinas inflamatorias. [50]
Tanto TLR3 como TLR4 utilizan la vía dependiente de TRIF, que se activa mediante dsRNA y LPS, respectivamente. Para TLR3, el dsRNA conduce a la activación del receptor, reclutando el adaptador TRIF . TRIF activa las quinasas TBK1 y RIPK1 , lo que crea una rama en la vía de señalización. El complejo de señalización TRIF/TBK1 fosforila IRF3 permitiendo su translocación al núcleo y la producción de interferón tipo I. Mientras tanto, la activación de RIPK1 provoca la poliubiquitinación y la activación de la transcripción de TAK1 y NFκB de la misma manera que la vía dependiente de MyD88. [50]
La señalización de TLR conduce en última instancia a la inducción o supresión de genes que orquestan la respuesta inflamatoria. En total, miles de genes se activan mediante la señalización de TLR y, en conjunto, los TLR constituyen una de las puertas de entrada más pleiotrópicas pero estrechamente reguladas para la modulación genética.
TLR4 es el único TLR que utiliza los cuatro adaptadores. El complejo que consta de TLR4, MD2 y LPS recluta adaptadores que contienen el dominio TIR TIRAP y MyD88 y, por lo tanto, inicia la activación de NFκB (fase temprana) y MAPK. El complejo TLR4-MD2-LPS luego sufre endocitosis y en el endosoma forma un complejo de señalización con adaptadores TRAM y TRIF. Esta vía dependiente de TRIF conduce nuevamente a la activación de IRF3 y a la producción de interferones tipo I, pero también activa la activación de NFκB de fase tardía. Se requiere la activación de NFκB tanto en la fase tardía como en la temprana para la producción de citoquinas inflamatorias. [50]
El imiquimod (utilizado cardinalmente en dermatología ) es un agonista de TLR7, y su sucesor, el resiquimod , es un agonista de TLR7 y TLR8. [54] Recientemente, se ha explorado el resiquimod como agente para la inmunoterapia contra el cáncer, [55] actuando mediante la estimulación de macrófagos asociados a tumores.
Varios ligandos de TLR están en desarrollo clínico o se están probando en modelos animales como adyuvantes de vacunas , [56] con el primer uso clínico en humanos en una vacuna recombinante contra el herpes zoster en 2017, que contiene un componente de monofosforil lípido A.
Se han informado niveles de expresión del ARN mensajero de TLR7 en animales lecheros en un brote natural de fiebre aftosa. [57]
Se ha demostrado que TLR4 es importante para los efectos secundarios a largo plazo de los opioides . Su activación conduce a la liberación de moduladores inflamatorios, incluidos TNF-α e IL-1β , y se cree que la liberación constante de bajo nivel de estos moduladores reduce la eficacia del tratamiento con medicamentos opioides con el tiempo y está involucrada en la tolerancia a los opioides [58]. [59] hiperalgesia y alodinia . [60] [61] La activación de TLR4 inducida por morfina atenúa la supresión del dolor por los opioides y mejora el desarrollo de la tolerancia y adicción a los opioides , el abuso de drogas y otros efectos secundarios negativos como la depresión respiratoria y la hiperalgesia. [62] Se ha demostrado que los medicamentos que bloquean la acción del TNF-α o IL-1β aumentan los efectos analgésicos de los opioides y reducen el desarrollo de tolerancia y otros efectos secundarios, [63] [64] y esto también se ha demostrado con medicamentos que bloquean el propio TLR4.
Los enantiómeros "no naturales" de los fármacos opioides como la (+)-morfina y la (+)-naloxona carecen de afinidad por los receptores opioides y aún producen la misma actividad en TLR4 que sus enantiómeros "normales". [65] [66] Por lo tanto, los entianómeros "no naturales" de opioides, como la (+)-naloxona, se pueden usar para bloquear la actividad TLR4 de los analgésicos opioides sin tener ninguna afinidad por el receptor μ-opioide [67] [66] [ 68]
Cuando se reconoció por primera vez a los microbios como la causa de enfermedades infecciosas, inmediatamente quedó claro que los organismos multicelulares debían ser capaces de reconocerlos cuando estaban infectados y, por tanto, debían ser capaces de reconocer moléculas exclusivas de los microbios. Una gran cantidad de literatura, que abarca la mayor parte del siglo pasado, da fe de la búsqueda de moléculas clave y sus receptores. Hace más de 100 años, Richard Pfeiffer , alumno de Robert Koch , acuñó el término " endotoxina " para describir una sustancia producida por bacterias Gram-negativas que podía provocar fiebre y shock en animales de experimentación . En las décadas siguientes, la endotoxina se caracterizó e identificó químicamente como un lipopolisacárido (LPS) producido por la mayoría de las bacterias Gram negativas. Este lipopolisacárido es parte integral de la membrana gramnegativa y se libera tras la destrucción de la bacteria. Se demostró que otras moléculas ( lipopéptidos bacterianos , flagelina y ADN no metilado ) provocan a su vez respuestas del huésped que normalmente son protectoras. Sin embargo, estas respuestas pueden resultar perjudiciales si son excesivamente prolongadas o intensas. Lógicamente, debía haber receptores para tales moléculas, capaces de alertar al huésped de la presencia de infección, pero estos siguieron siendo difíciles de alcanzar durante muchos años. Los receptores tipo peaje se cuentan ahora entre las moléculas clave que alertan al sistema inmunológico sobre la presencia de infecciones microbianas.
El miembro prototípico de la familia, el receptor de peaje ( P08953 ; Tl) en la mosca de la fruta Drosophila melanogaster , fue descubierto en 1985 por los premios Nobel de 1995 Christiane Nüsslein-Volhard y Eric Wieschaus y sus colegas. Era conocido por su función de desarrollo en la embriogénesis al establecer el eje dorsal - ventral . Debe su nombre a la exclamación de Christiane Nüsslein-Volhard de 1985: " Das ist ja toll! " ("¡Eso es asombroso!"), en referencia a la porción ventral subdesarrollada de una larva de mosca de la fruta. [4] Fue clonado por el laboratorio de Kathryn Anderson en 1988. [69] En 1996, Jules A. Hoffmann y sus colegas descubrieron que el peaje tenía un papel esencial en la inmunidad de la mosca a la infección por hongos , que lograba activando la síntesis de péptidos antimicrobianos. [19]
El primer receptor humano tipo toll fue descrito por Nomura y sus colegas en 1994, [70] mapeado en un cromosoma por Taguchi y sus colegas en 1996. [71] Debido a que en ese entonces no se conocía la función inmune de toll en Drosophila , se asumió que TIL (ahora conocido como TLR1) podría participar en el desarrollo de los mamíferos. Sin embargo, en 1991 (antes del descubrimiento de TIL) se observó que una molécula con un claro papel en la función inmune en mamíferos, el receptor de interleucina-1 (IL-1), también tenía homología con Drosophila toll; las porciones citoplasmáticas de ambas moléculas eran similares. [72]
En 1997, Charles Janeway y Ruslan Medzhitov demostraron que un receptor tipo peaje ahora conocido como TLR4 podría, cuando se ligaba artificialmente mediante anticuerpos, inducir la activación de ciertos genes necesarios para iniciar una respuesta inmune adaptativa . [7] Bruce A. Beutler y sus colegas descubrieron la función TLR 4 como receptor sensor de LPS . [73] Estos trabajadores utilizaron la clonación posicional para demostrar que los ratones que no podían responder al LPS tenían mutaciones que abolían la función de TLR4. Esto identificó a TLR4 como uno de los componentes clave del receptor de LPS.

A su vez, los otros genes TLR fueron eliminados en ratones mediante selección genética, principalmente en el laboratorio de Shizuo Akira y sus colegas. Actualmente se cree que cada TLR detecta un conjunto discreto de moléculas (algunas de origen microbiano y otras productos del daño celular) y señala la presencia de infecciones. [74]
Los homólogos de plantas de peaje fueron descubiertos por Pamela Ronald en 1995 (arroz XA21) [75] y Thomas Boller en 2000 ( Arabidopsis FLS2). [76]
En 2011, Beutler y Hoffmann recibieron el Premio Nobel de Medicina o Fisiología por su trabajo. [77] Hoffmann y Akira recibieron el Premio Internacional Gairdner de Canadá en 2011. [78]
En términos generales, los TLR 1, 2, 4 a 6 y 10 se expresan en la membrana plasmática, y los TLR 3, 7 a 9 y 11 a 13 están confinados a los endosomas.
{{cite journal}}: Mantenimiento CS1: ubicación ( enlace )