El síndrome de X frágil ( FXS ) es un trastorno genético caracterizado por una discapacidad intelectual de leve a moderada . [1] El coeficiente intelectual promedio en hombres con FXS es inferior a 55, mientras que aproximadamente dos tercios de las mujeres afectadas tienen discapacidad intelectual. [3] [4] Las características físicas pueden incluir una cara larga y estrecha , orejas grandes, dedos flexibles y testículos grandes . [1] Aproximadamente un tercio de los afectados tienen características del autismo , como problemas con las interacciones sociales y retraso en el habla. [1] La hiperactividad es común y las convulsiones ocurren en aproximadamente el 10%. [1] Los hombres suelen verse más afectados que las mujeres. [1]
Este trastorno y hallazgo del síndrome de X frágil tiene una herencia dominante ligada al cromosoma X. [1] Por lo general , es causada por una expansión de la repetición del triplete CGG dentro del gen FMR1 (ribonucleoproteína 1 mensajera del X frágil) en el cromosoma X. [1] Esto da como resultado el silenciamiento ( metilación ) de esta parte del gen y una deficiencia de la proteína resultante (FMRP), que es necesaria para el desarrollo normal de las conexiones entre las neuronas . [1] El diagnóstico requiere pruebas genéticas para determinar el número de repeticiones CGG en el gen FMR1 . [5] Normalmente, hay entre 5 y 40 repeticiones; El síndrome del X frágil ocurre con más de 200. [1] Se dice que una premutación está presente cuando el gen tiene entre 55 y 200 repeticiones; Las mujeres con una premutación tienen un mayor riesgo de tener un hijo afectado. [1] Las pruebas para detectar portadores de premutaciones pueden permitir el asesoramiento genético . [5]
No existe cura. [2] Se recomienda la intervención temprana, ya que brinda la mayor oportunidad para desarrollar una gama completa de habilidades. [6] Estas intervenciones pueden incluir educación especial , terapia del habla , fisioterapia o terapia conductual . [2] [7] Se pueden usar medicamentos para tratar las convulsiones asociadas , los problemas del estado de ánimo, el comportamiento agresivo o el TDAH . [8] El síndrome X frágil tiende a mostrar más síntomas en los hombres afectados, ya que las mujeres tienen otro cromosoma X que puede compensar el dañado. [4] [9]

La mayoría de los niños pequeños no muestran ningún signo físico de FXS. [10] No es hasta la pubertad que las características físicas del FXS comienzan a desarrollarse. [10] Además de la discapacidad intelectual, las características destacadas del síndrome pueden incluir una cara alargada, orejas grandes o salientes , pies planos, testículos más grandes ( macroorquidia ) y tono muscular bajo . [11] [12] La otitis media recurrente (infección del oído medio) y la sinusitis son comunes durante la primera infancia. El habla puede ser confusa o nerviosa. Las características de comportamiento pueden incluir movimientos estereotipados (p. ej., aleteo de las manos) y desarrollo social atípico, particularmente timidez, contacto visual limitado, problemas de memoria y dificultad con la codificación facial. Algunas personas con síndrome de X frágil también cumplen con los criterios de diagnóstico del autismo . [13]
Los hombres con una mutación completa muestran una penetrancia prácticamente completa y, por lo tanto, casi siempre mostrarán síntomas de FXS, mientras que las mujeres con una mutación completa generalmente muestran una penetrancia de aproximadamente el 50 % como resultado de tener un segundo cromosoma X normal. [14] Las mujeres con FXS pueden tener síntomas que varían de leves a graves, aunque generalmente se ven menos afectadas que los hombres debido a la variabilidad en la inactivación de X. [15] [16]
Las personas con FXS pueden presentarse en cualquier lugar de un espectro que va desde problemas de aprendizaje en el contexto de un cociente intelectual (CI) normal hasta discapacidad intelectual grave , con un coeficiente intelectual promedio de 40 en hombres que tienen un silenciamiento completo del gen FMR1 . [12] Las mujeres, que tienden a verse menos afectadas, generalmente tienen un coeficiente intelectual normal o al borde de las dificultades de aprendizaje. Las principales dificultades en las personas con FXS son con la memoria de trabajo y a corto plazo, la función ejecutiva , la memoria visual, las relaciones visoespaciales y las matemáticas, y las habilidades verbales no se ven relativamente afectadas. [12] [20]
Los datos sobre el desarrollo intelectual en FXS son limitados. Sin embargo, existe cierta evidencia de que el coeficiente intelectual estandarizado disminuye con el tiempo en la mayoría de los casos, aparentemente como resultado de un desarrollo intelectual más lento. Un estudio longitudinal que analizó pares de hermanos en los que un niño estaba afectado y el otro no encontró que los niños afectados tuvieran una tasa de aprendizaje intelectual que fuera un 55% más lenta que la de los niños no afectados. [20]
Las personas con FXS a menudo demostraron problemas de lenguaje y comunicación. [21] Esto puede estar relacionado con la función muscular de la boca y los déficits del lóbulo frontal. [21]
El síndrome de X frágil coexiste con el autismo en muchos casos y se sospecha que es una causa genética del autismo en estos casos. [11] [22] Este hallazgo ha dado lugar a que la detección de la mutación FMR1 se considere obligatoria en niños diagnosticados con autismo. [11] Entre las personas con síndrome de X frágil, se ha estimado que la prevalencia del trastorno del espectro autista (TEA) concurrente está entre el 15 y el 60 %, y la variación se debe a diferencias en los métodos de diagnóstico y a la alta frecuencia de características autistas en personas con síndrome de X frágil. El síndrome X no cumple con los criterios del DSM para un TEA. [22]
Aunque las personas con FXS tienen dificultades para formar amistades, aquellos con FXS y TEA también tienen dificultades para mantener conversaciones recíprocas con sus compañeros. Las conductas de retraimiento social, incluidas la evitación y la indiferencia, parecen ser los mejores predictores del TEA en el FXS, y la evitación parece estar más correlacionada con la ansiedad social, mientras que la indiferencia se correlaciona más fuertemente con el TEA. [22] Cuando tanto el autismo como el FXS están presentes, se observa un mayor déficit de lenguaje y un coeficiente intelectual más bajo en comparación con los niños con FXS solo. [23]
También se ha demostrado que los modelos genéticos de ratón con FXS tienen comportamientos similares al autismo. [24] [25] [26] [27] [28]
El FXS se caracteriza por ansiedad social , que incluye contacto visual deficiente, aversión a la mirada, tiempo prolongado para comenzar la interacción social y dificultades para establecer relaciones con pares. [29] La ansiedad social es una de las características más comunes asociadas con el FXS, y hasta el 75% de los hombres en una serie se caracterizan por tener timidez excesiva y el 50% tienen ataques de pánico. [22] La ansiedad social en personas con FXS está relacionada con desafíos con la codificación facial, la capacidad de reconocer una cara que uno ha visto antes. [30]
Parece que las personas con FXS están interesadas en la interacción social y muestran mayor empatía que los grupos con otras causas de discapacidad intelectual, pero muestran ansiedad y retraimiento cuando se les coloca en situaciones desconocidas con personas desconocidas. [22] [29] Esto puede variar desde un retraimiento social leve, que se asocia predominantemente con la timidez, hasta un retraimiento social severo, que puede estar asociado con un trastorno del espectro autista coexistente. [22]
Las mujeres con FXS frecuentemente muestran timidez, ansiedad social y evitación o retraimiento social. [12] Además, se ha descubierto que la premutación en las mujeres está asociada con la ansiedad social.
Las mujeres con FXS muestran una activación disminuida en las regiones prefrontales del cerebro. [31] [ cita necesaria ]
El trastorno por déficit de atención con hiperactividad (TDAH) se encuentra en la mayoría de los hombres con FXS y en el 30% de las mujeres, lo que lo convierte en el diagnóstico psiquiátrico más común en personas con FXS. [11] [29] Los niños con X frágil tienen períodos de atención muy cortos, son hiperactivos y muestran hipersensibilidad a los estímulos visuales, auditivos, táctiles y olfativos . Estos niños tienen dificultades en grandes multitudes debido a los ruidos fuertes y esto puede provocar rabietas debido a la hiperexcitación . La hiperactividad y el comportamiento disruptivo alcanzan su punto máximo en los años preescolares y luego disminuyen gradualmente con la edad, aunque los síntomas de falta de atención generalmente duran toda la vida. [29]
Aparte de los rasgos característicos de la fobia social, una variedad de otros síntomas de ansiedad se asocian muy comúnmente con el FXS, y los síntomas generalmente abarcan varios diagnósticos psiquiátricos pero no cumplen ninguno de los criterios en su totalidad. [29] Los niños con FXS se alejan del contacto ligero y pueden encontrar irritantes las texturas de los materiales. Las transiciones de un lugar a otro pueden resultar difíciles para los niños con FXS. En algunos casos, se puede utilizar la terapia conductual para disminuir la sensibilidad del niño. [19] Comportamientos como agitar las manos y morder, así como la agresión, pueden ser una expresión de ansiedad. [ cita necesaria ]
La perseveración es una característica comunicativa y de comportamiento común en el FXS. Los niños con FXS pueden repetir una determinada actividad ordinaria una y otra vez. En el habla la tendencia no es sólo repetir la misma frase sino también hablar continuamente del mismo tema. Es común observar un habla y un diálogo interno desordenados . El diálogo interno incluye hablar con uno mismo usando diferentes tonos y tonos. [19] Aunque sólo una minoría de los casos de FXS cumplirán los criterios del trastorno obsesivo-compulsivo (TOC), una mayoría significativa tendrá síntomas de obsesión. Sin embargo, como las personas con FXS generalmente encuentran placenteras estas conductas, a diferencia de las personas con TOC, se las denomina con mayor frecuencia conductas estereotipadas. [ cita necesaria ]
Los síntomas del estado de ánimo en personas con FXS rara vez cumplen con los criterios de diagnóstico de un trastorno del estado de ánimo importante, ya que generalmente no tienen una duración sostenida. [29] En cambio, estos suelen ser transitorios y están relacionados con factores estresantes, y pueden implicar un estado de ánimo lábil (fluctuante), irritabilidad, autolesiones y agresión. [ cita necesaria ]
Es probable que las personas con síndrome de ataxia/temblor asociado al cromosoma X frágil (FXTAS, por sus siglas en inglés) experimenten combinaciones de demencia , trastornos del estado de ánimo y de ansiedad . Se encontró que los hombres con la premutación FMR1 y evidencia clínica de FXTAS tenían una mayor aparición de somatización , trastorno obsesivo-compulsivo , sensibilidad interpersonal, depresión, ansiedad fóbica y psicoticismo . [32]
Los problemas oftalmológicos incluyen el estrabismo . Esto requiere una identificación temprana para evitar la ambliopía . Por lo general, se necesita cirugía o parches para tratar el estrabismo si se diagnostica a tiempo. Los errores de refracción en pacientes con FXS también son comunes. [23]
Las personas con FXS tienen un mayor riesgo de desarrollar convulsiones , con tasas reportadas en la literatura entre el 10% y el 40%. [33] En poblaciones de estudio más grandes, la frecuencia varía entre 13% y 18%, [12] [33] en consonancia con una encuesta reciente de cuidadores que encontró que el 14% de los hombres y el 6% de las mujeres experimentaron convulsiones. [33] Las convulsiones tienden a ser parciales , generalmente no son frecuentes y son susceptibles de tratamiento con medicamentos. [ cita necesaria ]
Las personas que son portadoras de alelos de premutación corren el riesgo de desarrollar el síndrome de ataxia/temblor asociado al cromosoma X frágil (FXTAS), una enfermedad neurodegenerativa progresiva. [14] [34] Se observa en aproximadamente la mitad de los portadores masculinos mayores de 70 años, mientras que la penetrancia en las mujeres es menor. Por lo general, el inicio del temblor ocurre en la sexta década de la vida, con la posterior progresión a ataxia (pérdida de coordinación) y deterioro cognitivo gradual. [34]
A partir de los 40 años, los hombres con FXS comienzan a desarrollar problemas progresivamente más graves al realizar tareas que requieren el ejecutivo central de la memoria de trabajo . La memoria de trabajo implica el almacenamiento temporal de información "en la mente", mientras se procesa la misma información u otra. La memoria fonológica (o memoria de trabajo verbal) se deteriora con la edad en los hombres, mientras que la memoria visoespacial no está directamente relacionada con la edad. Los varones suelen experimentar un deterioro en el funcionamiento del bucle fonológico . La longitud del CGG se correlaciona significativamente con el ejecutivo central y la memoria visoespacial. Sin embargo, en un individuo con premutación, la longitud de CGG solo se correlaciona significativamente con el ejecutivo central, no con la memoria fonológica ni con la memoria visoespacial. [35]
Alrededor del 20% de las mujeres portadoras de la premutación del X frágil se ven afectadas por insuficiencia ovárica primaria relacionada con el X frágil (FXPOI) , que se define como menopausia prematura , que es la menopausia que ocurre antes de los 40 años de edad (la edad promedio en la menopausia es de 51 años). años en Estados Unidos). [14] [34] El número de repeticiones CGG se correlaciona con la penetrancia y la edad de aparición, pero no es una relación lineal. [36] [14] Sin embargo, la menopausia prematura es más común en portadoras de premutación que en mujeres con la mutación completa, y el mayor riesgo de FXPOI se observa en mujeres con entre 70 y 100 repeticiones de riesgo de FXPOI. [37] [38] La insuficiencia ovárica primaria asociada al cromosoma X frágil (FXPOI) es uno de los tres trastornos asociados al cromosoma X frágil (FXD) causados por cambios en el gen FMR1. FXPOI afecta a mujeres portadoras de una premutación, causada por el gen FMR1, cuando sus ovarios no funcionan correctamente. Las mujeres con FXPOI pueden presentar cambios en los ciclos menstruales y cambios en los niveles hormonales, pero no se las considera menopáusicas. Las mujeres con FXPOI todavía tienen la posibilidad de quedar embarazadas en aproximadamente el 10% de los casos, porque sus ovarios ocasionalmente liberan óvulos viables a través de la ovulación de "escape". [39] [40]
FMRP es una proteína de unión a cromatina que actúa en la respuesta al daño del ADN . [41] [42] FMRP también ocupa sitios en los cromosomas meióticos y regula la dinámica de la maquinaria de respuesta al daño del ADN durante la espermatogénesis . [41]
El síndrome de X frágil es un trastorno genético que se produce como resultado de una mutación del gen de la ribonucleoproteína 1 mensajera del cromosoma X frágil ( FMR1 ) en el cromosoma X , más comúnmente un aumento en el número de repeticiones del trinucleótido CGG en la región 5' no traducida de FMR1. . [14] [34] La mutación en ese sitio se encuentra en 1 de cada 2000 hombres y 1 de cada 259 mujeres . La incidencia del trastorno en sí es aproximadamente de 1 de cada 3.600 hombres y de 1 de cada 4.000 a 6.000 mujeres. [43] Aunque esto representa más del 98% de los casos, el FXS también puede ocurrir como resultado de mutaciones puntuales que afectan a FMR1 . [14] [34]
En individuos no afectados, el gen FMR1 contiene de 5 a 44 repeticiones de la secuencia CGG, más comúnmente 29 o 30 repeticiones. [14] [34] [44] Entre 45 y 54 repeticiones se considera una "zona gris", y generalmente se considera que un alelo de premutación tiene entre 55 y 200 repeticiones de longitud. Los individuos con síndrome de X frágil tienen una mutación completa del alelo FMR1 , con más de 200 repeticiones CGG. [11] [44] [45] En estos individuos con una expansión repetida superior a 200, hay metilación de la expansión repetida CGG y del promotor FMR1 , lo que lleva al silenciamiento del gen FMR1 y a la falta de su producto.
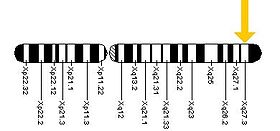
Se cree que esta metilación de FMR1 en la banda del cromosoma Xq27.3 da como resultado la constricción del cromosoma X, que parece "frágil" bajo el microscopio en ese punto, un fenómeno que dio nombre al síndrome. Un estudio encontró que el silenciamiento de FMR1 está mediado por el ARNm de FMR1. El ARNm de FMR1 contiene el tracto de repetición CGG transcrito como parte de la región 5' no traducida, que se hibrida con la porción complementaria de repetición CGG del gen FMR1 para formar un dúplex de ARN·ADN. [46]
Se ha descubierto que un subconjunto de personas con discapacidad intelectual y síntomas que se asemejan al síndrome de X frágil tienen mutaciones puntuales en FMR1. Este subconjunto carecía de la expansión de repetición CGG en FMR1 tradicionalmente asociada con el síndrome de X frágil. [47] La primera secuencia de ADN completa de la expansión repetida en alguien con la mutación completa fue generada por científicos en 2012 utilizando la secuenciación SMRT . [48]
El síndrome de X frágil se ha considerado tradicionalmente una condición dominante ligada al cromosoma X con expresividad variable y posiblemente penetrancia reducida . [12] La probabilidad de transmisión depende del sexo de los padres, el cromosoma X que porta la mutación y el número de repeticiones CGG en la premutación.
Debido a la anticipación genética y la inactivación del cromosoma X en las mujeres, la herencia del síndrome de X frágil no sigue el patrón habitual de la herencia dominante ligada al cromosoma X, y académicos del Centro Médico de la Universidad de Chicago y del Hospital Universitario de Groningen publicaron un resumen en el American Journal of Medical Genetics que propone dejar de etiquetar los trastornos ligados al cromosoma X como dominantes o recesivos. [49] Los hombres con una mutación completa generalmente están afectados y son infértiles, mientras que las mujeres portadoras tienen un 50% de posibilidades de transmitir la mutación.
Antes de que se descubriera el gen FMR1 , el análisis de genealogías mostraba la presencia de portadores masculinos asintomáticos, y sus nietos se veían afectados por la enfermedad en mayor proporción que sus hermanos, lo que sugería que se estaba produciendo una anticipación genética . [14] Esta tendencia de que las generaciones futuras se vean afectadas con mayor frecuencia se conoció como la paradoja de Sherman después de su descripción en 1985. [14] [50] Debido a esto, los niños varones suelen tener un mayor grado de síntomas que sus madres. [51]
La explicación de este fenómeno es que los portadores masculinos transmiten su premutación a todas sus hijas, y la longitud de la repetición CGG de FMR1 generalmente no aumenta durante la meiosis , la división celular necesaria para producir espermatozoides. [14] [34] Por cierto, los machos con una mutación completa solo transmiten premutaciones a sus hijas. [34] Sin embargo, las mujeres con una mutación completa pueden transmitir esta mutación completa, por lo que, en teoría, existe un 50% de posibilidades de que un niño se vea afectado. [34] [44] Además, la duración de la repetición CGG con frecuencia aumenta durante la meiosis en mujeres portadoras de premutaciones debido a la inestabilidad y, por lo tanto, dependiendo de la duración de su premutación, pueden transmitir una mutación completa a sus hijos, quienes la heredarán. entonces verse afectado. Se considera que la expansión repetida es una consecuencia del deslizamiento de la cadena , ya sea durante la replicación del ADN o la síntesis de reparación del ADN . [52]
El mosaicismo se refiere a casos en los que los individuos tienen copias tanto de mutación completa como de premutación. El mosaicismo puede resultar de la inestabilidad en las repeticiones CGG, y los individuos afectados pueden mostrar síntomas clásicos, aunque alguna evidencia sugiere capacidades intelectuales más altas en comparación con aquellos con una mutación completa. [53]
La FMRP se encuentra en todo el cuerpo, pero en concentraciones más altas en el cerebro y los testículos. [11] [14] Parece ser el principal responsable de unirse selectivamente a alrededor del 4% del ARNm en el cerebro de los mamíferos y transportarlo fuera del núcleo celular y a las sinapsis de las neuronas . Se ha descubierto que la mayoría de estos objetivos de ARNm están ubicados en las dendritas de las neuronas, y el tejido cerebral de humanos con FXS y modelos de ratón muestra espinas dendríticas anormales , que son necesarias para aumentar el contacto con otras neuronas. Las anomalías posteriores en la formación y función de las sinapsis y el desarrollo de los circuitos neuronales dan como resultado un deterioro de la neuroplasticidad , una parte integral de la memoria y el aprendizaje. [11] [14] [54] Durante mucho tiempo se ha sospechado que los cambios en el conectoma están implicados en la fisiopatología sensorial [55] y más recientemente se ha demostrado una serie de alteraciones en los circuitos, que implican un aumento estructural de la conectividad local y una conectividad de largo alcance funcionalmente disminuida. [56]
Además, la FMRP ha estado implicada en varias vías de señalización a las que se dirigen varios fármacos que se encuentran en ensayos clínicos. La vía del receptor metabotrópico de glutamato del grupo 1 (mGluR), que incluye mGluR1 y mGluR5 , está implicada en la depresión a largo plazo (LTD) y la potenciación a largo plazo (LTP) dependientes de mGluR, los cuales son mecanismos importantes en el aprendizaje. [11] [14] La falta de FMRP, que reprime la producción de ARNm y, por tanto, la síntesis de proteínas, conduce a una LTD exagerada. FMRP también parece afectar las vías de dopamina en la corteza prefrontal, lo que se cree que resulta en déficit de atención, hiperactividad y problemas de control de impulsos asociados con el FXS. [11] [14] [29] La regulación negativa de las vías GABA , que cumplen una función inhibidora y están involucradas en el aprendizaje y la memoria, puede ser un factor en los síntomas de ansiedad que se observan comúnmente en el FXS. [ cita necesaria ]
La investigación en un modelo de ratón de FSX muestra que las neuronas corticales reciben información sensorial reducida (hiposensibilidad), contrariamente a la suposición común de que estas neuronas son hipersensibles, acompañadas de información contextual mejorada, acumulada a partir de experiencias previas. Por lo tanto, estos resultados sugieren que el fenotipo hipersensible de los individuos afectados podría surgir de una entrada contextual no coincidente en estas neuronas. [57]
El diagnóstico clínico se basa en la identificación de una variante de FMR1 asociada con una función disminuida junto con un deterioro intelectual de moderado a grave, particularmente en hombres o moderado en mujeres. Las pruebas de diagnóstico incluyen PCR para analizar el número de repeticiones CGG, análisis de transferencia Southern y examen de trinucleótidos AGG en la región del gen FMR1.
El análisis citogenético para el síndrome de X frágil estuvo disponible por primera vez a fines de la década de 1970, cuando el diagnóstico del síndrome y el estado de portador se podían determinar cultivando células en un medio deficiente en folato y luego evaluando los " sitios frágiles " (discontinuidad de la tinción en la región del trinucleótido). repetir) en el brazo largo del cromosoma X. [58] Sin embargo, esta técnica resultó poco confiable, ya que el sitio frágil a menudo se observaba en menos del 40% de las células de un individuo. Esto no fue un gran problema en los hombres, pero en las mujeres portadoras, donde el sitio frágil generalmente solo podía verse en el 10% de las células, la mutación a menudo no podía visualizarse. [ cita necesaria ]
Desde la década de 1990, se han utilizado técnicas moleculares más sensibles para determinar el estado de portador. [58] La anomalía del X frágil ahora se determina directamente mediante el análisis del número de repeticiones CGG mediante la reacción en cadena de la polimerasa (PCR) y el estado de metilación mediante análisis de transferencia Southern . [12] Al determinar el número de repeticiones CGG en el cromosoma X, este método permite una evaluación más precisa del riesgo para los portadores de premutaciones en términos de su propio riesgo de síndromes asociados al X frágil, así como su riesgo de tener hijos afectados. Debido a que este método solo prueba la expansión de la repetición CGG, las personas con FXS debido a mutaciones sin sentido o deleciones que involucran a FMR1 no serán diagnosticadas mediante esta prueba y, por lo tanto, deben someterse a la secuenciación del gen FMR1 si existe sospecha clínica de FXS. [ cita necesaria ]
Las pruebas prenatales con muestra de vellosidades coriónicas o amniocentesis permiten el diagnóstico de la mutación FMR1 mientras el feto está en el útero y parecen ser confiables. [12]
El diagnóstico temprano del síndrome de X frágil o el estado de portador es importante para brindar una intervención temprana en niños o fetos con el síndrome y permitir el asesoramiento genético con respecto a la posibilidad de que los futuros hijos de una pareja se vean afectados. La mayoría de los padres notan retrasos en las habilidades del habla y el lenguaje, dificultades en los ámbitos social y emocional, así como niveles de sensibilidad en determinadas situaciones con sus hijos. [59]
No existe cura para los defectos subyacentes del FXS. [2] El manejo del FXS puede incluir terapia del habla , terapia conductual , terapia ocupacional , educación especial o planes educativos individualizados y, cuando sea necesario, tratamiento de anomalías físicas. Se recomienda a las personas con síndrome de X frágil en sus antecedentes familiares que busquen asesoramiento genético para evaluar la probabilidad de tener hijos afectados y la gravedad de las deficiencias que puedan tener los descendientes afectados. [60]
Las tendencias actuales en el tratamiento del trastorno incluyen medicamentos para tratamientos basados en los síntomas que tienen como objetivo minimizar las características secundarias asociadas con el trastorno. Si a una persona se le diagnostica FXS, el asesoramiento genético para realizar pruebas a los miembros de la familia en riesgo de portar la mutación completa o la premutación es un primer paso fundamental. Debido a una mayor prevalencia de FXS en los niños, los medicamentos más utilizados son los estimulantes dirigidos a la hiperactividad, la impulsividad y los problemas de atención. [12] Para los trastornos comórbidos con FXS, se utilizan antidepresivos como los inhibidores selectivos de la recaptación de serotonina (ISRS) para tratar la ansiedad subyacente, las conductas obsesivo-compulsivas y los trastornos del estado de ánimo. Después de los antidepresivos, los antipsicóticos como la risperidona y la quetiapina se utilizan para tratar altas tasas de conductas autolesivas, agresivas y aberrantes en esta población (Bailey Jr et al., 2012). Los anticonvulsivos son otro conjunto de tratamientos farmacológicos que se utilizan para controlar las convulsiones y los cambios de humor en entre el 13% y el 18% de las personas con FXS. Los medicamentos dirigidos a los mGluR5 (receptores metabotrópicos de glutamato) que están relacionados con la plasticidad sináptica son especialmente beneficiosos para los síntomas específicos del FXS. [12] El litio también se está utilizando actualmente en ensayos clínicos con humanos, mostrando mejoras significativas en el funcionamiento conductual, el comportamiento adaptativo y la memoria verbal. Pocos estudios sugirieron el uso de ácido fólico, pero se necesitan más investigaciones debido a la baja calidad de esa evidencia. [61] Además de los tratamientos farmacológicos, las influencias ambientales, como el entorno del hogar y las capacidades de los padres, así como las intervenciones conductuales, como la terapia del habla, la integración sensorial, etc., se tienen en cuenta para promover el funcionamiento adaptativo de las personas con FXS. [60] Si bien la metformina puede reducir el peso corporal en personas con síndrome de X frágil, no está claro si mejora los síntomas neurológicos o psiquiátricos. [62]
El tratamiento farmacológico actual se centra en el manejo de conductas problemáticas y síntomas psiquiátricos asociados con el FXS. Sin embargo, como se han realizado muy pocas investigaciones en esta población específica, la evidencia que respalda el uso de estos medicamentos en personas con FXS es deficiente. [63]
El TDAH , que afecta a la mayoría de los niños y al 30% de las niñas con FXS, se trata frecuentemente con estimulantes . [11] Sin embargo, el uso de estimulantes en la población X frágil se asocia con una mayor frecuencia de eventos adversos que incluyen mayor ansiedad, irritabilidad y labilidad del estado de ánimo. [29] La ansiedad, así como el estado de ánimo y los síntomas obsesivo-compulsivos, pueden tratarse con ISRS , aunque estos también pueden agravar la hiperactividad y provocar un comportamiento desinhibido. [12] [29] Los antipsicóticos atípicos se pueden utilizar para estabilizar el estado de ánimo y controlar la agresión, especialmente en aquellos con TEA comórbido. Sin embargo, es necesario controlar los efectos secundarios metabólicos, incluidos el aumento de peso y la diabetes, así como los trastornos del movimiento relacionados con efectos secundarios extrapiramidales como la discinesia tardía . Las personas con un trastorno convulsivo coexistente pueden necesitar tratamiento con anticonvulsivos .
Una revisión de 2013 indicó que la esperanza de vida del FXS era 12 años menor que la de la población general y que las causas de muerte eran similares a las encontradas en la población general. [64]
El síndrome de X frágil es el trastorno del desarrollo neurológico humano más "traducido" que se está estudiando. Por tanto, la investigación sobre la etiología del FXS ha dado lugar a muchos intentos de descubrimiento de fármacos. [65] La mayor comprensión de los mecanismos moleculares de la enfermedad en el FXS ha llevado al desarrollo de terapias dirigidas a las vías afectadas. La evidencia de modelos de ratón muestra que los antagonistas (bloqueadores) de mGluR5 pueden rescatar anomalías dendríticas de la columna vertebral y convulsiones, así como problemas cognitivos y de comportamiento, y pueden resultar prometedores en el tratamiento del FXS. [11] [66] [67] Dos nuevos medicamentos, AFQ-056 ( mavoglurant ) y dipraglurant , así como el medicamento reutilizado fenobam , se encuentran actualmente en ensayos en humanos para el tratamiento del FXS. [11] [68] También existe evidencia preliminar de la eficacia del arbaclofeno , un agonista de GABA B , para mejorar el retraimiento social en personas con FXS y TEA. [11] [22] Además, hay evidencia de modelos de ratón de que la minociclina , un antibiótico utilizado para el tratamiento del acné , rescata las anomalías de las dendritas. Un ensayo abierto en humanos ha mostrado resultados prometedores, aunque actualmente no hay evidencia de ensayos controlados que respalden su uso. [11]
En 1943, el neurólogo británico James Purdon Martin y la genetista británica Julia Bell describieron un pedigrí de discapacidad intelectual ligada al cromosoma X, sin considerar la macroorquidia (testículos más grandes). [69] En 1969, Herbert Lubs observó por primera vez un "cromosoma X marcador" inusual en asociación con la discapacidad intelectual. [70] En 1970, Frederick Hecht acuñó el término "sitio frágil". Y, en 1985, Félix F. de la Cruz describió ampliamente las características físicas, psicológicas y citogenéticas de quienes padecen la afección, además de las perspectivas de terapia. [71] Su labor de promoción continua le valió más tarde un honor a través de la Fundación de Investigación FRAXA en diciembre de 1998. [72]