El síndrome de Wolff-Parkinson-White ( WPWS ) es un trastorno debido a un tipo específico de problema con el sistema eléctrico del corazón que involucra una vía accesoria capaz de conducir corriente eléctrica entre las aurículas y los ventrículos, evitando así el nódulo auriculoventricular . [2] [3] Aproximadamente el 60% de las personas con el problema eléctrico desarrollaron síntomas, [5] que pueden incluir latidos cardíacos anormalmente rápidos , palpitaciones , dificultad para respirar , aturdimiento o síncope . [1] En raras ocasiones, puede ocurrir un paro cardíaco . [1] El tipo más común de latido cardíaco irregular que ocurre se conoce como taquicardia supraventricular paroxística . [1]
La causa del WPW generalmente se desconoce y probablemente se deba a una combinación de factores aleatorios y genéticos. [2] Un pequeño número de casos se debe a una mutación del gen PRKAG2 que puede heredarse de forma autosómica dominante . [2] El mecanismo subyacente implica una vía de conducción eléctrica accesoria entre las aurículas y los ventrículos . [1] Se asocia con otras afecciones como la anomalía de Ebstein y la parálisis periódica hipopotasémica . [1] El diagnóstico de WPW se produce con una combinación de palpitaciones y cuando un electrocardiograma (ECG) muestra un intervalo PR corto y una onda delta. [3] Es un tipo de síndrome de preexcitación . [3]
El síndrome de WPW se puede controlar o tratar con medicamentos o con una ablación (que destruye los tejidos), como la ablación con catéter por radiofrecuencia . [4] Afecta a entre el 0,1 y el 0,3% de la población. [1] El riesgo de muerte en personas sin síntomas es aproximadamente del 0,5% anual en niños y del 0,1% anual en adultos. [5] En algunos casos, la monitorización no invasiva puede ayudar a estratificar el riesgo más cuidadosamente a los pacientes en una categoría de menor riesgo. [6] En aquellos sin síntomas, la observación continua puede ser razonable. [5] En aquellos con WPW complicado por fibrilación auricular , se puede usar cardioversión o el medicamento procainamida . [7] La afección lleva el nombre de Louis Wolff , John Parkinson y Paul Dudley White, quienes describieron los hallazgos del ECG en 1930. [3]
Las personas con WPW suelen ser asintomáticas cuando no tienen una frecuencia cardíaca rápida. Sin embargo, los individuos pueden experimentar palpitaciones , mareos , dificultad para respirar o, con poca frecuencia, síncope (desmayo o casi desmayo) durante los episodios de taquicardia supraventricular . WPW también se asocia con un riesgo muy pequeño de muerte súbita debido a alteraciones más peligrosas del ritmo cardíaco. [8]

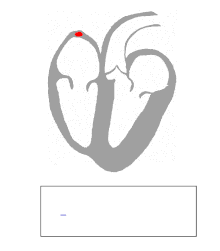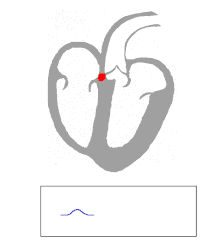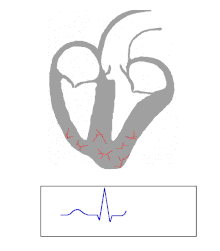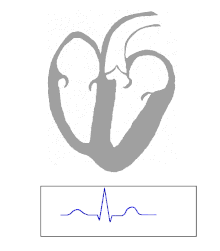
La actividad eléctrica en el corazón humano normal comienza cuando surge un potencial de acción cardíaco en el nódulo sinoauricular (SA), que se encuentra en la aurícula derecha . Desde allí, el estímulo eléctrico se transmite por vías internodales al nódulo auriculoventricular (AV). Después de un breve retraso en el nódulo AV, el estímulo viaja a través del haz de His hasta las ramas izquierda y derecha y luego hasta las fibras de Purkinje y el endocardio en el vértice del corazón y finalmente hasta el miocardio ventricular . [ cita necesaria ]
El nodo AV cumple una función importante como "guardián", limitando la actividad eléctrica que llega a los ventrículos. En situaciones en las que las aurículas generan una actividad eléctrica excesivamente rápida (como fibrilación auricular o aleteo auricular ), el nodo AV limita la cantidad de señales conducidas a los ventrículos. Por ejemplo, si las aurículas se activan eléctricamente a 300 latidos por minuto, la mitad de esos impulsos eléctricos pueden ser bloqueados por el nodo AV, de modo que los ventrículos se estimulan a sólo 150 latidos por minuto, lo que da como resultado un pulso de 150 latidos por minuto. Otra propiedad importante del nodo AV es que ralentiza los impulsos eléctricos individuales. Esto se manifiesta en el electrocardiograma como el intervalo PR (el tiempo desde la activación eléctrica de las aurículas hasta la activación eléctrica de los ventrículos ), que generalmente se acorta a menos de 120 milisegundos de duración. [ cita necesaria ]
Los individuos con WPW tienen una vía accesoria que comunica entre las aurículas y los ventrículos, además del nódulo AV. [6] Esta vía accesoria se conoce como haz de Kent. Esta vía accesoria no comparte las propiedades de desaceleración de la frecuencia del nódulo AV y puede conducir la actividad eléctrica a una frecuencia significativamente mayor que el nódulo AV. Por ejemplo, en el ejemplo anterior, si un individuo tenía una frecuencia auricular de 300 latidos por minuto, el haz accesorio puede conducir todos los impulsos eléctricos desde las aurículas a los ventrículos, haciendo que los ventrículos se contraigan a 300 latidos por minuto. Frecuencias cardíacas extremadamente rápidas como ésta pueden provocar inestabilidad hemodinámica o shock cardiogénico . En algunos casos, la combinación de una vía accesoria y ritmos cardíacos anormales puede desencadenar la fibrilación ventricular , una de las principales causas de muerte cardíaca súbita. [ cita necesaria ]
WPW puede estar asociado con PRKAG2 , una enzima proteína quinasa codificada por el gen PRKAG2 . [9]

El haz de Kent es una vía de conducción extra o accesoria anormal entre las aurículas y los ventrículos que está presente en un pequeño porcentaje (entre el 0,1 y el 0,3%) de la población general. [10] [11] [12] Esta vía puede comunicarse entre la aurícula izquierda y el ventrículo izquierdo, en cuyo caso se denomina "preexcitación tipo A", o entre la aurícula derecha y el ventrículo derecho, en cuyo caso En la antigua clasificación, actualmente abandonada, se denomina "preexcitación de tipo B". [13] Los problemas surgen cuando esta vía crea un circuito eléctrico que pasa por alto el nodo AV. El nódulo AV es capaz de disminuir la velocidad de conducción de impulsos eléctricos a los ventrículos, mientras que el haz de Kent carece de esta capacidad. Por lo tanto , cuando se establece una conexión eléctrica aberrante a través del haz de Kent, pueden producirse taquiarritmias. [ cita necesaria ]

El WPW se diagnostica comúnmente sobre la base del electrocardiograma en un individuo asintomático. En este caso, se manifiesta como una onda delta, que es un recorrido ascendente arrastrado en el complejo QRS que se asocia con un intervalo PR corto. El intervalo PR corto y la dificultad del complejo QRS reflejan que el impulso llega temprano a los ventrículos (a través de la vía accesoria) sin el retraso habitual que se experimenta en el nódulo AV. [ cita necesaria ]
Si una persona con WPW experimenta episodios de fibrilación auricular, el ECG muestra una taquicardia rápida polimórfica de complejo ancho (sin torsades de pointes ). Esta combinación de fibrilación auricular y WPW se considera peligrosa y la mayoría de los fármacos antiarrítmicos están contraindicados. [ cita necesaria ]
Cuando un individuo está en ritmo sinusal normal , las características ECG de WPW son un intervalo PR corto (menos de 120 milisegundos de duración), complejo QRS ensanchado (más de 120 milisegundos de duración) con carrera ascendente arrastrada del complejo QRS y repolarización secundaria. cambios (reflejados en el segmento ST - cambios en la onda T ). [ cita necesaria ]
En personas con WPW, la actividad eléctrica que se inicia en el nódulo SA viaja a través de la vía accesoria, así como a través del nódulo AV para activar los ventrículos a través de ambas vías. Dado que la vía accesoria no tiene las propiedades de desaceleración del impulso del nódulo AV, el impulso eléctrico activa primero los ventrículos a través de la vía accesoria e inmediatamente después a través del nódulo AV. Esto da el intervalo PR corto y el recorrido ascendente arrastrado del complejo QRS conocido como onda delta. [ cita necesaria ]
En el caso de preexcitación tipo A (conexiones auriculoventriculares izquierdas), se observa una onda R positiva en V1 ("delta positiva") en las derivaciones precordiales del electrocardiograma, mientras que en la preexcitación tipo B (conexiones auriculoventriculares derechas), una Se observa una onda delta predominantemente negativa en la derivación V1 ("delta negativa"). [13]
Las personas con WPW pueden tener más de una vía accesoria; en algunos casos, se han encontrado hasta ocho vías anormales. Esto se ha observado en personas con la anomalía de Ebstein . [14]
El síndrome de Wolff-Parkinson-White a veces se asocia con la neuropatía óptica hereditaria de Leber , una forma de enfermedad mitocondrial . [15]

WPW conlleva un pequeño riesgo de muerte súbita, presumiblemente debido a una fibrilación auricular de conducción rápida que causa fibrilación ventricular. Si bien el riesgo general es de aproximadamente 2,4 por 1000 personas-año, el riesgo en un individuo depende de las propiedades de la vía accesoria que causa la preexcitación. [8]
Los antecedentes de síncope pueden sugerir una vía accesoria de mayor riesgo, pero la estratificación del riesgo se realiza mejor evaluando la frecuencia con la que una vía puede conducir impulsos a los ventrículos, generalmente mediante estimulación eléctrica programada (PES) en el laboratorio de electrofisiología cardíaca . Este es un procedimiento invasivo pero generalmente de bajo riesgo durante el cual se estimulan las aurículas para intentar inducir taquicardia. Si se puede desencadenar una taquicardia que afecte a la vía accesoria, el cardiólogo puede evaluar la rapidez con la que la vía accesoria puede conducir. Cuanto más rápido pueda conducir, mayor será la probabilidad de que la vía accesoria pueda conducir lo suficientemente rápido como para desencadenar una taquicardia letal. [ cita necesaria ]
Las características de alto riesgo que pueden estar presentes durante el PES incluyen un período refractario efectivo de la vía accesoria de menos de 250 ms, vías múltiples, ubicación septal de la vía e inducibilidad de taquicardia supraventricular ( AVRT , fibrilación auricular). Las personas con cualquiera de estas características de alto riesgo generalmente se consideran con mayor riesgo de ECF o taquicardia sintomática y deben ser tratadas en consecuencia (es decir, ablación con catéter). [dieciséis]
No está claro si la estratificación del riesgo invasivo (con PES) es necesaria en el individuo asintomático. [17] Mientras que algunos grupos abogan por el PES para la estratificación del riesgo en todas las personas menores de 35 años, otros solo lo ofrecen a personas que tienen antecedentes sugestivos de taquiarritmia, ya que la incidencia de muerte cardíaca súbita es muy baja (menos del 0,6% en algunos casos). informes). [12] [18] [19]
Otros métodos de estratificación del riesgo incluyen la observación de la frecuencia ventricular durante la fibrilación auricular espontánea en un ECG de 12 derivaciones. Los intervalos RR de menos de 250 ms sugieren una vía de mayor riesgo. Durante la prueba de esfuerzo, la pérdida abrupta de la preexcitación a medida que aumenta la frecuencia cardíaca también sugiere una vía de menor riesgo. [8] Sin embargo, este enfoque se ve obstaculizado por la mejora normal en la conducción del nódulo AV durante el ejercicio, que también puede enmascarar la preexcitación a pesar de la conducción continua por la vía accesoria. [20]
Según el protocolo ACLS , las personas con WPW que experimentan ritmos cardíacos anormales rápidos ( taquiarritmias ) pueden requerir una cardioversión eléctrica sincronizada si presentan signos o síntomas graves (por ejemplo, presión arterial baja o letargo con estado mental alterado ). Si están relativamente estables, se pueden utilizar medicamentos. [21]
El patrón WPW con estabilidad hemodinámica y AVRT ortodrómica que conduce a una taquicardia regular de complejo estrecho puede tratarse de manera similar a otras taquicardias supraventriculares regulares de complejo estrecho: primero con maniobras vagales seguidas de una prueba de adenosina (tratamiento de primera línea). Las directrices ACC/AHA/HRS de 2015 recomiendan los betabloqueantes o bloqueadores de los canales de calcio como agentes de segunda línea, la cardioversión eléctrica se reserva para las arritmias refractarias. Sin embargo, si existe alguna duda sobre el diagnóstico de AVRT ortodrómica o si se observa una conducción aberrante que conduce a un QRS de complejo ancho, puede ser prudente tratarla como taquicardia de complejo ancho indiferenciada. [22]
Las personas con fibrilación auricular y respuesta ventricular rápida pueden recibir tratamiento con amiodarona [23] o procainamida [24] para estabilizar su frecuencia cardíaca. La procainamida y la cardioversión son tratamientos aceptados para la conversión de la taquicardia encontrada con WPW. [25] La amiodarona en la fibrilación auricular con WPW está relacionada con la fibrilación ventricular y, por lo tanto, puede ser peor que la procainamida. [23]
Los bloqueadores del nodo AV deben evitarse en fibrilación auricular y aleteo auricular con WPW o antecedentes de este; esto incluye adenosina , diltiazem , verapamilo , otros bloqueadores de los canales de calcio y betabloqueantes . [26] Pueden exacerbar el síndrome al bloquear la vía eléctrica normal del corazón (por lo tanto, favorecen la conducción auricular a ventrículo 1:1 a través de la vía de preexcitación, lo que potencialmente conduce a arritmias ventriculares inestables). [22]
El tratamiento definitivo del WPW es la destrucción de la vía eléctrica anormal mediante ablación con catéter . Dos tipos principales de ablación con catéter incluyen la ablación por radiofrecuencia con calor o la crioablación con energía fría. [6] Este procedimiento lo realizan electrofisiólogos cardíacos y tiene una alta tasa de éxito en manos de un electrofisiólogo experimentado. [27] Los hallazgos de 1994 indican tasas de éxito de hasta el 95% en personas tratadas con ablación con catéter por radiofrecuencia para WPW. [28] Si la ablación con catéter por radiofrecuencia se realiza con éxito, la afección generalmente se considera curada. Las tasas de recurrencia suelen ser inferiores al 5% después de una ablación exitosa. [27] Algunos pacientes, como aquellos con anomalía de Ebstein subyacente y miocardiopatías hereditarias , pueden tener múltiples vías accesorias. [29]
El haz de Kent lleva el nombre del fisiólogo británico Albert Frank Stanley Kent (1863-1958), quien describió ramas laterales en el surco auriculoventricular del corazón de mono (creyendo erróneamente que constituían el sistema de conducción auriculoventricular normal). [30] [31]
En 1915, Frank Norman Wilson (1890-1952) fue el primero en describir la afección que más tarde se denominaría síndrome de Wolff-Parkinson-White. [32] Alfred M. Wedd (1887–1967) fue el siguiente en describir la afección en 1921. [33] Los cardiólogos Louis Wolff (1898–1972), John Parkinson (1885–1976) y Paul Dudley White (1886–1973) se les atribuye la descripción definitiva del trastorno en 1930. [34]