Los tratamientos contra el cáncer son una amplia gama de tratamientos disponibles para los diferentes tipos de cáncer , y cada tipo de cáncer necesita su propio tratamiento específico. [1] Los tratamientos pueden incluir cirugía , quimioterapia , radioterapia , terapia hormonal , terapia dirigida que incluye medicamentos de moléculas pequeñas o anticuerpos monoclonales , [2] e inhibidores de PARP como olaparib . [3] Otras terapias incluyen hipertermia , inmunoterapia , terapia fotodinámica y terapia con células madre . [4] El tratamiento más común contra el cáncer implica una serie de terapias separadas, como quimioterapia antes de la cirugía. [4] Los inhibidores de la angiogénesis a veces se utilizan para mejorar los efectos de las inmunoterapias. [5]
La elección de la terapia depende de la ubicación y el grado del tumor y del estadio de la enfermedad, así como del estado general del paciente. Las pruebas de biomarcadores pueden ayudar a determinar el tipo de cáncer e indicar la mejor terapia. [6] Se están desarrollando continuamente varios tratamientos experimentales contra el cáncer . En 2023 se estimó que una de cada cinco personas será diagnosticada con cáncer en algún momento de su vida. [1]
El objetivo principal del tratamiento del cáncer es curarlo mediante su eliminación completa o prolongar considerablemente la vida del paciente. Los cuidados paliativos se utilizan cuando el pronóstico es malo y el cáncer se considera terminal . Existen muchos tipos de cáncer y muchos de ellos pueden tratarse con éxito si se detectan a tiempo. [1]
El tratamiento del cáncer ha experimentado cambios evolutivos a medida que se ha ido ampliando el conocimiento de los procesos biológicos subyacentes. Se han documentado cirugías de extirpación de tumores en el antiguo Egipto, y la terapia hormonal y la radioterapia se desarrollaron a finales del siglo XIX. La quimioterapia, la inmunoterapia y las terapias dirigidas más nuevas son productos del siglo XX. A medida que surja nueva información sobre la biología del cáncer, se desarrollarán y modificarán tratamientos para aumentar la eficacia, la precisión, la supervivencia y la calidad de vida.
Los tumores malignos pueden curarse si se extirpan completamente mediante cirugía . Pero si el cáncer ya se ha propagado ( metástasis ) a otros sitios, la escisión quirúrgica completa suele ser imposible. En el modelo halstediano de progresión del cáncer, los tumores crecen localmente, luego se propagan a los ganglios linfáticos y luego al resto del cuerpo. Esto ha dado lugar a la popularidad de los tratamientos exclusivamente locales, como la cirugía para cánceres pequeños. Incluso los tumores pequeños localizados se reconocen cada vez más como poseedores de potencial metastásico.
Entre los ejemplos de procedimientos quirúrgicos para el cáncer se incluyen la mastectomía y la lumpectomía para el cáncer de mama, la prostatectomía para el cáncer de próstata y la cirugía de cáncer de pulmón para el cáncer de pulmón de células no pequeñas. El objetivo de la cirugía puede ser la extirpación solo del tumor, del órgano completo o de parte del órgano. [7] Una sola célula cancerosa es invisible a simple vista, pero puede volver a crecer y convertirse en un nuevo tumor, un proceso llamado recurrencia. Por este motivo, el patólogo examinará la muestra quirúrgica para determinar si hay un margen de tejido sano, disminuyendo así la posibilidad de que queden células cancerosas microscópicas en el paciente.
Además de la extirpación del tumor primario, a menudo es necesaria la cirugía para la estadificación , por ejemplo, para determinar la extensión de la enfermedad y si ha hecho metástasis en los ganglios linfáticos regionales . La estadificación es un determinante importante del pronóstico y de la necesidad de terapia adyuvante . Ocasionalmente, es necesaria la cirugía para controlar los síntomas, como la compresión de la médula espinal o la obstrucción intestinal . Esto se conoce como tratamiento paliativo .
La cirugía puede realizarse antes o después de otras formas de tratamiento. El tratamiento antes de la cirugía a menudo se describe como neoadyuvante . En el cáncer de mama, la tasa de supervivencia de los pacientes que reciben quimioterapia neoadyuvante no es diferente de la de los que reciben tratamiento después de la cirugía. [8] La administración temprana de la quimioterapia permite a los oncólogos evaluar la eficacia de la terapia y puede facilitar la extirpación del tumor. Sin embargo, las ventajas de supervivencia del tratamiento neoadyuvante en el cáncer de pulmón son menos claras.
La radioterapia (radioterapia) es el uso de radiación ionizante para matar células cancerosas y reducir tumores dañando su ADN causando la muerte celular . [9] La radioterapia puede dañar el ADN directamente o crear partículas cargadas ( radicales libres ) dentro de las células que a su vez pueden dañar el ADN. La radioterapia se puede administrar externamente a través de radioterapia de haz externo o internamente a través de braquiterapia . Los efectos de la radioterapia son localizados y confinados a la región que se está tratando. Aunque la radiación daña tanto a las células cancerosas como a las células normales, la mayoría de las células normales pueden recuperarse de los efectos de la radiación y funcionar correctamente. El objetivo de la radioterapia es dañar tantas células cancerosas como sea posible, al tiempo que se limita el daño al tejido sano cercano. Por lo tanto, se administra en muchas fracciones, lo que permite que el tejido sano se recupere entre fracciones.
La radioterapia se puede utilizar para tratar casi todos los tipos de tumores sólidos y también se puede utilizar para tratar la leucemia y el linfoma . La dosis de radiación en cada sitio depende de varios factores, entre ellos la radiosensibilidad de cada tipo de cáncer y si hay tejidos y órganos cercanos que puedan resultar dañados por la radiación. Por lo tanto, como ocurre con cualquier forma de tratamiento, la radioterapia tiene sus efectos secundarios.
La radioterapia puede provocar sequedad de boca debido a la exposición de las glándulas salivales a la radiación, lo que produce una disminución de la secreción de saliva. Después de la terapia, las glándulas salivales volverán a funcionar, pero rara vez de la misma manera. La sequedad de boca causada por la radiación puede ser un problema permanente. [10]
La quimioterapia es el tratamiento del cáncer con medicamentos ("medicamentos contra el cáncer") que pueden destruir las células cancerosas. La quimioterapia se puede administrar de diversas formas, como inyecciones en los músculos, la piel, las arterias o las venas, o incluso se puede tomar por vía oral en forma de píldora. [11] En el uso actual, el término "quimioterapia" generalmente se refiere a medicamentos citotóxicos que afectan a las células que se dividen rápidamente en general, en contraste con la terapia dirigida (ver a continuación). Los medicamentos de quimioterapia interfieren con la división celular de varias formas posibles, por ejemplo, con la duplicación del ADN o la separación de los cromosomas recién formados . La mayoría de las formas de quimioterapia se dirigen a todas las células que se dividen rápidamente y no son específicas de las células cancerosas, aunque cierto grado de especificidad puede provenir de la incapacidad de muchas células cancerosas para reparar el daño del ADN , mientras que las células normales generalmente pueden hacerlo. Por lo tanto, la quimioterapia tiene el potencial de dañar el tejido sano, especialmente aquellos tejidos que tienen una alta tasa de reemplazo (por ejemplo, el revestimiento intestinal). Estas células generalmente se reparan a sí mismas después de la quimioterapia.
Debido a que algunos medicamentos funcionan mejor juntos que solos, a menudo se administran dos o más medicamentos al mismo tiempo. Esto se denomina "quimioterapia combinada"; la mayoría de los regímenes de quimioterapia se administran en combinación. [12]
Dado que la quimioterapia afecta a todo el cuerpo, puede tener una amplia gama de efectos secundarios. Los pacientes a menudo descubren que comienzan a perder el cabello, ya que los medicamentos que combaten las células cancerosas también atacan las células de las raíces del cabello. Este poderoso tratamiento también puede provocar fatiga, pérdida de apetito y vómitos, según la persona. [11]
El tratamiento de algunas leucemias y linfomas requiere el uso de quimioterapia en dosis altas y radioterapia corporal total (TBI). Este tratamiento elimina la médula ósea y, por lo tanto, la capacidad del cuerpo para recuperarse y repoblar la sangre. Por este motivo, la recolección de células madre de la médula ósea o de la sangre periférica se lleva a cabo antes de la parte ablativa de la terapia, para permitir el "rescate" después de que se haya administrado el tratamiento. Esto se conoce como trasplante autólogo de células madre .
La terapia dirigida, que se empezó a utilizar a finales de los años 90, ha tenido un impacto significativo en el tratamiento de algunos tipos de cáncer y actualmente es un área de investigación muy activa. Se trata del uso de agentes específicos para las proteínas desreguladas de las células cancerosas. Los fármacos de moléculas pequeñas son fármacos de terapia dirigida que, por lo general, son inhibidores de dominios enzimáticos en proteínas mutadas, sobreexpresadas o críticas de otro modo dentro de la célula cancerosa. Ejemplos destacados son los inhibidores de la tirosina quinasa imatinib (Gleevec/Glivec) y gefitinib (Iressa).
La terapia con anticuerpos monoclonales es otra estrategia en la que el agente terapéutico es un anticuerpo que se une específicamente a una proteína en la superficie de las células cancerosas. Algunos ejemplos incluyen el anticuerpo anti- HER2/neu trastuzumab (Herceptin) utilizado en el cáncer de mama y el anticuerpo anti-CD20 rituximab , utilizado en una variedad de neoplasias malignas de células B.
La terapia dirigida también puede implicar el uso de pequeños péptidos como "dispositivos de localización" que pueden unirse a los receptores de la superficie celular o a la matriz extracelular afectada que rodea el tumor. Los radionucleidos que se unen a estos péptidos (por ejemplo, los RGD) acaban matando a la célula cancerosa si el nucleido se desintegra en las proximidades de la célula. Los oligo o multímeros de estos motivos de unión son especialmente de gran interés, ya que pueden conducir a una mayor especificidad y avidez tumoral.
La terapia fotodinámica (TFD) es un tratamiento ternario para el cáncer que implica un fotosensibilizador, oxígeno tisular y luz (a menudo utilizando láseres [13] ). La TFD se puede utilizar como tratamiento para el carcinoma de células basales (CCB) o el cáncer de pulmón ; la TFD también puede ser útil para eliminar rastros de tejido maligno después de la extirpación quirúrgica de tumores grandes. [14] En febrero de 2019, los científicos médicos anunciaron que el iridio unido a la albúmina , creando una molécula fotosensibilizada , puede penetrar las células cancerosas y, después de ser irradiado con luz, destruir las células cancerosas. [15] [16]
El ultrasonido terapéutico de alta energía podría aumentar la carga de fármacos anticancerígenos de mayor densidad y nanomedicamentos dirigidos a sitios tumorales hasta 20 veces más que la terapia tradicional dirigida al cáncer. [17]
Las terapias dirigidas en desarrollo preclínico como posibles tratamientos contra el cáncer incluyen oligonucleótidos de conmutación de empalme de morfolino , que inducen la omisión de exones ERG en modelos de cáncer de próstata , [18] inhibidores de quinasas multiobjetivo que inhiben la PI3K [19] con otras vías que incluyen MEK [20] y PIM , [21] e inhibidores de NF-κB en modelos de resistencia a la quimioterapia. [22] [23] [24]
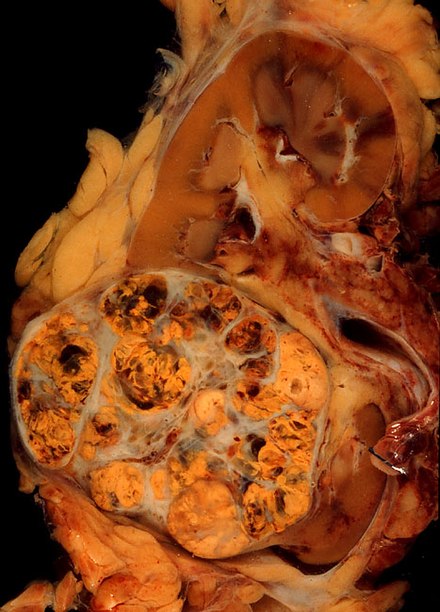
La inmunoterapia contra el cáncer se refiere a un conjunto diverso de estrategias terapéuticas diseñadas para inducir al sistema inmunológico del propio paciente a combatir el tumor. Los métodos contemporáneos para generar una respuesta inmunológica contra los tumores incluyen la inmunoterapia BCG intravesical para el cáncer de vejiga superficial y el uso de interferones y otras citocinas para inducir una respuesta inmunológica en pacientes con carcinoma de células renales y melanoma . Las vacunas contra el cáncer para generar respuestas inmunológicas específicas son objeto de una intensa investigación para una serie de tumores, en particular el melanoma maligno y el carcinoma de células renales. Sipuleucel-T es una estrategia similar a una vacuna para el cáncer de próstata en la que las células dendríticas del paciente se cargan con péptidos de fosfatasa ácida prostática para inducir una respuesta inmunológica específica contra las células derivadas de la próstata. Obtuvo la aprobación de la FDA en 2010.
El trasplante alogénico de células madre hematopoyéticas (generalmente de la médula ósea ) de un donante genéticamente no idéntico puede considerarse una forma de inmunoterapia, ya que las células inmunitarias del donante a menudo atacan al tumor en un fenómeno conocido como efecto injerto contra tumor . Por este motivo, el TPH alogénico conduce a una tasa de curación más alta que el trasplante autólogo para varios tipos de cáncer, aunque los efectos secundarios también son más graves.
La inmunoterapia celular, en la que se utilizan las células asesinas naturales (NK) y las células T citotóxicas del propio paciente , se practica en Japón desde 1990. Las células NK y las células T matan principalmente las células cancerosas cuando se desarrollan. Este tratamiento se administra junto con otros modos de tratamiento, como la cirugía, la radioterapia o la quimioterapia, y se denomina terapia de refuerzo inmunitario autóloga (AIET). [25] [26]
La terapia de puntos de control inmunitario se centra en dos proteínas de puntos de control inmunitario , la proteína asociada a los linfocitos T citotóxicos 4 (CTLA-4) y la proteína de muerte celular programada 1 (PD-1). En condiciones normales, el sistema inmunitario utiliza las proteínas de puntos de control como mecanismos de retroalimentación negativa para volver a la homeostasis una vez que los patógenos han sido eliminados del cuerpo. En un microambiente tumoral , las células cancerosas pueden comandar este sistema regulador fisiológico para "poner un freno" a la respuesta inmunitaria contra el cáncer y evadir la vigilancia inmunitaria. [27] El Premio Nobel de Medicina de 2018 se otorga al Dr. James Allison del Centro Oncológico MD Anderson de la Universidad de Texas en EE. UU. y al Dr. Tasuku Honjo de la Universidad de Kioto en Japón por sus contribuciones en el avance de la terapia de puntos de control inmunitario PD-1 y CTLA-4. [28]
El crecimiento de algunos cánceres se puede inhibir mediante la administración o el bloqueo de determinadas hormonas. Algunos ejemplos comunes de tumores sensibles a las hormonas son ciertos tipos de cáncer de mama y de próstata. El bloqueo de los estrógenos o la testosterona suele ser un tratamiento adicional importante. En ciertos cánceres, la administración de agonistas hormonales, como los progestágenos , puede resultar terapéuticamente beneficiosa. Aunque los efectos secundarios de la terapia hormonal varían según el tipo, los pacientes pueden experimentar síntomas como sofocos, náuseas y fatiga. [29]
Los inhibidores de la angiogénesis impiden el crecimiento extenso de los vasos sanguíneos ( angiogénesis ) que los tumores necesitan para sobrevivir y crecer. El crecimiento continuo permite la invasión de células en los tejidos vecinos y la metástasis en los tejidos distales. [30] Hay muchos inhibidores de la angiogénesis aprobados, incluidos bevacizumab , axitinib y cabozantinib . [30]
Se ha demostrado que los flavonoides regulan negativamente la estimulación angiogénica del VEGF y del factor inducible por hipoxia (HIF), pero ninguno ha llegado a ensayos clínicos . [31]
La prescripción de ejercicio se está convirtiendo en un tratamiento complementario convencional para el cáncer, [32] según estudios que muestran que el ejercicio (en comparación con ningún ejercicio) está asociado con tasas de recurrencia reducidas, mejores resultados de mortalidad y reducción de los efectos secundarios de los tratamientos tradicionales contra el cáncer. [33] [34] Aunque no está claro si los mejores resultados con el ejercicio están correlacionados o son causales, la relación beneficio-riesgo de incluir el ejercicio como parte del tratamiento del cáncer es grande, [35] ya que el ejercicio tiene más beneficios (por ejemplo, cardiovasculares, salud mental) sin mayores riesgos, aunque existe un pequeño riesgo de lesión por uso excesivo si se agrega de forma demasiado agresiva. [36] Los fisiólogos del ejercicio y los especialistas en medicina del ejercicio pueden ayudar a los oncólogos y médicos de atención primaria con la prescripción de ejercicio en pacientes con cáncer.

La letalidad sintética se produce cuando una combinación de deficiencias en la expresión de dos o más genes conduce a la muerte celular, mientras que una deficiencia en uno solo de estos genes no lo hace. Las deficiencias pueden surgir a través de mutaciones, alteraciones epigenéticas o inhibidores de uno o ambos genes.
Las células cancerosas frecuentemente son deficientes en un gen de reparación del ADN. [37] [38] (Ver también deficiencia de reparación del ADN en el cáncer ). Este defecto de reparación del ADN puede deberse a una mutación o, a menudo, a un silenciamiento epigenético (ver silenciamiento epigenético de la reparación del ADN ). Si este defecto de reparación del ADN está en una de las siete vías de reparación del ADN (ver vías de reparación del ADN ), y se inhibe una vía de reparación del ADN compensatoria, entonces las células tumorales pueden morir por letalidad sintética. Las células no tumorales, con la vía inicial intacta, pueden sobrevivir.
Las mutaciones en los genes de reparación del ADN BRCA1 o BRCA2 (activos en la reparación recombinacional homóloga ) son sintéticamente letales con inhibición del gen de reparación del ADN PARP1 (activo en la reparación por escisión de bases y en las vías de unión de extremos mediadas por microhomología de la reparación del ADN). [39] [40]
Los cánceres de ovario tienen un defecto mutacional en BRCA1 en aproximadamente el 18% de los pacientes (13% mutaciones de línea germinal y 5% mutaciones somáticas) (ver BRCA1 ). Olaparib , un inhibidor de PARP , fue aprobado en 2014 por la FDA de EE. UU. para su uso en el cáncer de ovario asociado a BRCA que previamente había sido tratado con quimioterapia. [41] La FDA, en 2016, también aprobó el inhibidor de PARP rucaparib para tratar a mujeres con cáncer de ovario avanzado que ya han sido tratadas con al menos dos quimioterapias y tienen una mutación del gen BRCA1 o BRCA2 . [42]
En el cáncer de colon, los defectos epigenéticos en el gen WRN parecen ser sintéticamente letales con la inactivación de TOP1 . En particular, la inactivación de TOP1 con irinotecán fue sintéticamente letal con expresión deficiente del gen de reparación de ADN WRN en pacientes con cáncer de colon. [43] En un estudio de 2006, 45 pacientes tenían tumores colónicos con promotores del gen WRN hipermetilados ( expresión de WRN silenciada ), y 43 pacientes tenían tumores con promotores del gen WRN no metilados , por lo que la expresión de la proteína WRN era alta. [43] El irinotecán fue más fuertemente beneficioso para los pacientes con promotores WRN hipermetilados (39,4 meses de supervivencia) que para aquellos con promotores WRN no metilados (20,7 meses de supervivencia). El promotor del gen WRN está hipermetilado en aproximadamente el 38% de los cánceres colorrectales . [43]
Hay cinco etapas diferentes del cáncer de colon y todas ellas tienen tratamiento:
Aunque el control de los síntomas del cáncer no suele considerarse un tratamiento dirigido al cáncer, es un determinante importante de la calidad de vida de los pacientes con cáncer y desempeña un papel importante en la decisión de si el paciente puede someterse a otros tratamientos. En general, los médicos tienen las habilidades terapéuticas para reducir el dolor, incluidas las náuseas y los vómitos inducidos por la quimioterapia , la diarrea, las hemorragias y otros problemas comunes en los pacientes con cáncer. La especialidad multidisciplinaria de los cuidados paliativos ha aumentado específicamente en respuesta a las necesidades de control de los síntomas de estos grupos de pacientes.
Los analgésicos , como la morfina , la oxicodona y los antieméticos son fármacos que suprimen las náuseas y los vómitos. Se utilizan con mucha frecuencia en pacientes con síntomas relacionados con el cáncer. Los antieméticos mejorados , como el ondansetrón y sus análogos, así como el aprepitant, han hecho que los tratamientos agresivos sean mucho más factibles en pacientes con cáncer.
El dolor oncológico puede estar asociado con daño tisular continuo debido al proceso de la enfermedad o al tratamiento (es decir, cirugía, radiación, quimioterapia). Siempre hay un papel para los factores ambientales y las alteraciones afectivas en la génesis de las conductas de dolor, sin embargo, estos no suelen ser los factores etiológicos predominantes en pacientes con dolor oncológico. Algunos pacientes con dolor severo asociado con el cáncer se están acercando al final de sus vidas, pero en todos los casos, se deben utilizar terapias paliativas para controlar el dolor. Cuestiones como el estigma social del uso de opioides y el consumo de atención médica pueden ser preocupaciones y es posible que deban abordarse para que la persona se sienta cómoda tomando los medicamentos necesarios para controlar sus síntomas. La estrategia típica para el manejo del dolor oncológico es lograr que el paciente se sienta lo más cómodo posible utilizando la menor cantidad de medicamentos posible, incluso si eso significa usar opioides, cirugía y medidas físicas.
Históricamente, los médicos se mostraban reacios a recetar narcóticos a pacientes con cáncer terminal debido a la adicción y la supresión de la función respiratoria. El movimiento de cuidados paliativos , una rama más reciente del movimiento de hospicios , ha generado un apoyo más amplio al tratamiento preventivo del dolor en pacientes con cáncer. La Organización Mundial de la Salud también señaló que el dolor oncológico no controlado es un problema mundial y estableció una "escalera" como guía para la forma en que los médicos deben tratar el dolor en pacientes con cáncer.
La fatiga relacionada con el cáncer es un síntoma muy común del cáncer y existen varios enfoques propuestos para ayudar a aliviarla. [45]
Los pacientes con cáncer se enfrentan a muchos obstáculos, y uno de ellos es la tensión mental. Es muy común que los pacientes con cáncer se sientan estresados, abrumados, inseguros e incluso deprimidos. [46] El uso de la quimioterapia es un tratamiento muy duro que provoca la muerte de las células del cuerpo. Los efectos físicos como este no solo infligen dolor, sino que también hacen que los pacientes se sientan mentalmente agotados y quieran darse por vencidos. Por muchas razones, incluidas estas, los hospitales ofrecen muchos tipos de terapia y curación mental. Algunas de ellas incluyen yoga, meditación, terapia de comunicación e ideas espirituales. [47] Todas ellas tienen como objetivo calmar y relajar la mente, o dar esperanza a los pacientes que pueden sentirse agotados.
Un trastorno común que sufren las personas que han sobrevivido a tratamientos contra el cáncer es el insomnio. Casi el 60% de los supervivientes de cáncer padecen insomnio y, si no se trata adecuadamente, puede tener efectos a largo plazo en la salud fisiológica y física. [48] El insomnio se define como la insatisfacción con la duración o la calidad del sueño y las dificultades para iniciar o mantener el sueño. [49] El insomnio puede reducir considerablemente la calidad de vida de una persona. Se ha observado que la terapia cognitiva conductual reduce el insomnio y la depresión en los supervivientes de cáncer. [50]
La disminución de la fuerza muscular es un efecto secundario común de muchos tratamientos contra el cáncer. Por este motivo, el ejercicio es muy importante, especialmente durante el primer año después del tratamiento. Se ha demostrado que el yoga, los ejercicios acuáticos y el pilates pueden mejorar el bienestar emocional y la calidad de vida de las supervivientes de cáncer de mama. [51]
Los cuidados paliativos se brindan en el hogar o en una institución especializada para enfermos terminales a personas con una enfermedad avanzada. [52] Si no se trata el cáncer, la enfermedad puede resultar terminal y, en ocasiones, se opta por renunciar al tratamiento y a sus efectos secundarios desagradables y optar, en su lugar, por los cuidados paliativos. El objetivo de los cuidados paliativos es brindar apoyo a las necesidades médicas, emocionales, sociales, prácticas, psicológicas y espirituales de la persona. [52]
La planificación anticipada de la atención médica (PAA) puede ayudar a una persona a decidir por sí misma sus deseos de atención futura a medida que se acerca al final de su vida. [53] La PAA ayuda a los adultos en cualquier etapa de su salud a decidir y registrar por escrito sus deseos sobre preferencias de tratamiento médico y deseos futuros, preferiblemente tal como se discutieron previamente con familiares o cuidadores. [53]
Los ensayos clínicos , también llamados estudios de investigación, prueban nuevos tratamientos en personas con cáncer. El objetivo de esta investigación es encontrar mejores formas de tratar el cáncer y ayudar a los pacientes con cáncer. Los ensayos clínicos prueban muchos tipos de tratamiento, como nuevos medicamentos, nuevos enfoques de cirugía o radioterapia, nuevas combinaciones de tratamientos o nuevos métodos, como la terapia génica .
Un ensayo clínico es una de las etapas finales de un largo y minucioso proceso de investigación del cáncer. La búsqueda de nuevos tratamientos comienza en el laboratorio, donde los científicos primero desarrollan y prueban nuevas ideas. Si un enfoque parece prometedor, el siguiente paso puede ser probar un tratamiento en animales para ver cómo afecta el cáncer en un ser vivo y si tiene efectos nocivos. Por supuesto, los tratamientos que funcionan bien en el laboratorio o en animales no siempre funcionan bien en las personas. Los estudios se realizan con pacientes de cáncer para averiguar si los tratamientos prometedores son seguros y eficaces.
Los pacientes que participan pueden beneficiarse personalmente del tratamiento que reciben. Reciben atención actualizada de expertos en cáncer y reciben un nuevo tratamiento en fase de prueba o el mejor tratamiento estándar disponible para su cáncer. Al mismo tiempo, los nuevos tratamientos también pueden tener riesgos desconocidos, pero si un nuevo tratamiento demuestra ser eficaz o más eficaz que el tratamiento estándar, los pacientes del estudio que lo reciben pueden estar entre los primeros en beneficiarse. No hay garantía de que un nuevo tratamiento en fase de prueba o un tratamiento estándar produzcan buenos resultados. En niños con cáncer, una encuesta de ensayos encontró que los inscritos en los ensayos en promedio no tenían más probabilidades de obtener mejores o peores resultados que los que recibían el tratamiento estándar; esto confirma que no se puede predecir el éxito o el fracaso de un tratamiento experimental. [54]
Los exosomas son microvesículas cubiertas de lípidos que los tumores sólidos desprenden en los fluidos corporales, como la sangre y la orina. Actualmente se están realizando investigaciones para intentar utilizar los exosomas como método de detección y control de una variedad de cánceres. [55] [56] La esperanza es poder detectar el cáncer con una alta sensibilidad y especificidad mediante la detección de exosomas específicos en la sangre o la orina. El mismo proceso también se puede utilizar para controlar con mayor precisión el progreso del tratamiento de un paciente. Se ha demostrado que el ensayo específico de lectina ligada a enzimas o ELLSA Archivado el 13 de julio de 2011 en Wayback Machine detecta directamente los exosomas derivados del melanoma a partir de muestras de fluidos. [57] Anteriormente, los exosomas se habían medido por el contenido total de proteínas en muestras purificadas y por efectos inmunomoduladores indirectos. ELLSA mide directamente las partículas de exosomas en soluciones complejas y ya se ha descubierto que es capaz de detectar exosomas de otras fuentes, incluido el cáncer de ovario y los macrófagos infectados con tuberculosis.
También se cree que los exosomas secretados por los tumores son responsables de desencadenar la muerte celular programada (apoptosis) de las células inmunes; interrumpir la señalización de las células T necesaria para generar una respuesta inmune; inhibir la producción de citocinas anticancerígenas, y tiene implicaciones en la propagación de la metástasis y permitir la angiogénesis. [58] Actualmente se están realizando estudios con "plasmaféresis por afinidad a la lectina" (LAP), [57] LAP es un método de filtración de sangre que se dirige selectivamente a los exosomas de los tumores y los elimina del torrente sanguíneo. Se cree que la disminución de los exosomas secretados por los tumores en el torrente sanguíneo de un paciente ralentizará la progresión del cáncer y, al mismo tiempo, aumentará la respuesta inmune del propio paciente.
Los tratamientos de medicina complementaria y alternativa (MCA) son un grupo diverso de sistemas, prácticas y productos médicos y de atención de la salud que no forman parte de la medicina convencional y que no han demostrado ser eficaces. [59] La "medicina complementaria" se refiere a los métodos y sustancias que se utilizan junto con la medicina convencional, mientras que la " medicina alternativa " se refiere a los compuestos que se utilizan en lugar de la medicina convencional. [60] El uso de la MCA es común entre las personas con cáncer; un estudio de 2000 encontró que el 69% de los pacientes con cáncer habían utilizado al menos una terapia de MCA como parte de su tratamiento contra el cáncer. [61] La mayoría de las medicinas complementarias y alternativas para el cáncer no se han estudiado ni probado rigurosamente. Algunos tratamientos alternativos que se han investigado y han demostrado ser ineficaces continúan comercializándose y promoviéndose. [62]
La incidencia de cáncer asociado al embarazo ha aumentado debido a la edad cada vez mayor de las madres embarazadas . [63] Los cánceres también pueden detectarse incidentalmente durante el cribado materno. [63]
El tratamiento del cáncer debe elegirse de forma que cause el menor daño posible tanto a la mujer como al embrión o feto. En algunos casos puede recomendarse un aborto terapéutico .
La radioterapia está descartada y la quimioterapia siempre conlleva el riesgo de aborto espontáneo y malformaciones congénitas. [64] Se sabe poco sobre los efectos de los medicamentos en el niño.
Incluso si se ha comprobado que un fármaco no atraviesa la placenta para llegar al niño, algunas formas de cáncer pueden dañar la placenta y hacer que el fármaco pase por encima de ella de todos modos. [64] Algunas formas de cáncer de piel pueden incluso hacer metástasis en el cuerpo del niño. [64]
El diagnóstico también se dificulta, ya que la tomografía computarizada no es factible debido a la alta dosis de radiación. Aun así, la resonancia magnética funciona normalmente. [64] Sin embargo, no se pueden utilizar medios de contraste , ya que atraviesan la placenta. [64]
Como consecuencia de las dificultades para diagnosticar y tratar adecuadamente el cáncer durante el embarazo, los métodos alternativos son realizar una cesárea cuando el niño sea viable para comenzar un tratamiento más agresivo contra el cáncer o, si el cáncer es lo suficientemente maligno como para que la madre no pueda esperar tanto tiempo, realizar un aborto para tratar el cáncer. [64]
A veces, los tumores fetales se diagnostican mientras el feto todavía está en el útero. El teratoma es el tipo más común de tumor fetal y, por lo general, es benigno. En algunos casos, se tratan quirúrgicamente mientras el feto todavía está en el útero .
El cáncer es un problema importante que afecta al mundo. Específicamente en los EE. UU., se esperaban 1.735.350 nuevos casos de cáncer y 609.640 muertes para fines de 2018. El tratamiento adecuado puede prevenir muchas muertes por cáncer, pero existen disparidades raciales y sociales en los tratamientos que tienen un factor significativo en las altas tasas de mortalidad. Las minorías tienen más probabilidades de recibir un tratamiento inadecuado, mientras que los pacientes blancos tienen más probabilidades de recibir tratamientos eficientes de manera oportuna. [65] Recibir un tratamiento satisfactorio de manera oportuna puede aumentar la probabilidad de supervivencia del paciente. Se ha demostrado que las posibilidades de supervivencia son significativamente mayores para los pacientes blancos que para los pacientes afroamericanos. [65]
La mortalidad media anual de los pacientes con cáncer colorrectal entre 1992 y 2000 fue de 27 y 18,5 por 100.000 pacientes blancos y de 35,4 y 25,3 por 100.000 pacientes negros. En una revista que analizó múltiples estudios que probaban las disparidades raciales al tratar el cáncer colorrectal se encontraron hallazgos contradictorios. La Administración de Veteranos de los EE. UU. y un ensayo adyuvante encontraron que no había evidencia para apoyar las diferencias raciales en el tratamiento del cáncer colorrectal. Sin embargo, dos estudios sugirieron que los pacientes afroamericanos recibieron un tratamiento menos satisfactorio y de peor calidad en comparación con los pacientes blancos. [66] Uno de estos estudios específicamente fue proporcionado por el Centro de Investigación Intramural. Encontraron que los pacientes negros tenían un 41% menos de probabilidades de recibir tratamiento colorrectal y tenían más probabilidades de ser hospitalizados en un hospital universitario con menos médicos certificados en comparación con los pacientes blancos. Además, los pacientes negros tenían más probabilidades de ser diagnosticados con secuelas oncológicas, que es una gravedad de la enfermedad como resultado de un cáncer mal tratado. Por último, por cada 1.000 pacientes en el hospital, hubo 137,4 muertes de pacientes negros y 95,6 muertes de pacientes blancos. [67]
Un artículo publicado en una revista sobre cáncer de mama analizó las disparidades en los tratamientos contra el cáncer de mama en los montes Apalaches. Se descubrió que las mujeres afroamericanas tenían tres veces más probabilidades de morir que las asiáticas y dos veces más probabilidades de morir que las mujeres blancas. [68] Según el estudio, las mujeres afroamericanas tienen una desventaja en términos de supervivencia en comparación con otras razas. [69] [68] Las mujeres negras también tienen más probabilidades de recibir un tratamiento menos exitoso que las mujeres blancas al no recibir cirugía o terapia. Además, el panel del Instituto Nacional del Cáncer de EE. UU . identificó los tratamientos contra el cáncer de mama administrados a mujeres negras como inadecuados e inadecuados en comparación con el tratamiento administrado a mujeres blancas. [70]
A partir de estos estudios, los investigadores han observado que existen disparidades claras en el tratamiento del cáncer, en particular en cuanto a quién tiene acceso al mejor tratamiento y puede recibirlo de manera oportuna. Esto, en última instancia, genera disparidades entre quién muere de cáncer y quién tiene más probabilidades de sobrevivir.
La causa de estas disparidades es generalmente que los afroamericanos tienen menos cobertura de atención médica, seguro y acceso a centros de cáncer que otras razas. [71] Por ejemplo, se demostró que los pacientes negros con cáncer de mama y cáncer colorrectal tenían más probabilidades de tener Medicaid o no tener seguro en comparación con otras razas. [67] La ubicación del centro de atención médica también juega un papel en por qué los afroamericanos reciben menos tratamiento en comparación con otras razas. [71] [67] Sin embargo, algunos estudios dicen que los afroamericanos no confían en los médicos y no siempre buscan la ayuda que necesitan y que esto explica por qué menos afroamericanos reciben tratamiento. [72] Otros sugieren que los afroamericanos buscan más tratamiento que los blancos y que es simplemente una falta de recursos disponibles para ellos. [72] En este caso, el análisis de estos estudios identificará las disparidades de tratamiento y buscará prevenirlas descubriendo las posibles causas de estas disparidades.
A pesar del reconocimiento de las mejoras en los resultados, el miedo visceral a la enfermedad es omnipresente y las personas pueden tener que luchar para controlarla. [73]
Entre los pacientes con cáncer de pulmón, el estigma, la vergüenza, el aislamiento social y la discriminación son comunes. [74] A estos pacientes a veces se les dice que merecen cáncer debido a que fuman. Esos pacientes también pueden tener sentimientos de culpa por tener cáncer. [75] [76] [77] El estigma en el cáncer de cuello uterino fue impulsado predominantemente por el miedo al juicio social y el rechazo, la autoinculpación y la vergüenza, con notables influencias negativas de las normas sociales y de género, ya que tanto la infección por el virus del papiloma humano como el cáncer de cuello uterino fueron estigmatizados debido a la percepción de que surgen de un comportamiento imprudente, como tener múltiples parejas sexuales o descuidar las pruebas de detección. [78] La resiliencia puede ser un potente mecanismo de protección contra la estigmatización. [79] La resiliencia en el contexto del tratamiento del cáncer es la capacidad fisiológica y psicológica del paciente para adaptarse, recuperarse y mantener un funcionamiento óptimo de manera efectiva frente a los desafíos médicos. Abarca la capacidad de afrontar y superar la adversidad, mantener el bienestar emocional y promover la salud general y la curación. [80]