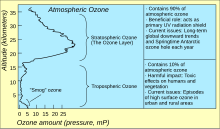
El agotamiento del ozono consta de dos eventos relacionados observados desde finales de la década de 1970: una disminución constante de alrededor del cuatro por ciento en la cantidad total de ozono en la atmósfera de la Tierra y una disminución mucho mayor en primavera del ozono estratosférico (la capa de ozono ) alrededor de las regiones polares de la Tierra. [1] Este último fenómeno se conoce como agujero de ozono . También hay eventos de agotamiento del ozono troposférico polar en primavera además de estos eventos estratosféricos.
Las principales causas del agotamiento de la capa de ozono y del agujero de la capa de ozono son los productos químicos manufacturados, especialmente los refrigerantes , solventes , propulsores y agentes espumantes de halocarbonos manufacturados ( clorofluorocarbonos (CFC), HCFC, halones ), conocidos como sustancias que agotan la capa de ozono (SAO). [2] Estos compuestos se transportan a la estratosfera mediante una mezcla turbulenta después de ser emitidos desde la superficie, mezclándose mucho más rápido de lo que las moléculas pueden asentarse. [3] Una vez en la estratosfera, liberan átomos del grupo halógeno mediante fotodisociación , que cataliza la descomposición del ozono (O 3 ) en oxígeno (O 2 ). [4] Se observó que ambos tipos de agotamiento de la capa de ozono aumentaban a medida que aumentaban las emisiones de halocarbonos.
El agotamiento de la capa de ozono y el agujero de la capa de ozono han generado preocupación mundial por el aumento de los riesgos de cáncer y otros efectos negativos. La capa de ozono impide que las longitudes de onda dañinas de la luz ultravioleta (UVB) atraviesen la atmósfera terrestre . Estas longitudes de onda causan cáncer de piel , quemaduras solares , ceguera permanente y cataratas , [5] que, según se prevé, aumentarán dramáticamente como resultado de la disminución del ozono, además de dañar plantas y animales. Estas preocupaciones llevaron a la adopción del Protocolo de Montreal en 1987, que prohíbe la producción de CFC, halones y otras sustancias químicas que agotan la capa de ozono. [6] Actualmente, [ ¿cuándo? ] Los científicos planean desarrollar nuevos refrigerantes para reemplazar a los más antiguos. [7]
La prohibición entró en vigor en 1989. Los niveles de ozono se estabilizaron a mediados de la década de 1990 y comenzaron a recuperarse en la década de 2000, a medida que el desplazamiento de la corriente en chorro en el hemisferio sur hacia el polo sur se detuvo e incluso podría estar revirtiéndose. [8] Se prevé que la recuperación continúe durante el próximo siglo, y se espera que el agujero de ozono alcance los niveles anteriores a 1980 alrededor de 2075. [9] En 2019, la NASA informó que el agujero de ozono era el más pequeño desde que se descubrió por primera vez. en 1982. [10] [11]
El Protocolo de Montreal se considera el acuerdo medioambiental internacional más exitoso hasta la fecha. [12] [13] Tras las prohibiciones de productos químicos que agotan la capa de ozono, la ONU proyecta que, según las regulaciones actuales, la capa de ozono se regenerará completamente para 2045, treinta años antes de lo previsto anteriormente. [14]

En el ciclo ozono-oxígeno intervienen tres formas (o alótropos ) de oxígeno : átomos de oxígeno (O u oxígeno atómico), oxígeno gaseoso ( O
2u oxígeno diatómico) y gas ozono ( O
3u oxígeno triatómico). [15] El ozono se forma en la estratosfera cuando las moléculas de gas oxígeno se fotodisocian después de absorber fotones UVC. Esto convierte una sola O
2en dos radicales atómicos de oxígeno . Los radicales atómicos de oxígeno luego se combinan con O separados
2moléculas para crear dos O
3moléculas. Estas moléculas de ozono absorben la luz UVB, tras lo cual el ozono se divide en una molécula de O
2y un átomo de oxígeno. Luego, el átomo de oxígeno se une a una molécula de oxígeno para regenerar el ozono. Este es un proceso continuo que termina cuando un átomo de oxígeno se recombina con una molécula de ozono para formar dos O
2moléculas. Vale la pena señalar que el ozono es el único gas atmosférico que absorbe la luz UVB.

La cantidad total de ozono en la estratosfera está determinada por un equilibrio entre la producción fotoquímica y la recombinación.
El ozono puede ser destruido por varios catalizadores de radicales libres ; los más importantes son el radical hidroxilo (OH·), el radical óxido nítrico (NO·), el radical cloro (Cl·) y el radical bromo (Br·). El punto es una notación para indicar que cada especie tiene un electrón desapareado y, por tanto, es extremadamente reactiva. Todos estos tienen fuentes tanto naturales como artificiales; En la actualidad, la mayor parte del OH· y NO· de la estratosfera se produce de forma natural, pero la actividad humana ha aumentado drásticamente los niveles de cloro y bromo. [16] Estos elementos se encuentran en compuestos orgánicos estables, especialmente los clorofluorocarbonos , que pueden viajar a la estratosfera sin ser destruidos en la troposfera debido a su baja reactividad. Una vez en la estratosfera, los átomos de Cl y Br se liberan de los compuestos originales por la acción de la luz ultravioleta, p.
El ozono es una molécula altamente reactiva que se reduce fácilmente a una forma de oxígeno más estable con la ayuda de un catalizador. Los átomos de Cl y Br destruyen las moléculas de ozono mediante una variedad de ciclos catalíticos . En el ejemplo más simple de tal ciclo, [17] un átomo de cloro reacciona con una molécula de ozono ( O
3), tomando un átomo de oxígeno para formar monóxido de cloro (ClO) y dejando una molécula de oxígeno ( O
2). El ClO puede reaccionar con una segunda molécula de ozono, liberando el átomo de cloro y produciendo dos moléculas de oxígeno. La abreviatura química para estas reacciones en fase gaseosa es:
El efecto general es una disminución en la cantidad de ozono, aunque la velocidad de estos procesos puede disminuir por los efectos de los ciclos nulos . También se han descubierto mecanismos más complicados que conducen a la destrucción del ozono en la estratosfera inferior.
Un solo átomo de cloro destruiría continuamente el ozono (por lo tanto, un catalizador) durante hasta dos años (la escala de tiempo para el transporte de regreso a la troposfera), excepto en reacciones que lo eliminan de este ciclo formando especies reservorio como el cloruro de hidrógeno (HCl). y nitrato de cloro ( ClONO
2). El bromo es incluso más eficaz que el cloro para destruir el ozono átomo por átomo, pero actualmente hay mucho menos bromo en la atmósfera. Tanto el cloro como el bromo contribuyen significativamente al agotamiento general del ozono. Los estudios de laboratorio también han demostrado que los átomos de flúor y yodo participan en ciclos catalíticos análogos. Sin embargo, los átomos de flúor reaccionan rápidamente con el vapor de agua, el metano y el hidrógeno para formar fluoruro de hidrógeno (HF) fuertemente unido en la estratosfera de la Tierra, [18] mientras que las moléculas orgánicas que contienen yodo reaccionan tan rápidamente en la atmósfera inferior que no alcanzan la estratosfera en cantidades significativas. [19]
Un solo átomo de cloro es capaz de reaccionar con una media de 100.000 moléculas de ozono antes de ser eliminado del ciclo catalítico. Este hecho, sumado a la cantidad de cloro liberado a la atmósfera anualmente por los clorofluorocarbonos (CFC) y los hidroclorofluorocarbonos (HCFC), demuestra el peligro de los CFC y los HCFC para el medio ambiente. [20] [21]

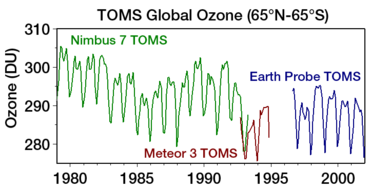
El agujero de ozono generalmente se mide por la reducción de la columna total de ozono sobre un punto de la superficie de la Tierra. Normalmente se expresa en unidades Dobson ; abreviado como "DU". La disminución más destacada del ozono se ha producido en la estratosfera inferior. Se han observado marcadas disminuciones en la columna de ozono en la primavera antártica y principios del verano en comparación con principios de la década de 1970 y antes, utilizando instrumentos como el Espectrómetro de Mapeo del Ozono Total (TOMS). [22]
Continúan las reducciones de hasta el 70 por ciento en la columna de ozono observadas en la primavera austral (hemisférico sur) sobre la Antártida y reportadas por primera vez en 1985 (Farman et al.). La columna total de ozono antártico en septiembre y octubre ha seguido siendo entre un 40 y un 50 por ciento más baja que los valores anteriores al agujero de ozono desde la década de 1990. [1] En 2016 se informó de una tendencia gradual hacia la "curación". [23] En 2017, la NASA anunció que el agujero de ozono era el más débil desde 1988 debido a las condiciones estratosféricas cálidas. Se espera que se recupere alrededor de 2070. [24]
La cantidad perdida varía más de un año a otro en el Ártico que en la Antártida. Las mayores disminuciones del Ártico se producen en invierno y primavera, alcanzando hasta el 30 por ciento cuando la estratosfera es más fría. [25]
Las reacciones que tienen lugar en las nubes estratosféricas polares (PSC) desempeñan un papel importante en el aumento del agotamiento del ozono. [26] Las PSC se forman más fácilmente en el frío extremo de la estratosfera ártica y antártica. Esta es la razón por la que los agujeros de ozono se formaron por primera vez, y son más profundos, sobre la Antártida. Los primeros modelos no tuvieron en cuenta las PSC y predijeron un agotamiento global gradual, razón por la cual el repentino agujero de ozono en la Antártida fue una sorpresa para muchos científicos. [27] [28] [29]
Es más exacto hablar de agotamiento de la capa de ozono en latitudes medias que de agujeros. La columna total de ozono disminuyó por debajo de los valores anteriores a 1980 entre 1980 y 1996 en latitudes medias. En las latitudes medias del norte, aumentó desde el valor mínimo en aproximadamente un dos por ciento entre 1996 y 2009, cuando las regulaciones entraron en vigor y la cantidad de cloro en la estratosfera disminuyó. En las latitudes medias del hemisferio sur, el ozono total permaneció constante durante ese período. No hay tendencias significativas en los trópicos, en gran parte porque los compuestos que contienen halógenos no han tenido tiempo de descomponerse y liberar átomos de cloro y bromo en las latitudes tropicales. [1] [30]
Se ha demostrado que las grandes erupciones volcánicas tienen efectos sustanciales, aunque desiguales, en el agotamiento del ozono, como se observó con la erupción del Monte Pinatubo en Filipinas en 1991. [31]
El agotamiento del ozono también explica gran parte de la reducción observada en las temperaturas de la estratosfera y la troposfera superior. [32] [33] La fuente del calor de la estratosfera es la absorción de la radiación ultravioleta por el ozono, por lo que la reducción del ozono conduce al enfriamiento. También se predice cierto enfriamiento estratosférico debido al aumento de los gases de efecto invernadero como el CO .
2y los propios CFC; sin embargo, el enfriamiento inducido por el ozono parece ser dominante. [34]
Las predicciones de los niveles de ozono siguen siendo difíciles, pero la precisión de las predicciones de los valores observados por parte de los modelos y la concordancia entre las diferentes técnicas de modelización han aumentado constantemente. [1] El Proyecto Global de Investigación y Monitoreo del Ozono de la Organización Meteorológica Mundial—Informe No. 44 se pronuncia firmemente a favor del Protocolo de Montreal , pero señala que una Evaluación del PNUMA de 1994 sobrestimó la pérdida de ozono para el período 1994-1997. [35]
Los clorofluorocarbonos (CFC) y otras sustancias halogenadas que agotan la capa de ozono (SAO) son los principales responsables del agotamiento químico del ozono provocado por el hombre. La cantidad total de halógenos efectivos (cloro y bromo) en la estratosfera se puede calcular y se conoce como cloro estratosférico efectivo equivalente (CESE). [36]
Los CFC como refrigerantes fueron inventados por Thomas Midgley, Jr. en la década de 1930. [37] Se utilizaron en unidades de aire acondicionado y refrigeración, como propulsores de aerosoles antes de la década de 1970 y en los procesos de limpieza de equipos electrónicos delicados. También ocurren como subproductos de algunos procesos químicos. Nunca se han identificado fuentes naturales importantes de estos compuestos; su presencia en la atmósfera se debe casi por completo a la fabricación humana. Como se mencionó anteriormente, cuando estas sustancias químicas que agotan la capa de ozono llegan a la estratosfera, la luz ultravioleta las disocia para liberar átomos de cloro. Los átomos de cloro actúan como catalizadores y cada uno puede descomponer decenas de miles de moléculas de ozono antes de ser eliminado de la estratosfera. Dada la longevidad de las moléculas de CFC, los tiempos de recuperación se miden en décadas. Se calcula que una molécula de CFC tarda una media de cinco a siete años en llegar desde el nivel del suelo hasta la atmósfera superior, y puede permanecer allí durante aproximadamente un siglo, destruyendo hasta cien mil moléculas de ozono durante ese tiempo. [38] [ se necesita verificación ]
El 1,1,1-tricloro-2,2,2-trifluoroetano , también conocido como CFC-113a, es uno de los cuatro químicos artificiales descubiertos recientemente en la atmósfera por un equipo de la Universidad de East Anglia. El CFC-113a es el único CFC conocido cuya abundancia en la atmósfera sigue aumentando. Su origen sigue siendo un misterio, pero algunos sospechan de su fabricación ilegal. El CFC-113a parece haberse estado acumulando sin cesar desde 1960. Entre 2012 y 2017, las concentraciones del gas aumentaron un 40 por ciento. [39]
Un estudio realizado por un equipo internacional de investigadores publicado en Nature encontró que desde 2013 las emisiones provenientes predominantemente del noreste de China han liberado a la atmósfera grandes cantidades del químico prohibido clorofluorocarbono-11 (CFC-11). Los científicos estiman que, si no se toman medidas, estas emisiones de CFC-11 retrasarán una década la recuperación del agujero de ozono del planeta. [40] [41] [42]
Los científicos han atribuido el agotamiento de la capa de ozono al aumento de compuestos halógenos (antropógenos) fabricados por el hombre a partir de CFC combinando datos de observación con modelos informáticos. Estos complejos modelos de transporte químico (p. ej. , SLIMCAT , CLaMS , modelo químico lagrangiano de la estratosfera) funcionan combinando mediciones de campos químicos y meteorológicos con constantes de velocidad de reacción química. Identifican reacciones químicas clave y procesos de transporte que ponen en contacto los productos de fotólisis de CFC con el ozono.

El agujero de ozono antártico es un área de la estratosfera antártica en la que los niveles recientes de ozono han caído hasta un 33 por ciento de sus valores anteriores a 1975. [44] El agujero de ozono ocurre durante la primavera antártica, desde septiembre hasta principios de diciembre, cuando fuertes vientos del oeste comienzan a circular alrededor del continente y crean un contenedor atmosférico. Dentro de este vórtice polar , más del 50 por ciento del ozono estratosférico inferior se destruye durante la primavera antártica. [45]
Como se explicó anteriormente, la causa principal del agotamiento de la capa de ozono es la presencia de gases fuente que contienen cloro (principalmente CFC y halocarbonos relacionados). En presencia de luz ultravioleta, estos gases se disocian, liberando átomos de cloro, que luego catalizan la destrucción del ozono. El agotamiento del ozono catalizado por Cl puede tener lugar en la fase gaseosa, pero aumenta dramáticamente en presencia de nubes estratosféricas polares (PSC). [46]
Estas nubes estratosféricas polares se forman durante el invierno, en condiciones de frío extremo. Los inviernos polares son oscuros y constan de tres meses sin radiación solar (luz solar). La falta de luz solar contribuye a una disminución de la temperatura y el vórtice polar atrapa y enfría el aire. Las temperaturas oscilan alrededor o por debajo de los -80 °C. Estas bajas temperaturas forman partículas de nubes. Hay tres tipos de nubes PSC: nubes de trihidrato de ácido nítrico, nubes de hielo de agua que se enfrían lentamente y nubes de hielo de agua (nácaras) que se enfrían rápidamente, que proporcionan superficies para reacciones químicas cuyos productos, en la primavera, conducirán a la destrucción del ozono. [47]
Los procesos fotoquímicos implicados son complejos pero bien comprendidos. La observación clave es que, normalmente, la mayor parte del cloro de la estratosfera reside en compuestos "de depósito", principalmente nitrato de cloro ( ClONO
2) así como productos finales estables como HCl. La formación de productos finales esencialmente elimina el Cl del proceso de agotamiento del ozono. Los compuestos del reservorio secuestran Cl, que luego puede estar disponible mediante la absorción de luz en longitudes de onda inferiores a 400 nm. [48] Durante el invierno y la primavera antárticos, las reacciones en la superficie de las partículas de las nubes estratosféricas polares convierten estos compuestos "depósito" en radicales libres reactivos (Cl y ClO). La desnitrificación es el proceso por el cual las nubes eliminan NO
2de la estratosfera convirtiéndolo en ácido nítrico en partículas de PSC, que luego se pierden por sedimentación. Esto evita que el ClO recién formado se convierta nuevamente en ClONO.
2.
El papel de la luz solar en el agotamiento del ozono es la razón por la cual el agotamiento del ozono en la Antártida es mayor durante la primavera. Durante el invierno, aunque las PSC son más abundantes, no hay luz sobre el polo para impulsar reacciones químicas. Sin embargo, durante la primavera, la luz del sol regresa y proporciona energía para impulsar reacciones fotoquímicas y derretir las nubes estratosféricas polares, liberando una cantidad considerable de ClO, que impulsa el mecanismo del agujero. El aumento adicional de las temperaturas hacia el final de la primavera rompe el vórtice a mediados de diciembre. Tan cálido, ozono y NO
2-El aire rico fluye desde latitudes más bajas, las PSC se destruyen, el proceso de agotamiento de la capa de ozono se detiene y el agujero de la capa de ozono se cierra. [49]
La mayor parte del ozono que se destruye se encuentra en la estratosfera inferior, en contraste con el agotamiento mucho menor del ozono a través de reacciones homogéneas en fase gaseosa, que ocurre principalmente en la estratosfera superior. [50]
Dado que la capa de ozono absorbe la luz ultravioleta UVB del sol, el agotamiento de la capa de ozono aumenta los niveles de UVB en la superficie (en igualdad de condiciones), lo que podría provocar daños, incluido un aumento del cáncer de piel . Ésta fue la razón del Protocolo de Montreal. Aunque las disminuciones del ozono estratosférico están bien relacionadas con los CFC y los aumentos de los rayos UVB en la superficie, no hay evidencia observacional directa que vincule el agotamiento del ozono con una mayor incidencia de cáncer de piel y daño ocular en los seres humanos. Esto se debe en parte a que los rayos UVA , que también han sido implicados en algunas formas de cáncer de piel, no son absorbidos por el ozono, y a que es casi imposible controlar las estadísticas de los cambios en el estilo de vida a lo largo del tiempo. El agotamiento del ozono también puede influir en los patrones del viento. [51]
El ozono, aunque es un componente minoritario en la atmósfera terrestre, es responsable de la mayor parte de la absorción de la radiación UVB. La cantidad de radiación UVB que penetra a través de la capa de ozono disminuye exponencialmente con el espesor de la trayectoria inclinada y la densidad de la capa. [52] Cuando los niveles de ozono estratosférico disminuyen, niveles más altos de UVB llegan a la superficie de la Tierra. [1] [53] La formación fenólica impulsada por los rayos UV en los anillos de los árboles ha fechado el inicio del agotamiento de la capa de ozono en las latitudes septentrionales a finales del siglo XVIII. [54]
En octubre de 2008, la Agencia Espacial Ecuatoriana publicó un informe llamado HIPERION. El estudio utilizó instrumentos terrestres en Ecuador y datos de los últimos 28 años de 12 satélites de varios países, y encontró que la radiación ultravioleta que llega a las latitudes ecuatoriales era mucho mayor de lo esperado, con un índice ultravioleta que llegó a 24 en Quito ; la OMS considera el 11 como un índice extremo y de gran riesgo para la salud. El informe concluyó que los niveles agotados de ozono en las latitudes medias del planeta ya están poniendo en peligro a grandes poblaciones en estas áreas. [55] Posteriormente, la CONIDA, la Agencia Espacial Peruana, publicó su propio estudio, que arrojó casi los mismos hallazgos que el estudio ecuatoriano.
La principal preocupación pública con respecto al agujero de la capa de ozono han sido los efectos del aumento de la radiación ultravioleta superficial en la salud humana. Hasta ahora, el agotamiento del ozono en la mayoría de los lugares ha sido típicamente de un pequeño porcentaje y, como se señaló anteriormente, no se dispone de evidencia directa de daños a la salud en la mayoría de las latitudes. Si los altos niveles de agotamiento observados en el agujero de ozono fueran comunes en todo el mundo, los efectos podrían ser sustancialmente más dramáticos. Dado que el agujero de ozono sobre la Antártida en algunos casos ha crecido tanto que ha afectado partes de Australia , Nueva Zelanda , Chile , Argentina y Sudáfrica , a los ambientalistas les preocupa que el aumento de la radiación ultravioleta en la superficie pueda ser significativo. [56] La radiación ultravioleta excesiva (UVR) tiene efectos reductores sobre las tasas de fotosíntesis y el crecimiento de las comunidades de diatomeas bentónicas (especies de microalgas que aumentan la calidad del agua y son resistentes a la contaminación) que están presentes en aguas dulces poco profundas. [57]
El agotamiento del ozono magnificaría todos los efectos de los rayos UV en la salud humana , tanto positivos (incluida la producción de vitamina D) como negativos (incluidas quemaduras solares, cáncer de piel y cataratas). Además, el aumento de la radiación ultravioleta en la superficie conduce a un aumento del ozono troposférico, lo que supone un riesgo para la salud de los seres humanos. [58]
Las formas más comunes de cáncer de piel en humanos, los carcinomas de células basales y de células escamosas , se han relacionado fuertemente con la exposición a los rayos UV-B. El mecanismo por el cual los rayos UVB inducen estos cánceres se comprende bien: la absorción de la radiación UV-B hace que las bases pirimidínicas de la molécula de ADN formen dímeros , lo que provoca errores de transcripción cuando el ADN se replica. Estos cánceres son relativamente leves y rara vez mortales, aunque el tratamiento del carcinoma de células escamosas a veces requiere una cirugía reconstructiva extensa. Combinando datos epidemiológicos con resultados de estudios en animales, los científicos han estimado que cada uno por ciento de disminución del ozono estratosférico a largo plazo aumentaría la incidencia de estos cánceres en un 2%. [59]
Otra forma de cáncer de piel, el melanoma maligno , es mucho menos común pero mucho más peligrosa, siendo letal en alrededor del 15 al 20 por ciento de los casos diagnosticados. La relación entre el melanoma maligno y la exposición a los rayos ultravioleta aún no se comprende completamente, pero parece que tanto los rayos UV-B como los UV-A están involucrados. Debido a esta incertidumbre, es difícil estimar el efecto del agotamiento del ozono sobre la incidencia del melanoma. Un estudio demostró que un aumento del 10 por ciento en la radiación UV-B se asoció con un aumento del 19 por ciento en los melanomas en los hombres y del 16 por ciento en las mujeres. [60] Un estudio de personas en Punta Arenas , en el extremo sur de Chile , mostró un aumento del 56 por ciento en melanoma y un aumento del 46 por ciento en cáncer de piel no melanoma durante un período de siete años, junto con una disminución del ozono y un aumento de los niveles de UVB. [61]
Los estudios epidemiológicos sugieren una asociación entre las cataratas corticales oculares y la exposición a los rayos UV-B, utilizando aproximaciones crudas de la exposición y diversas técnicas de evaluación de cataratas. En un estudio realizado en Chesapeake Bay Watermen, se llevó a cabo una evaluación detallada de la exposición ocular a los rayos UV-B, donde los aumentos en la exposición ocular anual promedio se asociaron con un mayor riesgo de opacidad cortical. [62] En este grupo altamente expuesto de hombres predominantemente blancos, la evidencia que vincula las opacidades corticales con la exposición a la luz solar fue la más fuerte hasta la fecha. Según estos resultados, se predice que el agotamiento de la capa de ozono causará cientos de miles de cataratas adicionales para 2050. [63]
El aumento de la radiación ultravioleta en la superficie conduce a un aumento del ozono troposférico . Generalmente se reconoce que el ozono troposférico es un riesgo para la salud, ya que el ozono es tóxico debido a sus fuertes propiedades oxidantes . Los riesgos son particularmente altos para los niños pequeños, los ancianos y las personas con asma u otras dificultades respiratorias. En la actualidad, el ozono a nivel del suelo se produce principalmente por la acción de la radiación UV sobre los gases de combustión de los gases de escape de los vehículos. [64]
La vitamina D se produce en la piel mediante la luz ultravioleta. Por lo tanto, una mayor exposición a los rayos UVB aumenta la vitamina D humana en quienes tienen deficiencia de ella. [65] Investigaciones recientes (principalmente desde el Protocolo de Montreal) muestran que muchos humanos tienen niveles de vitamina D inferiores a los óptimos. En particular, en la población de EE. UU., según la información de la Encuesta Nacional de Examen de Salud y Nutrición, se encontró que la cuarta parte más baja de vitamina D (<17,8 ng/ml) estaba asociada con un aumento en la mortalidad por todas las causas en la población general. [66] Si bien un nivel sanguíneo de vitamina D superior a 100 ng/ml parece aumentar excesivamente el calcio en sangre y estar asociado con una mayor mortalidad, el cuerpo tiene mecanismos que impiden que la luz solar produzca vitamina D en exceso de las necesidades del cuerpo. [67]
Un informe de noviembre de 2011 realizado por científicos del Instituto de Zoología de Londres encontró que las ballenas frente a la costa de California han mostrado un fuerte aumento en el daño solar, y estos científicos "temen que la culpa sea del adelgazamiento de la capa de ozono". [68] El estudio fotografió y tomó biopsias de piel de más de 150 ballenas en el Golfo de California y encontró "evidencia generalizada de daño epidérmico comúnmente asociado con quemaduras solares agudas y graves", con células que se forman cuando el ADN se daña por la radiación ultravioleta. Los hallazgos sugieren que "el aumento de los niveles de radiación ultravioleta como resultado del agotamiento de la capa de ozono es el culpable del daño observado en la piel, de la misma manera que las tasas de cáncer de piel humana han aumentado en las últimas décadas". [69] Además de las ballenas, muchos otros animales como perros, gatos, ovejas y ecosistemas terrestres también sufren los efectos negativos del aumento de las radiaciones UV-B. [70]
Se esperaría que un aumento de la radiación ultravioleta afectara a los cultivos. Varias especies de plantas económicamente importantes, como el arroz , dependen de las cianobacterias que residen en sus raíces para la retención de nitrógeno . Las cianobacterias son sensibles a la radiación ultravioleta y se verían afectadas por su aumento. [71] "A pesar de los mecanismos para reducir o reparar los efectos del aumento de la radiación ultravioleta, las plantas tienen una capacidad limitada para adaptarse a niveles elevados de UVB, por lo tanto, el crecimiento de las plantas puede verse directamente afectado por la radiación UVB". [72]
Con el paso de los años, la capa de ozono del Ártico se ha agotado gravemente. Como consecuencia, las especies que viven por encima de la capa de nieve o en zonas donde la nieve se ha derretido abundantemente, debido a las altas temperaturas, se ven afectadas negativamente por la radiación ultravioleta que llega al suelo. [73] Inicialmente se asumiría que el agotamiento de la capa de ozono y permitir un exceso de radiación UVB aumentaría el daño causado al ADN de las plantas. Los informes han encontrado que cuando las plantas se exponen a radiación UVB similar al agotamiento del ozono estratosférico, no hubo cambios significativos en la altura de la planta o la masa foliar, pero mostraron una respuesta en la biomasa de los brotes y el área foliar con una pequeña disminución. [74] Sin embargo, se ha demostrado que la radiación UVB disminuye el rendimiento cuántico del fotosistema II. [75] El daño de los rayos UVB solo ocurre bajo exposición extrema, y la mayoría de las plantas también tienen flavonoides que absorben los rayos UVB, lo que les permite aclimatarse a la radiación presente. Las plantas experimentan diferentes niveles de radiación ultravioleta a lo largo del día. Se sabe que son capaces de cambiar los niveles y tipos de protectores solares UV (es decir, flavonoides) que contienen a lo largo del día. Esto les permite aumentar su protección contra la radiación UV. [76] Las plantas que han sido afectadas por la radiación durante todo el desarrollo se ven más afectadas por la incapacidad de interceptar la luz con un área foliar más grande que por tener sistemas fotosintéticos comprometidos. [77] Es más probable que el daño causado por la radiación UVB sea significativo en las interacciones entre especies que en las plantas mismas. [78]
Otro impacto significativo del agotamiento del ozono en la vida vegetal es el estrés que experimentan las plantas cuando se exponen a la radiación ultravioleta. Esto puede provocar una disminución del crecimiento de las plantas y un aumento del estrés oxidativo, debido a la producción de óxido nítrico y peróxido de hidrógeno. [79] En áreas donde se ha producido un agotamiento sustancial de la capa de ozono, el aumento de la radiación UV-B reduce la productividad de las plantas terrestres (y también el secuestro de carbono) en aproximadamente un 6%. [80]
Además, si las plantas están expuestas a altos niveles de radiación ultravioleta, pueden provocar la producción de compuestos orgánicos volátiles dañinos , como los isoprenos. La emisión de isoprenos al aire por parte de las plantas puede afectar gravemente al medio ambiente al aumentar la contaminación del aire y aumentar la cantidad de carbono en la atmósfera, contribuyendo en última instancia al cambio climático. [81]
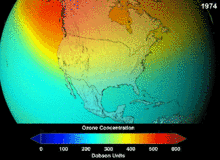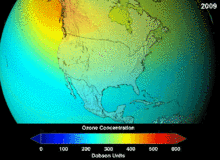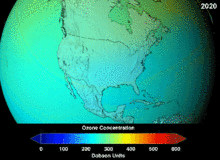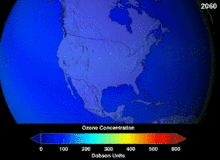
Se desconoce y no se conocerá hasta dentro de décadas el alcance total del daño que los CFC han causado a la capa de ozono; sin embargo, ya se han observado marcadas disminuciones en la columna de ozono. Las convenciones de Montreal y Viena se instalaron mucho antes de que se estableciera un consenso científico o se resolvieran importantes incertidumbres en el campo científico. [82] El caso del ozono fue comprendido comparablemente bien por los profanos, ya que, por ejemplo, el escudo de ozono o el agujero de ozono eran "metáforas puente útiles y fáciles de entender". [83] Los estadounidenses abandonaron voluntariamente los aerosoles, lo que resultó en una pérdida de ventas del 50 por ciento incluso antes de que se aplicara la legislación. [83]
Después de que un informe de 1976 de la Academia Nacional de Ciencias de los Estados Unidos concluyera que evidencia científica creíble respaldaba la hipótesis del agotamiento de la capa de ozono [84] , unos pocos países, entre ellos Estados Unidos, Canadá, Suecia, Dinamarca y Noruega, tomaron medidas para eliminar el uso de CFC. en latas de aerosol. [85] En ese momento, esto se consideró ampliamente como un primer paso hacia una política de regulación más integral, pero el progreso en esta dirección se desaceleró en los años siguientes, debido a una combinación de factores políticos (resistencia continua de la industria de los halocarbonos y un cambio general en actitud hacia la regulación ambiental durante los dos primeros años de la administración Reagan) y los avances científicos (evaluaciones posteriores de la Academia Nacional que indicaron que las primeras estimaciones de la magnitud del agotamiento de la capa de ozono habían sido demasiado grandes). Una importante patente de fabricación de DuPont para el freón expiraría en 1979 . Estados Unidos prohibió el uso de CFC en latas de aerosol en 1978. [85] La Comunidad Europea rechazó las propuestas para prohibir los CFC en aerosoles y, en Estados Unidos, los CFC continuaron utilizándose como refrigerantes y para limpiar placas de circuitos. La producción mundial de CFC cayó bruscamente después de la prohibición de los aerosoles en Estados Unidos, pero en 1986 había vuelto casi a su nivel de 1976. [85] En 1993, DuPont Canadá cerró sus instalaciones de CFC. [86]
La actitud del gobierno estadounidense comenzó a cambiar nuevamente en 1983, cuando William Ruckelshaus reemplazó a Anne M. Burford como Administradora de la Agencia de Protección Ambiental de Estados Unidos . Bajo Ruckelshaus y su sucesor, Lee Thomas, la EPA impulsó un enfoque internacional para las regulaciones de halocarbonos. En 1985, veinte naciones, incluidas la mayoría de los principales productores de CFC, firmaron la Convención de Viena para la Protección de la Capa de Ozono , que estableció un marco para negociar regulaciones internacionales sobre sustancias que agotan la capa de ozono. Ese mismo año se anunció el descubrimiento del agujero de ozono en la Antártida, lo que provocó un resurgimiento de la atención pública sobre el tema. En 1987, representantes de 43 naciones firmaron el Protocolo de Montreal . Mientras tanto, la industria de los halocarbonos cambió su posición y comenzó a apoyar un protocolo para limitar la producción de CFC. Sin embargo, este cambio fue desigual: DuPont actuó más rápidamente que sus homólogos europeos. Es posible que DuPont haya temido acciones judiciales relacionadas con el aumento del cáncer de piel, especialmente porque la EPA había publicado un estudio en 1986 afirmando que se esperaban 40 millones de casos adicionales y 800.000 muertes por cáncer en los EE.UU. en los próximos 88 años. [87] La UE también cambió su posición después de que Alemania abandonó su defensa de la industria de los CFC y comenzó a apoyar medidas hacia la regulación. Los gobiernos y las industrias de Francia y el Reino Unido intentaron defender sus industrias productoras de CFC incluso después de la firma del Protocolo de Montreal. [88]
En Montreal, los participantes acordaron congelar la producción de CFC a los niveles de 1986 y reducir la producción en un 50 por ciento para 1999. [85] Después de que una serie de expediciones científicas a la Antártida produjeron pruebas convincentes de que el agujero de la capa de ozono fue realmente causado por el cloro y el bromo A partir de organohalogenados artificiales, el Protocolo de Montreal se fortaleció en una reunión celebrada en 1990 en Londres. Los participantes acordaron eliminar por completo los CFC y los halones (aparte de una cantidad muy pequeña marcada para ciertos usos "esenciales", como los inhaladores para el asma ) para el año 2000 en los países que no operan al amparo del Artículo 5 y para 2010 en los signatarios del Artículo 5 (menos desarrollados). [89] En una reunión celebrada en 1992 en Copenhague, la fecha de eliminación se adelantó a 1996. [89] En la misma reunión, se añadió a la lista de productos controlados el bromuro de metilo (MeBr), un fumigante utilizado principalmente en la producción agrícola. sustancias. Para todas las sustancias controladas conforme al protocolo, los cronogramas de eliminación se retrasaron para los países menos desarrollados ("Artículo 5(1)"), y la eliminación en estos países fue respaldada por transferencias de experiencia, tecnología y dinero de países no incluidos en el Artículo 5(1). Partes en el Protocolo. Además, se podrían solicitar exenciones de los calendarios acordados en el marco del proceso de Exención de Uso Esencial (EUE) para sustancias distintas del metilbromuro y en el marco del proceso de Exención de Uso Crítico (CUE) para el metilbromuro. [90] [91]
La sociedad civil, incluidas especialmente las organizaciones no gubernamentales (ONG), desempeñó un papel fundamental en todas las etapas del desarrollo de políticas previas a la Conferencia de Viena, el Protocolo de Montreal y en la evaluación del cumplimiento posterior. [92] [93] [94] [95] Las principales empresas afirmaron que no existían alternativas a los HFC. [96] En un instituto tecnológico de Hamburgo, Alemania, se desarrolló un refrigerante de hidrocarburos seguro para la capa de ozono, que consiste en una mezcla de gases de hidrocarburos propano y butano , y en 1992 llamó la atención de la ONG Greenpeace. Greenpeace lo llamó "Greenfreeze". [97] [98] Luego, la ONG trabajó con éxito, primero con una empresa pequeña y en dificultades para comercializar un electrodoméstico, comenzando en Europa, luego en Asia y más tarde en América Latina, y recibió un premio del PNUMA en 1997. [99] [100] En 1995, Alemania ya había ilegalizado los refrigeradores con CFC. [100] Desde 2004, corporaciones como Coca-Cola, Carlsberg e IKEA han estado formando una coalición para promover las unidades Greenfreeze seguras para el ozono. La producción se extendió a empresas como Electrolux, Bosch y LG, cuyas ventas alcanzaron unos 300 millones de refrigeradores en 2008. [99] [101] En América Latina, una empresa nacional argentina inició la producción de Greenfreeze en 2003, mientras que el gigante Bosch de Brasil inició una año después. [102] [103] En 2013, lo utilizaban unos 700 millones de refrigeradores, lo que representaba alrededor del 40 por ciento del mercado. [96]
En Estados Unidos, sin embargo, el cambio ha sido mucho más lento. Hasta cierto punto, los CFC estaban siendo reemplazados por hidroclorofluorocarbonos ( HCFC ), menos dañinos, aunque también persisten preocupaciones con respecto a los HCFC. En algunas aplicaciones, se estaban utilizando hidrofluorocarbonos ( HFC ) para reemplazar a los CFC. Los HFC, que no contienen cloro ni bromo, no contribuyen en absoluto al agotamiento de la capa de ozono, aunque son potentes gases de efecto invernadero. El más conocido de estos compuestos es probablemente el HFC-134a ( R-134a ), que en los Estados Unidos ha reemplazado en gran medida al CFC-12 ( R-12 ) en los acondicionadores de aire de los automóviles. En los análisis de laboratorio (un antiguo uso "esencial") las sustancias que agotan la capa de ozono se pueden sustituir por otros disolventes diferentes. [104] Compañías químicas como Du Pont, cuyos representantes incluso menospreciaron a Greenfreeze como "esa tecnología alemana", maniobraron a la EPA para bloquear la tecnología en los EE. UU. hasta 2011. [105] [106] [107] [108] Ben & Jerry's de Unilever y General Electric, estimulados por Greenpeace, habían expresado formalmente en 2008 un interés que figuraba en la aprobación final de la EPA. [99] [109]
La UE reformuló su Reglamento sobre el Ozono en 2009. La ley prohíbe las sustancias que agotan la capa de ozono con el objetivo de proteger la capa de ozono. [110] La lista de SAO sujetas a la reglamentación es la misma que la del Protocolo de Montreal, con algunas adiciones. [111]
Más recientemente, los expertos en políticas han abogado por esfuerzos para vincular los esfuerzos de protección del ozono con los esfuerzos de protección del clima. [112] [113] Muchas SAO también son gases de efecto invernadero, algunos miles de veces más potentes agentes de forzamiento radiativo que el dióxido de carbono a corto y mediano plazo. Por lo tanto, las políticas que protegen la capa de ozono han tenido beneficios en la mitigación del cambio climático . De hecho, la reducción del forzamiento radiativo debido a las SAO probablemente enmascaró el verdadero nivel de los efectos del cambio climático de otros gases de efecto invernadero y fue responsable de la "desaceleración" del calentamiento global desde mediados de los años 90. [114] [ se necesitan citas adicionales ] Las decisiones políticas en un ámbito afectan los costos y la eficacia de las mejoras ambientales en el otro.
La OMI ha modificado la Regla 12 del Anexo VI del MARPOL en relación con las sustancias que agotan la capa de ozono. A partir del 1 de julio de 2010, todos los buques a los que se aplica el Anexo VI de MARPOL deben tener una lista de equipos que utilizan sustancias que agotan la capa de ozono. La lista debe incluir el nombre de las SAO, tipo y ubicación del equipo, cantidad en kg y fecha. Todos los cambios desde esa fecha deberían registrarse en un libro de registro de SAO a bordo en el que se registren todas las emisiones intencionadas o no intencionadas a la atmósfera. Además, también se deben registrar los nuevos suministros o desembarques de SAO en instalaciones costeras.

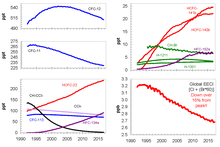
Desde que la adopción y el fortalecimiento del Protocolo de Montreal condujeron a reducciones en las emisiones de CFC, las concentraciones atmosféricas de los compuestos más importantes han ido disminuyendo. Estas sustancias se están eliminando gradualmente de la atmósfera; Desde que alcanzó su punto máximo en 1994, el nivel de cloro equivalente efectivo (EECl) en la atmósfera había disminuido aproximadamente un 10 por ciento en 2008. La disminución de las sustancias químicas que agotan la capa de ozono también se ha visto afectada significativamente por una disminución de las sustancias químicas que contienen bromo . Los datos sugieren que existen importantes fuentes naturales de bromuro de metilo atmosférico ( CH
3hermano ). [1] La eliminación gradual de los CFC significa que el óxido nitroso ( N
2O ), que no está cubierto por el Protocolo de Montreal, se ha convertido en la sustancia que agota la capa de ozono con mayores emisiones y se espera que siga siéndolo durante todo el siglo XXI. [115]
Según el Sexto Informe de Evaluación del IPCC, los niveles globales de ozono estratosférico experimentaron una rápida disminución en los años 1970 y 1980 y desde entonces han ido aumentando, pero no han alcanzado los niveles preindustriales. Aunque se espera una variabilidad considerable de un año a otro, incluso en las regiones polares donde el agotamiento es mayor, se espera que la capa de ozono continúe recuperándose en las próximas décadas debido a la disminución de las concentraciones de sustancias que agotan el ozono, suponiendo que se cumpla plenamente el Protocolo de Montreal. [116]
Se espera que el agujero de ozono en la Antártida continúe durante décadas. Las concentraciones de ozono en la estratosfera inferior sobre la Antártida aumentaron entre un 5 y un 10 por ciento para 2020 y volverán a los niveles anteriores a 1980 aproximadamente entre 2060 y 2075. Esto es entre 10 y 25 años más tarde de lo previsto en evaluaciones anteriores, debido a las estimaciones revisadas de las concentraciones atmosféricas de sustancias que agotan la capa de ozono, incluido un mayor uso futuro previsto en los países en desarrollo. Otro factor que puede prolongar el agotamiento de la capa de ozono es la extracción de óxidos de nitrógeno desde arriba de la estratosfera debido a los cambios en los patrones del viento. [117] En 2016 se informó de una tendencia gradual hacia la "curación". [23] En 2019, el agujero de ozono alcanzó su nivel más pequeño en los treinta años anteriores, debido a que la estratosfera polar más cálida debilitó el vórtice polar. [118] En septiembre de 2023, el agujero de ozono de la Antártida era uno de los más grandes jamás registrados, con 26 millones de kilómetros cuadrados. La pérdida anormalmente grande de ozono puede haber sido el resultado de la erupción volcánica de Tonga en 2022 . [119]
Los procesos físicos y químicos básicos que conducen a la formación de una capa de ozono en la estratosfera de la Tierra fueron descubiertos por Sydney Chapman en 1930. La radiación ultravioleta de longitud de onda corta descompone el oxígeno ( O
2) molécula en dos átomos de oxígeno (O), que luego se combinan con otras moléculas de oxígeno para formar ozono. El ozono se elimina cuando un átomo de oxígeno y una molécula de ozono se "recombinan" para formar dos moléculas de oxígeno, es decir, O + O.
3→ 2O
2. En la década de 1950, David Bates y Marcel Nicolet presentaron pruebas de que varios radicales libres, en particular el hidroxilo (OH) y el óxido nítrico (NO), podrían catalizar esta reacción de recombinación, reduciendo la cantidad total de ozono. Se sabía que estos radicales libres estaban presentes en la estratosfera, por lo que se los consideraba parte del equilibrio natural; se estimó que, en su ausencia, la capa de ozono sería aproximadamente el doble de gruesa de lo que es actualmente.
En 1970 Paul Crutzen señaló que las emisiones de óxido nitroso ( N
2O ), un gas estable y de larga vida producido por bacterias del suelo, de la superficie de la Tierra podría afectar la cantidad de óxido nítrico (NO) en la estratosfera. Crutzen demostró que el óxido nitroso vive lo suficiente como para llegar a la estratosfera, donde se convierte en NO. Crutzen luego señaló que el aumento del uso de fertilizantes podría haber llevado a un aumento de las emisiones de óxido nitroso con respecto al entorno natural, lo que a su vez daría lugar a un aumento de la cantidad de NO en la estratosfera. Por tanto, la actividad humana podría afectar la capa de ozono estratosférica. Al año siguiente, Crutzen y (de forma independiente) Harold Johnston sugirieron que las emisiones de NO de los aviones de pasajeros supersónicos , que volarían en la estratosfera inferior, también podrían agotar la capa de ozono. Sin embargo, un análisis más reciente realizado en 1995 por David W. Fahey, un científico atmosférico de la Administración Nacional Oceánica y Atmosférica , encontró que la caída del ozono sería del 1 al 2 por ciento si se operara una flota de 500 aviones supersónicos de pasajeros. [120] Esto, expresó Fahey, no sería un obstáculo para el desarrollo avanzado de aviones supersónicos de pasajeros. [121]
En 1974, Frank Sherwood Rowland , profesor de química de la Universidad de California en Irvine, y su asociado postdoctoral Mario J. Molina sugirieron que los compuestos halógenos orgánicos de larga vida, como los CFC, podrían comportarse de manera similar a la que Crutzen había propuesto para el óxido nitroso. . James Lovelock había descubierto recientemente, durante un crucero por el Atlántico Sur en 1971, que casi todos los compuestos de CFC fabricados desde su invención en 1930 todavía estaban presentes en la atmósfera. Molina y Rowland concluyeron que, al igual que N
2O , los CFC llegarían a la estratosfera donde serían disociados por la luz ultravioleta, liberando átomos de cloro. Un año antes, Richard Stolarski y Ralph Cicerone, de la Universidad de Michigan, habían demostrado que el Cl es incluso más eficaz que el NO para catalizar la destrucción del ozono. Michael McElroy y Steven Wofsy de la Universidad de Harvard llegaron a conclusiones similares . Sin embargo, ninguno de los grupos se había dado cuenta de que los CFC eran una fuente potencialmente importante de cloro estratosférico; en cambio, habían estado investigando los posibles efectos de las emisiones de HCl del transbordador espacial , que son mucho más pequeñas.
La hipótesis de Rowland-Molina fue fuertemente cuestionada por representantes de las industrias de aerosoles y halocarbonos. El presidente de la junta directiva de DuPont fue citado diciendo que la teoría del agotamiento de la capa de ozono es "un cuento de ciencia ficción... un montón de basura... una completa tontería". [122] Robert Abplanalp , presidente de Precision Valve Corporation (e inventor de la primera válvula práctica de lata de aerosol), escribió al rector de UC Irvine para quejarse de las declaraciones públicas de Rowland. [123] Sin embargo, en tres años la mayoría de las suposiciones básicas hechas por Rowland y Molina fueron confirmadas por mediciones de laboratorio y por observación directa en la estratosfera. Las concentraciones de los gases fuente (CFC y compuestos relacionados) y las especies reservorios de cloro (HCl y ClONO
2) se midieron en toda la estratosfera y demostraron que los CFC eran de hecho la principal fuente de cloro estratosférico y que casi todos los CFC emitidos llegarían eventualmente a la estratosfera. Aún más convincente fue la medición, realizada por James G. Anderson y sus colaboradores, del monóxido de cloro (ClO) en la estratosfera. El ClO se produce por la reacción del Cl con el ozono; su observación demostró así que los radicales Cl no sólo estaban presentes en la estratosfera sino que también participaban en la destrucción del ozono. McElroy y Wofsy ampliaron el trabajo de Rowland y Molina al demostrar que los átomos de bromo eran catalizadores aún más eficaces para la pérdida de ozono que los átomos de cloro y argumentaron que los compuestos orgánicos bromados conocidos como halones , ampliamente utilizados en los extintores de incendios, eran una fuente potencialmente importante de contaminación estratosférica. bromo. En 1976, la Academia Nacional de Ciencias de los Estados Unidos publicó un informe en el que concluía que la hipótesis del agotamiento de la capa de ozono estaba firmemente respaldada por evidencia científica. En respuesta, Estados Unidos, Canadá y Noruega prohibieron el uso de CFC en latas de aerosol en 1978. Las primeras estimaciones fueron que, si la producción de CFC continuaba a los niveles de 1977, el ozono atmosférico total alcanzaría después de aproximadamente un siglo un estado estable, 15 hasta un 18 por ciento por debajo de los niveles normales. En 1984, cuando se disponía de mejores pruebas sobre la velocidad de las reacciones críticas, esta estimación se cambió a un agotamiento en estado estacionario del 5 al 9 por ciento. [124]
Crutzen, Molina y Rowland recibieron el Premio Nobel de Química en 1995 por su trabajo sobre el ozono estratosférico.
El descubrimiento del "agujero de ozono" en la Antártida por los científicos del Servicio Antártico Británico Farman , Gardiner y Shanklin (informado por primera vez en un artículo en Nature en mayo de 1985 [125] ) supuso un shock para la comunidad científica, porque la disminución observada en el ozono polar era mucho mayor de lo que nadie había previsto. [126] Las mediciones satelitales ( TOMS a bordo de Nimbus 7 ) que mostraban un agotamiento masivo de la capa de ozono alrededor del polo sur estaban disponibles al mismo tiempo. [127] Sin embargo, inicialmente estos fueron rechazados como irrazonables por los algoritmos de control de calidad de los datos (fueron filtrados como errores ya que los valores eran inesperadamente bajos); El agujero de la capa de ozono se detectó sólo en datos satelitales cuando los datos brutos se reprocesaron tras la evidencia del agotamiento de la capa de ozono en observaciones in situ . [88] Cuando el software se volvió a ejecutar sin las banderas, el agujero de ozono se vio ya en 1976. [128]
Susan Solomon , química atmosférica de la Administración Nacional Oceánica y Atmosférica (NOAA), propuso que las reacciones químicas en las nubes estratosféricas polares (PSC) en la fría estratosfera antártica causaron un aumento masivo, aunque localizado y estacional, en la cantidad de cloro presente en formas activas que destruyen el ozono. Las nubes estratosféricas polares en la Antártida sólo se forman cuando hay temperaturas muy bajas, de hasta -80 °C, y condiciones de principios de primavera. En tales condiciones, los cristales de hielo de la nube proporcionan una superficie adecuada para la conversión de compuestos de cloro no reactivos en compuestos de cloro reactivos, que pueden agotar el ozono fácilmente.
Además, el vórtice polar formado sobre la Antártida es muy denso y la reacción que se produce en la superficie de los cristales de las nubes es muy diferente a la que se produce en la atmósfera. Estas condiciones han provocado la formación de un agujero de ozono en la Antártida. Esta hipótesis fue confirmada decisivamente, primero por mediciones de laboratorio y posteriormente por mediciones directas, desde tierra y desde aviones de gran altitud , de concentraciones muy altas de monóxido de cloro (ClO) en la estratosfera antártica. [129]
También se probaron hipótesis alternativas, que atribuían el agujero de la capa de ozono a variaciones de la radiación ultravioleta solar o a cambios en los patrones de circulación atmosférica, y se demostró que eran insostenibles. [130]
Mientras tanto, el análisis de las mediciones de ozono de la red mundial de espectrofotómetros Dobson terrestres llevó a un panel internacional a concluir que la capa de ozono de hecho se estaba agotando, en todas las latitudes fuera de los trópicos. [30] Estas tendencias fueron confirmadas por mediciones satelitales. Como consecuencia, las principales naciones productoras de halocarbonos acordaron eliminar gradualmente la producción de CFC, halones y compuestos relacionados, proceso que se completó en 1996.
Desde 1981 el Programa de las Naciones Unidas para el Medio Ambiente , bajo los auspicios de la Organización Meteorológica Mundial, ha patrocinado una serie de informes técnicos sobre la Evaluación Científica del Agotamiento de la Ozono , basados en mediciones satelitales. El informe de 2007 mostró que el agujero en la capa de ozono se estaba recuperando y era el más pequeño en aproximadamente una década. [131] El informe de 2010 encontró: "Durante la última década, el ozono global y el ozono en las regiones árticas y antárticas ya no están disminuyendo pero aún no están aumentando. Se proyecta que la capa de ozono fuera de las regiones polares se recupere a su nivel anterior a 1980. niveles en algún momento antes de mediados de este siglo. Por el contrario, se espera que el agujero de ozono de primavera sobre la Antártida se recupere mucho más tarde". [132] En 2012, la NOAA y la NASA informaron que "las temperaturas del aire más cálidas por encima de la Antártida provocaron el segundo agujero de ozono estacional más pequeño en 20 años, con un promedio de 17,9 millones de kilómetros cuadrados. El agujero alcanzó su tamaño máximo para la temporada el 22 de septiembre, extendiéndose hasta 21,2 millones de kilómetros cuadrados." [133] En 2016 [23] y luego en 2017 se informó de una tendencia gradual hacia la "curación". [134] Se informa que la señal de recuperación es evidente incluso en las altitudes de saturación de pérdida de ozono. [135]
El agujero de la capa de ozono de la Tierra sobre el Polo Sur ha afectado la circulación atmosférica en el hemisferio sur hasta el ecuador. [136] El agujero de ozono ha influido en la circulación atmosférica hasta los trópicos y ha aumentado las precipitaciones en latitudes bajas y subtropicales en el hemisferio sur. [137]
El 3 de marzo de 2005, la revista Nature [138] publicó un artículo que relacionaba el inusualmente grande agujero de ozono del Ártico ocurrido en 2004 con la actividad del viento solar.
El 15 de marzo de 2011 se observó una pérdida récord de la capa de ozono, destruyéndose aproximadamente la mitad del ozono presente sobre el Ártico. [139] [140] [141] El cambio se atribuyó a inviernos cada vez más fríos en la estratosfera ártica a una altitud de aproximadamente 20 km (12 millas), un cambio asociado con el calentamiento global en una relación que aún está bajo investigación. [140] Para el 25 de marzo, la pérdida de ozono se había convertido en la mayor en comparación con la observada en todos los inviernos anteriores con la posibilidad de que se convirtiera en un agujero de ozono. [142] Esto requeriría que las cantidades de ozono cayeran por debajo de 200 unidades Dobson, de las 250 registradas en Siberia central. [142] Se predice que la capa adelgazante afectaría partes de Escandinavia y Europa del Este del 30 al 31 de marzo. [142]
El 2 de octubre de 2011 se publicó un estudio en la revista Nature , que decía que entre diciembre de 2010 y marzo de 2011 se destruyó hasta el 80 por ciento del ozono en la atmósfera a unos 20 kilómetros (12 millas) sobre la superficie. [143] El nivel de agotamiento de la capa de ozono fue lo suficientemente grave como para que los científicos dijeran que podría compararse con el agujero de ozono que se forma sobre la Antártida cada invierno. [143] Según el estudio, "por primera vez, se produjo una pérdida suficiente para describirse razonablemente como un agujero de ozono en el Ártico". [143] El estudio analizó datos de los satélites Aura y CALIPSO y determinó que la pérdida de ozono mayor de lo normal se debió a un período inusualmente largo de clima frío en el Ártico, unos 30 días más de lo normal, lo que permitió más Se crearán compuestos de cloro que destruyen la capa de ozono. [144] Según Lamont Poole, coautor del estudio, las partículas de nubes y aerosoles en las que se encuentran los compuestos de cloro "fueron abundantes en el Ártico hasta mediados de marzo de 2011, mucho más tarde de lo habitual, con cantidades promedio en algunas altitudes similares a los observados en la Antártida, y dramáticamente mayores que los valores cercanos a cero observados en marzo en la mayoría de los inviernos árticos". [144]
En 2013, los investigadores analizaron los datos y descubrieron que el evento ártico de 2010-11 no alcanzó los niveles de agotamiento de la capa de ozono para clasificarlo como un verdadero agujero. Un agujero en la capa de ozono generalmente se clasifica como 220 unidades Dobson o menos; [145] el agujero ártico no se acercó a ese nivel bajo. [146] [147] Desde entonces se ha clasificado como un "miniagujero". [148]
Tras el agotamiento de la capa de ozono en 1997 y 2011, en marzo de 2020 los globos meteorológicos midieron una caída del 90% de la capa de ozono sobre el Ártico, ya que normalmente registraban 3,5 partes por millón de ozono, en comparación con sólo alrededor de 0,3 partes por millón finalmente, debido a temperaturas frías jamás registradas desde 1979, y un fuerte vórtice polar que permitió que los productos químicos, incluidos el cloro y el bromo, fueran corroídos. [149]
En 2020 se estudió un raro agujero, resultado de temperaturas inusualmente bajas en la atmósfera sobre el Polo Norte. [150] [151]
Como los inviernos más fríos se ven más afectados, a veces se produce un agujero de ozono sobre el Tíbet. En 2006, se detectó un agujero de ozono de 2,5 millones de kilómetros cuadrados sobre el Tíbet. [152] También en 2011 apareció un agujero de ozono sobre las regiones montañosas del Tíbet , Xinjiang , Qinghai y el Hindu Kush , junto con un agujero sin precedentes sobre el Ártico, aunque el del Tíbet es mucho menos intenso que los del Ártico o la Antártida. . [153]
Una investigación realizada en 2012 demostró que el mismo proceso que produce el agujero de ozono sobre la Antártida ocurre sobre las nubes de tormenta de verano en los Estados Unidos y, por lo tanto, puede estar destruyendo el ozono allí también. [154] [155]
El físico Qing-Bin Lu, de la Universidad de Waterloo, afirmó haber descubierto un gran agujero de ozono permanente en la estratosfera inferior sobre los trópicos en julio de 2022. [156] Sin embargo, otros investigadores en el campo refutaron esta afirmación, afirmando que la investigación estuvo plagada de "errores graves y afirmaciones sin fundamento". [157] Según el Dr. Paul Young, autor principal de la Evaluación científica del agotamiento del ozono de la OMM y el PNUMA de 2022, "La identificación por parte del autor de un 'agujero de ozono tropical' se debe a que observó los cambios porcentuales en el ozono, en lugar de los cambios absolutos. , siendo este último mucho más relevante para los dañinos rayos UV que llegan a la superficie". Específicamente, el trabajo de Lu define el "agujero de ozono" como "un área con una pérdida de O3 en porcentaje superior al 25%, con respecto al valor de O3 no perturbado cuando no había CFC significativos en la estratosfera (~ en la década de 1960)" [ 158] de la definición general de 220 unidades Dobson o menos. La Dra. Marta Ábalos Álvarez añadió que "el agotamiento del ozono en los trópicos no es nada nuevo y se debe principalmente a la aceleración de la circulación Brewer-Dobson".
Al analizar los impactos atmosféricos de la temporada de incendios forestales en Australia 2019-20 , los científicos dirigidos por la investigadora del MIT Susan Solomon descubrieron que el humo destruyó entre el 3 y el 5 % del ozono en las zonas afectadas del hemisferio sur. Las partículas de humo absorben cloruro de hidrógeno y actúan como catalizador para crear radicales de cloro que destruyen el ozono. [159] [160] [161] [162]
Entre otros, Robert Watson tuvo un papel en la evaluación científica y en los esfuerzos de regulación del agotamiento de la capa de ozono y el calentamiento global . [82] Antes de la década de 1980, la UE, la NASA, la NAS, el PNUMA, la OMM y el gobierno británico tenían informes científicos discrepantes y Watson desempeñó un papel en el proceso de evaluaciones unificadas. Sobre la base de la experiencia con el caso del ozono, el IPCC comenzó a trabajar en una evaluación científica y de informes unificados [82] para llegar a un consenso para proporcionar el Resumen del IPCC para responsables de políticas .
Hay varias áreas de vínculo entre el agotamiento de la capa de ozono y la ciencia del calentamiento global:

En 2019, la NASA informó que no existía una relación significativa entre el tamaño del agujero de ozono y el cambio climático. [10]
Dado que las moléculas de CFC son más pesadas que el aire (nitrógeno u oxígeno), se cree comúnmente que las moléculas de CFC no pueden alcanzar la estratosfera en cantidades significativas. [166] Sin embargo, los gases atmosféricos no se clasifican por peso en estas altitudes; las fuerzas del viento pueden mezclar completamente los gases de la atmósfera. Los CFC más ligeros se distribuyen uniformemente por toda la turbosfera y alcanzan la atmósfera superior, [167] aunque algunos de los CFC más pesados no se distribuyen uniformemente. [168]

Otro concepto erróneo es que "generalmente se acepta que las fuentes naturales de cloro troposférico son de cuatro a cinco veces mayores que las artificiales". Si bien esta afirmación es estrictamente cierta, el cloro troposférico es irrelevante; es el cloro estratosférico el que afecta el agotamiento del ozono. El cloro procedente de las salpicaduras del océano es soluble y, por tanto, la lluvia lo lava antes de llegar a la estratosfera. Los CFC, por el contrario, son insolubles y de larga vida, lo que les permite llegar a la estratosfera. En la atmósfera inferior, hay mucho más cloro procedente de los CFC y haloalcanos relacionados que el HCl procedente de la niebla salina, y en la estratosfera los halocarbonos son dominantes. [169] Sólo el cloruro de metilo, que es uno de estos halocarbonos, tiene una fuente principalmente natural, [170] y es responsable de aproximadamente el 20 por ciento del cloro en la estratosfera; el 80 por ciento restante proviene de fuentes artificiales.
Las erupciones volcánicas muy violentas pueden inyectar HCl en la estratosfera, pero los investigadores [171] han demostrado que la contribución no es significativa en comparación con la de los CFC. Una afirmación errónea similar es que los compuestos halógenos solubles de la columna volcánica del Monte Erebus en la isla Ross, Antártida, son uno de los principales contribuyentes al agujero de ozono en la Antártida. [171]
Sin embargo, un estudio de 2015 [172] mostró que probablemente se subestimó el papel del volcán Monte Erebus en el agotamiento del ozono en la Antártida. Basándose en los datos de reanálisis de NCEP/NCAR de los últimos 35 años y utilizando el modelo de trayectoria HYSPLIT de NOAA , los investigadores demostraron que las emisiones de gases del volcán Erebus (incluido el cloruro de hidrógeno (HCl)) pueden llegar a la estratosfera antártica a través de ciclones de alta latitud y luego a la vórtice polar . Dependiendo de la actividad del volcán Erebus, la masa anual adicional de HCl que ingresa a la estratosfera desde Erebus varía de 1,0 a 14,3 kt.
GMB Dobson mencionó que cuando se midieron por primera vez los niveles de ozono primaveral en la Antártida sobre la Bahía Halley en 1956, se sorprendió al descubrir que eran ~320 DU, o alrededor de 150 DU por debajo de los niveles primaverales del Ártico de ~450 DU. Estos eran en ese momento los únicos valores conocidos de ozono antártico disponibles. Lo que Dobson describe es esencialmente la línea de base a partir de la cual se mide el agujero de la capa de ozono: los valores reales del agujero de la capa de ozono están en el rango de 150 a 100 DU. [173]
La discrepancia entre el Ártico y la Antártida observada por Dobson fue principalmente una cuestión de tiempo: durante la primavera del Ártico los niveles de ozono aumentaron suavemente, alcanzando su punto máximo en abril, mientras que en la Antártida se mantuvieron aproximadamente constantes a principios de la primavera, aumentando abruptamente en noviembre cuando el vórtice polar rompió.
El comportamiento observado en el agujero de ozono de la Antártida es completamente diferente. En lugar de permanecer constantes, los niveles de ozono a principios de la primavera caen repentinamente desde sus ya bajos valores invernales, hasta en un 50 por ciento, y los valores normales no se vuelven a alcanzar hasta diciembre. [174]
Algunas personas pensaban que el agujero de la capa de ozono debería estar por encima de las fuentes de CFC. Sin embargo, los CFC están bien mezclados a nivel mundial en la troposfera y la estratosfera . La razón de la aparición del agujero de ozono sobre la Antártida no es porque haya más CFC concentrados sino porque las bajas temperaturas ayudan a formar nubes estratosféricas polares. [175] De hecho, hay hallazgos de "agujeros de ozono" significativos y localizados sobre otras partes de la tierra, como sobre Asia Central. [176]
Las ideas erróneas y los malentendidos públicos sobre cuestiones complejas como el agotamiento del ozono son comunes. El limitado conocimiento científico del público generó confusión sobre el calentamiento global [177] o la percepción del calentamiento global como un subconjunto del "agujero de ozono". [178] Al principio, las ONG verdes clásicas se abstuvieron de utilizar el agotamiento de CFC para hacer campaña, ya que asumieron que el tema era demasiado complicado. [82] Se volvieron activos mucho más tarde, por ejemplo, en el apoyo de Greenpeace a un frigorífico sin CFC producido por la antigua empresa de Alemania Oriental VEB dkk Scharfenstein. [82] [179]
Las metáforas utilizadas en el debate sobre los CFC (escudo de ozono, agujero de ozono) no son "exactas" en el sentido científico. El "agujero de ozono" es más una depresión , menos "un agujero en el parabrisas". El ozono no desaparece a través de la capa ni se produce un "adelgazamiento" uniforme de la capa de ozono. Sin embargo, resonaron mejor entre los no científicos y sus preocupaciones. [83] El agujero de la capa de ozono fue visto como un "tema candente" y un riesgo inminente [180] ya que los legos temían graves consecuencias personales como cáncer de piel, cataratas, daños a las plantas y reducción de las poblaciones de plancton en la zona fótica del océano. No sólo a nivel político, la regulación del ozono en comparación con el cambio climático obtuvo mejores resultados en la opinión pública. Los estadounidenses abandonaron voluntariamente los aerosoles antes de que se aplicara la legislación, mientras que el cambio climático no logró generar una preocupación y una acción pública comparables. [83] La repentina identificación en 1985 de que había un "agujero" sustancial fue ampliamente reportada en la prensa. El rápido agotamiento de la capa de ozono en la Antártida hasta ahora se había descartado como un error de medición. [126] Se estableció un consenso científico después de la regulación. [82]
Si bien el agujero de ozono en la Antártida tiene un efecto relativamente pequeño sobre el ozono global, ha generado un gran interés público porque:
En 1994, la Asamblea General de las Naciones Unidas votó a favor de designar el 16 de septiembre como el Día Internacional para la Preservación de la Capa de Ozono , o "Día Mundial del Ozono". [185] La designación conmemora la firma del Protocolo de Montreal [186] en esa fecha en 1987. [187]
Por tanto, la química del flúor no representa un sumidero importante de ozono estratosférico.
Todo el flúor liberado por los gases fuente termina en forma de HF, que se acumula en la estratosfera (Fig. 8).
... La alta estabilidad del HF lo convierte en un trazador eficaz del aporte de flúor a la estratosfera procedente de gases antropogénicos fluorados.
El yodo es un componente de varios gases que se emiten naturalmente desde los océanos.
Aunque el yodo puede participar en las reacciones de destrucción del ozono, estos gases fuente que contienen yodo generalmente tienen una vida útil muy corta y, como resultado, sólo una fracción muy pequeña llega a la estratosfera.
Existen grandes incertidumbres sobre cómo varían estas emisiones según la estación y la región geográfica.
{{cite journal}}: CS1 maint: numeric names: authors list (link){{cite web}}: CS1 maint: numeric names: authors list (link){{cite web}}: CS1 maint: unfit URL (link)4. Reacciones de radicales libres para la eliminación de ozono: Reacción 4.1
{{cite journal}}: Enlace externo en |quote={{cite journal}}: CS1 maint: numeric names: authors list (link){{cite web}}: CS1 maint: unfit URL (link){{cite book}}: CS1 maint: location missing publisher (link){{cite web}}: CS1 maint: unfit URL (link){{cite press release}}: CS1 maint: unfit URL (link){{cite web}}: CS1 maint: unfit URL (link){{cite web}}: CS1 maint: unfit URL (link){{cite web}}: CS1 maint: numeric names: authors list (link){{cite web}}: CS1 maint: unfit URL (link)