
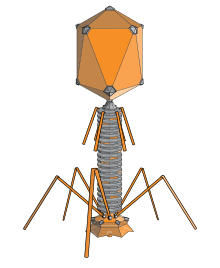

Un bacteriófago ( / b æ k ˈ t ɪər i oʊ f eɪ dʒ / ), también conocido informalmente como fago ( / ˈ f eɪ dʒ / ), es un virus que infecta y se replica dentro de bacterias y arqueas . El término se deriva de "bacteria" y del griego φαγεῖν ( fageína ), que significa "devorar". Los bacteriófagos están compuestos de proteínas que encapsulan un genoma de ADN o ARN y pueden tener estructuras simples o elaboradas. Sus genomas pueden codificar tan solo cuatro genes (por ejemplo, MS2 ) y hasta cientos de genes . Los fagos se replican dentro de la bacteria tras la inyección de su genoma en su citoplasma .
Los bacteriófagos se encuentran entre las entidades más comunes y diversas de la biosfera . [2] Los bacteriófagos son virus ubicuos que se encuentran dondequiera que existan bacterias. Se estima que hay más de 10 31 bacteriófagos en el planeta, más que todos los demás organismos de la Tierra, incluidas las bacterias, juntos. [3] Los virus son la entidad biológica más abundante en la columna de agua de los océanos del mundo, y el segundo componente más grande de la biomasa después de los procariotas , [4] donde se han encontrado hasta 9x10 8 viriones por mililitro en las esteras microbianas de la superficie. [5] y hasta el 70% de las bacterias marinas pueden estar infectadas por bacteriófagos. [6]
Los bacteriófagos se utilizaron desde los años 20 como alternativa a los antibióticos en la antigua Unión Soviética y en Europa Central, así como en Francia. [7] [8] Se consideran una posible terapia contra cepas de muchas bacterias resistentes a múltiples fármacos (ver terapia con fagos ). [9] [10] [11] [12]
Se sabe que los bacteriófagos interactúan con el sistema inmunológico tanto indirectamente a través de la expresión bacteriana de proteínas codificadas por fagos como directamente influyendo en la inmunidad innata y la eliminación bacteriana. [13] Las interacciones fago-huésped se están convirtiendo en áreas de investigación cada vez más importantes. [14]
Los bacteriófagos se encuentran en abundancia en la biosfera, con diferentes genomas y estilos de vida. Los fagos están clasificados por el Comité Internacional de Taxonomía de Virus (ICTV) según su morfología y ácido nucleico.


Se ha sugerido que los miembros de Picobirnaviridae infectan bacterias, pero no mamíferos. [dieciséis]
También hay muchos géneros no asignados de la clase Leviviricetes : Chimpavirus , Hohglivirus , Mahrahvirus , Meihzavirus , Nicedsevirus , Sculuvirus , Skrubnovirus , Tetipavirus y Winunavirus que contienen genomas lineales de ssRNA [17] y el género no asignado Lilyvirus del orden Caudovirales que contiene un genoma lineal de dsDNA.

En 1896, Ernest Hanbury Hankin informó que algo en las aguas de los ríos Ganges y Yamuna en la India tenía una marcada acción antibacteriana contra el cólera y podía pasar a través de un filtro de porcelana muy fino. [18] En 1915, el bacteriólogo británico Frederick Twort , superintendente de la Brown Institution de Londres, descubrió un pequeño agente que infectaba y mataba las bacterias. Creía que el agente debía ser uno de los siguientes:
La investigación de Twort se vio interrumpida por el inicio de la Primera Guerra Mundial , así como por la escasez de financiación y los descubrimientos de antibióticos.
Independientemente, el microbiólogo franco-canadiense Félix d'Hérelle , que trabaja en el Instituto Pasteur de París , anunció el 3 de septiembre de 1917 que había descubierto "un microbio invisible y antagonista del bacilo de la disentería ". Para d'Hérelle, no había dudas sobre la naturaleza de su descubrimiento: "En un instante lo entendí: lo que causaba mis manchas claras era en realidad un microbio invisible... un virus parásito de las bacterias". [20] D'Hérelle llamó al virus bacteriófago, un devorador de bacterias (del griego phagein , que significa "devorar"). También registró un relato dramático de un hombre que padecía disentería y que los bacteriófagos le devolvieron la buena salud. [21] Fue d'Hérelle quien realizó muchas investigaciones sobre los bacteriófagos e introdujo el concepto de terapia con fagos . [22] En 1919, en París, Francia, d'Hérelle llevó a cabo la primera aplicación clínica de un bacteriófago, y el primer uso informado en los Estados Unidos fue en 1922. [23]
En 1969, Max Delbrück , Alfred Hershey y Salvador Luria recibieron el Premio Nobel de Fisiología o Medicina por sus descubrimientos sobre la replicación de los virus y su estructura genética. [24] Específicamente, el trabajo de Hershey, como colaborador del experimento Hershey-Chase en 1952, proporcionó evidencia convincente de que el ADN, no las proteínas, era el material genético de la vida. Delbrück y Luria llevaron a cabo el experimento Luria-Delbrück que demostró estadísticamente que las mutaciones en las bacterias ocurren aleatoriamente y, por lo tanto, siguen principios darwinianos más que lamarckianos .

Se descubrió que los fagos eran agentes antibacterianos y se utilizaron en la antigua República Soviética de Georgia (cuyo pionero fue Giorgi Eliava con la ayuda del codescubridor de los bacteriófagos, Félix d'Hérelle ) durante las décadas de 1920 y 1930 para tratar infecciones bacterianas.
D'Herelle "aprendió rápidamente que los bacteriófagos se encuentran dondequiera que prosperen las bacterias: en las alcantarillas, en los ríos que recogen los desechos de las tuberías y en las heces de los pacientes convalecientes". [25]
Tuvieron un uso generalizado, incluido el tratamiento de los soldados del Ejército Rojo . [26] Sin embargo, fueron abandonados para uso general en Occidente por varias razones:
El uso de fagos ha continuado desde el final de la Guerra Fría en Rusia, [28] Georgia y otras partes de Europa central y oriental. El primer ensayo clínico regulado, aleatorizado y doble ciego se publicó en el Journal of Wound Care en junio de 2009, que evaluó la seguridad y eficacia de un cóctel de bacteriófagos para tratar úlceras venosas infectadas de la pierna en pacientes humanos. [29] La FDA aprobó el estudio como ensayo clínico de Fase I. Los resultados del estudio demostraron la seguridad de la aplicación terapéutica de bacteriófagos, pero no demostraron eficacia. Los autores explicaron que el uso de ciertas sustancias químicas que forman parte del cuidado estándar de las heridas (por ejemplo, lactoferrina o plata) puede haber interferido con la viabilidad de los bacteriófagos. [29] Poco después, en agosto de 2009 se informó en la revista Clinical Otolaryngology sobre otro ensayo clínico controlado en Europa occidental (tratamiento de infecciones de oído causadas por Pseudomonas aeruginosa ) . [30] El estudio concluye que las preparaciones de bacteriófagos eran seguras y efectivas para el tratamiento. de infecciones crónicas del oído en humanos. Además, se han realizado numerosos ensayos clínicos experimentales y en animales para evaluar la eficacia de los bacteriófagos para diversas enfermedades, como quemaduras y heridas infectadas e infecciones pulmonares asociadas a la fibrosis quística, entre otras. [30] Por otro lado, se ha demostrado que los fagos de Inoviridae complican las biopelículas involucradas en la neumonía y la fibrosis quística y protegen a las bacterias de los medicamentos destinados a erradicar la enfermedad, promoviendo así una infección persistente. [31]
Mientras tanto, los investigadores de bacteriófagos han estado desarrollando virus diseñados para superar la resistencia a los antibióticos y diseñando los genes de los fagos responsables de codificar las enzimas que degradan la matriz de la biopelícula, las proteínas estructurales de los fagos y las enzimas responsables de la lisis de la pared celular bacteriana. [5] [6] [7] Ha habido resultados que muestran que los fagos T4 que son pequeños en tamaño y de cola corta pueden ser útiles para detectar E. coli en el cuerpo humano. [32]
La eficacia terapéutica de un cóctel de fagos se evaluó en un modelo de ratón con infección nasal por A. baumannii multirresistente (MDR) . Los ratones tratados con el cóctel de fagos mostraron una tasa de supervivencia 2,3 veces mayor en comparación con los no tratados siete días después de la infección. [33]
En 2017, un paciente diabético de 68 años con pancreatitis necrotizante complicada por un pseudoquiste infectado con cepas de A. baumannii MDR estaba siendo tratado con un cóctel de azitromicina, rifampicina y colistina durante 4 meses sin resultados y su salud en general empeoraba rápidamente.
Debido a que había comenzado la discusión sobre la inutilidad clínica de un tratamiento adicional, se presentó y se aprobó un nuevo fármaco en investigación de emergencia (eIND, por sus siglas en inglés) como último esfuerzo para al menos obtener datos médicos valiosos de la situación, por lo que se sometió a una terapia con fagos utilizando un cóctel inyectado por vía percutánea (PC) que contenía nueve fagos diferentes que habían sido identificados como eficaces contra la cepa de infección primaria mediante técnicas de prueba y aislamiento rápido (un proceso que duró menos de un día). Esto resultó eficaz durante un período muy breve, aunque el paciente siguió sin responder y su salud siguió empeorando; pronto se recogieron aislados de una cepa de A. baumannii del drenaje del quiste que mostraba resistencia a este cóctel, y se añadió un segundo cóctel que se probó que era eficaz contra esta nueva cepa, esta vez mediante inyección intravenosa (IV). Había quedado claro que la infección era más generalizada de lo que se pensaba originalmente. [34]
Una vez que recibió la combinación de terapia intravenosa y PC, la trayectoria clínica descendente del paciente se revirtió y en dos días despertó del coma y reaccionó. Cuando su sistema inmunológico comenzó a funcionar, tuvieron que retirarle temporalmente el cóctel porque su fiebre subía a más de 104 °F (40 °C), pero después de dos días, los cócteles de fagos se reintrodujeron en niveles que podía tolerar. . El cóctel original de tres antibióticos fue reemplazado por minociclina después de que se descubrió que la cepa bacteriana no era resistente a ella y rápidamente recuperó la lucidez total, aunque no fue dado de alta del hospital hasta aproximadamente 145 días después de que comenzara la terapia con fagos. Hacia el final de la terapia se descubrió que las bacterias se habían vuelto resistentes a ambos cócteles de fagos originales, pero se continuó porque parecían impedir que se desarrollara resistencia a la minociclina en las muestras bacterianas recolectadas, por lo que tenían un efecto sinérgico útil. [34]
Los fagos se han utilizado cada vez más para proteger los productos alimenticios y prevenir las bacterias que los deterioran . [35] Desde 2006, la Administración de Medicamentos y Alimentos de los Estados Unidos (FDA) y el Departamento de Agricultura de los Estados Unidos (USDA) han aprobado varios productos de bacteriófagos. LMP-102 (Intralytix) fue aprobado para el tratamiento de productos cárnicos y aves de corral listos para el consumo (RTE). Ese mismo año, la FDA aprobó LISTEX (desarrollado y producido por Micreos ) utilizando bacteriófagos en el queso para matar la bacteria Listeria monocytogenes , con el fin de otorgarle un estado generalmente reconocido como seguro (GRAS). [36] En julio de 2007, se aprobó el uso del mismo bacteriófago en todos los productos alimenticios. [37] En 2011, el USDA confirmó que LISTEX es un coadyuvante de procesamiento de etiqueta limpia y está incluido en el USDA. [38] La investigación en el campo de la seguridad alimentaria continúa para ver si los fagos líticos son una opción viable para controlar otros patógenos transmitidos por los alimentos en diversos productos alimenticios. [39]
Los bacteriófagos, incluidos los específicos de Escherichia coli , se han empleado como indicadores de contaminación fecal en fuentes de agua. Debido a sus características estructurales y biológicas compartidas, los colifagos pueden servir como sustitutos de la contaminación fecal viral y la presencia de virus patógenos como rotavirus, norovirus y VHA. Las investigaciones realizadas en sistemas de tratamiento de aguas residuales han revelado disparidades significativas en el comportamiento de los colifagos en comparación con los coliformes fecales, lo que demuestra una clara correlación con la recuperación de virus patógenos al finalizar el tratamiento. Al establecer un umbral de descarga seguro, los estudios han determinado que las descargas por debajo de 3000 PFU/100 ml se consideran seguras en términos de limitar la liberación de virus patógenos. [40]
En 2011, la FDA autorizó el primer producto basado en bacteriófagos para uso diagnóstico in vitro. [41] La prueba de hemocultivo KeyPath MRSA/MSSA utiliza un cóctel de bacteriófagos para detectar Staphylococcus aureus en hemocultivos positivos y determinar la resistencia o susceptibilidad a la meticilina . La prueba arroja resultados en aproximadamente cinco horas, en comparación con los dos o tres días que tardan los métodos estándar de prueba de susceptibilidad e identificación microbiana. Fue la primera prueba acelerada de susceptibilidad a los antibióticos aprobada por la FDA. [42]
Las agencias gubernamentales de Occidente llevan varios años buscando ayuda en Georgia y la ex Unión Soviética para explotar fagos para contrarrestar armas biológicas y toxinas, como el ántrax y el botulismo . [43] Los desarrollos continúan entre los grupos de investigación en los EE. UU. Otros usos incluyen la aplicación por aspersión en horticultura para proteger plantas y productos vegetales contra la descomposición y la propagación de enfermedades bacterianas. Otras aplicaciones de los bacteriófagos son como biocidas para superficies ambientales, por ejemplo, en hospitales, y como tratamientos preventivos para catéteres y dispositivos médicos antes de su uso en entornos clínicos. Ya existe la tecnología para aplicar fagos a superficies secas, por ejemplo, uniformes, cortinas o incluso suturas para cirugía. Los ensayos clínicos publicados en Clinical Otolaryngology [30] muestran éxito en el tratamiento veterinario de perros con otitis .
El método de detección e identificación de bacterias de detección de cascadas de iones activadas por fagos (SEPTIC) utiliza la emisión de iones y su dinámica durante la infección por fagos y ofrece alta especificidad y velocidad de detección. [44]
La presentación en fagos es un uso diferente de los fagos que involucra una biblioteca de fagos con un péptido variable unido a una proteína de superficie. Cada genoma de fago codifica la variante de la proteína que se muestra en su superficie (de ahí el nombre), proporcionando un vínculo entre la variante peptídica y su gen codificante. Se pueden seleccionar fagos variantes de la biblioteca mediante su afinidad de unión a una molécula inmovilizada (por ejemplo, toxina del botulismo) para neutralizarla. Los fagos seleccionados unidos se pueden multiplicar reinfectando una cepa bacteriana susceptible, lo que les permite recuperar los péptidos codificados en ellos para su posterior estudio. [45]
Las proteínas de los fagos suelen tener actividad antimicrobiana y pueden servir como guías para peptidomiméticos , es decir, fármacos que imitan a los péptidos. [46] La tecnología de fagos-ligandos utiliza proteínas de fagos para diversas aplicaciones, como la unión de bacterias y componentes bacterianos (por ejemplo, endotoxinas ) y la lisis de bacterias. [47]
Los bacteriófagos son organismos modelo importantes para estudiar los principios de la evolución y la ecología . [48]
Los bacteriófagos presentes en el ambiente pueden provocar que el queso no fermente. Para evitar esto, se pueden utilizar cultivos iniciadores de cepas mixtas y regímenes de rotación de cultivos. [49] Se ha estudiado la ingeniería genética de microbios de cultivo, especialmente Lactococcus lactis y Streptococcus thermophilus , para el análisis y la modificación genética con el fin de mejorar la resistencia a los fagos . Esto se ha centrado especialmente en modificaciones cromosómicas recombinantes y de plásmidos . [50] [35]
Algunas investigaciones se han centrado en el potencial de los bacteriófagos como antimicrobianos contra patógenos transmitidos por los alimentos y la formación de biopelículas en la industria láctea. Dado que la propagación de la resistencia a los antibióticos es una de las principales preocupaciones de la industria láctea, los fagos pueden servir como una alternativa prometedora. [51]

El ciclo de vida de los bacteriófagos tiende a ser un ciclo lítico o un ciclo lisogénico . Además, algunos fagos muestran comportamientos pseudolisogénicos. [13]
Con fagos líticos como el fago T4 , las células bacterianas se abren (lisan) y se destruyen después de la replicación inmediata del virión. Tan pronto como se destruye la célula, la progenie del fago puede encontrar nuevos huéspedes para infectar. [13] Los fagos líticos son más adecuados para la terapia con fagos . Algunos fagos líticos experimentan un fenómeno conocido como inhibición de la lisis, donde la progenie de fagos completa no se eliminará inmediatamente de la célula si las concentraciones de fagos extracelulares son altas. Este mecanismo no es idéntico al del fago templado que permanece inactivo y suele ser temporal. [52]
Por el contrario, el ciclo lisogénico no produce la lisis inmediata de la célula huésped. Aquellos fagos capaces de sufrir lisogenia se conocen como fagos templados . Su genoma viral se integrará con el ADN del huésped y se replicará junto con él, de manera relativamente inofensiva, o incluso puede establecerse como un plásmido . El virus permanece latente hasta que las condiciones del huésped se deterioran, quizás debido al agotamiento de nutrientes, luego los fagos endógenos (conocidos como profagos ) se activan. En este punto inician el ciclo reproductivo, lo que resulta en la lisis de la célula huésped. A medida que el ciclo lisogénico permite que la célula huésped continúe sobreviviendo y reproduciéndose, el virus se replica en todos los descendientes de la célula. Un ejemplo de bacteriófago que se sabe que sigue el ciclo lisogénico y el ciclo lítico es el fago lambda de E. coli. [53]
A veces, los profagos pueden proporcionar beneficios a la bacteria huésped mientras están inactivos al agregar nuevas funciones al genoma bacteriano , en un fenómeno llamado conversión lisogénica . Algunos ejemplos son la conversión de cepas inofensivas de Corynebacterium diphtheriae o Vibrio cholerae por parte de bacteriófagos en otras altamente virulentas que causan difteria o cólera , respectivamente. [54] [55] Se han propuesto estrategias para combatir ciertas infecciones bacterianas dirigiéndose a estos profagos que codifican toxinas. [56]

Las células bacterianas están protegidas por una pared celular de polisacáridos , que son importantes factores de virulencia que protegen a las células bacterianas contra las defensas inmunes del huésped y los antibióticos . [57] Para ingresar a una célula huésped, los bacteriófagos se unen a receptores específicos en la superficie de las bacterias, incluidos los lipopolisacáridos , los ácidos teicoicos , las proteínas o incluso los flagelos . Esta especificidad significa que un bacteriófago puede infectar sólo ciertas bacterias que tienen receptores a los que pueden unirse, lo que a su vez determina el rango de huéspedes del fago. Las enzimas que degradan polisacáridos son proteínas asociadas a viriones que degradan enzimáticamente la capa exterior capsular de sus huéspedes en el paso inicial de un proceso de infección por fagos estrechamente programado. [ cita necesaria ] Las condiciones de crecimiento del huésped también influyen en la capacidad del fago para unirse e invadirlos. [58] Como los viriones de los fagos no se mueven de forma independiente, deben depender de encuentros aleatorios con los receptores correctos cuando están en solución, como la sangre, la circulación linfática, el riego, el agua del suelo, etc. [ cita necesaria ]
Los bacteriófagos de miovirus utilizan un movimiento similar al de una jeringa hipodérmica para inyectar su material genético en la célula. Después de contactar con el receptor apropiado, las fibras de la cola se flexionan para acercar la placa base a la superficie de la célula. Esto se conoce como unión reversible. Una vez adherido por completo, se inicia una unión irreversible y la cola se contrae, posiblemente con la ayuda del ATP presente en la cola, [6] inyectando material genético a través de la membrana bacteriana. [59] La inyección se logra mediante una especie de movimiento de flexión en el eje yendo hacia un lado, contrayéndose más cerca de la celda y empujando hacia arriba. Los podovirus carecen de una vaina de cola alargada como la de un miovirus, por lo que utilizan sus pequeñas fibras de cola en forma de dientes enzimáticamente para degradar enzimáticamente una porción de la membrana celular antes de insertar su material genético.
En cuestión de minutos, los ribosomas bacterianos comienzan a traducir el ARNm viral en proteína. Para los fagos basados en ARN, la ARN replicasa se sintetiza en una etapa temprana del proceso. Las proteínas modifican la ARN polimerasa bacteriana para que transcriba preferentemente el ARNm viral. La síntesis normal de proteínas y ácidos nucleicos del huésped se ve alterada y, en su lugar, se ve obligado a fabricar productos virales. Estos productos pasan a formar parte de nuevos viriones dentro de la célula, proteínas auxiliares que contribuyen al ensamblaje de nuevos viriones o proteínas involucradas en la lisis celular . En 1972, Walter Fiers ( Universidad de Gante , Bélgica ) fue el primero en establecer la secuencia de nucleótidos completa de un gen y, en 1976, del genoma viral del bacteriófago MS2 . [60] Algunos bacteriófagos de ADNbc codifican proteínas ribosómicas, que se cree que modulan la traducción de proteínas durante la infección por fagos. [61]
En el caso del fago T4 , la construcción de nuevas partículas virales implica la ayuda de proteínas auxiliares que actúan catalíticamente durante la morfogénesis del fago . [62] Las placas base se ensamblan primero y luego se construyen las colas sobre ellas. Las cápsides de la cabeza, construidas por separado, se ensamblarán espontáneamente con las colas. Durante el ensamblaje del virión del fago T4 , las proteínas morfogenéticas codificadas por los genes del fago interactúan entre sí en una secuencia característica. Mantener un equilibrio apropiado en las cantidades de cada una de estas proteínas producidas durante la infección viral parece ser fundamental para la morfogénesis normal del fago T4 . [63] El ADN se empaqueta eficientemente dentro de las cabezas. [64] Todo el proceso dura unos 15 minutos.
Los fagos pueden liberarse mediante lisis celular, extrusión o, en algunos casos, gemación. La lisis, por parte de los fagos con cola, se logra mediante una enzima llamada endolisina , que ataca y degrada el peptidoglicano de la pared celular . Un tipo de fago completamente diferente, el fago filamentoso , hace que la célula huésped secrete continuamente nuevas partículas de virus. Los viriones liberados se describen como libres y, a menos que sean defectuosos, son capaces de infectar una nueva bacteria. La gemación está asociada con ciertos fagos de Mycoplasma . A diferencia de la liberación de viriones, los fagos que muestran un ciclo lisogénico no matan al huésped y, en cambio, se convierten en residentes a largo plazo como profagos . [sesenta y cinco]
Una investigación realizada en 2017 reveló que el bacteriófago Φ3T produce una proteína viral corta que indica a otros bacteriófagos que permanezcan inactivos en lugar de matar a la bacteria huésped. Arbitrium es el nombre que le dieron a esta proteína los investigadores que la descubrieron. [66] [67]
Dados los millones de fagos diferentes que hay en el medio ambiente, los genomas de los fagos se presentan en una variedad de formas y tamaños. Los fagos de ARN como el MS2 tienen los genomas más pequeños, con sólo unas pocas kilobases. Sin embargo, algunos fagos del ADN, como el T4 , pueden tener genomas grandes con cientos de genes; el tamaño y la forma de la cápside varían junto con el tamaño del genoma. [68] Los genomas de bacteriófagos más grandes alcanzan un tamaño de 735 kb. [69]
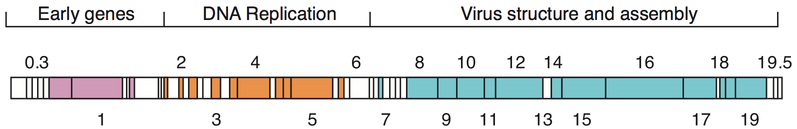
Los genomas de los bacteriófagos pueden ser muy mosaicos , es decir, el genoma de muchas especies de fagos parece estar compuesto de numerosos módulos individuales. Estos módulos pueden encontrarse en otras especies de fagos en diferentes disposiciones. Los micobacteriófagos , bacteriófagos con huéspedes micobacterianos , han proporcionado excelentes ejemplos de este mosaicismo. En estos micobacteriófagos, el surtido genético puede ser el resultado de casos repetidos de recombinación específica de sitio y de recombinación ilegítima (el resultado de la adquisición del genoma del fago de secuencias genéticas del huésped bacteriano). [71] Los mecanismos evolutivos que dan forma a los genomas de los virus bacterianos varían entre diferentes familias y dependen del tipo de ácido nucleico, las características de la estructura del virión y el modo del ciclo de vida viral. [72]
Algunos fagos de roseobacter marinos contienen desoxiuridina (dU) en lugar de desoxitimidina (dT) en su ADN genómico. Existe cierta evidencia de que este componente inusual es un mecanismo para evadir los mecanismos de defensa bacteriana, como las endonucleasas de restricción y los sistemas CRISPR/Cas , que evolucionaron para reconocer y escindir secuencias dentro de los fagos invasores, inactivándolos así. Se sabe desde hace mucho tiempo que otros fagos utilizan nucleótidos inusuales. En 1963, Takahashi y Marmur identificaron un fago de Bacillus que tiene dU sustituyendo a dT en su genoma, [73] y en 1977, Kirnos et al. identificó un cianófago que contiene 2-aminoadenina (Z) en lugar de adenina (A). [74]
El campo de la biología de sistemas investiga las complejas redes de interacciones dentro de un organismo, generalmente utilizando herramientas computacionales y modelos. [75] Por ejemplo, un genoma de fago que ingresa a una célula huésped bacteriana puede expresar cientos de proteínas de fago que afectarán la expresión de numerosos genes del huésped o el metabolismo del huésped . Todas estas interacciones complejas se pueden describir y simular en modelos informáticos. [75]
Por ejemplo, la infección de Pseudomonas aeruginosa por el fago templado PaP3 cambió la expresión del 38% (2160/5633) de los genes de su huésped. Muchos de estos efectos son probablemente indirectos, por lo que el desafío es identificar las interacciones directas entre bacterias y fagos. [76]
Se han realizado varios intentos para mapear las interacciones proteína-proteína entre fagos y su huésped. Por ejemplo, se descubrió que el bacteriófago lambda interactúa con su huésped, E. coli , mediante docenas de interacciones. Una vez más, la importancia de muchas de estas interacciones sigue sin estar clara, pero estos estudios sugieren que lo más probable es que existan varias interacciones clave y muchas interacciones indirectas cuyo papel aún no se ha caracterizado. [77]
Los bacteriófagos son una gran amenaza para las bacterias y los procariotas han desarrollado numerosos mecanismos para bloquear la infección o bloquear la replicación de los bacteriófagos dentro de las células huésped. El sistema CRISPR es uno de esos mecanismos, al igual que los retrones y el sistema antitoxina codificado por ellos. [78] Se sabe que el sistema de defensa de Thoeris implementa una estrategia única para la resistencia a los antifagos bacterianos a través de la degradación de NAD+ . [79]
Los fagos templados son bacteriófagos que integran su material genético en el huésped como episomas extracromosómicos o como profago durante un ciclo lisogénico . [80] [81] [82] Algunos fagos templados pueden conferir ventajas de aptitud física a su huésped de numerosas maneras, incluida la resistencia a los antibióticos mediante la transferencia o introducción de genes de resistencia a los antibióticos (ARG), [81] [83] protegiendo a los huéspedes de la fagocitosis. , [84] [85] proteger a los huéspedes de una infección secundaria mediante la exclusión de superinfección, [86] [87] [88] mejorar la patogenicidad del huésped, [80] [89] o mejorar el metabolismo o el crecimiento bacteriano. [90] [91] [92] [93] La simbiosis bacteriófago-huésped puede beneficiar a las bacterias al proporcionar ventajas selectivas al tiempo que replica pasivamente el genoma del fago. [94]
La metagenómica ha permitido la detección de bacteriófagos en el agua que antes no era posible. [95]
Además, los bacteriófagos se han utilizado en el rastreo y modelado hidrológico en sistemas fluviales , especialmente donde ocurren interacciones entre aguas superficiales y subterráneas . Se prefiere el uso de fagos al marcador de tinte más convencional porque se absorben significativamente menos cuando pasan a través de aguas subterráneas y se detectan fácilmente en concentraciones muy bajas. [96] El agua no contaminada puede contener aproximadamente 2×10 8 bacteriófagos por ml. [97]
Se cree que los bacteriófagos contribuyen ampliamente a la transferencia horizontal de genes en entornos naturales, principalmente mediante transducción , pero también mediante transformación . [98] Los estudios basados en la metagenómica también han revelado que los viromas de una variedad de entornos albergan genes de resistencia a los antibióticos, incluidos aquellos que podrían conferir resistencia a múltiples fármacos . [99]
Hallazgos recientes han mapeado el complejo y entrelazado arsenal de herramientas de defensa antifagos en las bacterias ambientales. [100]
Aunque los fagos no infectan a los humanos, existen innumerables partículas de fagos en el cuerpo humano, dado nuestro extenso microbioma . Nuestra población de fagos ha sido denominada fageoma humano , incluido el "fageoma intestinal sano" (HGP) y el "fageoma humano enfermo" (DHP). [101] Se ha estimado que el fagoma activo de un ser humano sano (es decir, profago integrado que se replica activamente en lugar de no replicarse ) comprende de docenas a miles de virus diferentes. [102] Existe evidencia de que los bacteriófagos y las bacterias interactúan en el microbioma intestinal humano de manera antagónica y beneficiosa. [103]
Estudios preliminares han indicado que los bacteriófagos comunes se encuentran en un promedio del 62% de los individuos sanos, mientras que su prevalencia se redujo en un 42% y un 54% en promedio en pacientes con colitis ulcerosa (CU) y enfermedad de Crohn (EC). [101] La abundancia de fagos también puede disminuir en los ancianos. [103]
Los fagos más comunes en el intestino humano, que se encuentran en todo el mundo, son los crAssphages . Los CrAssphages se transmiten de madre a hijo poco después del nacimiento y existe cierta evidencia que sugiere que pueden transmitirse localmente. Cada persona desarrolla sus propios grupos de crAssphage únicos. Además de los humanos , también pueden estar presentes fagos similares a CrAss en primates . [103]
Entre los innumerables fagos, sólo unos pocos se han estudiado en detalle, incluidos algunos fagos históricamente importantes que se descubrieron en los primeros días de la genética microbiana. Éstos, especialmente el fago T, ayudaron a descubrir principios importantes de la estructura y función de los genes.