
SDS-PAGE ( electroforesis en gel de dodecilsulfato de sodio-poliacrilamida ) es un sistema electroforético discontinuo desarrollado por Ulrich K. Laemmli que se utiliza comúnmente como método para separar proteínas con masas moleculares entre 5 y 250 kDa . [1] [2] El uso combinado de dodecilsulfato de sodio (SDS, también conocido como laurilsulfato de sodio) y gel de poliacrilamida elimina la influencia de la estructura y la carga, y las proteínas se separan por diferencias en su tamaño. Al menos hasta 2012, la publicación que lo describía era el artículo más citado por un solo autor y el segundo más citado en general. [3]
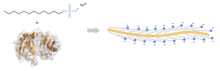

SDS-PAGE es un método de electroforesis que permite la separación de proteínas en masa. El medio (también denominado "matriz") es un gel discontinuo a base de poliacrilamida. El gel de poliacrilamida normalmente se intercala entre dos placas de vidrio en una losa de gel. Aunque históricamente se utilizaron geles en tubo (en cilindros de vidrio), rápidamente quedaron obsoletos con la invención de los geles en placa, más convenientes. [4] Además, se utiliza SDS ( dodecilsulfato de sodio ). Aproximadamente 1,4 gramos de SDS se unen a un gramo de proteína, [5] [6] [7] correspondiente a una molécula de SDS por cada dos aminoácidos . El SDS actúa como tensioactivo , enmascarando la carga intrínseca de la proteína y confiriendo relaciones carga-masa muy similares. Las cargas propias de las proteínas son despreciables en comparación con la carga de SDS y las cargas positivas también se reducen considerablemente en el rango de pH básico de un gel separador. Al aplicar un campo eléctrico constante, las proteínas migran hacia el ánodo, cada una con diferente velocidad, dependiendo de su masa. Este sencillo procedimiento permite una separación precisa de proteínas en masa.
El SDS tiende a formar micelas esféricas en soluciones acuosas por encima de una cierta concentración llamada concentración micelar crítica (CMC). Por encima de la concentración micelar crítica de 7 a 10 milimolar en soluciones, el SDS se presenta simultáneamente como moléculas individuales ( monómero ) y como micelas, por debajo de la CMC, el SDS se presenta solo como monómero en soluciones acuosas. En la concentración micelar crítica, una micela consta de aproximadamente 62 moléculas de SDS. [8] Sin embargo, sólo los monómeros de SDS se unen a las proteínas a través de interacciones hidrófobas, mientras que las micelas de SDS son aniónicas en el exterior y no adsorben ninguna proteína. [5] El SDS es de naturaleza anfipática, lo que le permite desplegar secciones polares y no polares de la estructura de la proteína. [9] En concentraciones de SDS superiores a 0,1 milimolar, comienza el despliegue de las proteínas, [5] y por encima de 1 mM, la mayoría de las proteínas se desnaturalizan. [5] Debido al fuerte efecto desnaturalizante del SDS y a la posterior disociación de los complejos proteicos, por lo general no se pueden determinar estructuras cuaternarias con SDS. Las excepciones son las proteínas estabilizadas mediante reticulación covalente (p. ej. enlaces -SS-) y los complejos proteicos resistentes al SDS, que son estables incluso en presencia de SDS (estos últimos, sin embargo, sólo a temperatura ambiente). Para desnaturalizar los complejos resistentes al SDS se requiere una alta energía de activación, que se consigue mediante calentamiento. La resistencia al SDS se basa en una metaestabilidad del pliegue proteico. Aunque la proteína nativa, completamente plegada y resistente al SDS no tiene suficiente estabilidad en presencia de SDS, el equilibrio químico de desnaturalización a temperatura ambiente se produce lentamente. Los complejos proteicos estables se caracterizan no sólo por la resistencia al SDS sino también por la estabilidad frente a proteasas y una mayor vida media biológica . [10]
Alternativamente, la electroforesis en gel de poliacrilamida también se puede realizar con los tensioactivos catiónicos CTAB en un CTAB-PAGE, [11] [12] [13] o 16-BAC en un BAC-PAGE. [14]
El método SDS-PAGE se compone de preparación de gel, preparación de muestras, electroforesis, tinción de proteínas o transferencia Western y análisis del patrón de bandas generado.


Cuando se utilizan diferentes tampones en el gel (electroforesis en gel discontinua), los geles se preparan hasta un día antes de la electroforesis, para que la difusión no conduzca a una mezcla de los tampones. El gel se produce mediante polimerización de radicales libres en un molde que consta de dos placas de vidrio selladas con espaciadores entre las placas de vidrio. En una configuración típica de minigel, los espaciadores tienen un espesor de 0,75 mm o 1,5 mm, lo que determina la capacidad de carga del gel. Para verter la solución de gel, las placas generalmente se sujetan en un soporte que sella temporalmente la parte inferior de las placas de vidrio, que de otro modo estaría abierta, con los dos espaciadores. Para la solución de gel, se mezcla acrilamida como formador de gel (generalmente 4 % V/V en el gel de apilamiento y 10-12 % en el gel de separación), metilenbisacrilamida como reticulante, tampón de gel de apilamiento o separación, agua y SDS. . Añadiendo el catalizador TEMED y el iniciador radical persulfato de amonio (APS) se inicia la polimerización. Luego se vierte la solución entre las placas de vidrio sin crear burbujas. Dependiendo de la cantidad de catalizador e iniciador de radicales y dependiendo de la temperatura, la polimerización dura entre un cuarto de hora y varias horas. El gel inferior (gel separador) se vierte primero y se cubre con unas gotas de un alcohol apenas soluble en agua (normalmente butanol o isopropanol saturado con tampón), que elimina las burbujas del menisco y protege la solución de gel del oxígeno captador de radicales . Después de la polimerización del gel separador, se desecha el alcohol y se elimina el alcohol residual con papel de filtro . Después de agregar APS y TEMED a la solución de gel de apilamiento, se vierte sobre el gel de separación de sólidos. A continuación se introduce un peine de muestra adecuado entre las placas de vidrio sin que se formen burbujas. El peine de muestra se retira con cuidado después de la polimerización, dejando bolsas para la aplicación de la muestra. Para el uso posterior de proteínas para la secuenciación de proteínas , los geles suelen prepararse el día antes de la electroforesis para reducir las reacciones de la acrilamida no polimerizada con las cisteínas en las proteínas.
Utilizando un mezclador de gradiente se pueden colar geles de gradiente con un gradiente de acrilamida (normalmente de 4 a 12%), que tienen un intervalo de separación de masas moleculares mayor. [15] Los sistemas de gel comerciales (los llamados geles prefabricados ) suelen utilizar tanto en el gel de apilamiento como en el gel de separación la sustancia tampón Bis-tris metano con un valor de pH entre 6,4 y 7,2. [16] [17] Estos geles se entregan moldeados y listos para usar. Como utilizan solo un tampón (electroforesis en gel continua) y tienen un pH casi neutro, pueden almacenarse durante varias semanas. Un pH más neutro ralentiza la hidrólisis y con ello la descomposición de la poliacrilamida. Además, en las proteínas hay menos cisteínas modificadas con acrilamida. [16] Debido al pH constante en la recolección y separación del gel, no hay efecto de apilamiento. Las proteínas de los geles BisTris no se pueden teñir con complejos de rutenio. [18] Este sistema de gel tiene un rango de separación comparativamente grande, que se puede variar usando MES o MOPS en el tampón de ejecución. [dieciséis]

Durante la preparación de la muestra, el tampón de muestra y, por tanto, el SDS, se añade en exceso a las proteínas y luego la muestra se calienta a 95 °C durante cinco minutos o, alternativamente, a 70 °C durante diez minutos. El calentamiento altera las estructuras secundarias y terciarias de la proteína al romper los enlaces de hidrógeno y estirar las moléculas. Opcionalmente, los puentes disulfuro pueden escindirse mediante reducción. Para ello se añaden al tampón de muestra tioles reductores como β-mercaptoetanol (β-ME, 5 % en volumen), ditiotreitol (DTT, 10 milimolar) o ditioeritritol (DTE, 10 milimolar). Después de enfriar a temperatura ambiente, cada muestra se pipetea en su propio pocillo en el gel, que previamente se sumergió en tampón de electroforesis en el aparato de electroforesis.
Además de las muestras, normalmente se carga en el gel un marcador de tamaño de peso molecular . Está compuesto por proteínas de tamaños conocidos y, por lo tanto, permite estimar (con un error de ± 10%) los tamaños de las proteínas en las muestras reales, que migran en paralelo en diferentes pistas del gel. [19] El marcador de tamaño a menudo se pipetea en el primer o último bolsillo de un gel.


Para la separación, las muestras desnaturalizadas se cargan en un gel de poliacrilamida, que se coloca en un tampón de electroforesis con electrolitos adecuados. A continuación, se aplica un voltaje (normalmente alrededor de 100 V, 10-20 V por cm de longitud del gel), lo que provoca una migración de moléculas cargadas negativamente a través del gel en dirección al ánodo cargado positivamente . El gel actúa como un colador. Las proteínas pequeñas migran con relativa facilidad a través de la malla del gel, mientras que es más probable que las proteínas más grandes sean retenidas y, por lo tanto, migren más lentamente a través del gel, lo que permite que las proteínas se separen por tamaño molecular. La electroforesis dura entre media hora y varias horas, dependiendo del voltaje y la longitud del gel utilizado.
Las proteínas que migran más rápido (con un peso molecular inferior a 5 kDa) forman el frente del tampón junto con los componentes aniónicos del tampón de electroforesis, que también migran a través del gel. El área del frente del tampón se hace visible añadiendo el colorante aniónico comparativamente pequeño azul de bromofenol al tampón de muestra. Debido al tamaño relativamente pequeño de la molécula del azul de bromofenol, migra más rápido que las proteínas. Mediante el control óptico de la banda coloreada que migra, se puede detener la electroforesis antes de que el tinte y también las muestras hayan migrado completamente a través del gel y lo abandonen.
El método más utilizado es el SDS-PAGE discontinuo. En este método, las proteínas migran primero a un gel colector con pH neutro, en el que se concentran, y luego a un gel separador con pH básico, en el que tiene lugar la separación propiamente dicha. Los geles de apilamiento y separación se diferencian por el diferente tamaño de poro (4-6 % T y 10-20 % T), fuerza iónica y valores de pH (pH 6,8 o pH 8,8). El electrolito utilizado con más frecuencia es un sistema tampón de Tris - glicina - cloruro que contiene SDS . A pH neutro, la glicina forma predominantemente la forma zwitteriónica , a pH alto las glicinas pierden cargas positivas y se vuelven predominantemente aniónicas. En el gel de recolección, los iones de cloruro más pequeños y con carga negativa migran delante de las proteínas (como iones principales) y los iones de glicinato, un poco más grandes, con carga negativa y parcialmente positiva, migran detrás de las proteínas (como iones finales iniciales), mientras que en el gel, comparativamente gel separador básico ambos iones migran delante de las proteínas. El gradiente de pH entre los tampones del gel de apilamiento y de separación conduce a un efecto de apilamiento en el borde del gel de apilamiento con respecto al gel de separación, ya que el glicinato pierde parcialmente sus cargas positivas de desaceleración a medida que aumenta el pH y luego, como el ion posterior anterior, lo supera. las proteínas y se convierte en un ion líder, lo que hace que las bandas de las diferentes proteínas (visibles después de la tinción) se vuelvan más estrechas y nítidas: el efecto de apilamiento. Para la separación de proteínas y péptidos más pequeños se utiliza el sistema tampón TRIS- Tricina de Schägger y von Jagow debido a la mayor dispersión de las proteínas en el rango de 0,5 a 50 kDa. [20]

Al final de la separación electroforética, todas las proteínas se clasifican por tamaño y luego pueden analizarse mediante otros métodos, por ejemplo, tinción de proteínas como la tinción de Coomassie (la más común y fácil de usar), [21] [22] tinción con plata (la más alta sensibilidad). ), [23] [24] [25] [26] [27 ] [28] tiñe todas las tinciones, tinción con negro Amido 10B , [22] tinción FCF verde rápido , [22] tinciones fluorescentes como la tinción de epicocconona [29] y Tinción naranja SYPRO, [30] y detección inmunológica como el Western Blot . [31] [32] Los tintes fluorescentes tienen una linealidad comparativamente más alta entre la cantidad de proteína y la intensidad del color de aproximadamente tres órdenes de magnitud por encima del límite de detección (la cantidad de proteína que se puede estimar por la intensidad del color). Cuando se utiliza el colorante proteico fluorescente tricloroetanol , se omite una tinción proteica posterior si se añadió a la solución de gel y el gel se irradió con luz ultravioleta después de la electroforesis. [33] [34]
En la tinción de Coomassie , el gel se fija en una solución de etanol al 50% y ácido acético glacial al 10% durante 1 hora. Luego se cambia la solución por una nueva y después de 1 a 12 horas el gel se cambia a una solución colorante (50% metanol, 10% ácido acético glacial, 0,1% azul brillante de coomassie) seguido de decolorar cambiando varias veces una solución decolorante del 40% metanol, ácido acético glacial al 10%.
La tinción de proteínas en el gel crea un patrón de bandas documentable de las distintas proteínas.
La documentación del patrón de bandas generalmente se realiza mediante fotografía o escaneo. Para una posterior recuperación de las moléculas en bandas individuales se puede realizar una extracción en gel .

Después de la tinción de proteínas y la documentación del patrón de bandas, el gel de poliacrilamida se puede secar para su almacenamiento en archivos. De él se pueden extraer proteínas más adelante. El gel se coloca en un marco de secado (con o sin calor) o en un secador al vacío. El marco de secado consta de dos partes, una de las cuales sirve como base para una película de celofán húmeda a la que se le añade el gel y una solución de glicerol al uno por ciento. A continuación se aplica una segunda película de celofán húmeda sin burbujas, se coloca encima la segunda parte del marco y se sella el marco con clips. La eliminación de las burbujas de aire evita la fragmentación del gel durante el secado. El agua se evapora a través de la película de celofán. A diferencia del bastidor de secado, un secador de vacío genera un vacío y calienta el gel a unos 50 °C.

Para una determinación más precisa del peso molecular se miden en el gel separador las distancias de migración relativas de las distintas bandas de proteínas. [37] [38] Las mediciones generalmente se realizan por triplicado para una mayor precisión. La movilidad relativa (llamada valor Rf o valor Rm) se define como la distancia migrada por la banda de proteína dividida por la distancia migrada por el frente amortiguador. Cada una de las distancias se mide desde el comienzo del gel de separación. La migración del frente del tampón corresponde aproximadamente a la migración del colorante contenido en el tampón de muestra. Los Rf del marcador de tamaño se representan de forma semilogarítmica frente a sus pesos moleculares conocidos. Por comparación con la parte lineal del gráfico generado o mediante un análisis de regresión, el peso molecular de una proteína desconocida se puede determinar por su movilidad relativa. [37] [39]
Las bandas de proteínas con glicosilaciones pueden verse borrosas, [35] ya que la glicosilación suele ser heterogénea. [40] Las proteínas con muchos aminoácidos básicos (p. ej. histonas ) [41] pueden provocar una sobreestimación del peso molecular o incluso no migrar al gel, ya que se mueven más lentamente en la electroforesis debido a las cargas positivas o incluso a la dirección opuesta. Por otro lado, muchos aminoácidos ácidos pueden provocar una migración acelerada de una proteína y una subestimación de su masa molecular. [42]
La SDS-PAGE en combinación con una tinción de proteínas se utiliza ampliamente en bioquímica para la separación rápida y exacta y el análisis posterior de proteínas. Tiene costos de instrumentos y reactivos comparativamente bajos y es un método fácil de usar. Debido a su baja escalabilidad , se utiliza principalmente con fines analíticos y menos con fines preparativos, especialmente cuando se deben aislar grandes cantidades de una proteína.
Además, SDS-PAGE se utiliza en combinación con Western blot para determinar la presencia de una proteína específica en una mezcla de proteínas o para el análisis de modificaciones postraduccionales . Las modificaciones postraduccionales de las proteínas pueden conducir a una movilidad relativa diferente (es decir, un cambio de banda ) o a un cambio en la unión de un anticuerpo de detección utilizado en la transferencia Western (es decir, desaparece o aparece una banda).
En espectrometría de masas de proteínas, SDS-PAGE es un método ampliamente utilizado para la preparación de muestras antes de la espectrometría, principalmente mediante digestión en gel . En lo que respecta a la determinación de la masa molecular de una proteína, la SDS-PAGE es un poco más exacta que una ultracentrifugación analítica , pero menos exacta que una espectrometría de masas o - ignorando modificaciones postraduccionales - un cálculo de la masa molecular de la proteína a partir del ADN. secuencia .
En el diagnóstico médico, la SDS-PAGE se utiliza como parte de la prueba del VIH y para evaluar la proteinuria . En la prueba del VIH, las proteínas del VIH se separan mediante SDS-PAGE y posteriormente se detectan mediante Western Blot con anticuerpos específicos del VIH del paciente, si están presentes en su suero sanguíneo . SDS-PAGE para proteinuria evalúa los niveles de varias proteínas séricas en la orina, por ejemplo, albúmina , alfa-2-macroglobulina e IgG .
SDS-PAGE es el método más utilizado para la separación electroforética de proteínas en gel. La electroforesis en gel bidimensional combina secuencialmente el enfoque isoeléctrico o BAC-PAGE con una SDS-PAGE. Se utiliza PAGE nativa si se desea mantener el plegamiento de proteínas nativas. Para la separación de proteínas de membrana, se pueden utilizar BAC-PAGE o CTAB-PAGE como alternativa a SDS-PAGE. Para la separación electroforética de complejos proteicos más grandes, se puede utilizar la electroforesis en gel de agarosa , por ejemplo SDD-AGE . Algunas enzimas se pueden detectar mediante su actividad enzimática mediante zimografía .
Si bien es uno de los métodos de análisis y separación de proteínas más precisos y económicos, la SDS-PAGE desnaturaliza las proteínas. Cuando son necesarias condiciones no desnaturalizantes, las proteínas se separan mediante una PAGE nativa o diferentes métodos cromatográficos con cuantificación fotométrica posterior , por ejemplo, cromatografía de afinidad (o incluso purificación por afinidad en tándem ), cromatografía de exclusión por tamaño , cromatografía de intercambio iónico . [43] Las proteínas también se pueden separar por tamaño en una filtración de flujo tangencial [44] o una ultrafiltración . [45] Las proteínas individuales se pueden aislar de una mezcla mediante cromatografía de afinidad o mediante un ensayo desplegable . Algunos métodos de separación históricamente tempranos y rentables pero toscos generalmente se basan en una serie de extracciones y precipitaciones utilizando moléculas cosmotrópicas , por ejemplo, la precipitación con sulfato de amonio y la precipitación con polietilenglicol .
En 1948, Arne Tiselius recibió el Premio Nobel de Química por el descubrimiento del principio de electroforesis como la migración de átomos o moléculas cargados y disueltos en un campo eléctrico. [46] El uso de una matriz sólida (inicialmente discos de papel) en una electroforesis de zona mejoró la separación. La electroforesis discontinua de 1964 de L. Ornstein y BJ Davis permitió mejorar la separación mediante el efecto de apilamiento. [47] El uso de hidrogeles de poliacrilamida reticulados, a diferencia de los discos de papel o geles de almidón utilizados anteriormente, proporcionó una mayor estabilidad del gel y ninguna descomposición microbiana. El efecto desnaturalizante del SDS en geles continuos de poliacrilamida y la consiguiente mejora en la resolución fue descrito por primera vez en 1965 por David F. Summers en el grupo de trabajo de James E. Darnell para separar las proteínas del poliovirus. [48] La variante actual de SDS-PAGE fue descrita en 1970 por Ulrich K. Laemmli y se utilizó inicialmente para caracterizar las proteínas en la cabeza del bacteriófago T4 . [1]
{{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace ){{citation}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )