El imidazol (ImH) es un compuesto orgánico de fórmula C 3 N 2 H 4 . Es un sólido blanco o incoloro que es soluble en agua, produciendo una solución ligeramente alcalina . En química, es un heterociclo aromático , clasificado como diazol , y tiene átomos de nitrógeno no adyacentes en metasustitución .
Muchos productos naturales, especialmente los alcaloides , contienen el anillo imidazol. Estos imidazoles comparten el anillo 1,3-C 3 N 2 pero presentan sustituyentes variados. Este sistema de anillos está presente en importantes componentes biológicos, como la histidina y la hormona relacionada histamina . Muchos medicamentos contienen un anillo de imidazol, como ciertos medicamentos antimicóticos , la serie de antibióticos nitroimidazol y el sedante midazolam . [5] [6] [7] [8] [9]
Cuando se fusiona con un anillo de pirimidina , forma una purina , que es el heterociclo que contiene nitrógeno más abundante en la naturaleza. [10]
El nombre "imidazol" fue acuñado en 1887 por el químico alemán Arthur Rudolf Hantzsch (1857-1935). [11]
El imidazol es un anillo plano de 5 miembros que existe en dos formas tautoméricas equivalentes porque el hidrógeno puede unirse a uno u otro átomo de nitrógeno . El imidazol es un compuesto altamente polar, como lo demuestra su momento dipolar eléctrico de 3,67 D , [12] y es altamente soluble en agua. El compuesto se clasifica como aromático debido a la presencia de un anillo plano que contiene 6 electrones π (un par de electrones del átomo de nitrógeno protonado y uno de cada uno de los cuatro átomos restantes del anillo). Algunas estructuras de resonancia del imidazol se muestran a continuación:
El imidazol es anfótero , es decir que puede funcionar tanto como ácido como como base. Como ácido, el p K a del imidazol es 14,5, lo que lo hace menos ácido que los ácidos carboxílicos, los fenoles y las imidas, pero ligeramente más ácido que los alcoholes. El protón ácido es el que está unido al nitrógeno. La desprotonación da el anión imidazolida, que es simétrico. Como base, el p K a del ácido conjugado (citado como p K BH + para evitar confusión entre los dos) es aproximadamente 7, lo que hace que el imidazol sea aproximadamente sesenta veces más básico que la piridina . El sitio básico es el nitrógeno con el par solitario (y no unido al hidrógeno). La protonación da el catión imidazolio, que es simétrico.
El imidazol fue descrito por primera vez en 1858 por el químico alemán Heinrich Debus , aunque ya en la década de 1840 se habían descubierto varios derivados del imidazol. Se demostró que el glioxal , el formaldehído y el amoníaco se condensan para formar imidazol (glioxalina, como se llamó originalmente). [13] Esta síntesis, aunque produce rendimientos relativamente bajos, todavía se utiliza para generar imidazoles sustituidos con C.
En una modificación con microondas , los reactivos son bencilo , benzaldehído y amoníaco en ácido acético glacial , formando 2,4,5-trifenilimidazol ("lofina"). [14]
El imidazol se puede sintetizar mediante numerosos métodos además del método Debus . Muchas de estas síntesis también se pueden aplicar a diferentes imidazoles sustituidos y derivados de imidazol variando los grupos funcionales de los reactivos. Estos métodos se clasifican comúnmente según qué y cuántos enlaces se forman para formar los anillos de imidazol. Por ejemplo, el método Debus forma los enlaces (1,2), (3,4) y (1,5) en imidazol, utilizando cada reactivo como un fragmento del anillo y, por lo tanto, este método sería un método de tres enlaces. -formando síntesis. A continuación se presenta una pequeña muestra de estos métodos.
El enlace (1,5) o (3,4) puede formarse mediante la reacción de un imidato y un α-amino aldehído o α-amino acetal . El siguiente ejemplo se aplica al imidazol cuando R 1 = R 2 = hidrógeno.
Los enlaces (1,2) y (2,3) se pueden formar tratando un 1,2-diamino alcano , a altas temperaturas, con un alcohol , aldehído o ácido carboxílico . Se requiere un catalizador deshidrogenante, como platino sobre alúmina .
Los enlaces (1,2) y (3,4) también se pueden formar a partir de α-aminocetonas N -sustituidas y formamida con calor. El producto será un imidazol 1,4-disustituido, pero aquí como R 1 = R 2 = hidrógeno, el propio imidazol es el producto. El rendimiento de esta reacción es moderado, pero parece ser el método más eficaz para realizar la sustitución 1,4.
Este es un método general que puede dar buenos rendimientos para los imidazoles sustituidos. En esencia, se trata de una adaptación del método Debus denominada síntesis de imidazol de Debus-Radziszewski . Los materiales de partida son glioxal sustituido, aldehído, amina y amoníaco o una sal de amonio. [15]
El imidazol se puede sintetizar mediante la fotólisis del 1-viniltetrazol . Esta reacción dará rendimientos sustanciales sólo si el 1-viniltetrazol se elabora de manera eficiente a partir de un compuesto organoestaño , como el 2-tributilestanniltetrazol. La reacción, que se muestra a continuación, produce imidazol cuando R 1 = R 2 = R 3 = hidrógeno.
El imidazol también se puede formar en una reacción en fase de vapor. La reacción se produce con formamida , etilendiamina e hidrógeno sobre platino sobre alúmina , y debe tener lugar entre 340 y 480 °C. Esto forma un producto de imidazol muy puro.
La reacción de Van Leusen también se puede emplear para formar imidazoles a partir de TosMIC y una aldimina . La síntesis de imidazol de Van Leusen permite la preparación de imidazoles a partir de aldiminas mediante reacción con isocianuro de tosilmetilo (TosMIC). Posteriormente, la reacción se amplió a una síntesis de dos pasos en la que la aldimina se genera in situ: la reacción de tres componentes de Van Leusen (vL-3CR).
El imidazol se incorpora a muchos compuestos biológicos importantes. El más generalizado es el aminoácido histidina , que tiene una cadena lateral de imidazol . La histidina está presente en muchas proteínas y enzimas , por ejemplo uniéndose a cofactores metálicos, como se observa en la hemoglobina .
Los compuestos de histidina a base de imidazol desempeñan un papel muy importante en la amortiguación intracelular. [17] La histidina se puede descarboxilar a histamina . La histamina puede causar urticaria (ronchas) cuando se produce durante una reacción alérgica .
Los sustituyentes de imidazol se encuentran en muchos productos farmacéuticos. Los imidazoles sintéticos están presentes en muchos fungicidas y medicamentos antifúngicos , antiprotozoarios y antihipertensivos . El imidazol es parte de la molécula de teofilina , que se encuentra en las hojas de té y los granos de café, y que estimula el sistema nervioso central . Está presente en el medicamento anticancerígeno mercaptopurina , que combate la leucemia al interferir con las actividades del ADN .
Varios imidazoles sustituidos, incluido el clotrimazol , son inhibidores selectivos de la óxido nítrico sintasa , lo que los convierte en objetivos farmacológicos interesantes en la inflamación , las enfermedades neurodegenerativas y los tumores del sistema nervioso. [18] [19] Otras actividades biológicas del farmacóforo de imidazol se relacionan con la regulación negativa de los flujos intracelulares de Ca 2+ y K + y la interferencia con el inicio de la traducción. [20]
Los derivados de imidazol sustituidos son valiosos en el tratamiento de muchas infecciones fúngicas sistémicas . [21] Los imidazoles pertenecen a la clase de antifúngicos azólicos , que incluye ketoconazol , miconazol y clotrimazol .
A modo de comparación, otro grupo de azoles son los triazoles, que incluyen fluconazol , itraconazol y voriconazol . La diferencia entre los imidazoles y los triazoles involucra el mecanismo de inhibición de la enzima citocromo P450 . El N3 del compuesto imidazol se une al átomo de hierro hemo del citocromo férrico P450, mientras que el N4 de los triazoles se une al grupo hemo. Se ha demostrado que los triazoles tienen una mayor especificidad por el citocromo P450 que los imidazoles, lo que los hace más potentes que los imidazoles. [22]
Algunos derivados de imidazol muestran efectos sobre los insectos, por ejemplo, el nitrato de sulconazol muestra un fuerte efecto antialimentario en las larvas del escarabajo australiano de las alfombras, Anthrenocerus australis , que digiere queratina , al igual que el nitrato de econazol en la polilla común de la ropa Tineola bisselliella . [23]
El imidazol en sí tiene pocas aplicaciones directas. En cambio, es un precursor de una variedad de agroquímicos, incluidos enilconazol , escaladazol , clotrimazol , procloraz y bifonazol . [24]
El imidazol y sus derivados tienen una alta afinidad por los cationes metálicos. Una de las aplicaciones del imidazol es la purificación de proteínas marcadas con His en cromatografía de afinidad por metales inmovilizados (IMAC). El imidazol se utiliza para eluir proteínas marcadas unidas a iones de níquel adheridos a la superficie de las perlas en la columna de cromatografía . Se pasa un exceso de imidazol a través de la columna, lo que desplaza la etiqueta His de la coordinación del níquel, liberando las proteínas etiquetadas con His.
El imidazol es un tampón adecuado para pH de 6,2 a 7,8 [25] . El imidazol puro esencialmente no tiene absorbancia en longitudes de onda relevantes para las proteínas (280 nm), [26] [27] sin embargo, purezas más bajas de imidazol pueden dar una absorbancia notable a 280 nm. El imidazol puede interferir con el ensayo de proteínas de Lowry . [28]
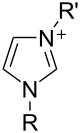
Las sales de imidazol en las que el anillo de imidazol es el catión se conocen como sales de imidazolio (por ejemplo, cloruro o nitrato de imidazolio ). [29] Estas sales se forman a partir de la protonación o sustitución en el nitrógeno del imidazol. Estas sales se han utilizado como líquidos iónicos y precursores de carbenos estables . También son bien conocidas las sales en las que un imidazol desprotonado es un anión ; estas sales se conocen como imidazolatos (por ejemplo, imidazolato de sodio, NaC 3 H 3 N 2 ).
El imidazol tiene una toxicidad aguda baja, como lo indica la LD 50 de 970 mg/kg (rata, oral). [24]
{{cite encyclopedia}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )