El indio es un elemento químico ; tiene símbolo In y número atómico 49. Es un metal de post-transición de color blanco plateado y uno de los elementos más blandos. Químicamente, el indio es similar al galio y al talio , y sus propiedades son en gran medida intermedias entre los dos. [10] Fue descubierto en 1863 por Ferdinand Reich y Hieronymous Theodor Richter mediante métodos espectroscópicos y recibió su nombre de la línea azul índigo en su espectro. [11]
El indio es un elemento tecnológico crítico que se utiliza principalmente en la producción de pantallas planas como óxido de indio y estaño (ITO) , un recubrimiento transparente y conductor aplicado al vidrio. [12] [13] [14] El indio también se utiliza en la industria de los semiconductores , [15] en aleaciones metálicas de bajo punto de fusión , como soldaduras y sellos de alto vacío de metales blandos. Se obtiene exclusivamente como subproducto durante el procesamiento de minerales de otros metales, principalmente de esfalerita y otros minerales de sulfuro de zinc . [dieciséis]
El indio no tiene ningún papel biológico y sus compuestos son tóxicos cuando se inhalan o se inyectan en el torrente sanguíneo, aunque se absorben mal después de la ingestión. [17] [18]
El nombre proviene de la palabra latina indicum que significa violeta o índigo . [19]

El indio es un metal de post-transición brillante, de color blanco plateado, muy dúctil y con un brillo brillante . [20] Es tan suave ( dureza Mohs 1,2) que se puede cortar con un cuchillo y deja una línea visible como un lápiz cuando se frota sobre papel. [21] Es miembro del grupo 13 de la tabla periódica y sus propiedades son en su mayoría intermedias entre sus vecinos verticales el galio y el talio . Al igual que el estaño , cuando se dobla el indio se escucha un grito agudo : un crujido debido al hermanamiento de los cristales . [20] Al igual que el galio, el indio puede humedecer el vidrio. Como ambos, el indio tiene un punto de fusión bajo , 156,60 °C (313,88 °F); más alto que su homólogo más ligero, el galio, pero más bajo que su homólogo más pesado, el talio, y más bajo que el estaño. [22] El punto de ebullición es 2072 °C (3762 °F), más alto que el del talio, pero más bajo que el galio, a la inversa de la tendencia general de los puntos de fusión, pero de manera similar a las tendencias a la baja de otros grupos de metales posteriores a la transición porque de la debilidad del enlace metálico con pocos electrones deslocalizados . [23]
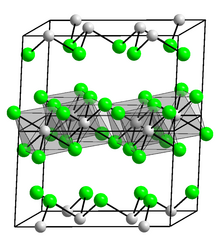
La densidad del indio, 7,31 g/cm 3 , también es mayor que la del galio, pero menor que la del talio. Por debajo de la temperatura crítica , 3,41 K , el indio se convierte en un superconductor . El indio cristaliza en el sistema cristalino tetragonal centrado en el cuerpo en el grupo espacial I 4/ mmm ( parámetros de red : a = 325 pm , c = 495 pm): [22] esta es una estructura cúbica centrada en las caras ligeramente distorsionada , donde cada indio Atom tiene cuatro vecinos a 324 pm de distancia y ocho vecinos un poco más lejos (336 pm). [24] El indio tiene mayor solubilidad en mercurio líquido que cualquier otro metal (más del 50 por ciento en masa de indio a 0 °C). [25] El indio muestra una respuesta viscoplástica dúctil , que se considera independiente del tamaño en tensión y compresión. Sin embargo, tiene un efecto de tamaño en la flexión y la indentación, asociado a una escala de longitud del orden de 50 a 100 μm, [26] significativamente grande en comparación con otros metales.
El indio tiene 49 electrones, con una configuración electrónica de [ Kr ]4d 10 5s 2 5p 1 . En los compuestos, el indio suele donar los tres electrones más externos para convertirse en indio (III), In 3+ . En algunos casos, el par de electrones 5s no se dona, lo que da como resultado indio(I), In + . La estabilización del estado monovalente se atribuye al efecto del par inerte , en el que los efectos relativistas estabilizan el orbital 5s, observado en elementos más pesados. El talio ( el homólogo más pesado del indio ) muestra un efecto aún más fuerte, haciendo que la oxidación a talio (I) sea más probable que a talio (III), [27] mientras que el galio (el homólogo más ligero del indio) comúnmente muestra solo el estado de oxidación +3. Así, aunque el talio (III) es un agente oxidante moderadamente fuerte , el indio (III) no lo es, y muchos compuestos de indio (I) son potentes agentes reductores . [28] Si bien la energía requerida para incluir los electrones s en el enlace químico es la más baja para el indio entre los metales del grupo 13, las energías de enlace disminuyen hacia abajo en el grupo, de modo que en el indio, la energía liberada para formar dos enlaces adicionales y alcanzar el +3 El estado no siempre es suficiente para compensar la energía necesaria para involucrar a los electrones 5s. [29] El óxido y el hidróxido de indio (I) son más básicos y el óxido y el hidróxido de indio (III) son más ácidos. [29]
Se informan varios potenciales de electrodo estándar, dependiendo de la reacción en estudio, [30] para el indio, lo que refleja la estabilidad disminuida del estado de oxidación +3: [24]
El indio metálico no reacciona con el agua, pero se oxida con agentes oxidantes más fuertes, como los halógenos, para dar compuestos de indio (III). No forma boruro , siliciuro o carburo , y el hidruro InH 3 tiene, en el mejor de los casos, una existencia transitoria en soluciones etéreas a bajas temperaturas, siendo lo suficientemente inestable como para polimerizar espontáneamente sin coordinación. [28] El indio es bastante básico en solución acuosa, mostrando sólo ligeras características anfóteras y, a diferencia de sus homólogos más ligeros, el aluminio y el galio, es insoluble en soluciones alcalinas acuosas. [31]
El indio tiene 39 isótopos conocidos , cuyo número de masa oscila entre 97 y 135. Sólo dos isótopos se encuentran naturalmente como nucleidos primordiales : el indio-113, el único isótopo estable , y el indio-115, que tiene una vida media de 4,41 × 10.14 años, cuatro órdenes de magnitud mayor que la edad del Universo y casi 30.000 veces mayor que la vida media del torio-232 . [32] La vida media del 115 In es muy larga porque la desintegración beta del 115 Sn está prohibida por el espín . [33] El indio-115 constituye el 95,7% de todo el indio. El indio es uno de los tres elementos conocidos (los otros son telurio y renio ) cuyo isótopo estable es menos abundante en la naturaleza que los radioisótopos primordiales de larga vida. [34]
El isótopo artificial más estable es el indio-111 , con una vida media de aproximadamente 2,8 días. Todos los demás isótopos tienen vidas medias inferiores a 5 horas. El indio también tiene 47 metaestados, entre los cuales el indio-114m1 (vida media de aproximadamente 49,51 días) es el más estable, más estable que el estado fundamental de cualquier isótopo de indio que no sea el primordial. Toda desintegración por transición isomérica . Los isótopos de indio más ligeros que el 113 In se desintegran predominantemente mediante captura de electrones o emisión de positrones para formar isótopos de cadmio , mientras que los isótopos de indio más pesados que el 113 In se desintegran predominantemente mediante la desintegración beta-menos para formar isótopos de estaño. [32]
El óxido de indio (III) , en 2 O 3 , se forma cuando el indio metálico se quema en el aire o cuando se calienta el hidróxido o el nitrato. [35] En 2 O 3 adopta una estructura similar a la alúmina y es anfótero, es decir, capaz de reaccionar tanto con ácidos como con bases. El indio reacciona con agua para reproducir hidróxido de indio (III) soluble , que también es anfótero; con álcalis para producir indatos (III); y con ácidos para producir sales de indio (III):
También se conocen los sesquicalcogenuros análogos con azufre , selenio y telurio . [36] El indio forma los trihaluros esperados . La cloración, bromación y yodación del In producen InCl 3 , InBr 3 incoloros e InI 3 amarillo . Los compuestos son ácidos de Lewis , algo parecidos a los trihaluros de aluminio más conocidos. De nuevo, al igual que el compuesto de aluminio relacionado, el InF 3 es polimérico. [37]
La reacción directa del indio con los pnictógenos produce los semiconductores III-V grises o semimetálicos . Muchos de ellos se descomponen lentamente en el aire húmedo, lo que requiere un almacenamiento cuidadoso de los compuestos semiconductores para evitar el contacto con la atmósfera. El nitruro de indio es fácilmente atacado por ácidos y álcalis. [38]
Los compuestos de indio (I) no son comunes. El cloruro, el bromuro y el yoduro tienen colores intensos, a diferencia de los trihaluros originales a partir de los cuales se preparan. El fluoruro se conoce únicamente como un compuesto gaseoso inestable. [39] El polvo negro de óxido de indio (I) se produce cuando el óxido de indio (III) se descompone al calentarlo a 700 °C. [35]
Con menos frecuencia, el indio forma compuestos en estado de oxidación +2 e incluso en estados de oxidación fraccionados. Por lo general, estos materiales presentan enlaces In-In, sobre todo en los haluros In 2 X 4 y [In 2 X 6 ] 2− , [40] y varios subcalcogenuros como In 4 Se 3 . [41] Se sabe que varios otros compuestos combinan indio (I) e indio (III), como In I 6 (In III Cl 6 )Cl 3 , [42] In I 5 (In III Br 4 ) 2 (In III Br 6 ), [43] y En I En III Br 4 . [40]
Los compuestos de organoindio presentan enlaces In-C. La mayoría son derivados de In(III), pero el ciclopentadienilidio(I) es una excepción. Fue el primer compuesto de organoindio (I) conocido, [44] y es polimérico y consta de cadenas en zigzag de átomos de indio alternos y complejos de ciclopentadienilo . [45] Quizás el compuesto organoindio más conocido sea el trimetilindio , In(CH 3 ) 3 , utilizado para preparar ciertos materiales semiconductores. [46] [47]
En 1863, los químicos alemanes Ferdinand Reich y Hieronymous Theodor Richter estaban probando minerales de las minas de los alrededores de Freiberg, Sajonia . Disolvieron los minerales pirita , arsenopirita , galena y esfalerita en ácido clorhídrico y destilaron cloruro de zinc en bruto . Reich, que era daltónico , empleó a Richter como asistente para detectar las líneas espectrales de colores. Sabiendo que los minerales de esa región a veces contienen talio , buscaron las líneas verdes del espectro de emisión de talio. En cambio, encontraron una línea azul brillante. Debido a que esa línea azul no coincidía con ningún elemento conocido, plantearon la hipótesis de que había un nuevo elemento presente en los minerales. Llamaron al elemento indio, por el color índigo que se ve en su espectro, en honor al latín indicum , que significa "de la India ". [48] [11] [49] [50]
Richter aisló el metal en 1864. [51] Se presentó un lingote de 0,5 kg (1,1 lb) en la Exposición Mundial de 1867. [52] Reich y Richter se pelearon más tarde cuando este último afirmó ser el único descubridor. [50]

El indio se crea mediante el proceso s (captura lenta de neutrones ) de larga duración (hasta miles de años) en estrellas de masa baja a media (rango de masa entre 0,6 y 10 masas solares ). Cuando un átomo de plata-109 captura un neutrón, se transmuta en plata-110, que luego sufre desintegración beta para convertirse en cadmio-110. Al capturar más neutrones, se convierte en cadmio-115, que se desintegra en indio-115 mediante otra desintegración beta . Esto explica por qué el isótopo radiactivo es más abundante que el estable. [53] El isótopo estable del indio, indio-113, es uno de los núcleos p , cuyo origen no se comprende completamente; aunque se sabe que el indio-113 se produce directamente en los procesos s y r (captura rápida de neutrones), y también como hijo del muy largo cadmio-113, que tiene una vida media de unos ocho mil billones de años, esto no puede explicar todo el indio-113. [54] [55]
El indio es el elemento número 68 más abundante en la corteza terrestre con aproximadamente 50 ppb . Esto es similar a la abundancia de plata , bismuto y mercurio en la corteza terrestre . Muy raramente forma sus propios minerales o se presenta en forma elemental. Se conocen menos de 10 minerales de indio como la roquesita (CuInS 2 ), y ninguno se encuentra en concentraciones suficientes para una extracción económica. [56] En cambio, el indio suele ser un oligoelemento de minerales más comunes, como la esfalerita y la calcopirita . [57] [58] De estos, se puede extraer como subproducto durante la fundición. [16] Si bien el enriquecimiento de indio en estos depósitos es alto en relación con su abundancia en la corteza terrestre, es insuficiente, a los precios actuales, para sustentar la extracción de indio como producto principal. [56]
Existen diferentes estimaciones sobre las cantidades de indio contenidas en los minerales de otros metales. [59] [60] Sin embargo, estas cantidades no se pueden extraer sin extraer los materiales anfitriones (ver Producción y disponibilidad). Así, la disponibilidad de indio está determinada fundamentalmente por el ritmo al que se extraen estos minerales, y no por su cantidad absoluta. Este es un aspecto que a menudo se olvida en el debate actual, por ejemplo, por el grupo Graedel de Yale en sus evaluaciones de criticidad [61] , lo que explica los tiempos de agotamiento paradójicamente bajos que citan algunos estudios. [62] [16]

El indio se produce exclusivamente como subproducto durante el procesamiento de minerales de otros metales. Su principal material de origen son los minerales de zinc sulfurados, donde se encuentra principalmente en esfalerita. [16] También se extraen cantidades menores de minerales de cobre sulfurados. Durante el proceso de tostación, lixiviación y electroobtención de fundición de zinc , el indio se acumula en los residuos ricos en hierro. De estos se puede extraer de diferentes formas. También se puede recuperar directamente de las soluciones del proceso. La purificación adicional se realiza mediante electrólisis . [64] El proceso exacto varía según el modo de funcionamiento de la fundición. [20] [16]
Su condición de subproducto significa que la producción de indio está limitada por la cantidad de minerales sulfurados de zinc (y cobre) extraídos cada año. Por lo tanto, su disponibilidad debe discutirse en términos de potencial de oferta. El potencial de oferta de un subproducto se define como la cantidad que se puede extraer económicamente de sus materiales anfitriones por año en las condiciones actuales del mercado (es decir, tecnología y precio). [65] Las reservas y los recursos no son relevantes para los subproductos, ya que no pueden extraerse independientemente de los productos principales. [16] Estimaciones recientes sitúan el potencial de suministro de indio en un mínimo de 1.300 t/año a partir de minerales de zinc sulfídicos y 20 t/año de minerales de cobre sulfídicos. [16] Estas cifras son significativamente mayores que la producción actual (655 t en 2016). [66] Por lo tanto, serán posibles aumentos importantes en el futuro en la producción de indio como subproducto sin aumentos significativos en los costos o precios de producción. El precio medio del indio en 2016 fue de 240 dólares EE.UU./kg , frente a 705 dólares EE.UU./kg en 2014. [67]
China es el principal productor de indio (290 toneladas en 2016), seguida de Corea del Sur (195 t), Japón (70 t) y Canadá (65 t). [66] La refinería de Teck Resources en Trail, Columbia Británica , es un gran productor de indio de fuente única, con una producción de 32,5 toneladas en 2005, 41,8 toneladas en 2004 y 36,1 toneladas en 2003.
El principal consumo de indio en todo el mundo es la producción de LCD . La demanda aumentó rápidamente desde finales de la década de 1990 hasta 2010 con la popularidad de los monitores de computadora LCD y los televisores, que ahora representan el 50% del consumo de indio. [14] La mayor eficiencia de fabricación y el reciclaje (especialmente en Japón) mantienen un equilibrio entre la oferta y la demanda. Según el PNUMA , la tasa de reciclaje del indio al final de su vida útil es inferior al 1%. [68]

En 1924, se descubrió que el indio tenía una valiosa propiedad de estabilizar metales no ferrosos , y ese se convirtió en el primer uso significativo del elemento. [69] La primera aplicación a gran escala del indio fue el revestimiento de cojinetes en motores de aviones de alto rendimiento durante la Segunda Guerra Mundial , para protegerlos contra daños y corrosión ; este ya no es un uso importante del elemento. [64] Se encontraron nuevos usos en aleaciones fusibles , soldaduras y electrónica . En la década de 1950, se utilizaban pequeñas perlas de indio para los emisores y colectores de los transistores de unión de aleación PNP . A mediados y finales de la década de 1980, el desarrollo de semiconductores de fosfuro de indio y películas delgadas de óxido de indio y estaño para pantallas de cristal líquido (LCD) despertó mucho interés. En 1992, la aplicación de películas finas se había convertido en el uso final más importante. [70] [71]
El óxido de indio (III) y el óxido de indio y estaño (ITO) se utilizan como revestimiento conductor transparente sobre sustratos de vidrio en paneles electroluminiscentes . [72] El óxido de indio y estaño se utiliza como filtro de luz en lámparas de vapor de sodio de baja presión . La radiación infrarroja se refleja nuevamente dentro de la lámpara, lo que aumenta la temperatura dentro del tubo y mejora el rendimiento de la lámpara. [71]
El indio tiene muchas aplicaciones relacionadas con los semiconductores . Algunos compuestos de indio, como el antimonuro de indio y el fosfuro de indio , [73] son semiconductores con propiedades útiles: un precursor suele ser el trimetilindio (TMI), que también se utiliza como dopante semiconductor en semiconductores compuestos II-VI . [74] InAs e InSb se utilizan para transistores de baja temperatura e InP para transistores de alta temperatura. [64] Los semiconductores compuestos InGaN e InGaP se utilizan en diodos emisores de luz (LED) y diodos láser. [75] El indio se utiliza en la energía fotovoltaica como semiconductor de seleniuro de cobre, indio y galio (CIGS), también llamado células solares CIGS , un tipo de célula solar de película delgada de segunda generación . [76] El indio se utiliza en transistores de unión bipolar PNP con germanio : cuando se suelda a baja temperatura, el indio no tensiona el germanio. [64]

El alambre de indio se utiliza como sello de vacío y conductor térmico en aplicaciones criogénicas y de vacío ultraalto , en aplicaciones de fabricación como juntas que se deforman para llenar huecos. [77] Debido a su gran plasticidad y adhesión a los metales, las láminas de indio a veces se utilizan para soldadura en frío en circuitos de microondas y uniones de guías de ondas , donde la soldadura directa es complicada. El indio es un ingrediente de la aleación galinstan de galio, indio y estaño , que es líquido a temperatura ambiente y reemplaza al mercurio en algunos termómetros . [78] Otras aleaciones de indio con bismuto , cadmio , plomo y estaño , que tienen puntos de fusión más altos pero aún bajos (entre 50 y 100 °C), se utilizan en sistemas de rociadores contra incendios y reguladores de calor. [64]
El indio es uno de los muchos sustitutos del mercurio en las pilas alcalinas para evitar que el zinc se corroa y libere gas hidrógeno . [79] Se agrega indio a algunas aleaciones de amalgama dental para disminuir la tensión superficial del mercurio y permitir menos mercurio y una amalgamación más fácil. [80]
La alta sección transversal de captura de neutrones del indio para neutrones térmicos lo hace adecuado para su uso en barras de control de reactores nucleares , típicamente en una aleación de 80% plata , 15% indio y 5% cadmio . [81] En ingeniería nuclear, las reacciones (n,n') de 113 In y 115 In se utilizan para determinar las magnitudes de los flujos de neutrones. [82]
En 2009, el profesor Mas Subramanian y ex estudiante de posgrado Andrew Smith de la Universidad Estatal de Oregón descubrieron que el indio se puede combinar con itrio y manganeso para formar un pigmento intensamente azul , no tóxico, inerte y resistente a la decoloración , el azul YInMn , el primer nuevo inorgánico. pigmento azul descubierto en 200 años. [83]
El indio no tiene ningún papel metabólico en ningún organismo. De manera similar a las sales de aluminio, los iones de indio (III) pueden ser tóxicos para el riñón cuando se administran mediante inyección. [18] El óxido de indio y estaño y el fosfuro de indio dañan los sistemas pulmonar e inmunológico, predominantemente a través del indio iónico, [85] aunque el óxido de indio hidratado es más de cuarenta veces más tóxico cuando se inyecta, medido por la cantidad de indio introducido. [18] El indio-111 radiactivo (en cantidades muy pequeñas sobre una base química) se utiliza en pruebas de medicina nuclear , como radiotrazador para seguir el movimiento de proteínas marcadas y glóbulos blancos en el cuerpo. [86] [87] Los compuestos de indio en su mayoría no se absorben tras la ingestión y sólo se absorben moderadamente tras la inhalación; tienden a almacenarse temporalmente en los músculos , la piel y los huesos antes de ser excretados, y la vida media biológica del indio es de aproximadamente dos semanas en humanos. [88]
Las personas pueden estar expuestas al indio en el lugar de trabajo por inhalación, ingestión, contacto con la piel y contacto con los ojos. El pulmón de indio es una enfermedad pulmonar caracterizada por proteinosis alveolar pulmonar y fibrosis pulmonar, descrita por primera vez por investigadores japoneses en 2003. Hasta 2010 [actualizar], se habían descrito 10 casos, aunque más de 100 trabajadores de indio habían documentado anomalías respiratorias. [17] El Instituto Nacional de Seguridad y Salud Ocupacional ha establecido un límite de exposición recomendado (REL) de 0,1 mg/m 3 durante una jornada laboral de ocho horas. [89]
{{cite book}}: Mantenimiento CS1: nombres numéricos: lista de autores ( enlace )