La calcitonina es una hormona peptídica de 32 aminoácidos secretada por las células parafoliculares (también conocidas como células C) de la tiroides (o endostilo ) en humanos y otros cordados [5] en el cuerpo ultimofaríngeo . [6] Actúa reduciendo el calcio en sangre (Ca 2+ ), oponiéndose a los efectos de la hormona paratiroidea (PTH). [7]
Su importancia en humanos no ha sido tan bien establecida como su importancia en otros animales, ya que su función no suele ser significativa en la regulación de la homeostasis normal del calcio . [8] Pertenece a la familia de proteínas similares a la calcitonina .
Históricamente la calcitonina también ha sido llamada tirocalcitonina. [9]
La calcitonina se forma mediante la escisión proteolítica de un prepropéptido más grande , que es producto del gen CALC1 ( CALCA ). Es funcionalmente un antagonista de la PTH y la vitamina D3. El gen CALC1 pertenece a una superfamilia de precursores de hormonas proteicas relacionadas, incluida la proteína precursora de amiloide de los islotes , el péptido relacionado con el gen de la calcitonina y el precursor de la adrenomedulina .
La secreción de calcitonina es estimulada por:
La hormona participa en el metabolismo del calcio (Ca 2+ ). En muchos sentidos, la calcitonina contrarresta la hormona paratiroidea (PTH) y la vitamina D.
Más específicamente, la calcitonina reduce los niveles de Ca 2+ en sangre de dos maneras:
Las altas concentraciones de calcitonina pueden aumentar la excreción urinaria de calcio y fosfato a través de los túbulos renales . [15] que conduce a una marcada hipocalcemia . Sin embargo, este es un efecto menor sin importancia fisiológica en humanos. También es un efecto de corta duración porque los riñones se vuelven resistentes a la calcitonina, como lo demuestra la excreción no afectada de calcio por los riñones en pacientes con tumores de tiroides que secretan un exceso de calcitonina. [dieciséis]
En sus acciones preservadoras del esqueleto, la calcitonina protege contra la pérdida de calcio del esqueleto durante los períodos de movilización de calcio, como el embarazo y, especialmente, la lactancia . Los mecanismos protectores incluyen la inhibición directa de la resorción ósea y el efecto indirecto mediante la inhibición de la liberación de prolactina de la glándula pituitaria. La razón proporcionada es que la prolactina induce la liberación de un péptido relacionado con la PTH que mejora la resorción ósea, pero aún está bajo investigación. [17] [18] [19]
Otros efectos son la prevención de la hipercalcemia posprandial resultante de la absorción de Ca 2+ . Además, la calcitonina inhibe la ingesta de alimentos en ratas y monos y puede tener una acción sobre el SNC que implica la regulación de la alimentación y el apetito.
La calcitonina reduce el calcio y el fósforo en sangre principalmente mediante la inhibición de los osteoclastos. Los osteoblastos no tienen receptores de calcitonina y, por tanto, no se ven directamente afectados por los niveles de calcitonina. Sin embargo, dado que la resorción ósea y la formación ósea son procesos acoplados, eventualmente la inhibición de la actividad osteoclástica por parte de la calcitonina conduce a un aumento de la actividad osteoblástica (como efecto indirecto). [dieciséis]

El receptor de calcitonina es un receptor acoplado a proteína G localizado en los osteoclastos [20], así como en las células renales y cerebrales. Está acoplado a una subunidad Gs α , estimulando así la producción de AMPc por la adenilato ciclasa en las células diana. También puede afectar los ovarios en las mujeres y los testículos en los hombres. [ cita necesaria ]
La calcitonina fue purificada por primera vez en 1962 por Douglas Harold Copp y B. Cheney en la Universidad de Columbia Británica , Canadá. [21] Inicialmente se pensó que era secretado por la glándula paratiroides , pero Iain Macintyre y su equipo de la Royal Post Graduate Medical School de Londres demostraron que era secretado por las células parafoliculares de la glándula tiroides . [22] El Dr. Copp nombró a la hormona descubierta calcitonina debido a su papel en "mantener el tono normal del calcio". [21]
El ensayo de calcitonina se utiliza para identificar pacientes con enfermedades nodulares de la tiroides . Es útil para realizar un diagnóstico temprano del carcinoma medular de tiroides. Una enfermedad maligna de las células parafoliculares, es decir, el cáncer medular de tiroides (MTC), normalmente produce un nivel elevado de calcitonina sérica. El pronóstico del MTC depende de la detección y el tratamiento tempranos.
La calcitonina también ha tenido un impacto significativo en la biología molecular , ya que el gen que codifica la calcitonina fue el primer gen descubierto en células de mamíferos que se empalmó alternativamente , lo que ahora se sabe que es un mecanismo ubicuo en eucariotas . [23] [24]
La calcitonina se ha utilizado clínicamente para los trastornos metabólicos óseos durante más de 50 años. [25] La calcitonina de salmón se utiliza para el tratamiento de:
Se ha investigado como un posible tratamiento no quirúrgico para la estenosis espinal . [31]
La siguiente información procede del Compendio de medicamentos electrónicos del Reino Unido [32]
La calcitonina de salmón se absorbe y elimina rápidamente. Las concentraciones plasmáticas máximas se alcanzan dentro de la primera hora después de la administración.
Los estudios en animales han demostrado que la calcitonina se metaboliza principalmente mediante proteólisis en el riñón después de la administración parenteral. Los metabolitos carecen de la actividad biológica específica de la calcitonina. La biodisponibilidad tras la inyección subcutánea e intramuscular en humanos es alta y similar para las dos vías de administración (71% y 66%, respectivamente).
La calcitonina tiene vidas medias de absorción y eliminación cortas, de 10 a 15 minutos y de 50 a 80 minutos, respectivamente. La calcitonina de salmón se degrada principalmente y casi exclusivamente en los riñones, formando fragmentos farmacológicamente inactivos de la molécula. Por lo tanto, el aclaramiento metabólico es mucho menor en pacientes con insuficiencia renal terminal que en sujetos sanos. Sin embargo, se desconoce la relevancia clínica de este hallazgo. La unión a proteínas plasmáticas es del 30% al 40%.
Existe una relación entre la dosis subcutánea de calcitonina y las concentraciones plasmáticas máximas. Tras la administración parenteral de 100 UI de calcitonina, la concentración plasmática máxima se sitúa entre aproximadamente 200 y 400 pg/ml. Los niveles sanguíneos más altos pueden estar asociados con una mayor incidencia de náuseas, vómitos y diarrea secretora.
Se han realizado estudios convencionales de toxicidad, reproducción, mutagenicidad y carcinogenicidad a largo plazo en animales de laboratorio. La calcitonina de salmón carece de potencial embriotóxico, teratogénico y mutagénico.
Se ha informado de una mayor incidencia de adenomas hipofisarios en ratas que recibieron calcitonina sintética de salmón durante 1 año. Esto se considera un efecto específico de cada especie y no tiene relevancia clínica. [33] La calcitonina de salmón no cruza la barrera placentaria.
En animales lactantes a los que se les administró calcitonina, se ha observado una supresión de la producción de leche. La calcitonina se secreta en la leche.
La calcitonina se extraía de las glándulas ultimobranquiales (glándulas similares a la tiroides) de los peces, en particular del salmón. La calcitonina de salmón se parece a la calcitonina humana, pero es más activa. En la actualidad, se produce mediante tecnología de ADN recombinante o mediante síntesis química de péptidos . Se ha demostrado que las propiedades farmacológicas de los péptidos sintéticos y recombinantes son cualitativa y cuantitativamente equivalentes. [32]
La calcitonina se puede utilizar terapéuticamente para el tratamiento de la hipercalcemia o la osteoporosis . [34] En un estudio clínico reciente, las inyecciones subcutáneas de calcitonina redujeron la incidencia de fracturas y redujeron la disminución de la masa ósea en mujeres con diabetes tipo 2 complicada con osteoporosis. [35]
Las inyecciones subcutáneas de calcitonina en pacientes con manía dieron como resultado una disminución significativa de la irritabilidad, la euforia y la hiperactividad y, por lo tanto, la calcitonina es prometedora para el tratamiento del trastorno bipolar . [36] Sin embargo, no se ha informado de ningún trabajo adicional sobre esta posible aplicación de la calcitonina.
Puede usarse para diagnóstico como marcador tumoral del cáncer medular de tiroides , en el que pueden estar presentes niveles elevados de calcitonina y niveles elevados después de la cirugía pueden indicar recurrencia. Incluso se puede utilizar en muestras de biopsia de lesiones sospechosas (p. ej., ganglios linfáticos inflamados ) para establecer si son metástasis del cáncer original.
Se ha sugerido que los valores de corte de calcitonina para distinguir casos de cáncer medular de tiroides son los siguientes, y un valor más alto aumenta la sospecha de cáncer medular de tiroides: [37]
Cuando sean mayores de 3 años, se podrán utilizar los límites de adulto
Una revisión sistemática Cochrane evaluó la precisión diagnóstica de la calcitonina basal y estimulada para el cáncer de tiroides medular. [38] Aunque las pruebas de calcitonina basal y combinada, basal y estimulada, presentaron una alta precisión ( sensibilidad : entre 82 % y 100 %; especificidad : entre 97,2 % y 100 %), estos resultados tuvieron un alto riesgo de sesgo debido a fallas de diseño de los ensayos incluidos. estudios. [38] En general, el valor de las pruebas de rutina de calcitonina para el diagnóstico y pronóstico del cáncer medular de tiroides sigue siendo incierto y cuestionable. [38]
También se han informado niveles elevados de calcitonina para otras afecciones. Incluyen: hiperplasia de células C, carcinoma de células de avena no tiroideo, carcinoma no tiroideo y otras neoplasias malignas no tiroideas, lesión renal aguda e insuficiencia renal crónica , hipercalcemia , hipergastrinemia y otros trastornos gastrointestinales, y enfermedad pulmonar . [39]
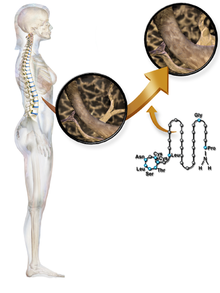
La calcitonina es una hormona polipeptídica de 32 aminoácidos, con un peso molecular de 3454,93 daltons. Su estructura comprende una única hélice alfa. [40] El corte y empalme alternativo del gen que codifica la calcitonina produce un péptido lejanamente relacionado de 37 aminoácidos, llamado péptido relacionado con el gen de la calcitonina (CGRP), de tipo beta. [41]
Las siguientes son las secuencias de aminoácidos del salmón y la calcitonina humana: [ cita necesaria ] [42]
Cys-Ser-Asn-Leu-Ser-Thr-Cys-Val-Leu-Gly-Lys-Leu-Ser-Gln-Glu-Leu-His-Lys-Leu-Gln-Thr-Tyr-Pro-Arg-Thr- Asn-Thr-Gly-Ser-Gly-Thr-Pro
Cys-Gly-Asn-Leu-Ser-Thr-Cys-Met-Leu-Gly-Thr-Tyr-Thr-Gln-Asp-Phe-Asn-Lys-Phe-His-Thr-Phe-Pro-Gln-Thr- Ala-Ile-Gly-Val-Gly-Ala-Pro
En comparación con la calcitonina del salmón, la calcitonina humana se diferencia en 16 residuos.
Además de las formas de dosificación inyectables y en aerosol nasal de la calcitonina de salmón, actualmente se encuentran en desarrollo clínico formulaciones orales no invasivas del péptido. La corta vida media de este péptido en suero desencadenó varios intentos de mejorar las concentraciones plasmáticas. El péptido forma un complejo con una macromolécula que actúa como potenciador de la absorción a través de la vía transcelular y, además, protege el péptido del pH severo y las condiciones enzimáticas del tracto gastrointestinal. Esta complejación es débil, no covalente y reversible y el fármaco permanece químicamente sin modificar. Después del paso a través del intestino, el agente de administración se disocia del péptido. Una de las formulaciones orales ampliamente estudiadas son las sales disódicas de calcitonina oral 5-CNAC. Esta nueva plataforma oral en una serie de ensayos clínicos en diferentes fases ha demostrado un perfil farmacocinético mejorado prometedor, una alta biodisponibilidad, una seguridad bien establecida y una eficacia comparable a la de la calcitonina nasal, especialmente para el tratamiento de la pérdida ósea posmenopáusica. [25]